零价铁修复铅污染水体的研究
2014-09-18刘晓宁李瑞娟
李 雅, 汪 葵, 吴 奇, 金 文, 刘晓宁, 李瑞娟
(1.西安航空学院 动力工程系,陕西 西安 710077;2.江西环境工程职业学院 林业与环境学院,江西 赣州 341000)
零价铁修复铅污染水体的研究
李 雅1, 汪 葵2, 吴 奇1, 金 文1, 刘晓宁1, 李瑞娟1
(1.西安航空学院 动力工程系,陕西 西安 710077;2.江西环境工程职业学院 林业与环境学院,江西 赣州 341000)
在实验室条件下,用零价铁去除Pb(II)。考察了铁粉的投加量及初始pH值对去除效果的影响,并探讨了零价铁修复铅污染水体的机制,为零价铁实际修复铅污染水体提供技术参考。结果表明:零价铁可以有效修复受重金属铅污染的水体,修复效果受铁粉的投加量及初始pH值的影响;零价铁去除铅的机制为氧化还原和混凝吸附。
零价铁;铅污染;氧化还原;混凝吸附
0 前言
水体重金属污染中,铅污染的问题尤为突出。铅可对许多人体器官造成不良影响,特别是对人的肺、肾脏、生殖系统、心血管系统。其不良影响主要表现为智力下降、肾脏损伤、不孕不育、孕妇流产和高血压等[1]。铅对儿童的危害很大。文献[2]指出:铅经过胃消化后,成人吸收11%,而儿童吸收高达30%~75%。
近几十年来,零价铁(zero valent iron,ZVI)作为水体污染修复剂得到了广泛的应用。它既可以修复水体中的有机污染物,又可以去除水体中的重金属污染物[3]。本文将严重危害人体健康的Pb(II)作为研究对象,在实验室条件下,用还原铁粉去除Pb(II)。考察了铁粉的投加量及初始pH值对去除效果的影响,并探讨了还原铁粉修复铅污染水体的机制,为零价铁实际修复铅污染水体提供技术参考。
1 实验
1.1 实验材料
还原铁粉(分析纯);硝酸铅(优级纯),配成质量浓度为100mg/L的标准储备液。实验用水为去离子水。
1.2 实验仪器
HZQ-R型气浴恒温振荡器,TDL-40B型离心机,AUX220型电子天平,DHG-9053A型电热恒温鼓风干燥箱,SZ-93型自动双重纯水蒸馏器,海尔BCD-235YH型冰箱,SB25-12DT型超声波清洗机,SHB-III型循环水式多用真空泵,Z-5000型原子吸收分光光度计,PHS-3C型pH 计,DDS-307型电导率仪。
1.3 实验方法
(1)铁粉酸洗预处理
将铁粉用一定浓度的稀HCl浸泡,产生气体后(大约3~5min),再用去离子水将残留的酸液洗去,直到洗涤液呈中性为止。
(2)批实验
将上述酸洗过的铁粉放入装有一定体积铅液的锥形瓶中,然后立即封口。将锥形瓶置于恒温振荡器中,在温度为(25.0±0.1)℃、转速为230~240 r/min的条件下振荡一段时间。之后,取一定量的上清液于离心试管中进行离心分离,过滤后取滤液分析,测定溶液中铅的质量浓度。铁粉的投加量为0.50g,铅液的质量浓度均为5mg/L,反应时间为60min。做三组平行实验,以保证其准确性。在实验中,只控制反应的初始条件,所有样品的采集和分析都在室温下完成。
1.4 分析测试
溶液的pH值和Eh值用PHS-3C型pH计测定。电导率用DDS-307型电导率仪测定。铅的测定采用火焰原子吸收法[4]。
2 结果与讨论
2.1 铁粉投加量的影响
增加反应物的投加量可以提高化学反应速率。因此,在零价铁去除铅的过程中,铅的去除速率随铁粉投加量的增加而加快。当铁粉的粒径不变时,所用的铁粉越多,则铁粉与铅的接触面积越大,铁粉对铅的去除率也越高。图1为铁粉的投加量对铅的去除率的影响。由图1可知:铁粉的投加量为1.00g时,铅的去除率明显高于0.50g和0.25g的。

图1 铁粉的投加量对铅的去除率的影响
不同铁粉投加量时pH值和Eh值的变化,如表1和表2所示。反应前的pH值和Eh值分别为1.46和291mV。从表1和表2中可以看出:零价铁修复铅的过程伴随着pH值的增大和Eh值的下降,且随着铁粉投加量的增加,两者的变化幅度增大。研究表明[5-6]:零价铁的去污过程伴随着pH值的增大及电导率的下降。

表1 不同铁粉投加量时pH值的变化

表2 不同铁粉投加量时Eh值的变化
2.2 初始pH值的影响
研究表明[7-8]:影响零价铁修复污染物的主要因素是pH值;pH值越低,污染物的去除效果越好。图2为初始pH值对铅的去除率的影响。不同初始pH值时溶液pH值的变化,如表3所示。

图2 初始pH值对铅的去除率的影响

表3 不同初始pH值时溶液pH值的变化
由图2可知:零价铁对铅的去除率随初始pH值升高而迅速下降。由表3可知:随着初始pH值的增大,溶液pH值的变化量减小。这与文献[9]的结论一致,即零价铁在低pH值下的去污效果较好。一方面是因为铁粉表面的氧化膜在酸性条件下容易被去除;另一方面是因为铁粉在酸性条件下容易被腐蚀,并且酸性条件有利于溶解态的亚铁离子存在。亚铁离子不但直接参与污染物的还原反应,还能防止铁粉表面迅速钝化。
2.3 零价铁去除铅的机制
Scherer等[10]认为:零价铁降解有机氯化物的主要机制是原电池反应、铁氧化物的半导体作用和铁腐蚀产物直接参与反应。而 Matheson等[11]认为:零价铁表面的直接还原、亚铁离子的还原和氢气的催化还原是零价铁降解有机氯化物的机制。
由于零价铁的活性高,容易与许多污染物发生反应,包括含氧酸根离子、重金属、有机氯化物和硝基苯类[3]。唐次来[12]在考察零价铁去除地下水中硝酸盐时,报道了以纳米铁修复污染物的机制。由于零价铁修复污染物的机制不是一成不变的,污染物不同,去除机制也不同。即使是同一种污染物,不同研究者的研究结果也不相同。为此,本文研究了零价铁修复铅污染的机制。
因为铁是一种活泼金属,其电极电位Eθ(Fe2+/Fe)=-0.440V,所以铁具有还原性。此外,亚铁离子也有还原能力,其电极电位Eθ(Fe3+/Fe2+)=0.771V。所以当水中有氧化剂存在时,亚铁离子可以被氧化成铁离子。而亚铁离子和铁离子在水中会形成Fe(OH)2和Fe(OH)3絮状沉淀。另外,Fe(OH)3还可能水解生成Fe(OH)2+,Fe(OH)+2等配位离子。这些配位离子都具有很强的絮凝能力,可以与重金属离子结合生成稳定的絮凝物,从而去除水中的重金属污染物。
Ponder等[13]利用纳米级零价铁还原去除水体中的六价铬和二价铅。将0.50g铁加入到200mL浓度为50mmol/L的铅液中,反应30d后通过XPS和XRD对铁粉进行分析。结果表明:二价铅被还原为铅,但可能还有其他产物,如Pb(OH)2和PbO·xH2O。铅的还原处理一般可用如下方程式表示:
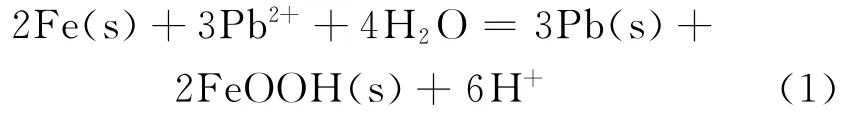
实验中发现:反应液由初始的无色、澄清变为黄色、有少许絮状物,还有些反应液变浑浊。这可能是因为铅与铁粉通过反应生成了沉淀物质,如Pb,Pb(OH)2和PbO·xH2O;或者是铅被一些配位离子[如Fe(OH)2+,Fe(OH)+2等]吸附,生成了絮状物。因此,可以得出零价铁去除铅的机制为氧化还原和混凝吸附。
3 结论
还原铁粉能够有效、快速地去除水体中的铅污染,其机制为氧化还原和混凝吸附,产物为Pb,Pb(OH)2和PbO·xH2O等。在零价铁去除铅的过程中,反应液的pH值升高而Eh值降低;增加铁粉的投加量,有利于铅的去除;反应液的初始pH值越低,零价铁对铅的去除效果越好。
:
[1]张正洁,李东红,许增贵.我国铅污染现状、原因及对策[J].环境保护科学,2005,15(4):41-42.
[2]姜楠,王鹤立,廉新颖.地下水铅污染修复技术应用与研究进展[J].环境科学与技术,2008,31(2):56-60.
[3]FARRELL J,KASON M,MELITAS N,et al.Investigation of the long-term performance of zero-valent iron for reductive dechlorination of trichloroethylene[J].Environmental Science& Technology,2000,34(3):514-521.
[4]中国环境保护总局.水和废水监测分析方法(第4版)[M].北京:中国环境科学出版社,2002.
[5]WILKIN R T,PULS R W,SEWELL G W.Long-term performance of permeable reactive barriers using zero-valent iron:Geochemical and microbiological effects[J].Ground Water,2003,41(4):493-503.
[6]WESTERHOFF P,JAMES J.Nitrate removal in zero-valent iron packed columns[J].Water Research,2003,37(8):1 818-1 830.
[7]HAO Z W,XU X H,WANG D H.Reductive denitrification of nitrate by scrap iron filings[J].Journal of Zhejiang University SCIENCE B,2005,6(3):182-186.
[8]李胜业,金朝晖,金晓秋,等.还原铁粉反应柱去除地下水中硝酸盐氮的研究[J].农业环境科学学报,2004,23(6):1 203-1 206.
[9]SU C,PULS R W.Arsenate and arsenite removal by zerovalent iron:Kinetics,redox transformation and implications for in situ groundwater remediation[J].Environmental Science & Technology,2001,35(7):1 487-1 492.
[10]SCHERER M M,BALKO B A,GALLAGHER D A.Correlation analysis of rate constants for dechlorination by zero-valent iron[J].Environmental Science & Technology,1998,32(19):3 026-3 033.
[11]MATHESON L J, TRATNYEK P G.Reductive dehalogenation of chlorinated methanes by iron metal[J].Environmental Science & Technology,1994,28(12):2 045-2 053.
[12]唐次来.Fe0还原黄土高原地下水中NO-3污染的模拟研究[D].杨凌:西北农林科技大学,2007.
[13]PONDER S M,DARAB J G,MALLOUK T E.Remediation of Cr(VI)and Pb(II)aqueous solutions using supported,nanoscale zero-valent iron[J].Environmental Science &Technology,2000,34(12):2 564-2 569.
A Research on Repair of Lead Polluted Water Using Zero Valent Ⅰron
LⅠ Ya1, WANG Kui2, WU Qi1, JⅠN Wen1, LⅠU Xiao-ning1, LⅠ Rui-juan1
(1.Department of Power Engineering,Xi’an Aeronautic University,Xi’an 710077,China;2.Forestry and Environment Institute,Jiangxi Environmental Engineering Vocational College,Ganzhou 341000,China)
Under laboratory conditions,Pb(II)was removed by zero valent iron.The influence of iron powder dosage and initial pH value on removal effect was investigated,and the mechanism of repairing lead polluted water with zero valent iron was explored,providing a technical reference for actual restoration of lead polluted water with zero valent iron.The results show that zero valent iron can effectively repair the water polluted by heavy metal lead,the repairing effect is affected by iron powder dosage and initial pH value;the mechanism for lead removal with zero valent iron is redox and coagulation adsorption.
zero valent iron;lead pollution;redox;coagulation adsorption
西安航空学院校级课题(No.12XQ306);江西省科技支撑计划项目(No.20132BBG70026);陕西省大学生创新创业训练计划项目(No.201211396003)
X 523
A
1000-4742(2014)03-0047-03
2012-11-08
