马钱子碱固体脂质纳米粒大鼠体内药动学研究
2014-09-14赵义军吕邵娃古立翠管庆霞李永吉高佳翔张欣媛
赵义军,吕邵娃,古立翠,管庆霞,张 亮,李永吉,高佳翔,张欣媛
(黑龙江中医药大学 药学院,哈尔滨 150040)
马钱子碱(Brucine)为马钱科植物马钱子(Strychons nuxvanica L.)的主要有效成分,为吲哚型的生物碱,具有抗癌、镇痛、促进骨修复及增强机体免疫力等作用,是极具研究潜力的抗肿瘤药物,但其体内消除半衰期短,具有明显的中枢毒性.固体脂质纳米粒(SLN)是一种以固体脂质为粒子基质,粒径在纳米范围内的新型药物传递系统[1],粒径小,生物毒性低,具有控释和长效制剂的优势.本文在马钱子碱固体脂质纳米粒制备工艺研究的基础上,对马钱子碱固体脂质纳米粒(B-SLN)的体内药物动力学进行研究,并与马钱子碱单体溶液的药代动力学参数相比较,为马钱子碱纳米制剂的研究提供科学依据.
1 仪器与试剂
1.1 仪器
美国Waters公司高效液相色谱仪系统:2996Photodiode Array Detector,2695Separations Module, Empow色谱工作站;色谱柱Diamonsi (R) 钻石C18(250×4.6 μm,5 μm);TGL-16C型离心机(上海安亭科学仪器厂);WH-1微型涡旋混合器(上海沪西分析仪器厂有限公司);微量移液器(大龙合资);MP2000电子天平(上海第二天平仪器厂);BCD-221B/HC RONGSHENG冰箱;氮吹仪(BF-2000).
1.2 试剂
马钱子碱对照品(质量分数≥98%,中国食品药品检定研究院);PoLoxamer 188(批号WPOG565B,上海宏运化工有限公司);卵磷脂(批号20101103,上海灵锦精细化工有限公司);单硬脂酸甘油酯(批号10517,阿拉丁化工有限公司);二氯甲烷(天津化学试剂厂);色谱甲醇(美国Dikma公司);娃哈哈纯净水,其他试剂均为市售分析纯.
1.3 实验动物
Wistar大鼠,体重(200±10)g,黑龙江中医药大学GLP实验室提供,合格证号SYXK(黑)2012-001.
2 实验方法
2.1 色谱条件
色谱柱:Dikma C18ODS( 250 mm×4.6 mm,5 μm);流动相:甲醇︰水-乙酸-三乙胺(30∶70);流速:1mL/min;检测波长:264 nm; 进样量:20 μL.
2.2 血浆样品处理
精密吸取100 μL血浆样品置具塞试管中,加入50 μL的1 moL/L氢氧化钠液,振摇混匀,涡旋5 min,冷水超声20 min,取出,加入0.5 mL提取液(二氯甲烷∶甲醇=9∶1),涡旋5 min,冷水超声20 min,取出离心10 min(10 000 r/min),分层,吸取下层液,再加0.5 mL提取液重新萃取1遍,合并两次二氯甲烷层,在45 ℃氮气吹干,残渣物用200 μL甲醇溶解,涡旋3 min,离心15 min(12 000 r/min),按2.1项下色谱条件进样20 μL,HPLC分析记录峰面积.
2.3 方法学考察
2.3.1 标准曲线与线性范围
精密吸取马钱子碱系列标准溶液200 μL,置于1.5 mL离心管中,分别精密加入空白血浆100 μL,涡旋混合1 min后,按2.2项下方法处理,HPLC分析测定,进样量20 μL,记录峰面积.以马钱子碱的质量浓度为横坐标,马钱子碱的峰面积为纵坐标绘制标准曲线.经计算机线性回归可知马钱子碱的质量浓度在0.60~38.40 μg/mL范围内线性关系良好,回归方程为Y=13 535X+3 059.5,r2=0.999 1.
2.3.2 专属性试验
分别制备空白血浆,空白血浆加对照品、给药后血浆,按2.2项下方法处理测定,进样20 μL,进行HPLC分析,记录色谱图,将色谱图相对照,结果表明在血浆样品处理过程中未引入干扰性杂质,且血浆中内源性物质不干扰测定.色谱图见图1.

图1 样品高效液相色谱图
2.3.3 精密度实验
精密吸取大鼠空白血浆100 μL,分别加入不同质量浓度的标准溶液200 μL,配制成相当于质量浓度为5.0、25.0、50.0 μg/mL的马钱子碱样品溶液,按2.2项下方法处理测定.每份样品连续进样5次,根据标准曲线将峰面积换算成马钱子碱质量浓度,计算日内精密度;连续5 d相同条件进样,根据标准曲线将峰面积换算成马钱子碱质量浓度,计算日内和日间精密度.结果见表1.日内精密度和日间精密度的RSD值均小于5%,精密度良好,符合生物样品分析指导原则的要求.
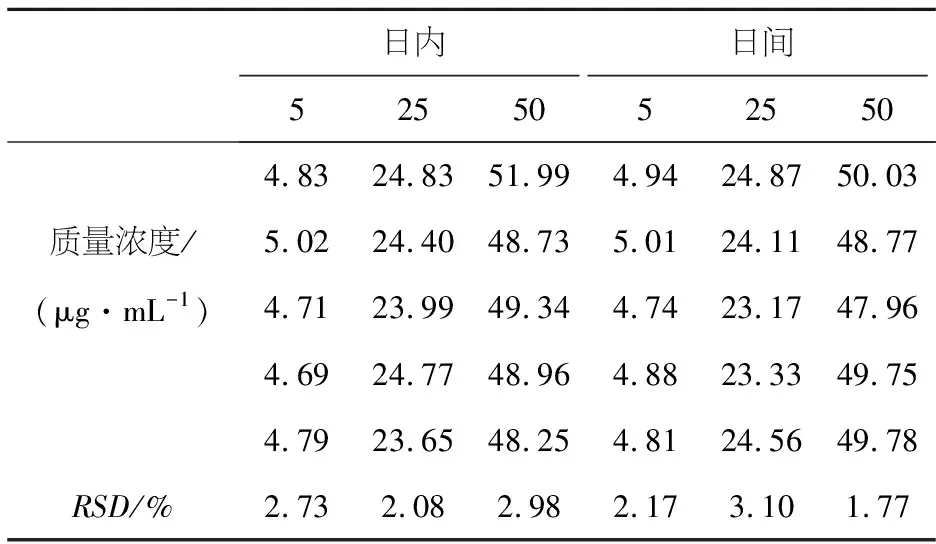
表1 日内、日间精密度结果
2.3.4 提取回收率
见表2.

表2 血浆中马钱子碱的提取回收率(n=5)
精密吸取大鼠空白血浆100 μL,加入不同质量浓度的标准溶液200 μL,配制成相当质量浓度为5.0、25.0、50.0 μg/mL的马钱子碱样品溶液,按2.2项下方法处理测定,进样20 μL,进行HPLC分析,记录峰面积,每个质量浓度平行作5份;另取质量浓度为5.0、25.0、50.0 μg/mL 的标准溶液,进行HPLC分析,记录峰面积,每个质量浓度平行作5份.上述计算方法回收率所记录的峰面积与此次操作相应质量浓度的样品的峰面积之比即得提取回收率,从而求得马钱子碱的提取回收率.
2.3.5 方法回收率
精密吸取大鼠空白血浆100 μL,分别加入不同质量浓度的标准溶液200 μL,配制成相当于质量浓度为5.0、25.0、50.0 μg/mL的马钱子碱样品溶液,按2.2项下方法处理测定,记录峰面积.每个质量浓度平行作5份,将测得样品的峰面积,代入马钱子碱大鼠血浆标准曲线中,得到样品的方法回收率.结果见表3.
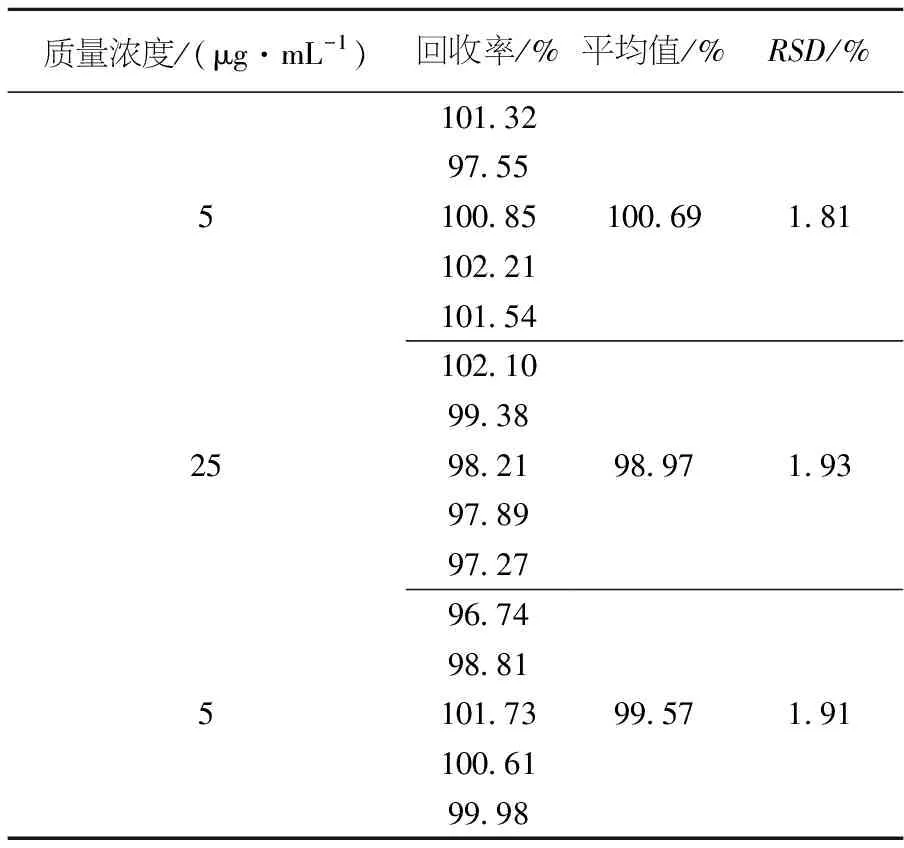
表3 血浆中马钱子碱的方法回收率(n=5)
2.4 大鼠体内药动学研究
将大鼠随机分为4组,每组6只,雌雄各半,根据文献[2-5]及预试验.尾静脉注射马钱子碱纳米粒组高、中、低剂量(15、10、5 mg/kg) ,马钱子碱溶液低剂量组(5 mg/kg).给药前12 h禁食,不禁水,给药方式为尾静脉注射给药.于给药后 5、10、20、40、60、90、120、150、180、210、240、360 min 从眼眶后静脉丛取血约400 μL,置1.5 mL肝素化离心管中,5 000 r/pm离心10 min,取上清液100 μL,置于-20 ℃中保存待测.取大鼠血浆100 μL,按2.2项下方法处理测定,进样20 μL进行HPLC分析,记录峰面积,计算各时间点血药质量浓度.
3 实验结果
血药质量浓度-时间数据采用3P97进行C-T曲线拟合处理,根据AIC值和拟合优度值最小为原则结合F检验,所确定的药物动力学行为均符合二室模型(权重系数为1/C/C),并求得了药动学参数.药物动力学参数分别见表4.

表4 不同给药组的大鼠药动学参数(n=6)
4 讨 论
本实验建立了大鼠血浆中马钱子碱含量测定的HPLC法,经过方法学考察,证实本法简便,准确,能够满足动物体内药物动力学研究的需要.实验发现马钱子碱溶液与马钱子碱固体脂质纳米粒在大鼠体内过程均符合二室模型,药物动力学试验结果表明,在相同给药剂量时马钱子碱溶液的T1/2α为0.74 min,T1/2β为50.20 min,AUC为417.32 (μg/mL)/min,血浆清除率为0.012 /kg/min.而马钱子碱固体脂质纳米粒的T1/2α和T1/2β分别为0.84 min和136.23 min,AUC值为2 336.03 (μg/mL)/min,血浆清除率为0.002 1 /kg/min.相对生物利用度为559.8%.马钱子碱固体脂质纳米粒的药动学特征显示了马钱子碱经纳米粒包裹后,显著延长了药物在循环系统中的滞留时间,生物利用度提高,血药质量浓度平稳,降低了清除率,起到一定的缓释作用,从而可以增强马钱子碱的疗效.
参考文献:
[1] MEHNERT W, MADER K. Solid lipid nanoparticles:production and applications[J]. Adv Drug DeL Rev.2006, 47(2-3):165-196.
[2] 王 琳, 蔡宝昌, 杨 欢, 等.马钱子碱溶液和马钱子碱脂质体在家兔体内的药代动力学比较研究[J]. 南京中医药大学学报,2 006, 5(3):22.
[3] 王 玮,陈 军,蔡宝昌,等.马钱子碱隐形脂质体在大鼠体内的药物动力学[J]. 南京中医药大学学报, 2009, 5(3): 25.
[4] 陈 军,胡 巍, 蔡宝昌, 等. 马钱子碱在大鼠体内的药动学[J].中国药学杂志, 2009, 5(10): 44.
[5] 李伟男,于 鑫,王莹莹,等.马钱子总生物碱树脂复合物的制备及结合机制[J].哈尔滨商业大学学报:自然科学版,2013,29(3):265-270.
