他汀类药物防治阿尔茨海默病疗效及安全性的Meta分析
2014-09-13唐士婷蔺心敬
唐士婷 黄 浩 蔺心敬
(广西壮族自治区人民医院神经内科,广西 南宁 530021)
阿尔茨海默病(AD)已经成为当今社会经济负担最重的疾病之一〔1〕。近年来治疗学家们对该病的病因学及治疗学做了大量的研究工作,逐渐认识到胆固醇升高是导致AD发病率上升的危险因素之一〔2〕,其机制可能如下:高胆固醇血症通过影响β-淀粉样前体蛋白(βAPP)的代谢,从而致使β-淀粉样蛋白(Aβ)沉积,即老年斑(SP)形成,而SP是AD的主要病理特征之一。大量研究〔3,4〕表明他汀类药物作为胆固醇生物合成限速酶——羟甲基戊二酰辅酶A还原酶的竞争性抑制剂,能有效地降低血浆中的胆固醇含量,从而降低AD的发病风险并有潜在的治疗作用。但仍有许多学者认为他汀类药物虽能显著地降低血清及脑内胆固醇含量,但并不能有效地降低AD的发病风险〔5,6〕。因此,针对他汀类药物在防治AD方面存在的争议,本文采用Meta分析方法对他汀类药物防治AD的疗效和安全性进行系统评价。
1 资料与方法
1.1纳入与排除标准
1.1.1研究类型 随机对照试验(RCT)。
1.1.2研究对象 ①预防性试验:参与者具备AD的高危因素,例如:高胆固醇血症,携带载脂蛋白E-4基因(APE4),经美国神经学会质量标准分会通过的轻度认知功能障碍(MCI)诊断标准诊断为MCI。②治疗性试验:须有明确的诊断标准且符合美国神经病学、语言障碍和脑卒中老年性痴呆和相关疾病学会(NINCDS/ADRDA)“很可能AD”诊断标准。
1.1.3干预措施 ①预防性试验:实验组使用适当剂量的某种他汀类药物,对照组使用相同剂量的安慰剂。②治疗性试验:实验组单独使用适当剂量的某种他汀类药物或者联用其他能改善认知功能的药物;对照组单独使用相同剂量的安慰剂或者联用相同剂量其他能改善认知功能的药物。
1.1.4结局指标 ①预防性试验:主要指标:认知功能:韦氏智力量表缩短本(WASI),韦氏智力量表第三版(WMS-Ⅲ),受控词语联想测验(COWA);次要指标:药物的副作用,血液及脑脊液生化指标:总胆固醇(TC),甘油三酯(TG),高密度脂蛋白胆固醇(HDL-C),低密度脂蛋白胆固醇(LDL-C),总tau(t-tau),Aβ42等含量。②治疗性试验:主要指标:阿尔茨海默病评价量表-认知部分(ADAS-Cog),简易智能精神状态量表(MMSE);次要指标:药物的副作用,实验对象的生活质量。
1.1.5排除标准 ①纳入研究的终点观察指标不是本系统评价需要的结局指标;②无法获得全文且无详细数据的文献;③研究质量及评价等级不高的文献。
1.2检索策略 计算机检索PubMed,EM-BASE,Cochrane Library,中国学术期刊全文数据库(CNKI),万方数据库(WanFang Data),中国生物医学数据库(CBM)。检索日期截至2012年4月,文献无语言限制。
英文检索式为:#1:“Alzheimer disease” or Alzheimer$ or dement$;#2:stain$ or lovastatin or simvastatin or cervistatin or atorvastatin or rosuvastatin or provastatin or fluvastatin or Hydroxymethlglutaryl-CoA Inhibitors;#3:“random controlled trials” OR “random” OR “control” OR “trials”;#4: #1 and #2 and #3。中文检索式:#1:“阿尔茨海默病”或“痴呆”;#2:“他汀类药物” 或“洛伐他汀” 或“辛伐他汀” 或“西立伐他汀” 或“阿托伐他汀” 或“瑞舒伐他汀” 或“普伐他汀” 或“氟伐他汀” 或“羟甲基戊二酰辅酶A”;#3:“随机对照试验”或“随机”或“对照”或“试验”;#4:#1并且#2并且#3。
1.3数据提取 参照Cochrane Handbook 5.1.0制定的“文献信息提取表”,由2位研究者独立提取资料,进行交叉核对,如有分歧,通过双方讨论或请第3位研究者协助解决。
1.4文献质量评价 严格按照Cochrane Handbook 5.1.0制定的“偏倚风险标准”,对纳入文献的以下方法学指标进行评价:①随机方法是否正确;②分配方案隐藏情况;③是否实施盲法;④结果数据是否完整;⑤是否有选择性研究报告;⑥其他偏倚来源。
1.5统计学分析 采用Review Manager5.1.0软件。连续性变量采用加权均数差(WMD)及其95%CI表示,对分类变量采用相对危险度(RR)及其95%CI表示。异质性检验采用P≤0.10和I2≥50%作为显著性判断标准,当P>0.10和I2<50%时,采用固定效应模型分析;当P≤0.10和I2≥50%时,应先分析导致异质性的原因,可用亚组分析进行合并统计量的计算,若经以上处理后,仍存在异质性,可采用随机效应模型进行分析。如因纳入研究的方法学质量不一而导致存在明显统计学异质性,可去除低质量研究进行敏感性分析。
2 结 果
2.1文献检索结果 初检出827篇文献,经剔除重复文献,阅读文献标题、摘要,并进一步阅读全文后,最终纳入3个RCT。其中预防性研究0个;治疗性研究3个,共8篇文献〔7~14〕。文献筛选流程见图1。纳入研究的基本特征见表1。
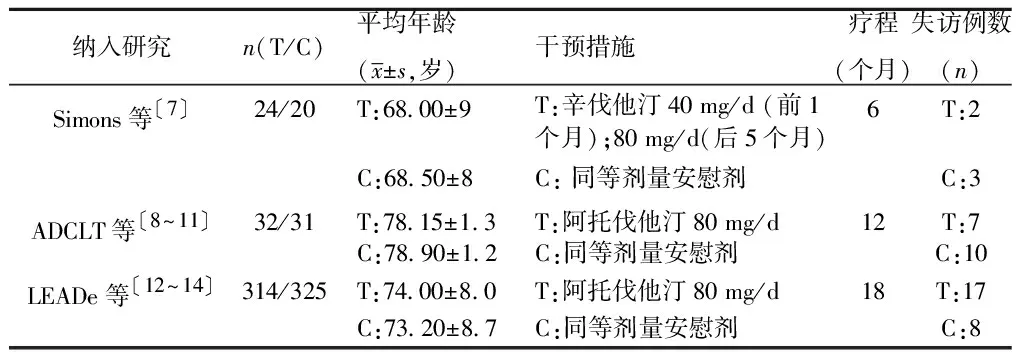
表1 纳入研究的基本特征
T:实验组;C:对照组

图1 文献筛选流程及结果
2.2纳入研究的文献质量评价 纳入的3个试验均提及随机分组及实验分配隐藏,其中2个试验说明了具体的随机分组方法(ADCLT 2005采用随机数字表法,Simons 2002应用计算机软件进行随机分化组)。3个试验都为双盲,故不存在选择性偏移和测量性偏移的可能性。3个实验都描述了失访人数及失访的具体原因,且提示无基金支持。故本系统评价纳入的文献具有较高的质量。
2.3Meta分析结果
2.3.1预防性研究 因没有符合纳入标准的文献,无法进行Meta分析。
2.3.2治疗性研究
2.3.2.1ADAS-Cog评分 ADCLT2005〔8~11〕和LEADe〔12~14〕治疗组药物均为阿托伐他汀80 mg/d,但疗程分别为6个月和18个月;Simons等〔7〕的治疗方案为:先用辛伐他汀40 mg/d治疗1个月,后5个月将辛伐他汀的剂量改为80 mg/d。不考虑药物类型及剂量的影响,将上述3个RCT 6个月ADAS-Cog评分进行Meta分析,结果显示他汀类药物组与对照组之间差异无统计学意义〔MD=-0.02,95%CI(-1.10,1.05),P=0.96〕。不考虑药物类型、治疗剂量及疗程的影响,将上述3个RCT的ADAS-Cog评分进行Meta分析,结果提示所纳入的研究存在同质性差异〔chi2=6.08,P=0.05,I2=67%〕,故采用随机效应模型进行分析,结果仍无统计学差异〔MD=1.09,95%CI(-1.77,-3.94),P=0.46〕。
为明确不同类型他汀类药物在改善ADAS-Cog评分方面的疗效是否存在差异,本研究进行了亚组分析。治疗疗程为6个月时,阿托伐他汀与辛伐他汀在改善ADAS-Cog评分方面差异无统计学意义〔MD=-0.22,95%CI(-1.12,0.67),P=0.62;MD=0.70,95%CI(-3.32,4.72),P=0.73〕;不考虑疗程的影响,上述两类药物之间的差异仍无统计学意义〔MD=-0.08,95%CI(-1.19,1.03),P=0.89;MD=0.70,95%CI(-3.32,4.72),P=0.73〕。值得注意的是,ADCLT 2005对携带APE4的参加者进行了亚组分析,结果显示经6个月的治疗后,阿托伐他汀能在一定程度上改善携带APE4 AD患者的ADAS-Cog评分,与对照组相比,差异具有统计学意义〔MD=-3.66,95%CI(-6.15,-1.17),P=0.004〕。
2.3.2.2MMSE评分 将3个RCT的数据进行Meta分析,结果显示经他汀类药物治疗后MMSE评分低于对照组,差异具有统计学意义〔MD=0.44,95%CI(0.02,0.87),P=0.04〕,但纳入的3个研究之间存在同质性差异〔chi2=6.19,P=0.05,I2=68%〕,故使用随机效应模型进行分析,结果无统计学差异〔MD=1.09,95%CI(-0.17,2.35),P=0.09〕。将3个RCT 6个月的MMSE评分进行Meta分析,结果表明治疗组与对照组之间差异无统计学意义〔MD=0.37,95%CI(-0.07,0.80),P=0.1〕。
不考虑疗程的影响,亚组分析结果提示,在改善MMSE评分方面,阿托伐他汀与安慰剂疗效相当〔MD=0.36,95%CI(-0.07,0.79),P=0.10〕,而辛伐他汀的疗效优于安慰剂〔MD=2.10,95%CI(0.16,4.04),P=0.03〕。为了解疗程对亚组分析结果是否有影响,我们对3个RCT 6个月的MMSE评分进行分析,结果仍表明阿托伐他汀组与安慰剂组的差异无统计学意义〔MD=0.27,95%CI(-0.17,0.72),P=0.22〕,而辛伐他汀组与安慰剂组的差异具有统计学意义〔MD=2.10,95%CI(0.16,4.04),P=0.03〕。
2.3.2.3不良反应 本研究纳入的3个RCT均给出了不良反应发生的具体情况,将3个研究进行同质性检验,结果提示所纳入的研究同质性较好〔χ2= 0.99,P=0.61,I2=0%〕,故采用固定效应模型进行Meta分析,结果显示,两组差异无统计学意义〔RR=3.31,95%CI(1.07,10.26),P=0.04〕,故可认为他汀类药物具有较高的安全性。
2.3.2.4生活质量 3个RCT中,只有LEADe 2010对该项目进行了描述,评价指标是照顾者负荷问卷及病人卫生资料利用率,但未报道原始数据。
3 讨 论
3.1疗效分析与临床意义 针对预防性研究,共检索出4个相关的RCT〔15~18〕,通过仔细阅读全文,本研究发现Sjogren等〔15〕、Hoglund等〔16〕的研究对象不符合纳入标准,而Muldoon等〔17〕、 Carlsson等〔18〕研究因原始数据不详,无法提取数据进行Meta分析。Muldoon等〔17〕研究结果显示经过为期6个月的治疗后,在改善高胆固醇血症患者认知功能方面,辛伐他汀的疗效优于安慰剂。Carlsson等〔18〕研究指出辛伐他汀不仅能降低参与者的血脂水平,同时还具备改善AD高危人群(携带APE4)的认知功能。但由于上述两个研究的原始数据不详,未能对结局指标进行Meta分析,对于他汀类药物是否可降低AD的发病率目前尚缺乏统计学依据。
针对治疗性研究,共有3个RCT(748例)符合本系统评价的纳入标准,其中只有1个RCT〔11〕研究表示,他汀类药物可以改善AD患者的认知功能并延缓病情的发展。本Meta分析结果显示:他汀类药物组与安慰剂组在ADAS-Cog评分方面疗效相当;在MMSE评分上,因纳入研究结果间存在同质性差异,采用随机效应模型分析后,两组之间的差异也无统计学意义。亚组分析结果显示:阿托伐他汀与安慰剂在ADAS-Cog、MMSE评分上差异无统计学意义,辛伐他汀与安慰剂在ADAS-Cog评分上也无统计学差异,但辛伐他汀组在改善MMSE评分上疗效优于安慰剂组。需要指出的是,ADCLT 2005针对特定的人群(携带APE4的AD患者)进行了队列研究,结果表明与安慰剂相比,阿托伐他汀可明显改善携带APE4的AD患者ADAS-Cog评分。上述Meta分析结果表明他汀类药物中的某一类型(辛伐他汀、阿托伐他汀)可能改善AD患者或某些特殊人群(携带APE4的AD患者)的认知功能,但因研究较少,样本量不够,该结论尚需进一步论证。关于不良反应,纳入的3个RCT经Meta分析结果显示,他汀类药物与安慰剂不良反应发生率之间的差异无统计学意义,表明他汀类药物具有较高的安全性。
3.2研究质量及局限性 采用Cochrane Handbook 5.1.0推荐的“偏倚风险评估”工具对纳入的RCT进行方法学质量评价。该评估工具对每一项目的评价均有明确的标准,减少了主观因素的干扰,保证了评估结果的可靠性。本系统评价纳入的3个RCT通过“偏倚风险评估”工具评价后均为高质量研究,除LEADe 2010未描述随机序列的产生及分配方案的隐藏方法外,余2个RCT经该工具评价后,6个条目的评估结果均为低度偏倚。但本系统评价纳入研究的RCT数目小,且样本量不足,使该系统评价的推广性受到一定限制。在改善MMSE评分上,他汀类药物的疗效优于安慰剂,但研究结果存在异质性,本研究对临床问题进行了分析,未找到异质性的原因,推测与参与者的种族、环境及临床措施的具体实施有关,因为纳入的RCT数量小,未能进一步分析,这影响了该系统评价的可靠性。针对纳入文献存在的不足,本研究认为需要指出的有:今后的RCT除了在设计、实施及报告等方面需更加的科学、严谨、客观外,疾病的病死率、患者的生活质量、药物的不良事件及疾病的经济学研究等指标也应被列入结局指标中。
通过对所纳入RCT的Meta分析,本研究认为:在防治AD的疗效方面,他汀类药物未能显示出明显的优势,但具有较高的安全性。本系统评价需特别指出的是:辛伐他汀在改善MMSE评分上疗效优于安慰剂,阿托伐他汀能在一定程度上改善携带APE4 AD患者的ADAS-Cog评分,但鉴于样本量过少,未能进一步研究。由于本系统评价纳入样本量及RCT数量有限,在药物干预方面,不同类型及剂量的他汀类药物研究较少;在结局指标方面,疾病的病死率、经济学研究及患者的生活质量等未被研究,因此,对他汀类药物防治AD的临床疗效尚需进一步开展严格设计的随机双盲对照试验,特别是大样本多中心的随机双盲对照试验来加以证明。
4 参考文献
1Ferri CP,Prince M,Brayne C,etal.Global prevalence of dementia:a Delphi consensus study〔J〕.Lancet.2005;366(9503):2112-7.
2Reiss AB,Voloshyna I.Regulation of cerebral cholesterol metabolism in Alzheimer disease〔J〕.J Investig Med,2012;60(3):576-82.
3Sparks DL,Kryscio RJ,Sabbagh MN,etal.Reduced risk of incident AD with elective statin use in a clinical trial cohort〔J〕.Curr Alzheimer Res,2008;5(4):416-21.
4Haag MD,Hofman A,Koudstaal PJ,etal.Statins are associated with a reduced risk of Alzheimer disease regardless of lipophilicity.The Rotterdam Study〔J〕.J Neurol Neurosurg Psychiatry,2009;80(1):13-7.
5Li G,Higdon R,Kukull WA,etal.Statin therapy and risk of dementia in the elderly:a community-based prospective cohort study〔J〕.Neurology,2004;63(9):1624-8.
6Arvanitakis Z,Schneider JA,Wilson RS,etal.Statins,incident Alzheimer disease,change in cognitive function,and neuropathology〔J〕.Neurology,2008;70(19 Pt 2):1795-802.
7Simons M,Schwarzler F,Lutjohann D,etal.Treatment with simvastatin in normocholesterolemic patients with Alzheimer's disease:a 26-week randomized,placebo-controlled,double-blind trial〔J〕.Ann Neurol,2002;52(3):346-50.
8Sparks DL,Connor DJ,Sabbagh MN,etal.Circulating cholesterol levels,apolipoprotein E genotype and dementia severity influence the benefit of atorvastatin treatment in Alzheimer's disease:results of the Alzheimer's Disease Cholesterol-Lowering Treatment(ADCLT)trial〔J〕.Acta Neurol Scand Suppl,2006;185(1):3-7.
9Sparks DL,Sabbagh M,Connor D,etal.Statin therapy in Alzheimer's disease〔J〕.Acta Neurol Scand Suppl,2006;185:78-86.
10Sparks DL,Sabbagh MN,Connor DJ,etal.Atorvastatin for the treatment of mild to moderate Alzheimer disease:preliminary results〔J〕.Arch Neurol,2005;62(5):753-7.
11Sparks DL,Sabbagh MN,Connor DJ,etal.Atorvastatin therapy lowers circulating cholesterol but not free radical activity in advance of identifiable clinical benefit in the treatment of mild-to-moderate AD〔J〕.Curr Alzheimer Res,2005;2(3):343-53.
12Feldman HH,Doody RS,Kivipelto M,etal.Randomized controlled trial of atorvastatin in mild to moderate Alzheimer disease:LEADe〔J〕.Neurology,2010;74(12):956-64.
13Jones RW,Kivipelto M,Feldman H,etal.The Atorvastatin/Donepezil in Alzheimer's Disease Study(LEADe):design and baseline characteristics〔J〕.Alzheimers Dement,2008;4(2):145-53.
14Feldman HH,Jones RW,Kivipelto M,etal.The LEADe Study:a randomized,controlled trial investigating the effect of atorvastatin on cognitive and global function in patients with mild-to-moderate Alzheimer’s disease receiving background therapy of donepezil〔J〕.Neurology,2008;71:153-6.
15Sjogren M,Gustafsson K,Syversen S,etal.Treatment with simvastatin in patients with Alzheimer's disease lowers both alpha-and beta-cleaved amyloid precursor protein〔J〕.Dement Geriatr Cogn Disord,2003;16(1):25-30.
16Hoglund K,Thelen KM,Syversen S,etal.The effect of simvastatin treatment on the amyloid precursor protein and brain cholesterol metabolism in patients with Alzheimer's disease〔J〕.Dement Geriatr Cogn Disord,2005;19(5-6):256-65.
17Muldoon MF,Ryan CM,Sereika SM,etal.Randomized trial of the effects of simvastatin on cognitive functioning in hypercholesterolemic adults〔J〕.Am J Med,2004;117(11):823-9.
18Carlsson CM,Gleason CE,Hess TM,etal.Effects of simvastatin on cerebrospinal fluid biomarkers and cognition in middle-aged adults at risk for Alzheimer's disease〔J〕.J Alzheimers Dis,2008;13(2):187-97.
