包裹125 I标记多肽的二氧化硅纳米颗粒的动物实验研究
2014-09-13王风秀王加芬陆小伟
王风秀,王加芬,陆小伟
(1.滨州市人民医院药学部,山东滨州256600;2.滨州市人民医院检验科,山东滨州256600;3.南京医科大学医学科学部,江苏南京210029)
包裹125I标记多肽的二氧化硅纳米颗粒的动物实验研究
王风秀1,王加芬2,陆小伟3
(1.滨州市人民医院药学部,山东滨州256600;2.滨州市人民医院检验科,山东滨州256600;3.南京医科大学医学科学部,江苏南京210029)
目的探讨纳米二氧化硅是否可作为生物大分子药物口服载体。方法研究钙离子的量对二氧化硅纳米颗粒形态的影响、不同钙离子存在下二氧化硅纳米颗粒对蛋白或多肽的包裹率、蛋白或多肽从二氧化硅纳米颗粒中释放情况、二氧化硅包裹蛋白酶解情况、以及二氧化硅纳米颗粒包裹125I标记多肽在小鼠体内释放情况。结果实验表明合成的二氧化硅纳米颗粒包裹多肽在小白鼠体内可以顺利通过胃酸到达小肠,有作为生物活性大分子口服药物载体的潜力。结论蛋白或多肽比较容易在碱性条件下释放,在pH 2的酸性条件下释放极少(胃酸的pH值),制备的二氧化硅纳米颗粒有作为口服药物载体的潜力。
纳米二氧化硅;药物口服系统;蛋白质和多肽
包裹良好、性能稳定且在酸性条件下不易释放的二氧化硅纳米颗粒,其良好的性能可能作为口服药物载体[1-3]。为了研究其是否能用作口服药物载体,将进一步研究包裹多肽的二氧化硅纳米颗粒在小鼠体内的分布情况。现有的常规分析手段很难检测生物体内的二氧化硅纳米颗粒[4],而放射性示踪技术却可以简单有效地解决这个问题。目前,已经有多种放射性同位素被用于研究材料的生物分布,包括14C、111In、86Y、64Cu、99mTc和125I等,这些材料均可以用来标记化合物作为一种示踪剂或分析试剂,可以用来测定机体内微量物质的浓度,是具有很高灵敏度的示踪与分析方法。参照放射性同位素标记蛋白的方法,选用具有适中半衰期(60.2天)的125I来标记多肽[5]。
1 材料与方法
1.1 试剂 FITC-GDDYHHHHHH>95%50mg上海科肽生物科技有限公司;Na125I(无载体)/原子高科股份有限公司;偏正亚硫酸钠AR 500 g国药集团化学试剂有限公司;丙酮AR 500mL国药集团化学试剂有限公司;Iodogen/苏州大学医学院核医学实验室提供;三氯甲烷AR国药集团化学试剂有限公司;G15填料100 g Sigma-Aldrich;纸薄层色谱/兴万电子厂;环己烷AR国药集团化学试剂有限公司;正己醇AR国药集团化学试剂有限公司;Triton X-100 GR Sigma-Aldrich;氯化钙AR 500 g国药集团化学试剂有限公司;TEOSGR Sigma-Aldrich;氨水GR国药集团化学试剂有限公司;丙酮AR国药集团化学试剂有限公司;乙醇AR国药集团化学试剂有限公司;氯胺-T>99%100 g北京中诺泰安科技有限公司。
1.2 实验方法 本文实验部分主要是做了以下实验:氯胺-T法125I标记多肽;Iodogen法125I标记多肽;包裹125I标记多肽的二氧化硅纳米颗粒实验;包裹125I与多肽的简单混合液实验;包裹125I标记多肽的二氧化硅纳米颗粒体外释放实验;包裹125I标记多肽的二氧化硅纳米颗粒在小鼠体内的分布实验。
2 结果
2.1 FITC-GDDYHHHHHH的125I标记 FITC-GDDYHHHHHH峰位置的确定:为了大致确定FITC-GDDYHHHHHH淋洗的出峰位置,在相同的淋洗条件下,用G15柱分离FITC-GDDYHHHHHH。样品一加入凝胶柱便开始收集淋洗液。将每管的液体分别用紫外分光光度计测其在495 nm处的吸收。由图知道进样后,淋洗7mL左右FITC-GDDYHHHHHH开始出峰。

图1 FITC-GDDYHHHHHH的淋洗曲线Fig.1 The elution curve of FITC-GDDYHHHHHH solution
125I标记FITC-GDDYHHHHHH的制备:图2和图3给出了反应后混合溶液的淋洗曲线。其中图2为Iodogen法标记多肽的淋洗曲线,图3为氯胺-T法标记多肽的淋洗曲线。图中的纵坐标为样品的相对计数率(counts permin,cpm),横坐标为淋出液样品体积。从图2中只得到一个峰;从图3中能看到2个分得很开的峰。根据流出体积与空白试验比较确定第一个峰是FITC-GDDYHHHHHH出峰的位置,是标记产物;第二个峰是小分子峰,主要是游离的碘离子。

图2 Iodogen法125 I标记FITC-GDDYHHHHHH反应混合液的淋洗曲线Fig.2 Elution curve on a Sephadex G-15 column of a reaction mixture solution of FITC-GDDYHHHHHH and Na125 Ioxidized by iodogen
为了确定第一个峰是经过反应而得到的稳定的125I-FITCGDDYHHHHHH,而不是125I靠吸附或者其他非共价的作用结合到FITC-GDDYHHHHHH上,将Na125I溶液和FITCGDDYHHHHHH溶液简单混合,放置5~20min后用与标记反应相同的淋洗条件淋洗,得到图4。结果发现,所有的放射性都出现在后面的小分子峰位置,而前面FITC-GDDYHHHHHH应该出现的位置没有测到放射性。
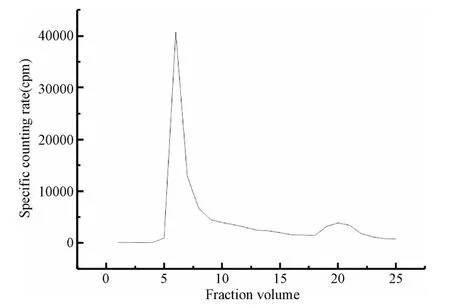
图3 氯胺-T法125 I标记FITC-GDDYHHHHHH反应混合液的淋洗曲线Fig.3 Elution curve on a Sephadex G-15 column of a reaction mixture solution of FITC-GDDYHHHHHH and Na125 Ioxidized by chloramine-T

图4 Na125 I和FITC-GDDYHHHHHH的简单混合的淋洗曲线Fig.4 Elution curve on a Sephadex G-15 column of a simplemixture solution of FITC-GDDYHHHHHH and Na125 I
125I-FITC-GDDYHHHHHH的放化纯度和稳定性检测:将经淋洗纯化后的125I-FITC-GDDYHHHHHHH溶液放置3天,用纸薄层色谱检测标记物的放化纯度和稳定性。用丙酮/水的体积比为10:1的溶液为展开剂,室温下展开,取出晾干,将薄层色版平均分成7等分的纸条,依次用γ计数器测其放射性。γ计数器的本底为50 cpm,放置3天后的稳定性为(678.41-50)/(678.41 +73+62+83.5+85.07+53-50·7)=97%。由此可见,标记化合物相当稳定,没有发生明显的125I脱落。
2.2 包裹125I标记多肽的二氧化硅纳米颗粒的制备 将FITC-GDDYHHHHHH与无载体的Na125I简单混合后,用同样的包裹条件反应。反应结束后,同样将丙酮、乙醇、pH 2 PBS清洗后的上清液进行放射性检测,结果如表1,可见经过依次清洗后,被二氧化硅纳米颗粒包裹的125I放射性小于0.36%,因此可以得出二氧化硅纳米颗粒对无载体Na125I的吸附影响很小,可以忽略不计。

表1 纳米颗粒溶液各部分放射情况Tab.1 Nanoparticle solution of each part of the radiological situation
125I-FITC-GDDYHHHHHH稳定性检测:将经过丙酮,乙醇,pH 2缓冲液清洗后的125I-FITC-GDDYHHHHHH样品用纸薄层色谱检测标记物的放化纯度和稳定性。用丙酮/水的体积比为10:1的溶液为展开剂,室温下展开,取出晾干,将薄层色版平均分成六等分的纸条,依次用γ计数器测其放射性。γ计数器的本底为50 cpm,放置3天后的稳定性为:(773.78-20)/(773.78+ 40.88+19.37+42.4+24.36+11.92-20.6)=95%。
125I-FITC-GDDYHHHHHH样品浓度的测定:将125I-FITCGDDYHHHHHH样品用20mL PBS pH 7.5溶解,取0.5mL再加入0.5mL PBS溶液,用紫外可见分光光度计测量其紫外吸收,得到320 nm时A=1.02288,由此知0.5 mL的二氧化硅纳米颗粒溶液中含有0.360mg二氧化硅,则20mL体积中共有14.4mg二氧化硅纳米颗粒。
2.3 包裹125I标记多肽的二氧化硅纳米颗粒在小鼠体内的分布 图5中给出的是二氧化硅纳米颗粒包裹125I标记的FITCGDDYHHHHHH在小白鼠体内的释放情况,由图可以看出,放射性的125I大部分分布在小肠和大肠中,少部分进入血液和其它组织。为了检测自由的125I在小白鼠体内的分布情况,将无载体的Na125I经口服灌胃进入小白鼠体内,结果如图6所示,大部分的125I都经膀胱由尿液排出体外,只有极少部分存在其它各组织、器官中。比较图5与6,看出,包裹125I标记的FITC-GDDYHHHHHH实验中,甲状腺中没有检测到放射性,同时血液中放射性含量也很低。

图5 125 I-FITC-GDDYHHHHHH在小白鼠体内分布Fig.5 The biodistribution of 125 I-FITC-GDDYHHHHHH in mouse

图6 Na125 I在小白鼠体内分布比较Fig.6 The biodistribution of Na125 I in mouse
3 讨论
125I的标记方法:125I的标记方法有很多种,但应用较多的是氯胺-T法,Iodegen法,乳过氧化物酶法,固相氧化法,连接标记法等[6-8]。采用用于标记蛋白较多的两种方法:氯胺-T法和Iodegen法相比较来得到最简单有效的标记方法[9-10]。氯胺-T法具有操作简单、标记效率高、重复性好、试剂易得等优点,因而迅速被广泛使用,如今仍然是实验室最常用的碘化方法之一[11-12]。氯胺-T(Chloramine-T)即N-氯代对甲苯磺酰胺钠盐,是一种比较温和的氧化剂,在水溶液中水解产生次氯酸,后者使碘离子氧化成活泼的碘分子,然后碘分子取代被标记物上的可被碘原子结合的基团,从而生成碘标记化合物[13]。碘与被结合基团之间以共价键的形式结合。此反应受多种因素影响:氯胺-T的用量;酸碱度,最佳pH值一般在7~8之间;反应体积,50~300μL比较好;反应温度和时间,室温下反应几分钟即可,对于非活性被标记物,时间可长些。
Iodogen是一种与氯胺-T同属氯酰胺类化合物的新型碘化剂,难溶于水,故可溶于有机溶剂,涂于管底,并使之干燥。用Iogogen为氧化剂,对蛋白质和多肽抗原进行碘化标记,把125I直接引进分子中的酪氨酸残基上。标记过程中被标记样品与Iogogen混合,标记后取出样品即停止反应,不使用任何还原剂[14]。同样反应受多种因素影响:碘化时间,碘化反应时间7 min时标记率达最高,10 min时略有减少;酸碱度,pH为6.0~8.5时,标记率最高;125I与被标记物的分子之比,碘化时,当125I与多肽分子之比为1~1.2时标记率较佳;Iodogen与蛋白质的比率是标记率的函数,最大的标记率是1克分子的Iodogen与8克分子或再多量之比[15]。
由本文实验中可以看出Iodogen法不能成功的标记多肽FITC-GDDYHHHHHH而氯胺-T法比较适合标记此条多肽且标记率很高。同时,在得到的标记化合物中,125I与FITCGDDYHHHHHH间的作用并非是吸附或其它弱的非共价相互作用,而应该是共价化学反应。通过比较Iodogen法和氯胺-T法碘标FITC-GDDYHHHHHH的比较,采用了氯胺-T法制备了FITCGDDYHHHHHH的125I标记物并证明碘原子通过共价键与多肽结合。实验结果表明标记物的放化纯度高,稳定性好,适用于动物实验。在动物实验中多肽在胃液中释放量很少,和体外实验结果一致。同时说明纳米二氧化硅包裹多肽能够保护多肽免于胃酸的破坏。但血液中放射量低也说明在小肠中的释放吸收不好,这也是蛋白质和多肽的共同问题,需要通过进一步添加吸收促进剂来改进。
本研究证实钙离子在一定浓度范围内可以明显提高纳米二氧化硅包裹多肽的能力,当超过一定浓度范围钙离子则会破坏反应的微乳体系。蛋白或多肽比较容易在碱性条件下释放,在pH 2的酸性条件下释放极少(这也是胃酸的pH大小),制备的二氧化硅纳米颗粒有作为口服药物载体的潜力。
[1] 王浩,候惠民.多肽与蛋白质类药物给药系统的研究现状.中国医药工业杂志,1994,25(9),421-426.
[2]吴梧桐.下一个10年的生物技术与生物制药.中国药学杂志,1999,34(01),3-3.
[3] Edman P,Björk E.Nasal delivery of peptide drugs.Adv Drug Deliv Rev,1992,8(12),165-177.
[4] 戴洁,吴克和.蛋白质及多肽类药物鼻腔给药的研究.药物进展,1992,16(8),202-204.
[5]Ho N FH,Barsuhn C L,Burton P S et al.Mechanistic insights to buccal delivery of proteinaceous substances.Adv Drug Deliv Rev,1992,8(12),197-203.
[6]De Boer A G,Van Hoogdalem E J,Breimer D D.Improvementof drug absorption through enhancers.Eur JDrug Metab Pharmacokinet,1990,15(9),155-157.
[7]Ping Q N.The development of new dosage forms of protein drugs.Food and drug,2005,7(11),1-5.
[8] 于彬.蛋白质药物:新世纪的朝阳产业.中国新技术新产品,2008,4(8),54-56.
[9] 马利敏,张强,李玉珍.载多肽和蛋白质药物的纳米粒给药系统的研究进展.中国药学杂志,2000,7(1),437-440.
[10]Alleman E,Guvny R,Doelker E.Drug-load nanoparticles preparation methods and drug targeting issues.Eur J Pharm Biopharm,1993,39 (12),173-191.
[11]Sayani A P,Chien Y W.Systemic delivery of peptides and proteins across absorptivemucosae.Crit Rev Ther Drug Carrier Syst,1996,13 (7),85-184.
[12]Pappo P,Ermak T H.Uptake and translocation of fluorescent latex particles by rabbit Peyer's patch follicle epithelium:A quantitative model for M cell uptake.Clin Exp Immunol,1989,76(18),144-148.
[13]Van der Lubben IM,Konings F A,Borchard G et al.In vivo uptake of chitosanmicroparticles bymurine Peyerˋs patches:Visualization studies using confocoal laser scanning microscopy and immunohistochemistry.J Drug Target,2001,9(12),39-47.
[14]Ermak T H,Dougherty E P,Bhagat H R et al.Uptake and transport of copolymer biodegradable microspheres by rabbit Peyerˋs patch M cells.Cell Tissue Res,1995,279(10),433-436.
[15]Stubbe B,Martis B,Moonter G V.In vitro evaluation of azo containing polyscaccharide gels for colon delivery.JControlled Release,2001,75 (12),103-114.
(编校:谭玲)
Animal experiment study of silica nanoparticles labeled peptides w ith125I
WANG Feng-xiu1,WANG Jia-fen2,LU Xiao-wei3
(1.Department of Pharmacy,Binzhou People's Hospital,Binzhou 256600,China;2.Department of Laboratory,Binzhou People's Hospital,Binzhou 256600,China;3.Department of Medical Sciences,Nanjing Medical University,Nanjing 210029,China)
ObjectiveTo study whether the silica nanoparticles can be used as a biomacromolecular carrier of oral drugs.MethodsStudyed the influence of the amount of calcium ions on nano silica nanoparticlesmorphology,the encapsulation rate of silica nanoparticles on proteins or peptides in the presence of different calcium ions,the situation of proteins or peptides released from silica nanoparticles,enzymolysis of protein packaged by silica,silica nanoparticles labeled peptideswith125I released inmice.ResultsExperiments showed that the synthetic silica nanoparticles packaged with peptides could smoothly reach the small intestine through the gastric acid in mice,it had potential to be biomacromolecular carrier of oral drug.ConclusionProteins or peptides is easy to release in alkaline condition,but release few in acidic condition of pH2(PH of gastric acid).The silica nanoparticles prepared have the potential to be oral drug carrier.
silica nanoparticles;oral drug system;protein and peptide
R318.08
A
1005-1678(2014)07-0066-04
国家自然科学基金(81100858)
王风秀,女,本科,副主任药师,研究方向:药学方面,邮箱:qch1821460075@163.com。
