IVF/ICSI术后用黄体酮阴道缓释凝胶作黄体支持的临床情况分析
2014-09-04许丽华车小群宋丽君陈碧庞小艳
许丽华 车小群 宋丽君 邹 琳 陈碧 庞小艳
IVF/ICSI术后用黄体酮阴道缓释凝胶作黄体支持的临床情况分析
许丽华 车小群 宋丽君 邹 琳 陈碧 庞小艳
目的 探讨阴道放置黄体酮阴道缓释凝胶(商品名:雪诺同8%)在体外受精(IVF)和卵细胞浆内单精子注射(ICSI)术后黄体支持的临床疗效。方法 回顾性分析了进行体外受精-胚胎移植(IVF-ET) 138个新鲜周期的患者临床资料, 按不同黄体支持方法分两组:黄体酮肌内注射组(A组)60例,阴道放置雪诺同8% (B组)78例。观察两组的着床率、临床妊娠率、早期流产率以及药物不良反应发生率。结果 138个新鲜周期中, 术后随访期间妊娠共81例, 总临床妊娠率为58.7%(81/138), B组的临床妊娠率高于A组的临床妊娠率, 差异有统计学意义(P<0.05), B组的不良反应率明显低于A组的不良反应率, 差异有统计学意义(P<0.05)。B组的着床率、早期流产率与A组比较, 差异均无统计学意义(P>0.05)。结论 阴道放置雪诺酮8%在IVF-ET术后进行黄体支持是有效的黄体支持方案, 可提高临床妊娠率,且使用简便, 可避免患者由于注射黄体酮产生的不良反应。
体外受精-胚胎移植(IVF-ET);雪诺同8%;黄体支持
在体外受精-胚胎移植(in vitro fertilization-embryo transfer, IVF-ET)辅助生育技术中应用控制性超促排卵会影响黄体期激素水平, 导致黄体功能不全及妊娠率下降, 黄体支持是成功妊娠的关键环节之一。在IVF-ET治疗中, 多数中心还是采用以GnRHa长方案降调节联合Gn行控制性卵巢刺激(COS)为主流, 对于长方案调节后的最佳黄体支持方案, 目前尚无定论。黄体酮是多数生殖中心黄体支持的首选药物。但目前的黄体酮制剂存在疗效差、不良反应多、使用不便等多种问题。本文分析了广东医学院附属医院生殖中心IVF-ET 138个新鲜周期的患者临床资料, 分析其着床率、临床妊娠率、早期流产率以及药物不良反应发生率, 评价雪诺同8%(雪诺酮)在IVF-ET术后黄体支持的临床疗效, 以期寻找更合适的黄体支持的方案。
1 资料与方法
1.1 一般资料 选择2013年1月~ 2014年3月在广东医学院附属医院生殖中心进行IVF-ET的患者为研究对象, 共138个新鲜周期, 进行回顾性分析。患者年龄22~39岁, 平均30岁, 不孕时间1~16年, 平均4年。研究对象均符合以下条件:卵巢储备功能较好;采用标准黄体中期降调节方案,进行COS;首次接受常规IVF或单精子卵胞浆内注射(ICSI)助孕治疗。
1.2 方法
1.2.1 降调节 COS的前1周期月经第8~10天开始B超监测卵泡发育, 直至确定排卵日;或于月经第5天开始口服妈富隆, 1片/d。排卵后5~7 d或服妈富隆15 d, B超检查若无直径≥10 mm的残余卵泡或黄素化卵泡或其他生理性囊肿,用长效GnRH-a 1/3 ~1/2支, 5 d后B超检查卵巢有无囊肿, 若有囊肿则行囊肿穿刺, 或用短效GnRH-a 0.05~0.1 mg/d (至HCG日)。月经来潮第2天起测血清激素及B超监测降调节情况。用GnRHa约14 d后, 检查垂体降调节是否达到以下标准:卵泡直径≤5 mm左右;子宫内膜≤5 mm;血E2<50 ng/L、FSH<5 IU/L、LH<5 IU/L。若未达上述标准, 继续降调。
1.2.2 Gn启动 垂体达到降调节标准后(通常为降调14 d后)开始给予Gn。
Gn启动剂量:根据患者的年龄、基础FSH值、ACF数目、BMI以及既往Gn使用情况决定Gn启动剂量。常规启动剂量为:150 ~225 IU/d。用Gn 4 ~5 d, 阴道B超监测卵泡发育并测血E2、LH、FSH水平, 根据检测结果个体化调整Gn用量。此后, 隔1~2 d B超监测卵泡发育。当主导卵泡≥14 mm后每日B超监测1次, 同时测血E2、LH、P水平, 作为调整Gn剂量及注射HCG时间的重要指标。
1.2.3 HCG的使用时机 至少1个卵泡直径达19 mm时,或2个卵泡直径达18 mm时, 或3个卵泡直径达17 mm, 血E2达到平均每个优势卵泡(≥16 mm)250~300 ng/L时, 或>16 mm的卵泡数达60%以上时当晚注射HCG 5000~10000 IU,注射后34~36 h取卵。
1.2.4 取卵当天加精或单精子卵泡浆内注射。移植时间在受精后第3天进行卵裂期胚胎移植。
1.2.5 黄体支持 取卵后根据患者意愿应用黄体支持药物, A组予黄体酮注射液60~80 mg/d肌内注射, 从取卵日起共17 d。B组使用雪诺同90 mg/d, 从取卵日起共17 d。两组间年龄、不孕年限、原发不孕比例、基础性激素、Gn用量、获卵数、优胚率、胚胎移植数等差异均无统计学意义。
1.2.6 妊娠的确立 胚胎移植后14 d查尿HCG / 血β-HCG,确定是否妊娠。如阴性则停用黄体支持等待月经来潮, 如阳性继续黄体支持至妊娠10~12周, 雪诺同药渣大多能自行排出, 个别患者需每2周回院清除药渣。妊娠者于移植术后28 d B超检查, 见妊娠囊为临床妊娠, 否则为生化妊娠。还应当注意妊娠囊的数目及有无宫外孕, 特别要注意宫内外同时妊娠的情况。
1.3 统计学方法 以简明统计软件10.32进行统计学处理。计量资料用均数±标准差(s)表示, 采用成组t检验, 如方差不齐则用t’检验。计数资料采用两样本率比较(四格表),采用χ2检验。P<0.05表示差异有统计学意义。
2 结果
2.1 两组患者一般临床资料比较 A组和B组患者年龄、不孕年限、原发不孕比例、基础性激素、HCG日性激素、Gn用量及天数等比较, 差异无统计学意义(P>0.05)。见表1。
2.2 两组不同黄体支持方法的实验室及临床指标比较 138个新鲜周期中, 术后随访期间妊娠共81例, 总临床妊娠率为58.7%(81/138)。B组的获卵数、MⅡ卵数、优胚率、胚胎移植数与A组相比, 差异无统计学意义(P>0.05)。B组的临床妊娠率高于A组的临床妊娠率, 差异有统计学意义(P<0.05), B组的着床率、早期流产率与A组比较, 差异均无统计学意义(P>0.05)。见表2。
2.3 药物不良反应 主要指注射局部红肿硬结炎性反应及变态反应, 甚至出现人工性脂膜炎。A组患者有11.7%(7/60)臀部出现黄体酮注射局部红肿、硬结、压痛, 经局部治疗后好转。B组所有患者均未出现该药物不良反应。B组的不良反应率明显低于A组的不良反应率, 差异有统计学意义(P<0.05)。见表2。
3 讨论
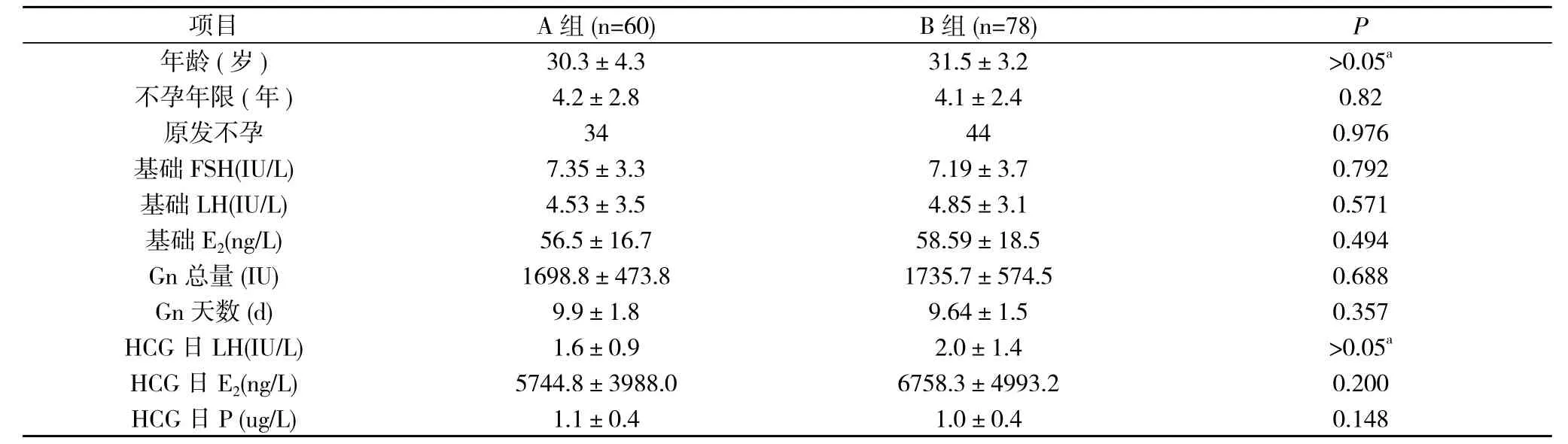
表1 两组患者一般临床资料比较
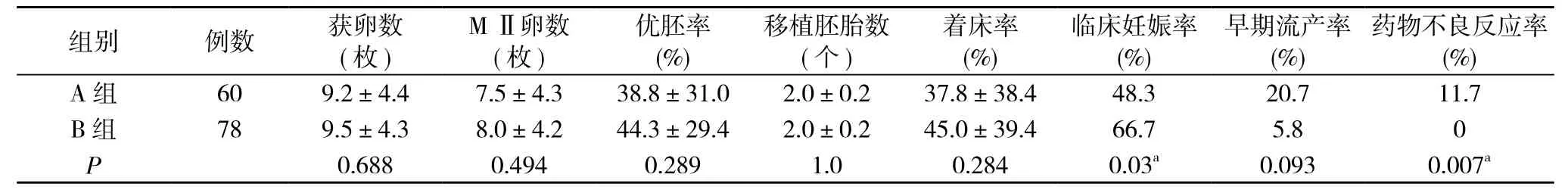
表2 两组患者的实验室及临床指标比较
自然妊娠的妇女由于有排卵后的黄体形成, 血液中的黄体酮水平于排卵4 d后上升到一定水平, 并持续1周。胚胎着床后HCG对妊娠黄体的刺激使黄体酮分泌增加, 血液中的黄体酮水平足以支持胚胎的发育。但在辅助生育技术IVF-ET促排卵过程中, 大多使用降调节即促性腺激素释放激素类似物(GnRHa)降调节, 停药后垂体分泌促性腺激素的能力未能迅速从降调节中恢复, 取卵时间通常还在垂体降调节的有效时间内, 内源性的LH还处于低水平。另外, 多卵泡发育导致的高雌激素水平, 及取卵时使颗粒黄体细胞减少,导致黄体功能不足, 致妊娠率下降。Dor J等[1]在对接受长方案治疗妇女的颗粒细胞进行体外研究时, 发现这些颗粒细胞对HCG刺激的反应下降, 表现为孕酮产生量的减少, 可能是取卵术中卵母细胞卵丘复合物颗粒细胞的损失, 抽出将来成为大黄体细胞的颗粒细胞, 卵巢大黄体细胞不足引起的,所以ET后有必要进行黄体支持。Cheng CK等[2]研究认为GnRHa抑制人颗粒细胞孕激素的产生, GnRHa可能降低颗粒细胞对HCG的反应。黄体功能不全与孕激素缺乏密切相关,辅助生育技术是导致黄体功能不全的重要原因, ART周期黄体支持能有效提高妊娠率。所以黄体支持已成为垂体降调节超促排卵之后的常规步骤之一。
目前黄体支持的方案及最小有效剂量无统一标准, 很多中心采用较大剂量(80 mg/d或100 md/d)预防黄体功能不足,大剂量的黄体酮肌内注射不易吸收, 长期注射易造成注射部位肿痛、炎性反应及变态反应等。因此有必要进行合理的个体化黄体支持, 探索应用黄体酮的最小剂量。目前的黄体酮制剂主要有注射液、口服片剂或胶囊、阴道置胶囊、阴道置凝胶等。口服黄体酮制剂使用方便, 无痛苦, 但与其他口服药物一样, 存在肝脏首过效应, 黄体酮被大量代谢, 血药浓度不稳定, 生物利用率降低, 疗效不确切, 目前多采用黄体酮口服制剂与黄体酮针剂联合应用[3]。由于黄体酮注射液可以达到较高的血药浓度, 而且价格便宜, 目前的黄体支持大多使用黄体酮注射液, 剂量20 ~100 mg/d不等, 针剂能提高黄体期血清孕酮浓度, 改善黄体功能, 提高胚胎种植率和妊娠率, 改善IVF结局, 疗效较为肯定。但肌内注射黄体酮要到医院进行, 长期用药会给患者带来不便, 存在不良反应多等多种问题。据资料统计, 肌内注射黄体酮吸收最好, 但黄体酮为油剂, 有报道可以引起局部严重的变态反应[4]。患者在注射部位红肿, 出现硬结, 且注射时疼痛, 每天注射不方便, 给有些患者带来一定的痛苦和麻烦。甚至出现人工性脂膜炎[5]。药物性脂膜炎的形成机制:黄体酮以油剂为溶媒, 刺激脂肪层炎性反应。同一部位反复针刺物理作用也诱发脂膜炎。临床表现:局部红肿热痛, 瘙痒伴触痛明显, 质硬,易扩散至股外侧, 腰腹等非注射部位。
Zarutskie PW 等[6]Meta分析显示阴道给黄体酮与肌内注射黄体酮进行黄体支持, 临床妊娠率未见明显差别, 流产率无明显差别。雪诺酮, 也称黄体酮阴道缓释凝胶是微粒化黄体酮颗粒包裹于交联聚合体(聚卡波非)中, 聚卡波非通过氢键结合在阴道上皮细胞表面, 缓释给药, 每日只需用药1次, 疗效持久平稳。国外学者通过体外模型实验证实了雪诺酮的子宫首过效应, 并显示了黄体酮浓度在子宫内膜呈稳定性变化[7]。研究也证实了雪诺同与阴道胶囊相比给药更简单、更方便、麻烦少, 患者更愿意使用[8]。龚斐等[9]研究认为予黄体酮阴道缓释凝胶进行黄体支持, 无论在长方案还是超长方案中, 着床率、早期流产率优于安琪坦组, 超长方案中黄体酮阴道缓释凝胶的临床妊娠率也高于安琪坦组。迟洪滨等[10]报告了黄体酮阴道缓释凝胶在辅助生殖技术中作为黄体支持具有满意的疗效和安全性, 相比于传统给药方式, 患者更愿接受黄体酮凝胶阴道给药。总体满意度达到89.7%。候晓红等[11]报告了阴道予黄体酮阴道缓释凝胶和肌内注射黄体酮针剂两种黄体支持方法对IVF-ET术后及冻融胚胎移植中效果相近, 黄体酮阴道缓释凝胶更具有使用方便的优势。Silverberg KM等[12]研究认为IVF-ET术后予雪诺酮8%进行黄体支持与肌内注射黄体酮相比, 妊娠率更高。
本研究中, B组使用雪诺酮进行黄体支持与A组使用黄体酮进行黄体支持后的临床情况比较如下, B组着床率(45±39.4)%比A组着床率(37.8±38.4)%高, 但差异无统计学意义(P>0.05);B组的临床妊娠率(66.7%)比A组的临床妊娠率(48.3%)高, 差异有统计学意义(P<0.05);B组的早期流产率(5.8%)比A组的早期流产率(20.7%)低, 但差异无统计学意义。B组与A组药物不良反应方面比较, B组没有发生注射部位红肿, 硬结, 疼痛及人工性脂膜炎等不良反应,且患者自行用药, 使用简便, 避免一定的痛苦和麻烦, 使黄体支持过程较舒适。可见阴道放置雪诺同进行黄体支持是有效的黄体支持方案, 在一定程度上可避免患者由于注射黄体酮产生的不良反应。雪诺酮可以镇静子宫, 有效降低宫缩频率, 从而起到松驰子宫平滑肌的作用, 可以有效降低ET时宫缩频率, 及利用子宫首过效应, 保证子宫局部有效的黄体支持, 从而提高妊娠率。但雪诺酮所使用的费用较肌注黄体酮高, 如为避免肌内注射引起的不良反应, 不考虑费用问题,可以提倡使用雪诺同进行黄体支持。由于回顾性分析的周期数较少, 还有待于扩大样本量进一步研究。
[1] Dor J, Bider D, Shulman A, et al.Effects of gonadotrophin-releasing hormone agonists on human ovarian steroid secretion in vivo and in vitro-Results of a prospective, randomized in-vitro fertilization study.Human Reprod, 2000, l5(6):1225-1230.
[2] Cheng CK, Leung PC.Molecular biology of gonadotropin-releasing hormone (GnRH)-I, GnRH-II, and their receptors in humans.Endocr Rev, 2005, 26(2):283-306.
[3] 张韶珍, 吴青, 冯云.不同药物体外受精一胚胎移植的黄体支持比较.同济大学学报(医学版), 2011, 32(1):61-64.
[4] Tavaniotou A, Smitz J, Bourgain C, et al.Comparison between different routes of progesterone administration as luteal phase support in infertility treatments.Hum Reprod Update, 2000, 6(2):139-148.
[5] 孙青苗, 金彦, 陈捷, 等.肌内注射黄体酮致局部不良反应相关因素分析.中国药物应用与监测, 2009, 6(5):300-302.
[6] Zarutskie PW, Philips JA.A meta-analysis of the route of administration of luteal phase support in assisted reproductive technology: vaginal versus intramuscular progesterone.Fertil Steril, 2009 , 92(1):163-169.
[7] Bulletti C, de Z iegler D, Flamigni C, et al.T argeted drug delivery in gynaecology: the first uterine pass effect.Hum Reprod, 1997, 12(5):1073-1079.
[8] Simunic V, Tomic V, Tomic J, et al.Com parative study of the efficacy and tolerability of two vaginal progesterone formulations, Crinone 8% gel and Utrogestan capsules, used for luteal support.Fertil Steril, 2007, 87(1):83-87.
[9] 龚斐, 蔡素芬, 卢光瑗.两种阴道给药黄体支持药物在IVFET/ICSI后用药的比较研究.实用妇产科杂志, 2012, 28(3):199-201.
[10] 迟洪滨, 周灿权, 王树玉, 等.黄体酮阴道缓释凝胶在IVF/ ICSI周期中作为黄体支持的初步应用.实用妇产科杂志, 2012, 28(11):973-976.
[11] 侯晓红, 黄永刚, 张慧娜, 等.评估两种黄体支持方法在IVF/ ICSI新鲜及冻融胚胎激素替代周期妊娠周期结局的对比研究.实用妇产科杂志, 2013, 29(2):152-154.
[12] Silverberg KM, Vaughn TC, Hansard LJ, et al.Vaginal (Crinone 8%) gel vs intramuscular progesterone in oil for luteal phase support in in vitro fertilization: a large prospective trial.Fertil Steril, 2012, 97(2):344-348.
Analysis of clinical information of progesterone sustained-released vaginal gel as luteal phase support in in-vitro fertilization and intracytoplamsic sperm injection cycles
XU Li-hua, CHE Xiao-qun, SONG Li-jun, et al. Center of Reproductive Medicine, Affiliated Hospital of Guangdong Medical College, Zhanjiang 524001, China
Objective To investigate the therapeutic effect of progesterone sustained-rel eased vaginal gel( Crinone8%) as luteal phase support in in-vitro fertilization(IVF) and intracytoplamsic sperm injection( ICSI) cycles.Methods Clinical data of 138 cycles were analyzed retrospectively.They were divided into two groups according different luteal support randomly.Group A:60 cases, with progesterone as luteal support.Group B:78 cases, with Crinone 8% Gel as luteal support.Implantation rate, clinical pregnancy rate, miscarriage rate and adverse drug reaction rate were observed.Results All of the 138 cases, 81 became pregnant within the follow up.The total clinical pregnancy rates were 58.7%(81/138).The pregnancy rates of group B were significantly higher than group A.T he adverse drug reaction rate of group B was lower than gr oup A, its’differences had statistic significance(P<0.05).There were no statistical differences between the 2 groups in implantation rate and miscarriage rate(P>0.05).Conclusion It is an effective program with vaginal administration of Crinone 8% gel as luteal support in in- vitro fertilization-embryo transfert.It can improve clinical pregnancy rate.Furthermore, it can avoid adverse drug reaction from the injection of progesterone and use conveniently.
In-vitro fertilization-embryo transfer; Progesterone sustained-released vaginal gel; L uteal phase support
2014-03-31]
524001 湛江, 广东医学院附属医院生殖医学中心
