拉米夫定预防HBsAg阳性乳腺癌患者化学治疗中病毒再激活的疗效
2014-08-22刘宇李展翼黄泽楠黄勇
刘宇 李展翼 黄泽楠 黄勇
我国是HBV的中度流行国家,有研究显示,我国1~59岁一般人群HBsAg阳性率为7.18%,我国现有的慢性HBV感染者约9 300万人,其中慢性乙型病毒性肝炎(乙肝)患者约2 000万例[1]。乳腺癌是女性常见的恶性肿瘤之一,近年来乳腺癌的发病率逐年升高,而在发展中国家和HBV高流行地区乳腺癌携带HBV患者并不少见,Zhong等于2004年报道乳腺癌患者中约12%为慢性HBV携带者。
乳腺癌是严重威胁女性身体健康的常见病,随着乳腺癌早期诊断和综合治疗技术的发展,乳腺癌的病死率已逐年下降。在综合治疗中,乳腺癌新辅助化学治疗、术后辅助化学治疗起着重要的作用,对延长乳腺癌患者的生存期至关重要。但是在接受化学治疗的患者中,HBV携带者病毒的再激活率可达41%~56%[2-3]。接受细胞毒性药物化学治疗或免疫抑制治疗的HBV携带者也可出现HBV的再激活,从而导致严重的肝损害甚至死亡。HBV再激活的患者中,50%~70%的患者会推迟化学治疗时间甚至中断化学治疗,影响患者预后[4-11]。 因此,预防HBV的再激活在HBsAg阳性乳腺癌患者的化学治疗过程中十分重要。
拉米夫定是我国第一个用于治疗HBV感染的核苷类似物,研究发现在使用细胞毒性化学治疗或免疫抑制治疗前预防性使用拉米夫定对降低HBV的再激活率可能有一定疗效[11-12]。笔者见目前关于拉米夫定对防治HBsAg阳性乳腺癌患者在化学治疗过程中HBV的再激活的疗效及安全性的报道不多,故进行了本研究,现将结果报告如下。
对象与方法
一、研究对象
将2009年1月至2012年12月在我院接受治疗的HBsAg阳性的乳腺癌患者25例设为治疗组,将同期在我院接受乳腺癌治疗但不同意进行抗病毒治疗的HBsAg阳性乳腺癌患者20例设为对照组。两组均经病理检查证实乳腺癌诊断,按《慢性乙型肝炎防治指南》诊断标准,均为HBV携带者或慢性乙肝患者,既往无接受抗HBV治疗。治疗组25例均为女性,年龄21~67(45)岁,肿瘤分期为Ⅰ期12例(48%)、Ⅱ期10例(40%)、Ⅲ期2例(8%)、Ⅳ期1例(4%),HBsAg全阳性,HBeAg阳性5例(20%),HBcAb全阳性,HBeAb阳性12例(48%);对照组20例均为女性,年龄25~64(44)岁,肿瘤分期为Ⅰ期4例、Ⅱ期13例、Ⅲ期1例、Ⅳ期2例,HBsAg全阳性,HBeAg阳性4例(20%),HBcAb全阳性,HBeAb阳性10例(50%);两组主要血液生化指标比较见表1,两组一般资料具可比性,P均>0.05。两组均排除肝功能失代偿,排除患甲、丙、丁、戊型病毒性肝炎及脂肪肝、酒精性肝病、自身免疫性肝病等肝脏疾病。本研究经我院伦理委员会批准,且患者对治疗方案知情同意。

表1 治疗组与对照组治疗前主要血液生化指标比较 [全距(中位数)]
二、治疗方法
治疗组化学治疗时间为6个疗程,每隔21 d进行一疗程,每次1 d,化学治疗方案为5-氟尿嘧啶500 mg/m2+表柔比星75 mg/m2+环磷酰胺500 mg/m2,从化学治疗前1周开始至化学治疗结束后12周配合使用拉米夫定0.1 mg/d。对照组化学治疗方法同治疗组,并于治疗前后按肝功能情况适当使用护肝药物如复方甘草酸苷、还原型谷胱甘肽及水飞蓟素等。
三、观察指标
于最后一次化学治疗后比较两组HBV再激活率,HBV感染再激活指在免疫化学治疗过程中或结束后即出现肝炎,即HBeAg阳性和(或) HBV DNA 升高超过10倍或升高至1012copies/L[4]。最后一次化学治疗后查HBV YMDD变异株。化学治疗期间定期行血液生化检查,明确肝损害等情况,药物性肝损害的诊断标准参考CIOMS标准和Maria标准。记录提前结束或延期治疗患者比例以及其他与拉米夫定有关的不良反应。
四、统计学处理
采用SPSS 18.0统计软件处理数据,分类变量资料采用χ2检验或Fisher’s精确检验,等级资料采用秩和检验,P<0.05为比较差异有统计学意义。
结 果
治疗组患者接受6个周期的化学治疗后无出现HBV再激活者,3例出现化学治疗药物所致的轻度肝损害,无患者延迟或中断化学治疗,患者对拉米夫定的耐受性好,无明显的拉米夫定相关不良反应(包括过敏、凝血系统异常及泌尿系统结石等)。对照组接受6个周期的化学治疗后,6例出现HBV再激活,3例出现化学治疗药物性肝损害,5例因肝损害而提前终止或延迟化学治疗,见表2。
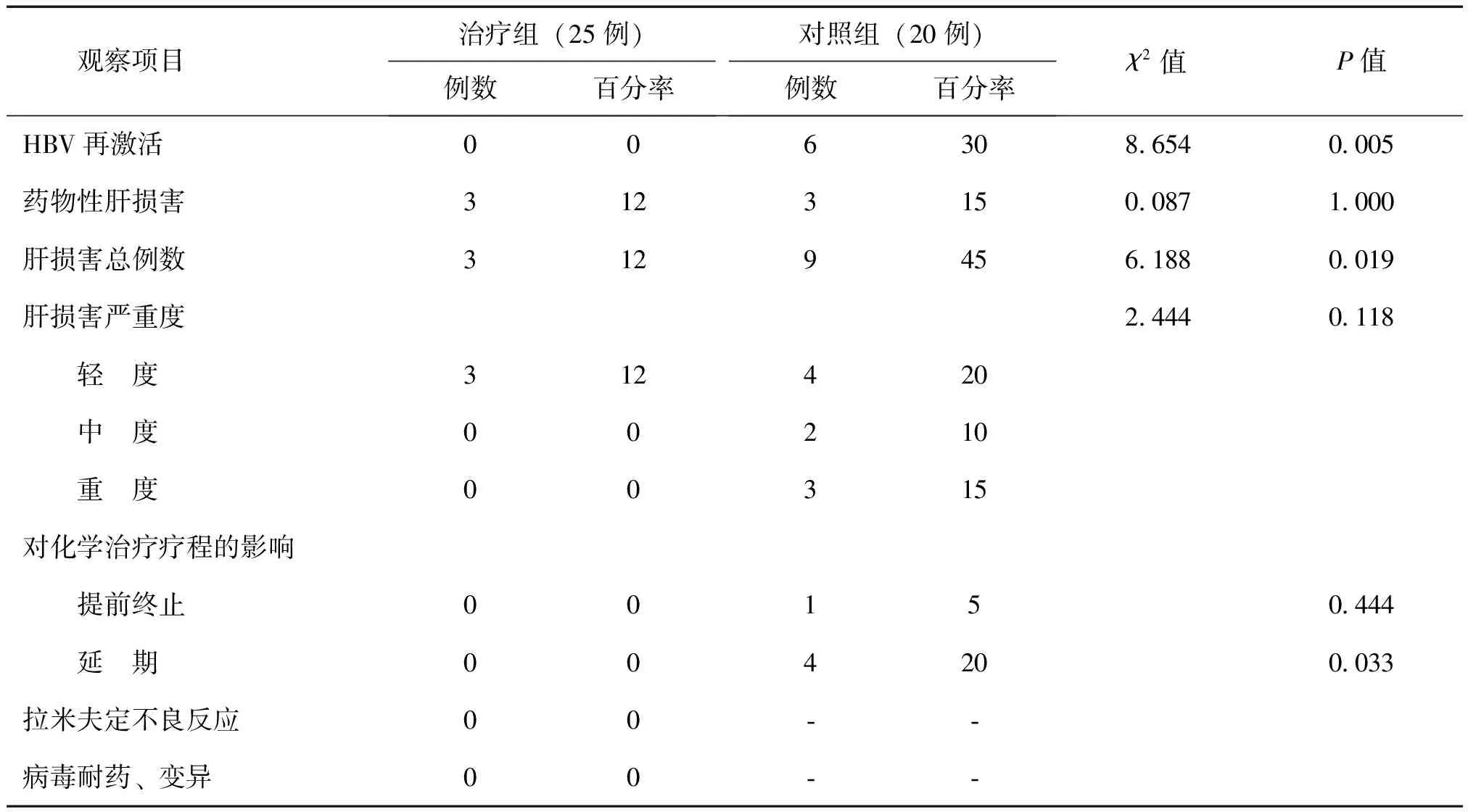
表2 治疗组与对照组治疗后各观察项目比较结果
讨 论
大量的研究证明,HBV感染者因患肿瘤、自身免疫性疾病、过敏性疾病或于移植治疗后使用抗排斥药物而需接受化学治疗或免疫抑制剂治疗时可出现HBV的再激活。此类患者若出现HBV再激活则可能致命,因HBV再激活可导致严重的肝损害,Katz等于2008年报道这种严重的肝损害病死率最高可达60%,严重影响患者的预后。因此,在HBV感染者接受化学治疗时,防止HBV再激活对化学治疗的顺利进行、减轻患者的痛苦、改善患者的预后十分重要[3]。
在过去的十多年,于化学治疗中预防性使用拉米夫定预防HBV再激活,从而降低治疗过程中乙肝的发病率,以及减少因HBV再激活所致化学治疗的提前终止、延期及药物减量的疗效已被证实,但此类研究多为针对淋巴瘤患者,在乳腺癌患者中类似的研究不多[14-16]。HBsAg阳性的乳腺癌化学治疗患者治疗前预防性使用拉米夫定抗病毒治疗是否能使患者获益,是我们十分关注的问题。近年来,一些关于HBsAg阳性的乳腺癌患者接受化学治疗前预防性使用拉米夫定抗病毒治疗的研究已开展,这些研究结果表明预防性使用拉米夫定抗病毒治疗可降低HBV再激活率,但对化学治疗的进行及出现肝损害情况无明显影响[17]。本研究结果也支持预防性使用拉米夫定抗病毒治疗可降低HBV再激活率这一结论,本研究结果还显示治疗组出现肝损害的百分率低于对照组,且对照组化学治疗延期的百分率高于治疗组。另外,学者们关注的使用拉米夫定抗病毒治疗可能会出现病毒耐药、变异的情况在本研究中无出现,考虑原因可能为乳腺癌患者接受6个周期化学治疗的总时间一般为4~5个月,而使用拉米夫定抗病毒治疗出现病毒YMDD株变异一般发生于连续使用6个月后,所以,本研究结果提示乳腺癌患者使用拉米夫定抗病毒治疗不会增加HBV变异、耐药的风险。同时,本研究表明使用拉米夫定治疗的患者耐受性良好,并未出现明显的药物不良反应。
综上所述,本研究结果表明,HBsAg阳性的乳腺癌患者接受化学治疗前预防性使用拉米夫定抗病毒治疗可使患者明显获益,包括HBV再激活率低、肝损害发生率低、化学治疗延期率低,但本研究非严格的前瞻性研究,且入组患者例数较少,尚需进一步行多中心、大样本的临床研究。
[1] 中华医学会肝病学分会,中华医学会感染病学分会.慢性乙型肝炎防治指南(2010年版).中华肝脏病杂志, 2011, 19:13-24.
[2] Zheng Y, Zhang S, Tan Grahn HM, et al. Prophylactic lamivudine to improve the outcome of breast cancer patients with HBsAg positive during chemotherapy: a meta-analysis. Hepat Mon,2013,13:e6496.
[3] 瞿晴, 沈坤. 应重视乳腺癌化疗相关乙型肝炎病毒再激. 中华医学杂志, 2012, 92:2377-2378.
[4] 魏丽,董敏,林曲,等.拉米夫定预防非霍奇金淋巴瘤免疫化学治疗后HBV 感染再激活失败5 例分析.新医学,2012,43:33-35.
[5] Yun J, Kim KH, Kang ES, et al. Prophylactic use of lamivudine for hepatitis B exacerbation in post-operative breast cancer patients receiving anthracycline-based adjuvant chemotherapy. Br J Cancer, 2011,104:559-563.
[6] Manzano-Alonso ML, Castellano-Tortajada G. Reactivation of hepatitis B virus infection after cytotoxic chemotherapy or immunosuppressive therapy. World J Gastroenterol ,2011,17: 1531-1537.
[7] Lok AS, Ward JW, Perrillo RP, et al. Reactivation of hepatitis B during immunosuppressive therapy: potentially fatal yet preventable. Ann Intern Med, 2012,156:743-745.
[8] Wang Y, Luo XM, Yang D, et al. Testing for hepatitis B infection in prospective chemotherapy patients: a retrospective study. World J Gastroenterol, 2013,19: 923-930.
[9] Hwang JP, Fisch MJ, Zhang H, et al. Low rates of hepatitis B virus screening at the onset of chemotherapy. J Oncol Pract, 2012,8:e32-e39.
[10] Jang JW. Hepatitis B virus reactivation in patients with hepatocellular carcinoma undergoing anti-cancer therapy. World J Gastroenterol,2014,20: 7675-7685.
[11] Liu CJ, Chen PJ, Chen DS, et al. Hepatitis B virus reactivation in patients receiving cancer chemotherapy: natural history, pathogenesis, and management. Hepatol Int,2013,7:316-326.
[12] Huang YW, Chung RT. Management of hepatitis B reactivation in patients receiving cancer chemotherapy. Therap Adv Gastroenterol,2012,5:359-370.
[13] Huang YH, Lin HC, Lee SD. Management of chemotherapy-induced hepatitis B virus reactivation. J Chin Med Assoc, 2012,75:359-362.
[14] Villadolid J, Laplant KD, Markham MJ, et al. Hepatitis B reactivation and rituximab in the oncology practice. Oncologist, 2010,15:1113-1121.
[15] Chen J, Wang J, Yang J, et al. Concurrent infection of hepatitis B virus negatively affects the clinical outcome and prognosis of patients with non-hodgkin’s lymphoma after chemotherapy. PLoS One,2013,8:e69400.
[16] Evens AM, Jovanovic BD, Su YC, et al. Rituximab-associated hepatitis B virus (HBV) reactivation in lymphoproliferative diseases: meta-analysis and examination of FDA safety reports. Ann Oncol,2011,22:1170-1180.
[17] Long M, Jia W, Li S, et al. A single-center, prospective and randomized controlled study: can the prophylactic use of lamivudine prevent hepatitis B virus reactivation in hepatitis B s-antigen seropositive breast cancer patients during chemotherapy? Breast Cancer Res Treat,2011,127:705-712.
