废磷酸三异戊酯有机溶剂的间接电化学氧化分解行为研究
2014-08-08李辉波袁洁琼朱桐宇苏明业
李辉波,袁洁琼,苏 哲,朱桐宇,苏明业
(1.中国原子能科学研究院 放射化学研究所,北京 102413;
2.中核四〇四有限公司,甘肃 兰州 732850)
磷酸三异戊酯(TiAP)常温下为淡黄色透明液体,与煤油有良好的互溶性,稀释后的溶液为无色。与乏燃料水法后处理工艺过程中广泛使用的磷酸三丁酯(TBP)萃取剂相比,其化学结构相似,均属于中性磷类萃取剂。由于其具有在萃取过程中不易形成三相、在水中溶解度低等优点[1-3],被认为是一种可弥补TBP不足的最有前景的萃取剂,尤其适宜处理HNO3溶液中钚浓度较高的体系。
与TBP在乏燃料后处理中的应用过程相似,考虑到经济因素和废物最小化,通常将使用过的TiAP/煤油体系经酸碱洗涤后再循环使用,直至其萃取性能恶化到不能再满足工艺需求,将其视为有机放射性废物进行处理。
对有机放射性废液,通常采用焚烧、热解和氧化破坏等方式进行处理,其中焚烧和热解两种方式均要求在高温环境下运行。因焚烧产物中含有P2O5,对设施的腐蚀性强,同时可能会产生含放射性气体,因此设施的建造和维护均存在一定困难。已研究过的氧化过程包括化学过程、电化学过程等[4]。其中化学过程有酸消化过程和过氧化氢湿法氧化过程,两者的优点是均可降低操作温度(前者约250 ℃,后者约100 ℃)和压力,不足是除前者会产生二次污染废物(强酸)外,其氧化破坏效率均不高。相比之下,间接电化学氧化(MEO)法作为一种替代焚烧技术,通过一系列的电子传递过程(通常以金属离子作为媒介体)将有机物氧化为CO2和H2O。该技术通常以Ag2+、Co3+和Ce4+等离子作为氧化介质[5-8],其优势表现在:在低温(30~70 ℃)、常压下运行,设备和操作过程简单,易于实行自动化控制和维护,且用该技术处理后放射性核素仍集中于液相中,便于进一步处理,易于核材料回收利用。本文以银作氧化介质进行间接电化学氧化破坏废TiAP有机相的研究,获取其氧化分解过程的影响因素,寻找适宜的工艺条件。
1 实验
1.1 原料和仪器
TiAP:分析纯,四川大学研制;加氢煤油:中核四〇四有限公司提供;AgNO3、HNO3,化学纯,北京化工厂。
GC-2014气相色谱仪,日本岛津公司;CIC-100型离子色谱仪,青岛盛瀚色谱技术有限公司;3100型TOC/TN分析仪,德国耶拿分析仪器股份公司;H型电解槽,自制;阴阳电极均为抛光铂电极,规格为20 mm×30 mm×0.2 mm,天津艾达泽明金属材料有限公司;磁力搅拌器,IKA公司;MPS505电源,TRADEX公司。
1.2 基本原理
以银作氧化介质,在HNO3溶液体系中进行间接电化学氧化破坏废TiAP有机相的基本原理是:在阳极将Ag+氧化为高价态的Ag2+,进而利用Ag2+的强氧化性分解TiAP和稀释剂(TiAP的分子式为(C5H11)3PO4;稀释剂为加氢煤油,是C9~C13的长链烷烃混合物,C11~C13的烷烃占90%以上,故本研究以C12H26作为其代表分子式),反应后的金属离子重新还原至低价态,并重新在阳极被氧化至高价态,通过这种循环实现有机相的完全分解破坏。此过程称为银媒介间接电化学氧化过程(Ag/MEO),也称为“银催化”电化学氧化过程。
在上述体系中,阴阳两极的反应如下。
阳极:
(1)
CO2+H2O+Ag++H3PO4
(2)
阴极:
(3)
为降低因阴极HNO2的形成而造成的HNO3的损失,本研究在阴极室通入氧气,将生成的HNO2迅速转化为HNO3,反应式如下:
(4)
综上所述,废TiAP有机相分解破坏的总反应式可表示为:
(5)
(6)
上述总反应式虽仅是理论反应过程,不能反应整个过程的真实过程,但其可在宏观上评价反应现象和计算反应分解率等。
1.3 实验方法
图1为间接电化学氧化破坏TiAP有机相的实验装置简图。该装置主要由阳极室和阴极室两部分构成,材质为玻璃。中间用烧结玻璃纱膜隔开以防止在阳极被氧化的银离子又在阴极上被还原,阴阳极均为铂金电极。实验时,阴极室溶液为70 mL、8 mol/L的HNO3溶液,阳极室按V(有机相)∶V(水相)=1∶2~1∶5加入与阴极室相同体积的溶液,水相为含0.1~0.5 mol/L AgNO3的4~10 mol/L HNO3溶液。在电解过程中,阳极室通过电磁搅拌装置进行水相与有机相的充分混合,阴极室采用鼓氧气的操作方式。
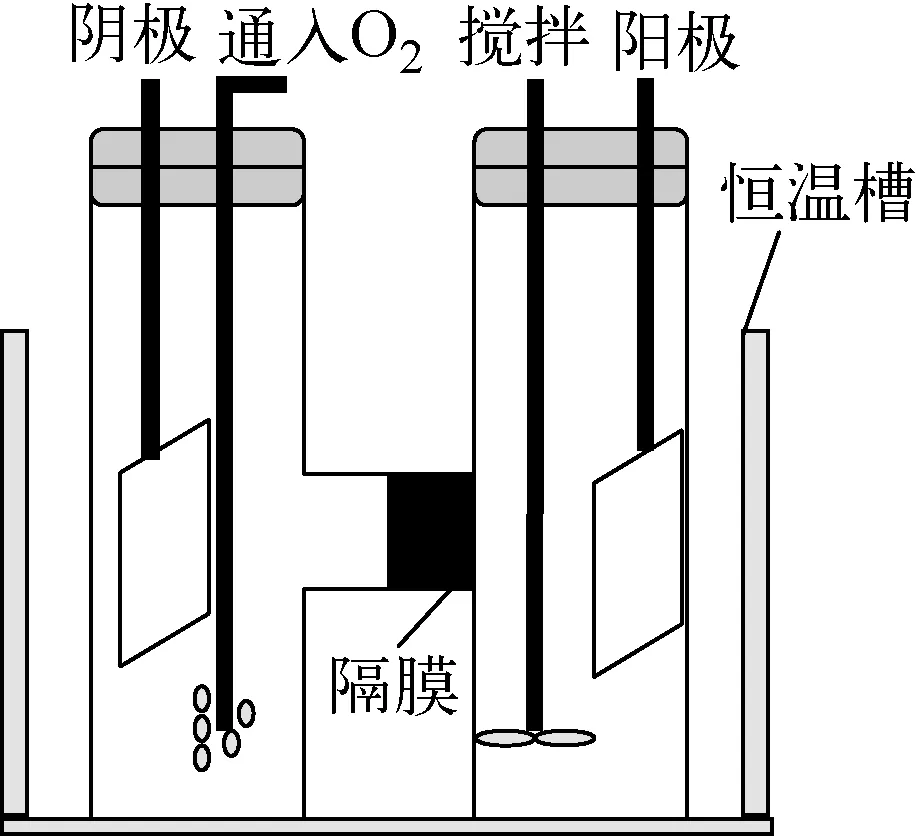
图1 间接电化学氧化破坏废TiAP有机相的实验装置示意图
1.4 分析方法
1) Ag2+浓度的测定:取1 mL不同反应时间下的阳极溶液,将其加入2 mL含0.5 mol/L Co(NO3)2和3.5 mol/L HNO3的混合溶液中,用Ag2+将Co2+氧化为Co3+,在606 nm 波长下测定吸光度,并与事先绘制的标准曲线对比得到Ag2+的浓度。
2 结果与讨论
2.1 Ag2+产生量的影响因素
间接电化学氧化处理有机物的关键在于高价金属离子的产生,实际上阳极室产生Ag2+的过程影响因素较复杂。首先阳极在将Ag+氧化成Ag2+的同时也会发生水分子的氧化电解,两者的氧化反应化学式和标准电位(25 ℃)如下:

(7)
(8)
从两者的标准电位来看,阳极在将Ag+氧化至Ag2+的过程中,水分子的电解对Ag+氧化有一定的影响,同时Ag2+是一种强氧化剂,它也可将水分子氧化(式(9)),此过程会消耗部分Ag2+。
(9)
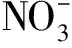
综上所述,溶液中HNO3浓度、温度等条件对Ag2+的生成和稳定的影响较复杂。本研究首先研究温度、AgNO3初始浓度、HNO3浓度等条件对Ag2+产生量的影响。
1) 阳极室水溶液中AgNO3初始浓度对Ag2+产生量的影响
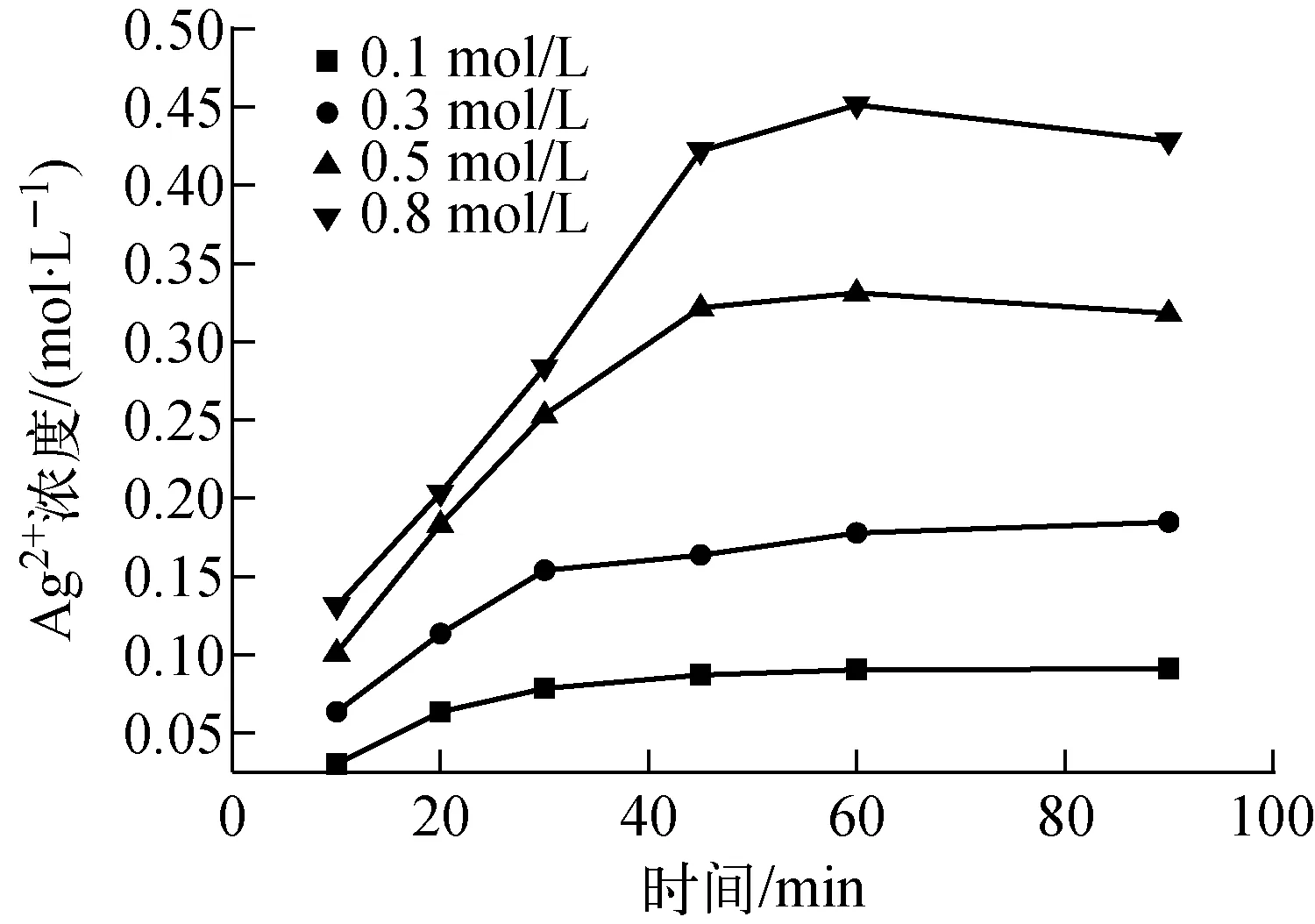
图2 AgNO3初始浓度对溶液中Ag2+产生量的影响
当阳极室水相HNO3浓度为8 mol/L、电解操作温度恒定为25 ℃、电流密度I为0.5 A/cm2时,阳极室水溶液中初始AgNO3浓度对Ag2+产生量的影响示于图2。图2表明,当阳极室水相HNO3浓度为8 mol/L时,溶液中初始AgNO3浓度越高,通过阳极氧化产生的Ag2+的浓度也越高。另外,尽管初始浓度有差异,通电50 min后,溶液中的Ag2+浓度均趋于稳定。
2) 操作温度对Ag2+产生量的影响
取阳极室AgNO3浓度为0.1 mol/L,其他条件不变,温度对Ag2+产生量的影响示于图3。图3表明,Ag2+的产生量随操作温度的升高而下降。产生这种现象的主要原因是温度的升高提高了Ag2+与H2O的反应速度(式(9)),消耗了一部分Ag2+。

图3 操作温度对溶液中Ag2+产生量的影响
3) 溶液中HNO3浓度对Ag2+产生量的影响

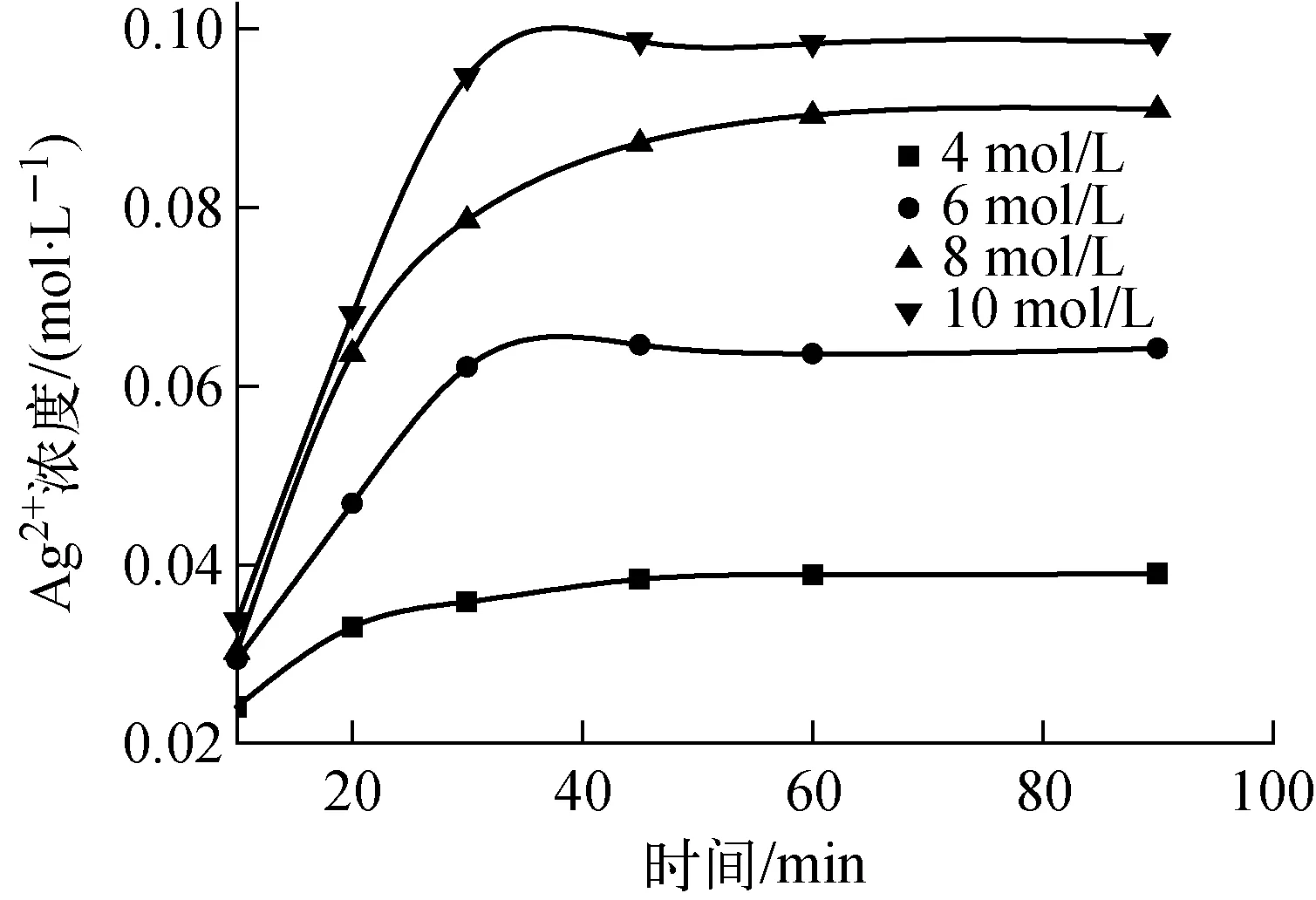
图4 溶液中HNO3浓度对Ag2+产生量的影响
2.2 溶液中Ag2+对TiAP的氧化分解行为研究
综合2.1节的结果,选择8 mol/L HNO3和0.5 mol/L AgNO3的混合溶液作为阳极室水溶液体系来考察其对TiAP的氧化分解过程,同时研究操作温度、电流密度等条件对TiAP氧化分解的影响。
1) TiAP氧化分解过程研究
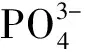
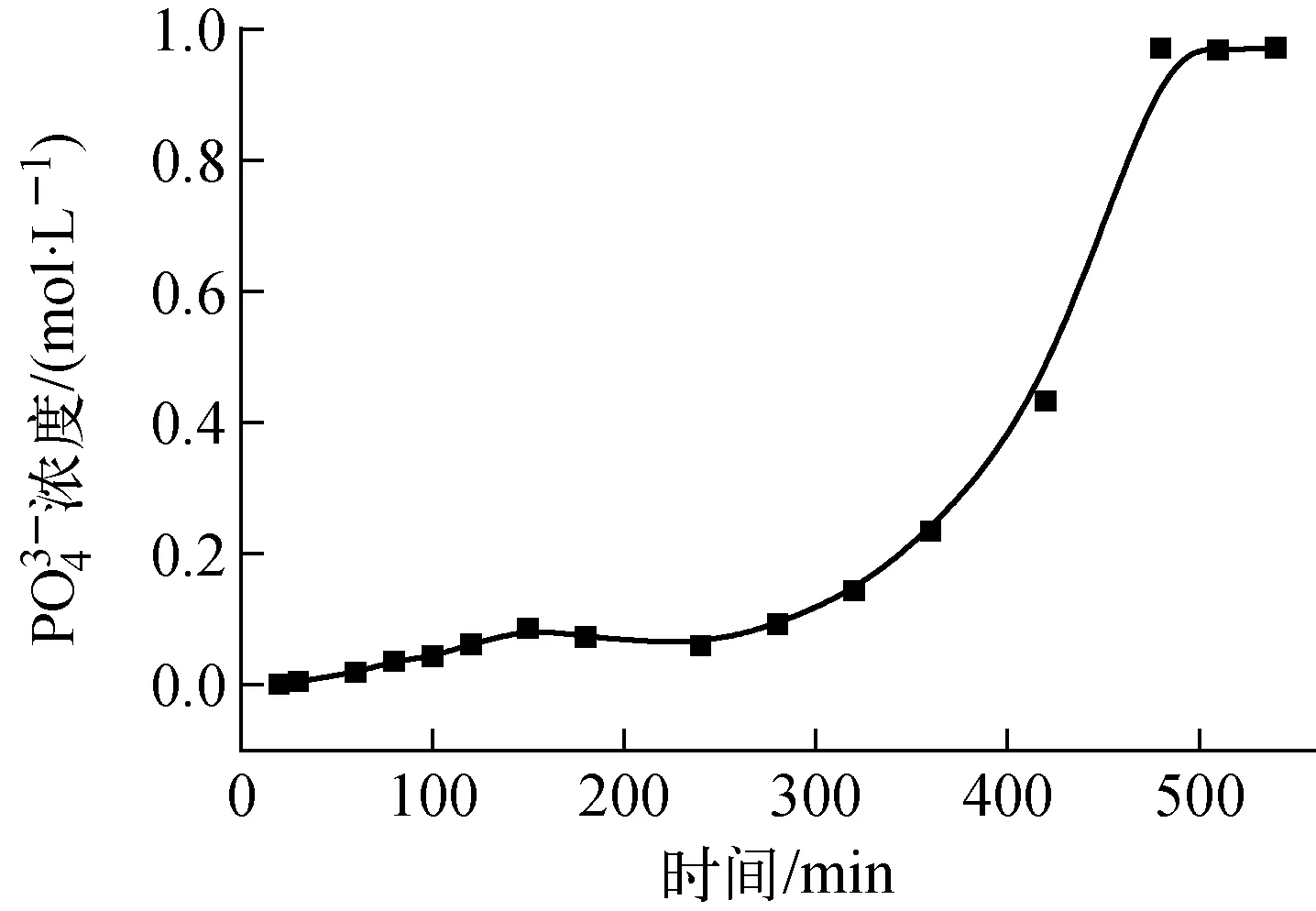
图5 阳极室溶液中浓度随氧化时间的变化
2) 操作温度对TiAP氧化分解速率的影响
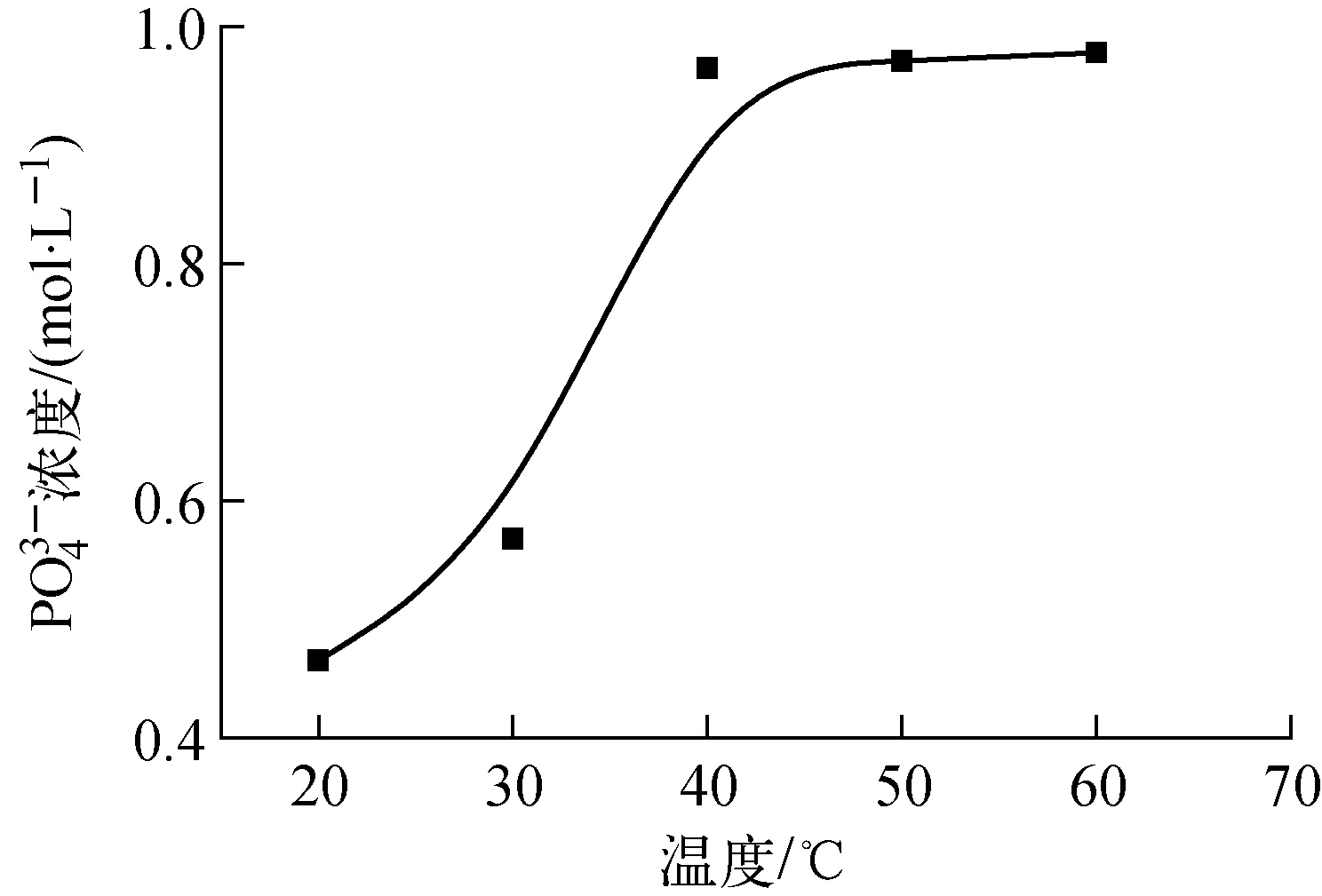
图6 阳极室溶液中磷酸浓度随操作温度的变化
图6为操作温度分别为20、30、40、50 和60 ℃,电解氧化8 h后溶液中磷酸含量的变化。图6显示,在20~40 ℃下,水溶液中磷酸的含量随操作温度的升高而迅速增加,大于40 ℃后,水溶液中磷酸的含量随操作温度的升高变化不明显。产生这种现象的主要原因是Ag/MEO体系氧化分解TiAP有机溶剂包括两个过程:一是Ag2+在阳极的产生;二是Ag2+氧化分解TiAP。尽管升高温度有利于加快TiAP的氧化分解速度,但低温更有利于Ag2+的稳定。因此,本研究操作温度控制在40~50 ℃。
3) 电流密度对TiAP降解的影响
表1为恒温40 ℃、TiAP电化学氧化分解8 h后阳极室溶液中磷酸浓度随电流密度的变化,其中阳极室加入22 mL TiAP,阴阳两室溶液总体积均为70 mL。表1数据表明,当电流密度在0.1~0.8 A/cm2内变化时,溶液中磷酸浓度随电流密度的增大而增大,表明操作电流密度越大越有利于TiAP氧化分解。但实验现象表明,随着电流密度的增大,阴阳两极室的溶液温度也随之升高,同时阴极室HNO3溶液颜色逐渐由浅黄色变为墨绿色,阴阳两极表面出现的气泡越来越多,操作电压越来越高。当电流密度增大至1 A/cm2时,氧化0.5 h出现电极隔膜击穿。综上所述,选择将电流密度控制在0.3~0.5 A/cm2之间。

表1 阳极室溶液中磷酸浓度随电流密度的变化
3 结论
1) 氧化分解过程中溶液体系HNO3浓度、操作温度等条件对Ag2+的产生量和稳定性均有一定的影响。溶液中Ag+和HNO3浓度的增大有利于Ag2+的生成;操作温度的升高,不利于Ag2+的生成。
2) 在用Ag/MEO体系对TiAP氧化过程中,首先将TiAP分解为易溶于水的小分子物质,再进一步分解为磷酸、CO2和H2O。
3) 在温度为40 ℃、HNO3浓度为8 mol/L和电流密度为0.5 A/cm2的条件下,氧化电解8 h可将99.9%的TiAP分解破坏。
参考文献:
[1] 于恩江,刘黎明,黄怀安. 磷酸丁酯萃取钚(Ⅳ)时生成第三相的研究[J]. 核化学与放射化学,1986,8(3):134-138.
YU Enjiang, LIU Liming, HUANG Huaian. Investigation on the formation of a third phase in the extraction of Pu(Ⅳ) nitrate with tributyl phosphate[J]. Journal of Nuclear and Radiochemistry, 1986, 8(3): 134-138(in Chinese).
[2] 程琦福,罗方祥,刘协春,等. 磷酸三异戊酯对Pu(Ⅳ)的萃取性能[M]∥中国原子能科学研究院年报. 北京:原子能出版社,2006:234.
[3] 焦荣洲,韩升印. 磷酸三异戊酯萃取U、Np、Pu性能的研究[J]. 原子能科学技术,1995,29(2):161-166.
JIAO Rongzhou, HAN Shengyin. Study on the extraction performance of tri-isoamyl phosphate for U, Np, Pu[J]. Atomic Energy Science and Technology, 1995, 29(2): 161-166(in Chinese).
[4] 顾忠茂. 核废物处理技术[M]. 北京:原子能出版社,2009:237-246.
[5] GALLA U, KRITZER P, BRINGMANN J, et al. Process for total degradation of organic wastes by mediated electro-oxidation[J]. Chem Eng Technol, 2000, 23(3): 230-233.
[6] BRINGMANN J, EBERT K, GALLA U, et al. Electrochemical mediators for total oxidation of chlorinated hydrocarbons: Formation kinetics of Ag(Ⅱ), Co(Ⅲ) and Ce(Ⅳ)[J]. Journal of Applied Electrochemistry, 1995, 25: 846-851.
[7] FARMER J C, WANG F T, LEWIS P R, et al. Destruction of chlorinated organics by cobalt(Ⅲ)-mediated electro-chemical oxidation[J]. J Electrochem Soc, 1992, 139(11): 3 025-3 029.
[8] KIRWIN J B, PEAT F D, PROLL P J, et al. A kinetic and spectro-photometric examination of silver(Ⅱ) in perchlorate media[J]. J Phys Chem, 1963, 67: 1 617-1 621.
