基于石墨烯的功能化复合材料及其在电化学储能中的应用
2014-08-07魏志凯郑明森董全峰
魏志凯,张 焕,郑明森,董全峰
(厦门大学化学化工学院,福建 厦门 361005)
发展清洁和可再生能源是我国社会经济发展的重大战略.在新能源技术的各个层次中,电化学储能具有极其重要的地位,也是当前科学研究的热点问题.作为一种新型二维结构导电材料,石墨烯的应用在这一领域具有重要意义和极大的发展潜力.
自2004年,Novoselov和Geim[1]通过简单的胶带剥离法将单层石墨烯从高温有序裂解石墨的表面剥离下来以来,石墨烯因其独特的单原子层结构和丰富而奇特的物理化学性质(见表1)吸引了科研和工业界的广泛关注.而其在储能领域中的应用研究也获得了重大的进展和引人瞩目的成果,具有极大的应用价值和发展潜力.
作为sp2杂化碳材料基元结构的单层石墨烯(图1),是一种优异的二维载体材料,在设计和调控纳米活性材料中起着重要的作用.石墨烯是由单层碳原子组成的二维蜂窝状结构,其基本结构单元为有机材料中最稳定的六元环结构,具有良好的化学稳定性,是二维纳米材料的典型代表.将之应用于储能器件中,同其他碳材料相比具有以下优点:
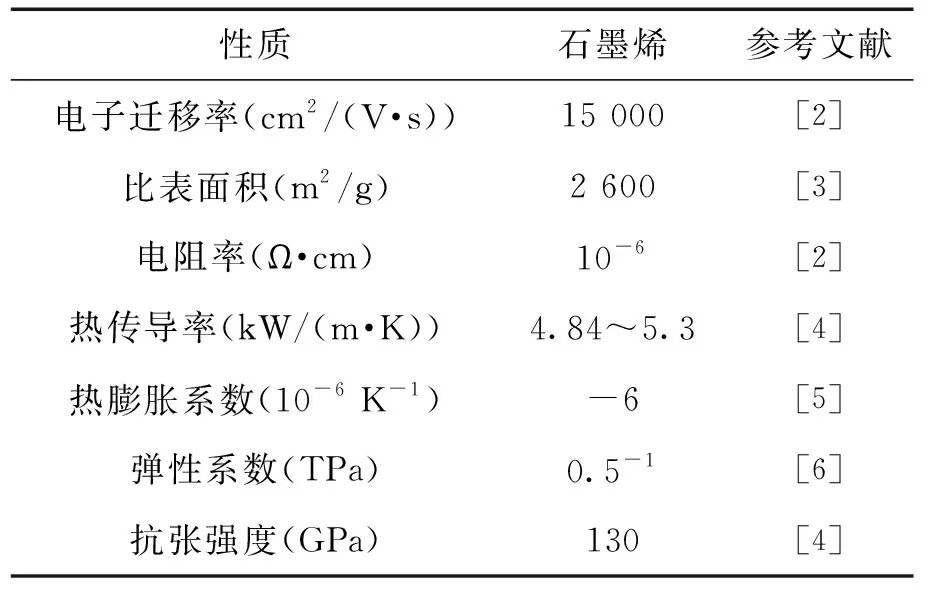
表1 石墨烯的重要物理性质Tab.1 Important physical properties of graphene
1) 石墨烯的比表面积高达2 600 m2/g,有助于纳米材料在其表面的分散,能够有效阻止纳米颗粒的团聚,同时也能为电化学反应提供较大的反应界面.
2) 石墨烯的电子电导率约为105S/m,有助于改善复合材料的导电性,以及电化学反应过程中电子电荷的传递.
3) 石墨烯本身为柔性的二维材料,具有更加灵活的空间构筑特性,石墨烯片层之间可以相互缠绕交叠,构成丰富的孔道结构.这些孔道结构在电化学储能器件中有利于电解液的渗透和离子的扩散,提高反应过程中的离子电导率.

图1 石墨烯作为碳材料结构基元构成富勒烯、碳纳米管和石墨Fig.1 Graphene as the basic cell to compose fullence,carbon nanotube and graphite
4) 石墨烯具有很多的边缘结构,另外,还原石墨烯表面也会残留很多的缺陷位和官能团,这使得石墨烯具有很多的表面和边缘缺陷位,使其具有一定的离子吸附能力和催化活性.
5) 石墨烯相对于富勒烯或碳纳米管来说,较为容易制备,且成本低.
所以基于石墨烯所制备的复合材料应用于储能器件可具有更加优越的电化学性能,且有望发展成为高性能的电极材料.而现有研究结果也显示石墨烯能够显著改善储能材料的容量特性、快速充放电能力以及循环寿命,在超级电容器、锂离子电池、锂硫电池体系、锂氧电池体系以及燃料电池等体系中具有巨大的应用潜力[7].本文主要涉及石墨烯的合成和以石墨烯为基础的复合材料的制备,及其在电化学储能方面的应用,包括超级电容器体系、锂离子电池体系、锂硫电池以及锂氧电池体系等方面.
1 石墨烯的合成
有关石墨烯合成方法的研究早已成为科研和工业界的一大研究热点.从首次剥离石墨烯至今,已经建立了几种相对成熟的石墨烯合成方法,并取得广泛的应用,如机械剥离方法[1]、化学氧化剥离[8]和化学气相沉积方法(CVD)[9].而另外一些报导的合成方法,如碳管展开方法[10]和醇纳水热合成法[11],由于产量较低或合成过程复杂等问题,需要进一步的发展.这些方法可分为两类,一类为基于石墨材料的剥离方法,即top-down方法;另一类是基于碳原子的生长方法,即bottom-up方法.
作为首次剥离石墨烯的合成方法,机械剥离法是一种属于top-down的纳米技术,该类方法使用简单的透明胶带或AFM针尖,在层状结构材料表面产生横向或纵向作用力,从而将单层或少数几层材料从基底上剥离下来.石墨材料是由单层的石墨烯通过微弱的范德华力堆叠而成,层间距为0.334 nm,层间键能为2 eV/nm2,对应的机械剥离外力要达到300 nN/μm2才能将单原子层的石墨烯从石墨表面剥离.早在1999年,Ruoff等[12]就首次提出机械剥离法的概念,仅获得极薄的纳米石墨片(约200 nm).直到2004年,Novoselov和Geim[1]才通过胶带剥离的方法首次制备得到单层的石墨烯,并对其电学性质进行了测试,且凭借这一工作,他们于2010年获得诺贝尔物理学奖.机械剥离方法能够得到缺陷极少的高纯度石墨烯,得到的石墨烯多用于场效应晶体管等电子元件的基础研究中.而且这种方法也应用于其他的二维材料的制备,如氮化硼,二硫化钼等.但是,该方法存在着产量低、可重复性差、无法大规模生产的缺点.另外针对有效剥离大尺寸、高质量石墨烯的工艺研究,也是该方法的一大挑战.
化学剥离方法可以分为两类:一类是基于有机溶剂的超声剥离方法,即依靠有机溶液分子同石墨表面的作用力,在超声的条件下将石墨剥离开;另一类是碱金属插层剥离方法,即依靠碱金属较易同石墨形成石墨插层化合物的性质,通过这些插层化合物同水或乙醇等溶剂的反应将石墨层剥离.Viculis等[13]于2003年首次报道了通过钾的石墨插层化合物剥离制备少数几层的石墨(现在称之为石墨烯).钾、钠等碱金属具有小于石墨层间距的原子半径,因此很容易嵌入石墨层中形成石墨插层化合物.后来Viculis等[14]又尝试了使用其他碱金属如铯和钠-钾合金,通过同样的方法进行剥离.铯相比于钾更容易同石墨反应,使插层反应能够在更低的温度下进行.这为常温条件下在溶液中大量剥离制备石墨烯提供了一种有效的方法.但是对于石墨插层化合物剥离方法来说,如何控制得到厚度均一的剥离产物,如何剥离得到单层或双层石墨烯仍是一个挑战,有待进一步的研究.在2008年,Hernandez等[15]报道了一种新型的有机溶剂超声剥离方法,该方法中纯的石墨粉末被分散在N-甲基吡咯烷酮(NMP)中,然后经过简单的超声过程就可以在上层清液中得到高质量的单层石墨烯.该方法得到的单层石墨烯产率约为1%(质量分数),而将原料和溶液循环利用可将产率提高到7%~12%(质量分数).Lotya等[16]报道了一种使用表面活性剂-水溶液对石墨进行剥离的方法,在该方法中十二烷基苯磺酸钠(SDBS)起到剥离剂和稳定剂的作用,得到的产物大多数为小于5层的石墨烯,有3%为单层的石墨烯,而且由于表面活性剂在石墨烯表面的包覆,从而防止了石墨烯的团聚效应,其所得溶液能够保存6周不发生沉聚.这种溶液超声剥离方法是依靠有机溶剂分子或表面活性剂分子同石墨的表面具有较强的相互作用,在外力(超声)的作用下将石墨剥离为石墨烯并分散在溶液中.这些方法相对简便易行,成本低而且所得石墨烯质量高,缺陷少,并均匀分散在溶液中,适合于制备透明薄膜电极或薄膜晶体管器件.但该方法也具有剥离量低,剥离层数不均匀等缺点,并不适合应用于大规模石墨烯的合成以及制备基于石墨烯的复合材料.
化学氧化剥离方法也是一种top-down 的剥离技术,并且是首个制备石墨烯的化学方法.早在1958年,Hummers等[17]就报导了使用这一氧化剥离技术剥离鳞片石墨得到氧化石墨——后来经石墨烯的发现者Andre Geim证实为单层的氧化石墨烯(graphene oxide,GO).化学氧化剥离制备石墨烯的方法涉及以下合成过程:鳞片石墨在强酸和强氧化环境中氧化得到氧化石墨,然后氧化石墨在超声作用下在水溶液中剥离得到单层的GO,最后再经还原反应得到还原石墨烯.Hummers等[17]制备GO的方法在当时并没有引起人们的广泛关注,直到2006年Ruoff等[18]通过这种化学剥离氧化-还原的方法得到单原子层的石墨烯后,这种方法才被广泛地应用于石墨烯及其复合材料的制备中.在高程度的氧化条件下,其石墨层的表面具有丰富的羟基和环氧基官能团[19].这些亲水性的官能团在超声条件下有助于水分子嵌入氧化石墨层间,加速其在水溶液中的剥离.以这些超声后均匀分散的GO为原料,经过一个化学还原(联氨,碘化氢等还原剂)处理过程即可得到具有化学修饰的还原石墨烯[18].除此之外,热还原的方法也被用来还原经超声剥离的GO.2006年Michael等[20]报道了通过热膨胀法成功地得到了单层的还原石墨烯.这种方法是依靠快速升温过程中GO表面官能团的分解产生气体使还原石墨烯保持单层的分散,因此该方法具有操作简单,不易引入杂质,石墨烯还原程度高等优点,但其还原产物中团聚现象仍然存在,部分产物为多层石墨烯.总结上述报道,这种化学氧化剥离的方法可以大量剥离制备单层的GO,适用于复合材料的制备.但是,进一步的化学还原过程较易引入表面活性剂等杂质,并且还原的GO还原程度不完全,表面具有较多的缺陷和官能团,这会降低石墨烯的一些物理性质,如电导率、热传导率等.而热还原方法虽然能够得到较高还原程度的石墨烯,但是无法避免在热处理过程中单层石墨烯的团聚问题.因此针对还原方法的研究,开发出一种能够得到高还原程度石墨烯的同时并保持单层石墨烯分散性的还原方法,仍是当前石墨烯合成及其复合材料制备中的研究重点.
CVD是一种bottom-up的石墨烯合成方法,其主要是通过将基底材料暴露在热裂解气相前驱体中,在高温条件下将所需产物沉积在基底表面.而通常为了降低反应所需温度,采用结合微波或等离子体辅助方法来促进反应的进行.2006年,Somani等[21]首次报道了通过CVD方法在Ni表面合成石墨烯的工作.该工作中使用樟脑作为前驱体,通过先沉积后热裂解的两步处理过程得到大约35层堆叠的石墨烯片,这种CVD方法为后来合成大尺寸石墨烯薄膜奠定了基础.2008年,Yu等[22]报道使用甲烷通过CVD沉积在多晶Ni表面制备3~4层高质量石墨烯的方法,文章中指出石墨烯的生成取决于碳原子在Ni中的表面溶解和析出过程,因此冷却速度对石墨烯的生长具有很大的影响.在合成大尺寸石墨烯方面,具有突破性的工作是由Ruoff工作组[23]于2009年建立的以铜箔为基底的CVD沉积技术.他们使用甲烷等碳氢化合物经过高温CVD过程在Cu箔表面得到尺寸为1 cm2的单层石墨烯薄膜,并且报道了一种石墨烯转移技术,通过将Cu箔刻蚀后可将石墨烯薄膜转移到任何基底上,为石墨烯的应用提供了一个途径.Ruoff等[24]在2010年报道了一种roll to roll的石墨烯薄膜生产工艺,通过这种工艺设备可以生产出9.144 m大小的石墨烯薄膜,并且可以通过控制工艺参数调节沉积石墨烯薄膜的厚度.CVD技术是一种极具工业化生产前景的石墨烯制备技术,具有可生产高质量、大尺寸石墨烯薄膜的优点,而且当前的合成工艺已较为成熟.但是这种方法所需生产设备造价较高,且需要高温处理,不适合在聚合物基底上直接制备石墨烯(虽然可以通过转印技术将石墨烯薄膜转移到聚合物基底上,但是需要繁琐的刻蚀和转移工序).因此,当前在该领域的研究主要集中在低温CVD和非金属基底CVD技术的研究上.另外,该方法所得石墨烯为薄膜状,主要用于石墨烯薄膜材料的制备,并不适用于石墨烯复合材料的制备.
外延生长法也是一种bottom-up的制备石墨烯的方法,能够在单晶的SiC表面生长单层的高质量石墨烯.在1975年,van Bommel等[25]报道了在高真空环境中(~10-8Pa) 1 000~1 500 ℃下SiC会沿(0001)晶面生长得到石墨.2007年,de Heer等[26]报道了使用热裂解的方法在6H-SiC晶片表面沿(0001)得到1~2层的石墨烯.基于外延生长法制备石墨烯的研究因其具有规模制备的潜力和得到极高质量石墨烯的特点,从而引起了学术界和工业界的广泛关注.其最大的优点是该过程直接在绝缘体或半导体表面生长得到石墨烯薄膜,可以直接应用于基于CMOS的电子器件.然而这种技术需要较高的生长温度和高真空环境,对仪器的要求较高,导致生产成本较高,限制了其大规模的应用.
随着现代纳米科技的发展,一些新颖的bottom-up 石墨烯合成方法也随之涌现,比如全有机合成石墨烯量子点、醇钠合成石墨烯以及模板法CVD合成石墨烯等方法.
如果将石墨烯看为共轭的芳香环碳氢化合物(polycyclic aromatic hydrocarbons,PAH),那么有机合成途径也将是一种有效、可控的合成不同大小石墨烯的方法,而设计和合成PAH则是获得高质量石墨烯的关键步骤.Mullen和Schulte在该领域做出了极其突出的贡献[27].例如Mullen等[27]于2002年提出一种结合Diels-Alder反应和氧化脱氢环化反应制备石墨烯纳米片的反应途径,得到含有222个碳原子的PAH大分子.2008年Mullen等[28]又报道了一种通过有机合成途径制备12 nm长的石墨烯纳米带的方法.然而随着分子尺寸的增大通常会导致溶解度降低和边缘反应的发生,因此获得具有形状、大小和边缘结构可控的大石墨烯分子仍然是有机合成领域的一大挑战.
2008年,Choucair等[11]报道了一种通过醇钠溶剂热合成石墨烯的方法.该方法将乙醇和金属钠以1∶1的摩尔比放入密封的反应釜中,在220 ℃下热处理72 h,然后将得到的粉末前驱体快速热裂解,最终得到石墨烯粉末.该方法具有较高的产率,1 mL乙醇能得到的0.1 g石墨烯,然而得到的石墨烯质量较差(氧质量分数为17.35%),层数不均一(厚度6~8 nm).
2009年,Wei等[29]报道一种以CVD生长的ZnS纳米带为模板,CVD沉积石墨烯纳米带的方法.2011年,Cheng等[30]报道了使用泡沫Ni为模板,CVD沉积石墨烯后刻蚀去Ni基底得到一种三维缠绕结构的石墨烯基底.该三维的石墨烯骨架中,石墨烯质量很高,相互之间接触良好,因此这种石墨烯基底可以直接应用于锂电池和超级电容器中作为导电基底和骨架材料.
石墨烯作为一种新兴碳材料,展现了很多优异的物理、化学性质,并吸引了很多研究人员的兴趣,从合成工艺到生长机理,从物理性质到材料应用,这些课题仍都处于学术研究之中.值得强调的是尽管已经建立了一些石墨烯合成方法,但是当前的合成方法仍不能满足其应用的需要,尤其是应用于复合材料的大规模、高质量石墨烯的合成方法仍需要完善.
2 石墨稀在储能中的应用
2.1 石墨烯在超级电容器中的应用
超级电容器(supercapacitors),又称电化学电容器(electrochemical capacitors),具有功率密度高、充放电时间短、循环寿命长、工作温度范围宽等优点[31].按其储能原理,超级电容器可分为2类:1) 电化学双电层电容(EDLCs),依靠阴阳离子在电极表面的吸附/脱附储存和释放能量;2) 法拉第赝电容,依靠电极表面快速的氧化还原反应储存和释放能量[32].EDLCs的容量来源于电极和电解质界面所形成的双电层电容,因此其电极材料多采用具有较大比表面积的碳材料,比如活性炭、碳气凝胶、碳纳米管、介孔碳等[33].石墨烯同传统的碳材料相比具有更大的比表面积,同时具有很高的电导率,而且单层石墨烯能够相互缠绕构成丰富的多孔结构,这些特性使得石墨烯作为电极材料在超级电容器中的应用具有诱人的前景[34].

图2 Shi课题组所合成的石墨烯气凝胶的图片(小图),电镜图(a)和组装成超级电容器器件的电化学性能图(b)[41]Fig.2 The photo image,SEM images (a) and the electrochemical performance (b) of the graphene hydrogel synthesised by Shi′s group[41]
2008年,Stoller等[35]首次将石墨烯应用于超级电容器中,并组装成电容器器件测试其电化学性能.但是由于单层石墨烯在还原过程中再度团聚导致其表面积仅为705 m2/g,该材料仅有100 F/g左右的容量,但倍率性能良好.Chen等[36]则是使用还原性较弱的氢溴酸将石墨烯部分还原,而石墨烯表面残留的含氧官能团能够在一定程度上阻止石墨烯的团聚,改善石墨烯的亲水性,有利于电解液的渗透,而且官能团本身还能提供一定的赝电容.研究结果表明在1 mol/L硫酸溶液中、0.2 A/g电流密度下测试,材料容量最高可以达到348 F/g,但是由于材料本身电导率较低,倍率性能表现不好,并且这些官能团也会降低材料的循环稳定性.同时,热处理还原石墨烯[37]用于超级电容器的研究也有见诸报道.Wei等[38]发现利用200 ℃的低温热处理GO,会在石墨烯层与层之间引入大的狭缝孔结构,有利于离子在石墨烯表面形成双电层.得利于这种开放的孔结构和低温处理得到的特殊石墨烯表面结构,该材料在水系和有机体系电容器器件中分别具有264和122 F/g的电容容量.另外Du等[39]也使用类似的低温处理技术,在2 mol/L KOH溶液中1 A/g下测试,得到232 F/g的电容容量.
在大多数情况下,通过化学还原或热还原得到的石墨烯在组装电容器器件的过程中都会相互堆积、层叠,从而导致没有足够的孔隙结构以便于电解液渗透,因此需要以石墨烯构筑一种三维立体的结构.这种由单层石墨烯构筑的三维结构电极,单层石墨烯间没有发生团聚,不需要黏结剂,并且具有合适的孔道结构以方便电解液的渗透,从而引起了研究人员的关注和研究[40].Shi课题组[41]对这种三维结构的石墨烯材料——石墨烯气凝胶(graphene hydrogel)在超级电容器方面的应用进行了研究和报道.
从图2电镜图可以看到,这种石墨烯材料是由单层石墨烯相互缠绕构成,具有相互连通的三维孔道结构,孔道尺寸几百纳米到几十微米不等.材料的电化学性能研究表明其最好的材料在1 A/g下容量为220 F/g,而电流密度增大到100 A/g,其容量仍能保持74%,并且2 000圈容量保持率为92%.
另外一项重要的工作是由Ruoff课题组[42]报道的一种KOH活化的石墨烯应用用于超级电容器器件的研究工作.他们利用KOH在高温下对碳的刻蚀活化作用,在还原石墨烯表面刻蚀出1~10 nm的连续孔洞结构,使得材料的比表面积达到3 100 m2/g,同时保留石墨烯的单层结构和较高电导率特性.该材料在BMIMBF4/AN这种离子液体中,5.7 A/g电流密度下具有166 F/g的容量,其相应的能量密度能够达到70 Wh/kg.另外在2.5 A/g下循环10 000圈能量保持率为97%.
以上报道的是以石墨烯作为电极材料的双电层电容器的应用,石墨烯还可以作为载体材料应用于赝电容超级电容器器件中,负载具有较高赝电容的活性材料比如导电聚合物[43]或金属氧化物材料[44]等,以改善所负载活性材料的电化学性能.在这些导电聚合物和金属氧化物材料中,聚苯胺(PANI)材料具有高容量、低成本并易于制备的优点,被认为是最具应用潜力的材料之一[45].但是由于导电聚合物类的材料电导率低,并且聚合物长链不稳定,导致PANI材料的倍率性能不佳,循环性能差.而将PANI材料同石墨烯复合,能够结合石墨烯材料优异的电学性能和机械性能,以及PANI材料较高赝电容的优点,使得复合材料表现出优异的电化学性能.
Wang等[46]报道通过原位聚合的方法将PANI包覆于GO的表面,制备了一种基于PANI掺杂的GO电极材料(GO-PANI).该材料具有高达531 F/g的比容量,要远高于纯PANI的容量,表明PANI同GO之间具有一定的协同效应,可以促进其电化学性能的提高.在另外一项相关工作中,Xu等[47]使用比较简便的化学聚合方法将一维的PANI纤维直立生长在二维GO表面,如图3所示在这种独特的结构中,PANI和GO之间的协同效应不仅能提高复合材料的容量,也能改善材料的循环性能,在0.2 A/g电流密度下容量可达555 F/g,2 A/g下仍具有227 F/g,2 000圈后的容量保持率可达92%(纯PANI材料的容量保持率仅为74%).

图3 一维PANI纳米纤维生长在GO表面的电镜图Fig.3 One dimensional PANI nanofiber aligned vertically on GO surface
由于GO的电化学不稳定性,以及较低的电导率,GO-PANI复合材料并不能充分利用石墨烯的优异性质.而相比来说还原石墨烯更适合掺杂于PANI中.Wang等[48]报道了一种三步合成石墨烯-PANI复合材料的方法,依次为GO表面原位聚合PANI,NaOH还原GO-PANI去掺杂反应,PANI酸掺杂反应.通过该方法合成的复合材料具有高达1 126 F/g的容量.Yan等[49]报道将还原石墨烯分散于水溶液中,同时掺杂少量碳纳米管以支持石墨烯结构,再将PANI原位复合于碳材料表面上,从而得到石墨烯/碳纳米管/PANI复合材料.该材料在1 mV/s循环伏安扫描速度下表现出1 035 F/g的容量.
金属氧化物或氢氧化物材料如RuO2,MnO2,Ni(OH)2,Co3O4等也是超级电容器材料研究的一个重要方面.通过原位复合的方法将金属氧化物纳米颗粒均匀分散在石墨烯表面可以极大提升氧化物材料的电化学性能[50].Wu等[51]制备了不同RuO2负载量的石墨烯复合材料并进行了电化学性能的研究,结果显示该复合材料相比于RuO2和石墨烯材料具有较高的容量、倍率性能和稳定的循环性能.Dong等[52]使用水热方法在三维结构的石墨烯泡沫材料表面原位负载Co3O4纳米线并研究其电化学性能,测试结果表明该三维石墨烯-Co3O4复合材料10 A/g电流密度下具有高达1 100 F/g的比容量和稳定的循环性能.Wang等[53]使用原位生长的方法在石墨烯表面生长Ni(OH)2纳米片,材料表征结果显示该复合材料中石墨烯具有极高的电导率,而负载在其表面的Ni(OH)2纳米片厚度约为10 nm,该材料在2.8 A/g下具有高达1 335 F/g的容量,而在45.7 A/g下仍保持了953 F/g的容量.而Yan等[54]则使用微波辅助合成法合成花状Ni(OH)2-石墨烯复合材料,将该材料作为正极同石墨烯电极组装成不对称超级电容器装置,可获得218 F/g的比容量,能量密度高达77.8 Wh/kg,3 000圈循环后容量保持率高达94.3%.
由以上的文献介绍可以得出基于石墨烯的超级电容器材料(石墨烯及其复合材料)具有相当吸引人的应用价值.从理论上来说,石墨烯比表面积高达2 600 m2/g,同时也具有很高的电导率,是理想的超级电容器材料.虽然在实际应用中存在很多的问题,比如单层石墨烯容易团聚,导致其有效比表面积降低;化学还原法制备的石墨烯电导率差等.而针对这些问题的研究已经取得一定的成果.以低成本、高效的方式获得高质量单层石墨烯的制备方法的研究,以及在制备复合材料的过程中防止石墨烯团聚的复合方法的研究和设计则是今后研究的一个重要方向.
2.2 石墨烯在锂硫电池体系中的应用
锂硫电池体系是一种可反复充放电的锂电池体系,它的正极采用的是硫或硫复合材料,负极则是使用金属锂.硫与锂的电化学反应所具有的比容量高达1 675 mAh/g(以硫计算),是现阶段嵌入/脱出型正极材料比容量的8~10倍,而其比能量也能达到2 600 Wh/kg,是现有正极材料能量密度的5倍.另外,同现有正极材料相比,硫材料还具有成本低、资源丰富、易于制备加工等优点.因此,高容量锂硫电池体系一直吸引着电池开发研究者的兴趣[51].
与现有商品化的锂离子电池正极材料的嵌入/脱出反应机理不同,锂硫电池的反应机理属于转化反应机理,依靠正极材料中硫的硫—硫键的断裂/恢复来释放/储存能量.
早在1964年,通用汽车公司Selis等[52]就提出了以硫为正极材料的热电池,并将该电池用于他们早期的电动汽车计划.随后陆续出现有关有机溶液体系中硫电池的文献报道[53],但是其性能表现都不理想.直到2006年,Sion power公司报道其公司制作的锂硫电池达到实用化水准,可以为无人驾驶太阳能飞机Zephyr提供夜间动力[55].近几年来,随着纳米材料的发展,高容量锂硫电池的研究取得了极大的进展,无论是电池体系中硫材料的利用率,充放电倍率性能,还是电池体系的稳定性和循环性能都取得了很大的改善.
当前锂硫电池体系研究开发的重点主要在于硫正极材料,这主要还是由于硫元素所具有的特殊物理性质和电化学性质给锂硫电池体系的开发和应用带来极大的困难.
首先,硫单质为分子晶体,晶格是由S8分子紧密堆积而成,分子与分子之间仅靠微弱的范德华作用力相互作用,电子被定域在每个S8分子的范围内,所以硫在常温下的电导率极低,仅为6×10-30S/m,是离子和电子绝缘体[56].并且,锂硫电池放电产物为Li2S2或Li2S,也是电子绝缘体.因此,电子在锂硫电池正极中的传导性低是制约锂硫电池体系发展的首要问题,直接造成硫材料在放电过程中利用率较低,使得电池体系放电容量低、倍率性能差.另外,Li2S2或Li2S的电子绝缘性,也造成该电池体系的电化学可逆性差.研究表明[57],在放电过程中一旦生成较大颗粒Li2S,就会造成体系容量的不可逆衰减.
其次,硫正极在电化学反应过程中存在较大的体积膨胀收缩效应.S8密度为2.09 g/cm3,而理性状态下的放电产物Li2S密度仅为1.66 g/cm3.因此在放电过程中,硫与锂发生转化反应过程中硫正极会发生约80%的体积膨胀,于此同时锂负极溶剂造成负极体积略微减少,电池总体积净膨胀约为正极材料原体积的60%.而在充电过程中,锂离开正极重新沉积在负极中,造成正极体积缩减.因此,剧烈的体积变化始终伴随在锂硫电池充放电过程中,使得硫活性材料从导电网络上脱离,造成电池容量的不可逆衰减[58].
针对锂硫电池的研究重点仍是硫复合正极材料的研究,通过构筑导电骨架结构,负载电绝缘的硫材料,缓解反应过程中的体积膨胀并且同时能够限制多硫离子的溶解.而导电骨架的选择多集中在导电聚合物,(如PANI[59],聚吡咯[60],聚噻吩[61]等)和各种形貌的碳材料上.在这些研究工作中,碳材料,如多孔炭[62]、介孔碳[63]、碳纳米管[64]、空心碳球[64]、空心碳纤维[65]以及炭气凝胶[66]等多种形貌和结构的碳材料都被用来同硫复合,在一定程度上改善了硫正极材料的电化学性能.而石墨烯作为导电骨架材料用于硫正极复合材料则在近3年来吸引了研究人员广泛的关注,并取得较好的结果[67-69].
Ji等[67]利用GO表面的氧化性,使用原位的化学合成方法在石墨烯表面包覆一层硫单质,厚度为几纳米到十几纳米不等.该方法得到的复合材料具有相互缠绕的石墨烯导电骨架,并且S材料在石墨烯表面分散均匀,而且还原石墨烯表面官能团同硫具有一定的相互作用,从而使得该材料具有较高的容量和较稳定的循环性能,在材料中硫含量达到66%的条件下,0.02 C的充放电电流(1 C为1 675 mA/g,电流密度和容量均基于材料中硫的质量)下首圈容量可达1 320 mAh/g,0.1 C条件下循环50圈,能够稳定在954 mAh/g左右,表明材料具有稳定的循环保持率.但是由于材料中的石墨烯是由GO还原而来,并且还原程度较低,使得材料的倍率性能较差,1 C容量为550 mAh/g,而2 C下容量仅有370 mAh/g.Li等[69]报道使用热还原GO得到的热裂解石墨烯(TG)同硫进行热复合,然后用化学还原石墨烯(rGO)经液相处理包覆在复合材料(TG-S)表面得到rGO包覆TG-S的复合材料结构.这样复合材料中以TG作为导电骨架,具有足够的电导率,同时外表面包覆的rGO又能在一定程度上限制多硫离子的扩散,改善材料循环稳定性,使得材料的倍率性能和循环性能都有一定的提升.在复合材料中硫含量为63%的前提下,在充放电范围为1.0~3.0 V内测试,6.4 A/g(3.8 C)下容量可达794 mAh/g,而1.6 A/g(0.95 C)下循环200圈容量保持在667 mAh/g,可见这种石墨烯材料的设计可以很大程度提升硫材料的倍率性能和循环性能.
可见,石墨烯材料用于锂硫电池体系相比于其他碳材料具有以下优势:1) 单层石墨烯比表面积大,能够有效分散硫于表面(即使在硫含量大于60%的条件下);2) 石墨烯的二维层状结构是一种柔性的导电结构,能够缓冲硫在充放电过程中所产生的体积膨胀收缩效应;3) 石墨烯表面的π电子结构和rGO残留的官能团同硫和多硫离子之间具有电子相互作用,能有效防止充放电过程中硫从导电骨架上脱落,并限制多硫离子从正极扩散,从而改善硫材料的循环性能.由此可见,石墨烯是一种适合于锂硫电池体系的导电骨架材料,极具应用潜力.但是,当前的研究工作中,石墨烯-硫复合材料中的石墨烯多为rGO,表面残留的含氧官能团较多,降低了石墨烯的电导率,从而限制了复合材料倍率性能的提升.因而,如何设计新颖的基于石墨烯的导电骨架材料,改进石墨烯合成工艺和方法,寻找适合于硫正极的石墨烯骨架材料则是今后重要的研究方向.
2.3 石墨烯在锂-空气电池体系中的应用
锂-空气电池是一种金属-空气电池,利用锂金属在阳极氧化,氧气在阴极还原来产生电流.锂-空气电池最主要的优势就是其极高的能量密度,是电动汽车的理想动力来源.同锂离子电池的正极材料不同,锂-空气电池的正极活性材料为空气中的氧气,因此其理论上可以提供的能量密度可达到12 kWh/kg(若计算氧气质量则为3.6 kWh/kg).而内燃机中汽油的能量密度约为13 kWh/kg,扣除内燃机工作效率,其供应能量约为1 700 Wh/kg.所以,从理论上来讲,锂-空气电池足以取代内燃机成为汽车的动力来源.随着近年来新能源经济的发展,人们对环境问题关注度的提高,锂-空气电池吸引了世界上能源研究工作者广泛的关注,并取得了长足的进步和发展.
依照所使用的电解液,锂-空气电池体系设计可划分为以下4种类型:水系、有机系、水-有机混合体系和全固态体系[70].在这些锂-空气电池体系中,有机体系锂-空气电池具有的电池结构相对简单,同现有的商用锂离子电池结构相似,区别只在其碳电极(阴极)暴露在氧气或空气之中.因此,有关该体系的研究相对较为广泛,也最具应用价值.研究表明,该体系电池性能受碳阴极结构、有机电解液、氧气分压、CO2含量以及空气中的杂质等因素影响,其中碳阴极结构以及碳材料上所负载催化剂材料的种类和结构则是影响其性能的主要因素.这是由于,首先,阴极碳材料以及所负载的催化剂(贵金属,金属氧化物等)放电时催化氧气还原反应(ORR),充电时催化氧气生成反应(OER),而氧还原/生成反应则是整个电池反应的关键控速步骤,因此,由碳材料和催化剂所构成的阴极的催化性能决定了整个电池的性能;其次,氧气在阴极还原,同锂离子反应生成Li2O2并释放出容量,因而由碳材料所构成的阴极骨架所具备的孔结构所能容纳的Li2O2量则决定了锂-空气电池所具有的容量.综上所述,锂-空气电池碳阴极需要具有较高的比表面积以提供较多的反应活性位点,同时也要具有极大的孔体积以容纳反应生成的Li2O2.
二维结构的石墨烯可相互缠绕构成丰富的孔道结构,易于氧气在其中扩散,层与层之间具有较大的空间,便于容纳放电产物.而且,由石墨氧化剥离得到的还原石墨烯具有较多的边缘缺陷位、表面缺陷位以及表面官能团,这些缺陷位和官能团作为活性点位对ORR和OER反应具有一定的催化活性[71].因此,以石墨烯为骨架,或再加以负载催化剂材料,将之应用于锂-空气电池阴极的研究逐渐引起科研工作者的关注.
Zhou课题组[72]的研究结果表明石墨烯电极所显示的放电平台同20%(质量分数)碳载Pt的电位相近,说明石墨烯在所测试的有机电解液中的催化活性与碳载Pt催化剂的催化活性相当.Xiao等[73]以石墨烯构筑三维的具有不同等级孔道结构的骨架材料,并将之应用于锂-空气电池中,测试结果表明该材料所具备的特殊孔道结构为氧还原反应提供良好的三相界面,便于氧气扩散,同时也能容纳足够的放电产物,使得其具有高达15 000 mAh/g(基于石墨烯质量计算)的放电容量.Wang等[74]使用泡沫镍为基底,将氧化石墨下凝胶负载于泡沫镍中,经冻干处理后在800 ℃氮气中煅烧,从而得到以泡沫镍支持的石墨烯电极,该电极中材料具有多级孔道结构,并且无需黏结剂黏接,从而消除了黏结剂对材料性能的影响.该电极的性能测试显示,归功于其独特的电极结构设计和独有的石墨烯孔道结构,其放电比容量0.2 mA/cm3电流密度下为11 060 mAh/g,当电流密度增加到2 mA/cm3(2.8 A/g)时,仍具有2 020 mAh/g的容量,是所报道的最高的锂-空气电池倍率性能.并且,该电极的充电电压平台为3.7 V左右,相较于其他碳材料4.0 V的充电平台,有了极大的降低(在相同电解液中),说明该电极具有更好的OER催化活性.除了以上介绍的以石墨烯直接作为电极材料应用于锂-空气电池体系外,石墨烯还可以负载MnO2,Co3O4以及Fe2O3等金属氧化物催化剂制备得到复合材料用于锂-空气电池中.Dong课题组[75]成功控制在石墨烯表面原位生长α-MnO2纳米棒复合材料,对氧的还原及析出具有优异的催化作用,在200 mA/g的电流密度下,放电比容量高达11 500 mAh/g.
由上述介绍可见,石墨烯用于锂-空气电池的应用研究已经取得了很好的成果,但仍面临很多的问题和挑战.一方面需要通过合理的设计石墨烯电极结构,改进石墨烯合成工艺和方法,最大限度的发挥石墨烯的优异性能;另一方面需要寻找高效的催化剂,并通过合适的复合方法将催化剂分散于石墨烯表面,以期得到具有高效催化活性的空气电极.
3 结论和展望
作为一种二维结构材料,石墨烯不仅可以构筑电子导电网络,也可实现对反应活性物种状态的设计和调控.进而改变反应的热力学和动力学,在电化学储能系统中具有十分重要的意义.自2004年首次成功制备单层石墨烯以来,石墨烯合成方法取得了巨大的突破,多种新颖高效的石墨烯合成方法不断涌现.而在石墨烯合成方面的进展也推动其在实际应用方面研究的快速发展,使得石墨烯成为近几年来的“明星”材料,吸引了众多科研领域研究人员的关注.基于石墨烯的复合材料的设计、合成和应用方面的研究也取得了长足的进步和令人瞩目的成果,同时石墨烯在储能器件方面,如超级电容器、锂硫电池以及锂-空气电池方面也展现了巨大的潜力和应用价值.但要实现其工业化应用,还面临很大的挑战和许多亟待解决的问题.
首先,当前仍然缺少一种高效、低成本的制备高质量、大面积单层石墨烯的方法.自然界中石墨来源丰富,价格低廉,以石墨为原料来制备石墨烯是石墨烯制备的理想路线.机械剥离法能够从石墨中剥离得到单层石墨烯,但由于产量低,操作繁琐,并不是理想的量产路线.从电化学储能角度而言,石墨经氧化剥离制备GO,再还原得到石墨烯,应该是一种较理想的石墨烯合成路线,并能够大规模应用于基于石墨烯的储能材料复合材料的制备.然而在GO还原过程中面临着单层石墨烯再度团聚、活性材料在石墨烯中的分散控制等问题,限制了石墨烯在储能领域的大规模应用.其次,尽管基于石墨烯的功能化复合材料能够较大幅度地改善活性物种的电化学性能.然而,这需要有效地控制复合材料中石墨烯的分散状态、活性物种和石墨烯间的相互作用等.目前这种复合材料尚难于使用普通的合成方法大量制备,多局限在实验室水平.因此,在基于石墨烯的储能复合材料方面,如何实现其对活性物种及状态的功能化调控、深入认识其相互作用及反应机理也将是一项长期艰巨的任务.
[1] Novoselov K S,Geim A K,Morozov S V,et al.Electric field effect in atomically thin carbon films[J].Science,2004,306(5696):666-669.
[2] Choi W,Lahiri I,Seelaboyina R,et al.Synthesis of graphene and its applications:a review [J].Critical Reviews in Solid State and Materials Sciences,2010,35(1):52-71.
[3] Rao C N R,Sood A K,Subrahmanyam K S,et al.Graphene:the new two-dimensional nanomaterial [J].Angewandte Chemie International Edition,2009,48(42):7752-7777.
[4] Kuilla T,Bhadra S,Yao D,et al.Recent advances in graphene based polymer composites [J].Progress in Polymer Science,2010,35(11):1350-1375.
[5] Fuhrer M S,Lau C N,Macdonald A H.Graphene:materially better carbon[J].MRS Bulletin,2010,35(4):289-295.
[6] Soldano C,Mahmood A,Dujardin E.Production,properties and potential of graphene [J].Carbon,2010,48(8):2127-2150.
[7] Sun Y,Wu Q,Shi G.Graphene based new energy materials [J].Energy & Environmental Science,2011,4(4):1113-1132.
[8] Park S,Ruoff R S.Chemical methods for the production of graphenes [J].Nature Nanotech,2009,4(4):217-224.
[9] Reina A,Jia X,Ho J,et al.Large area,few-layer graphene films on arbitrary substrates by chemical vapor deposition[J].Nano Lett,2009,9(1):30-35.
[10] Jiao L,Zhang L,Wang X,et al.Narrow graphene nanoribbons from carbon nanotubes [J].Nature,2009,458(7240):877-880.
[11] Choucair M,Thordarson P,Stride J A.Gram-scale production of graphene based on solvothermal synthesis and sonication [J].Nature Nanotech,2008,4(1):30-33.
[12] Lu X,Yu M,Huang H,et al.Tailoring graphite with the goal of achieving single sheets [J].Nanotechnology,1999,10(3):269-272.
[13] Viculis L M,Mack J J,Kaner R B.A chemical route to carbon nanoscrolls[J].Science,2003,299(5611):1361-1364.
[14] Viculis L M,Mack J J,Mayer O M,et al.Intercalation and exfoliation routes to graphite nanoplatelets [J].Journal of Materials Chemistry,2005,15(9):974-978.
[15] Hernandez Y,Nicolosi V,Lotya M,et al.High-yield production of graphene by liquid-phase exfoliation of graphite [J].Nature Nanotech,2008,3(9):563-568.
[16] Lotya M,Hernandez Y,King P J,et al.Liquid phase production of graphene by exfoliation of graphite in surfactant/water solutions[J].J Am Chem Soc,2009,131(10):3611-3620.
[17] Hummers W S,Offeman R E.Preparation of graphitic oxide [J].J Am Chem Soc,1958,80(6):1339.
[18] Stankovich S,Dikin D A,Dommett G H B,et al.Graphene-based composite materials [J].Nature,2006,442:282-286.
[19] Jeong H K,Lee Y P,Lahaye R J W E,et al.Evidence of graphitic AB stacking order of graphite oxides[J].J Am Chem Soc,2008,130(4):1362-1366.
[20] Schniepp H C,Li J L,Mcallister M J,et al.Functionalized single graphene sheets derived form splitting graphite oxide [J].J Phys Chem B,2006,110:8535-8539.
[21] Somani P R,Somani S P,Umeno M.Planer nano-graphenes from camphor by CVD [J].Chemical Physics Letters,2006,430(1/2/3):56-59.
[22] Yu Q,Lian J,Siriponglert S,et al.Graphene segregated on Ni surfaces and transferred to insulators [J].Applied Physics Letters,2008,93(11):113103.
[23] Li X,Cai W,An J,et al.Large-area synthesis of high-quality and uniform graphene films on copper foils[J].Science,2009,324(5932):1312-1314.
[24] Bae S,Kim H,Lee Y,et al.Roll-to-roll production of 30-inch graphene films for transparent electrodes [J].Nature Nanotech,2010,5(8):574-578.
[25] van Bommel A J,Crombeen J E,Van tooren A.LEED and auger electron observations of the SiC(0001) surface [J].Surface Science,1975,48(2):463-472.
[26] de Heer W A,Berger C,Wu X,et al.Epitaxial graphene [J].Solid State Communications,2007,143(1/2):92-100.
[27] Simpson C D,Brand J D,Berresheim A J,et al.Synthesis of a giant 222 carbon graphite sheet [J].Chemistry-A European Journal,2002,8(6):1424-1429.
[28] Yang X,Dou X,Rouhanipour A,et al.Two-dimensional graphene nanoribbons[J].J Am Chem Soc,2008,130(13):4216-4217.
[29] Wei D,Liu Y,Zhang H,et al.Scalable synthesis of few-layer graphene ribbons with controlled morphologies by a template method and their applications in nanoelectromechanical switches[J].J Am Chem Soc,2009,131(31):11147-11154.
[30] Chen Z,Ren W,Gao L,et al.Three-dimensional flexible and conductive interconnected graphene networks grown by chemical vapour deposition [J].Nat Mater,2011,10:424-428.
[31] Winter M,Brood R J.What are batteries,fuel cells,and supercapacitors?[J].Chem Rev,2004,104(10):4245-4270.
[32] Zhang L L,Zhao X S.Carbon-based materials as supercapacitor electrodes [J].Chemical Society Reviews,2009,38(9):2520-2531.
[33] Mayer S T,Pekala R W,Kaschmitter J L.The aerocapacitor:an electrochemical double-layer energy-storage device[J].J Electrochem Soc,1993,140(2):446-451.
[34] Pumera M.Graphene-based nanomaterials for energy storage [J].Energy & Environmental Science,2011,4(3):668-674.
[35] Stoller M D,Park S J,Zhu Y W,et al.Graphene-based ultracapacitors[J].Nano Lett,2008,8(10):3498-3502.
[36] Chen Y,Zhang X,Zhang D,et al.High performance supercapacitors based on reduced graphene oxide in aqueous and ionic liquid electrolytes [J].Carbon,2011,49(2):573-580.
[37] Wu Z S,Ren W,Gao L,et al.Synthesis of high-quality graphene with a pre-determined number of layers [J].Carbon,2009,47(2):493-499.
[38] Lü W,Tang D M,He Y B,et al.Low-temperature exfoliated graphenes:vacuum-promoted exfoliation and electrochemical energy storage [J].ACS Nano,2009,3(11):3730-3736.
[39] Du Q,Zheng M,Zhang L,et al.Preparation of functionalized graphene sheets by a low-temperature thermal exfoliation approach and their electrochemical supercapacitive behaviors [J].Electrochimica Acta,2010,55(12):3897-3903.
[40] Zhang X,Sui Z,Xu B,et al.Mechanically strong and highly conductive graphene aerogel and its use as electrodes for electrochemical power sources [J].Journal of Materials Chemistry,2011,21(18):6494-6497.
[41] Zhang L,Shi G.Preparation of highly conductive graphene hydrogels for fabricating supercapacitors with high rate capability[J].J Phys Chem C,2011,115(34):17206-17212.
[42] Zhu Y,Murali S,Stoller M D,et al.Carbon-based supercapacitors produced by activation of graphene[J].Science,2011,332(637):1537-1541.
[43] Mez G H,Ram M K,Alvi F,et al.Graphene-conducting polymer nanocomposite as novel electrode for supercapacitors [J].Journal of Power Sources,2011,196(8):4102-4108.
[44] Yu G,Hu L,Liu N,et al.Enhancing the supercapacitor performance of graphene/MnO2nanostructured electrodes by conductive wrapping[J].Nano Lett,2011,11(10):4438-4442.
[45] Prasad K R,Munichandraiah N.Fabrication and evaluation of 450 F electrochemical redox supercapacitors using inexpensive and high-performance,polyaniline coated,stainless-steel electrodes [J].Journal of Power Sources,2002,112(2):443-451.
[46] Wang H L,Hao Q L,Yang X J,et al.Graphene oxide doped polyaniline for supercapacitors [J].Electrochem Commun,2009,11(6):1158-1161.
[47] Xu J,Wang K,Zu S Z,et al.Hierarchical nanocomposites of polyaniline nanowire arrays on graphene oxide sheets with synergistic effect for energy storage[J].ACS Nano,2010,4(9):5019-5026.
[48] Wang H,Hao Q,Yang X,et al.A nanostructured graphene/polyaniline hybrid material for supercapacitors [J].Nanoscale,2010,2(10):2164-2170.
[49] Yan J,Wei T,Fan Z,et al.Preparation of graphene nanosheet/carbon nanotube/polyaniline composite as electrode material for supercapacitors [J].Journal of Power Sources,2010,195(9):3041-3045.
[50] He Y,Chen W,Li X,et al.Freestanding three-dimensional graphene/MnO2composite networks as ultralight and flexible supercapacitor electrodes [J].ACS Nano,2012,7(1):174-182.
[51] Wu Z S,Wang D W,Ren W,et al.Anchoring hydrous RuO2on graphene sheets for high-performance electrochemical capacitors[J].Advanced Functional Materials,2010,20(20):3595-3602.
[52] Dong X C,Xu H,Wang X W,et al.3D graphene-cobalt oxide electrode for high-performance supercapacitor and enzymeless glucose detection [J].ACS Nano,2012,6(4):3206-3213.
[53] Wang H,Casalongue H S,Liang Y,et al.Ni(OH)2nanoplates grown on graphene as advanced electrochemical pseudocapacitor materials [J].J Am Chem Soc,2010,132(21):7472-7477.
[54] Yan J,Fan Z,Sun W,et al.Advanced asymmetric supercapacitors based on Ni(OH)2graphene and porous graphene electrodes with high energy density [J].Advanced Functional Materials,2012,22(12):2632-2641.
[55] Noth A,Eengel M W,Siegwart R.Flying solo and solar to Mars [J].IEEE Robotics Automation Magazine,2006,13(3):44-52.
[56] Steudel R.Elemental sulfur and sulfur-rich compounds II[M].[S.l.]:Springer,2004.
[57] Ryu H S,Guo Z,Ahn H J,et al.Investigation of discharge reaction mechanism of lithium| liquid electrolyte| sulfur battery [J].Journal of Power Sources,2009,189(2):1179-1183.
[58] He X,Ren J,Wang L,et al.Expansion and shrinkage of the sulfur composite electrode in rechargeable lithium batteries [J].Journal of Power Sources,2009,190(1):154-156.
[59] Wang J,Yang J,Xie J,et al.A novel conductive polymer-sulfur composite cathode material for rechargeable lithium batteries [J].Advanced Materials,2002,14(13/14):963.
[60] Fu Y,Manthiram A.Enhanced cyclability of lithium-sulfur batteries by a polymer acid-doped polypyrrole mixed ionic—electronic conductor[J].Chemistry of Materials,2012,24(15):3081-3087.
[61] Wu F,Wu S,Chen R,et al.Sulfur-polythiophene composite cathode materials for rechargeable lithium batteries[J].Electrochem Solid-State Lett,2010,13(4):A29-A31.
[62] Liang C,Dudney N J,Howe J Y.Hierarchically structured sulfur/carbon nanocomposite material for high-energy lithium battery[J].Chemistry of Materials,2009,21(19):4724-4730.
[63] Wang J,Chew S Y,Zhao Z W,et al.Sulfur-mesoporous carbon composites in conjunction with a novel ionic liquid electrolyte for lithium rechargeable batteries [J].Carbon,2008,46(2):229-235.
[64] Rfler D S,Hagen M,Althues H,et al.High capacity vertical aligned carbon nanotube/sulfur composite cathodes for lithium—sulfur batteries [J].Chemical Communications,2012,48(34):4097-4099.
[65] Zheng G,Yang Y,Cha J J,et al.Hollow carbon nanofiber-encapsulated sulfur cathodes for high specific capacity rechargeable lithium batteries[J].Nano Lett,2011,11(10):4462-4467.
[66] He G,Ji X,Nazar L.High “C” rate Li-S cathodes:sulfur imbibed bimodal porous carbons[J].Energy Environ Sci,2011,4(8):2878-2883.
[67] Ji L,Rao M,Zheng H,et al.Graphene oxide as a sulfur immobilizer in high performance lithium/sulfur cells[J].J Am Chem Soc,2011,133(46):18522-18525.
[68] Evers S,Nazar L F.Graphene-enveloped sulfur in a one pot reaction:a cathode with good coulombic efficiency and high practical sulfur content [J].Chemical Communications,2012,48(9):1233-1235.
[69] Li N,Zheng M,Lu H,et al.High-rate lithium-sulfur batteries promoted by reduced graphene oxide coating [J].Chemical Communications,2012,48(34):4106-4108.
[70] Kitaura H,Zhou H.Electrochemical performance of solid-state lithium-air batteries using carbon nanotube catalyst in the air electrode[J].Advanced Energy Materials,2012,2(7):889-894.
[71] Wang H,Maiyalagan T,Wang X.Review on recent progress in nitrogen-doped graphene:synthesis,characterization,and its potential applications[J].ACS Catal,2012,2(5):781-794.
[72] Yoo E,Zhou H.Li-air rechargeable battery based on metal-free graphene nanosheet catalysts[J].ACS Nano,2011,5(4):3020-3026.
[73] Xiao J,Mei D,Li X,et al.Hierarchically porous graphene as a lithium-air battery electrode[J].Nano Lett,2011,11(11):5071-5078.
[74] Wang Z L,Xu D,Xu J J,et al.Graphene oxide gel-derived,free-standing,hierarchically porous carbon for high-capacity and high-rate rechargeable Li-O2batteries [J].Advanced Functional Materials,2012,22(17):3699-3705.
[75] Cao Y,Wei Z,He J,et al.α-MnO2nanorods grown in situ on graphene as catalysts for Li-O2batteries with excellent electrochemical performance [J].Energy & Environmental Science,2012,5(12):9765-9768.
