土壤活性组分提取剂的研制及初步试验结果
2014-08-02吴昆明魏朝俊梁颖博
吴昆明,魏朝俊,刘 云,梁颖博
(北京农学院,北京 102208)
目前已有大量调查结果显示,在自然和人类活动联合影响下,一些化学元素在表层土壤中出现了程度不同的累积,由此产生了大量土壤地球化学异常[1-4],评价这些地球化学异常生态效应是当前以及今后一段时期内地球化学调查评价工作面临的紧迫而艰巨的任务。已有研究结果表明,在土壤地球化学异常评价工作中,相对于土壤的元素全量而言,其活性组分能够更好地反映土壤实际污染状况及其对环境的危害水平。元素的活性组分含量是环境地球化学调查与评价工作的关键技术指标,而对土壤活性组分的测试通常采用各种土壤浸提剂。浸提剂不同,测定的含量差异很大,因此选择适当的土壤浸提剂是准确评价土壤活性组分的关键技术。目前我国有关土壤浸提剂的应用研究较多,而研制有关土壤浸提剂相对滞后,研制适应各种类型土壤的通用提取剂成为本研究的基础。
国外对通用型提取剂的研究始于20世纪70年代末80年代初,其中具有代表性的是Mehlich 3提取剂[5-8],Mehlich 3可显著提取活性P[4],同时可提取活性Ca、Mg、Na、S,提取方法简便,但对活性K的提取效果不佳,对重金属元素的提取测试结果差异也较大。另一种提取剂是AB-DTPA,它对重金属活性组分提取结果稳定,但只适用于碱性土壤,对酸性土壤的提取效果较差[9-12]。盐酸提取剂常用来评估酸性土壤中植物对重金属元素的吸收情况,盐酸萃取土壤中重金属的机理是H+的交换作用以及对土壤矿物组分的风化作用,适合酸性土壤中大多数重金属元素有效态的提取。马建军等[13]的提取试验表明,盐酸提取剂提取的褐土有效态Ni量与小麦茎叶吸收Ni量之间呈极显著的正相关。刘玉荣等[14]研究发现,植物体内的元素Cd、Zn与提取剂醋酸提取的土壤有效态Cd、Zn有较好的相关性。
1979年由Tessier等[15]提出的沉积物中重金属形态分析的五步连续提取法已广泛应用于土壤样品的重金属形态分析[16],将金属元素分为离子交换态、碳酸盐结合态、铁锰氧化物结合态、有机物结合态以及残渣态,提取相态准确但步骤繁琐,过程周期长,各种相态在进行生态效应评价时存在的问题是,离子交换态的活动性比较高,容易被植物直接吸收,而碳酸盐结合态、有机物结合态、铁锰氧化物结合态在一定环境条件下,其中的一部分也可以对农作物产生影响,因此无法用于生态效应评价。我国勘查地球化学领域主要采用相态分析的方法研究土壤元素特别是重金属元素的存在形态,将重金属元素的存在形态分为水溶态、离子交换态、碳酸盐结合态、有机物结合态、铁锰氧化物态及残渣态等,进行分布连续提取,具有五步连续提取相态分析的相同局限。农业部门广泛采用的营养组分有效态提取方法,针对不同的元素组分采用不同的提取剂,测试结果准确,但由于测试方法分类过细,效率低,成本高,一份土壤样品要用不同提取剂多次提取,给大范围推广应用带来困难。
本文从丰富土壤中活性组分提取剂分析方法出发,针对提取剂的通用性,借鉴已有提取剂的化学组成特点及提取剂组分在提取剂中的作用,研制了一种新型活性组分提取剂——AIE(Activated Ions Extractant),以提高提取剂的缓冲能力和扩大元素的提取效果及适应的土壤类型。本研究以国家标准物质作为试验样品,将AIE提取有效态P、K、Mn、Cu,评价新型提取剂的适用性。将试制的AIE提取剂提取盐基离子(K、Na、Ca、Mg),Fe、Mn、P,重金属元素(Cd、Cu、Pb、Cr、Hg),并与三种通用型提取剂(Mehlich 3、AB-DTPA、盐酸)的结果进行比较,评价AIE的提取效果。同时用AIE对同一土壤进行多次提取测定,考察新型提取剂的重现性和实际应用的稳定性,为其在大面积土壤地球化学异常生态效应评价研究工作中的推广应用奠定基础。
1 AIE提取剂的研制和主要机理
研制AIE通用型提取剂的基本原则是,提取剂要满足对土壤中多个评价指标的活性组分进行同时提取的要求。从提取指标上说,通用型提取剂既要提取作物营养组分,又要提取重金属元素。从提取物组成上说,通用型提取剂提取的既是相态分析的活性部分,又包含有效态分析的有效态部分,因此通用型提取剂及其提取物的含义更加广泛。为了便于叙述和对比,本次研究将使用通用型提取剂提取出的土壤组分统称为土壤活性组分,并认为这部分组分可以产生直接的生物效用。
1.1 AIE提取剂的组成和配制方法
AIE提取剂的组成:0.25 mol/L醋酸,0.25 mol/L醋酸铵,0.005 mol/L DTPA,0.2%对苯二酚。
AIE提取剂的配制:称取1.97 g二乙三胺五乙酸(DTPA)溶解于800 mL蒸馏水中,称取79.06 g醋酸铵加入此溶液中,将其完全溶解后加入2 g对苯二酚和15.2 mL醋酸,用蒸馏水稀释至1 L。(现用现配,如需储存用时再加入2 g对苯二酚)。
所用试剂均为分析纯以上试剂;实验用水为二次蒸馏水。
1.2 AIE提取剂的主要机理和性能

DTPA是一种金属螯合剂[17],主要用于提取重金属组分。DTPA可以与金属离子(Zn、Fe、Mn、Cu)螯合,形成的螯合物具有很高的稳定性,从而减少了溶液中金属离子的活度,使土壤固相表面结合的金属离子解吸而补充到溶液中,因此在溶液中积累的螯合金属离子的量是土壤溶液中金属离子的活度(强度因素)和这些离子由土壤固相解吸补充到溶液中的量(容量因素)的总和。
对苯二酚具有还原作用,可以增加活性铁锰氧化物结合态的提取,以这种相态存在的元素为可释放的部分缓效态。
2 AIE提取剂的通用性评价
本实验选取国家标准物质作为实验土壤,该样品已有用国家标准方法测定的有效态磷、有效态钾、有效态锰、有效态铜的准确数值。现用试制的AIE提取剂提取土壤中活性组分P、K、Mn、Cu,提取结果与国家标准物质有效态的标准值进行对比,评价新型提取剂的通用性。
2.1 土壤样品特性
试验用土壤样品为土壤有效态成分分析国家标准物质。土壤的特性列于表1。
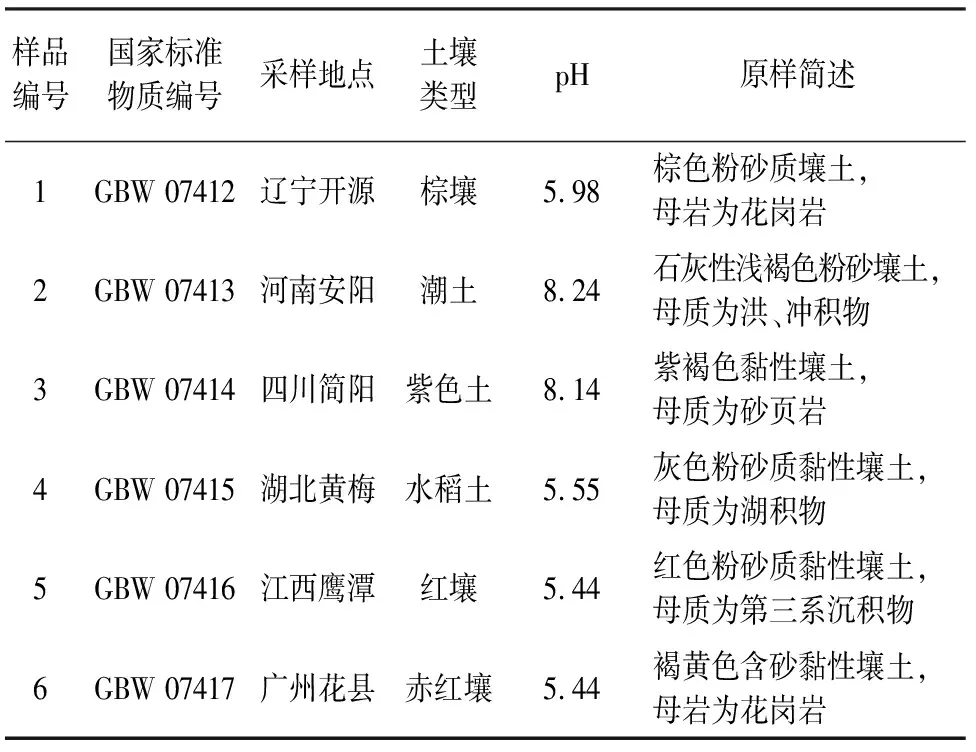
表1 土壤样品特性
2.2 元素有效态测定的国家标准方法
有效磷:用氟化铵、稀盐酸浸提-钼锑抗比色法测定酸性土,国家标准号:GB7853-87。碳酸氢钠浸提-钼锑抗比色法测定碱性土(石灰性土),国家标准号:GB12297-90。
速效钾:用乙酸铵浸提-原子吸收光谱法测定,国家标准号:GB7856-87。
有效锰:用对苯二酚-乙酸铵浸提-原子吸收光谱法测定,国家标准号:GB7883-87。
有效铜:用DTPA浸提-原子吸收光谱法测定碱性土(石灰性土),稀盐酸浸提-原子吸收光谱法测定酸性土,国家标准号:GB7879-87。
2.3 AIE浸提法与国家标准方法的结果比较
本研究试制的土壤活性组分提取剂AIE,所提取的元素组分是直接产生生物效用的元素部分,不是简单的有效态或相态分析中的任意一种相态,因此无法定量地找到可定义的准确数值。现将研制的提取剂提取P、K、Mn、Cu的数值与国家标准方法测定的标准值进行比较。
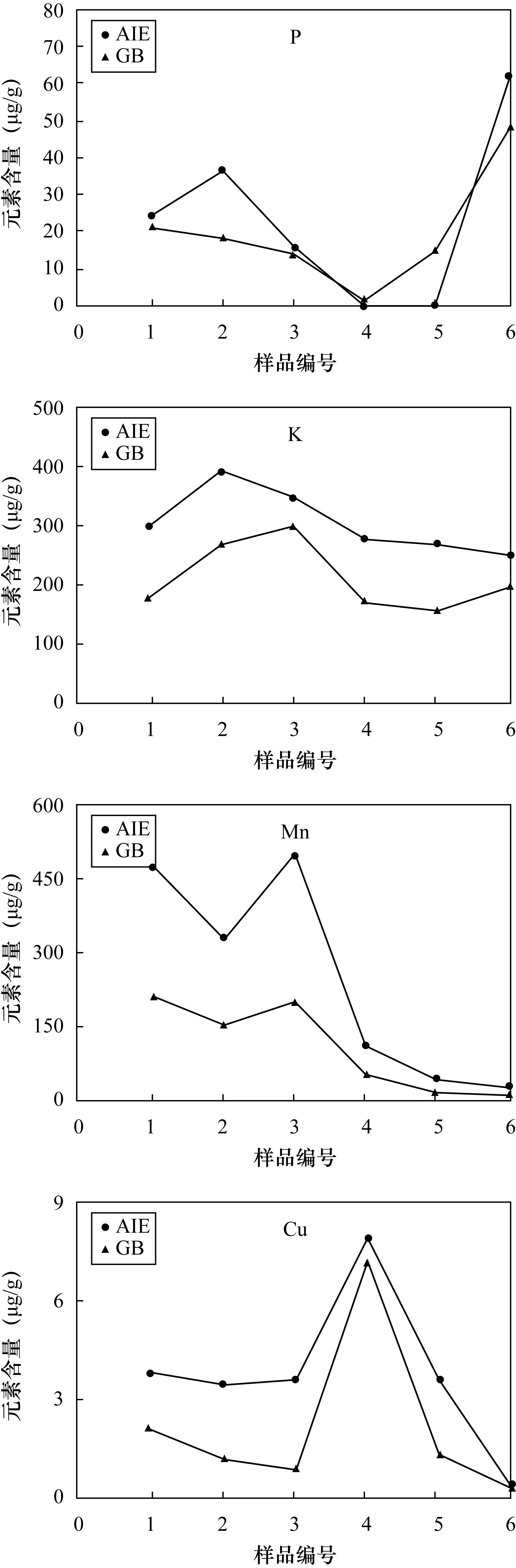
图1 两种提取液中部分离子的含量
按1.1节和2.2节步骤进行实验,以表1的样品编号为横坐标,以元素含量为纵坐标作图,部分离子的提取量变化曲线如图1所示。从图1可以看出,AIE提取剂与国家标准方法对比有很好的相关性。由于有效态是已经验证的对植物生长产生直接影响的元素部分,其土壤提取元素数值与植物体中含量数值有很好的相关性,可以推知研制的AIE提取剂也可与该数值有很好的相关性。另外,所有样品中除了一个样品(5号样品P的提取量),用AIE提取的元素含量均要高于国家标准方法提取的含量,这是由于研制提取剂AIE同时考虑了对土壤中有效态元素和部分缓效态元素的提取。而土壤中的缓效态组分对评价作物营养组分潜力具有较好的指示意义,在重金属元素预警研究中也可发挥一定作用。同时,由于所选择的试验土壤为不同地区、不同类型的土壤,国家标准方法测定有效态时是按照不同的土壤类型选择的分析方法,而研制的提取剂AIE对元素的提取没有受到土壤类型的影响,均表现很好的相关性,可以基本判定其通用性较好。
3 AIE提取剂与通用型提取剂比较
由于所提取的活性组分是土壤中可以对动植物产生生态效应的元素部分,是可以直接对生物产生影响的有效态和在一定时间内可释放的缓效态,并不是严格意义上的有效态也不是相态分析中的任意一种相态。因此对研制的提取剂的评价,需用有效态及国内外常用的提取剂提取结果进行相关性比较,而不是定量比较。
本实验将试制的AIE提取剂提取盐基离子(K、Na、Ca、Mg),Fe、Mn、P,重金属元素(Cd、Cu、Pb、Cr、Hg),获得的数据与三种通用型提取剂(Mehlich 3、AB-DTPA、盐酸)的结果进行比较,评价AIE的提取效果。
3.1 三种通用型提取剂试剂的配制
Mehlich 3提取剂的配制:将0.556 g氟化铵和0.292 g EDTA加入800 L蒸馏水中,称取20.01 g硝酸铵加入此溶液,再加入12 mL醋酸和0.82 mL硝酸。蒸馏水稀释至1 L。
AB-DTPA提取剂的配制:称取1.97 g的DTPA溶解于800 mL蒸馏水,加入2 mL 50%的氨水,称取79.06 g碳酸氢铵加入此溶液中,将其完全溶解,用氨水或盐酸将pH值调为7.6,蒸馏水稀释至1 L (在矿物油下保存)。
盐酸提取剂的配制:取9 mL浓盐酸,用水定容至1 L。
所用试剂均为分析纯以上试剂,实验用水为二次蒸馏水。
3.2 AIE和三种通用型提取剂待测液的制备
各种提取剂对土壤活性组分进行提取时需要使土壤的状态保持一致,待测液制备的步骤基本相似,以减小系统误差。通用型提取剂在浸提时土壤和提取剂比例参照其已有方法,新型提取剂在浸提时土壤和提取剂比例选取固液比较小的5.000 g土壤溶于50 mL提取剂,目的是最大程度地提取土壤活性组分。
AIE待测液的制备:准确称取5.000 g经室温自然风干、过80目尼龙筛的土壤样品于100 mL聚乙烯瓶中,加入50 mL的AIE浸提液,间歇振荡提取2 h,过滤后待测。过滤不完全的可用离心机离心10 min,弃去残渣。
Mehlich 3待测液的制备:准确称取5.000 g经室温自然风干、过80目尼龙筛的土壤样品于100 mL聚乙烯瓶中,加入50 mL的Mehlich 3浸提液间歇振荡提取2 h,过滤后待测。过滤不完全的可用离心机离心10 min,弃去残渣。
盐酸待测液的制备:准确称取10.000 g经室温自然风干、过80目尼龙筛的土壤样品于100 mL聚乙烯瓶中,加入50 mL盐酸浸提液,间歇振荡提取2 h,过滤后待测。过滤不完全的可用离心机离心10 min,弃去残渣。
AB-DTPA待测液的制备:准确称取20.000 g经室温自然风干、过80目尼龙筛的土壤样品于100 mL聚乙烯瓶中,加入40 mL的AB-DTPA浸提液,间歇振荡提取2 h,过滤后待测。过滤不完全的可用离心机离心10 min,弃去残渣。
3.3 盐基离子与重金属离子的测定方法
分取15 mL待测液于100 mL聚四氟乙烯烧杯中,加入2 mL硝酸、1 mL氢氟酸、1 mL高氯酸,在电热板上加热至白烟冒尽,加5 mL王水使其完全溶解,定容至25 mL,稀释10倍后,用Element XR型高分辨率电感耦合等离子体质谱法(HR-ICP-MS,美国ThermoFisher公司)测定Cd、Cu、Pb、Fe、Mn、P、Ca、Mg、K、Na、Cr含量。取10 mL待测液,用XDY-1101A原子荧光光谱仪(北京地质仪器厂研制)直接测定Hg的含量。
3.4 提取剂的提取效果比较
在国外较多的Mehlich 3和AB-DTPA研究中,Ostatek等[1]应用Mehlich 3评价澳大利亚土壤中的营养物质,土壤中Ca、Mg、Na、S、Mn的含量和作物中的含量有很好的相关性,而且Mehlich 3的提取效果优于0.1 mol/L盐酸的提取效果。Rodriguez-Suarez等[18]认为EDTA-醋酸铵和Mehlich 3可以有效提取酸性土壤中的有效P、K、Ca、Mg、Cu、Zn和Fe,其中Mehlich 3对Cu的提取量要高于EDTA-醋酸铵提取量的20%,而AB-DTPA的提取效果较差。Madurapperuma等[2]研究表明用AB-DTPA提取酸性水稻土时,其对K、Na、Mn、Fe的提取量同植物吸收量相关性好,而Ca、Mg的相关性较差。由于不同土壤状态下不同提取剂的表现情况不一致,无法用单一提取剂评价新型提取剂的实用性,因此将新型提取剂的提取结果与Mehlich 3、AB-DTPA和盐酸的提取结果进行定性分析。
3.4.1K、Na、Ca、Mg(盐基离子)
按1.1、3.1、3.2、3.3节步骤进行实验,以表1的样品编号为横坐标,以元素含量为纵坐标作图,作物营养组分盐基离子(K、Na、Ca、Mg)的提取量变化曲线如图2所示,从图2可以看出,AIE与Mehlich 3的提取量变化规律基本一致;AIE对Na、Ca的提取量高于其他提取剂,对K、Mg的提取量与Mehlich 3的提取含量相差不大。因Mehlich 3提取剂中加入了氟化铵,目的是增强对P组分的提取,但是容易产生CaF2沉淀从而影响Ca的提取效果。AIE对碱性土壤中Ca的提取量高于Mehlich 3和盐酸提取量的2~3倍,AB-DTPA对Ca的提取量极低,是由于AB-DTPA的pH值为碱性,不利于Ca的释放。盐酸对于Mg、Ca的提取变化趋势与AIE和Mehlich 3一致,但对Na、K的提取量与其他提取剂相比,无太大相关性。可见,在四种元素的提取中,AIE的提取效果总体上优于其他三种提取剂。
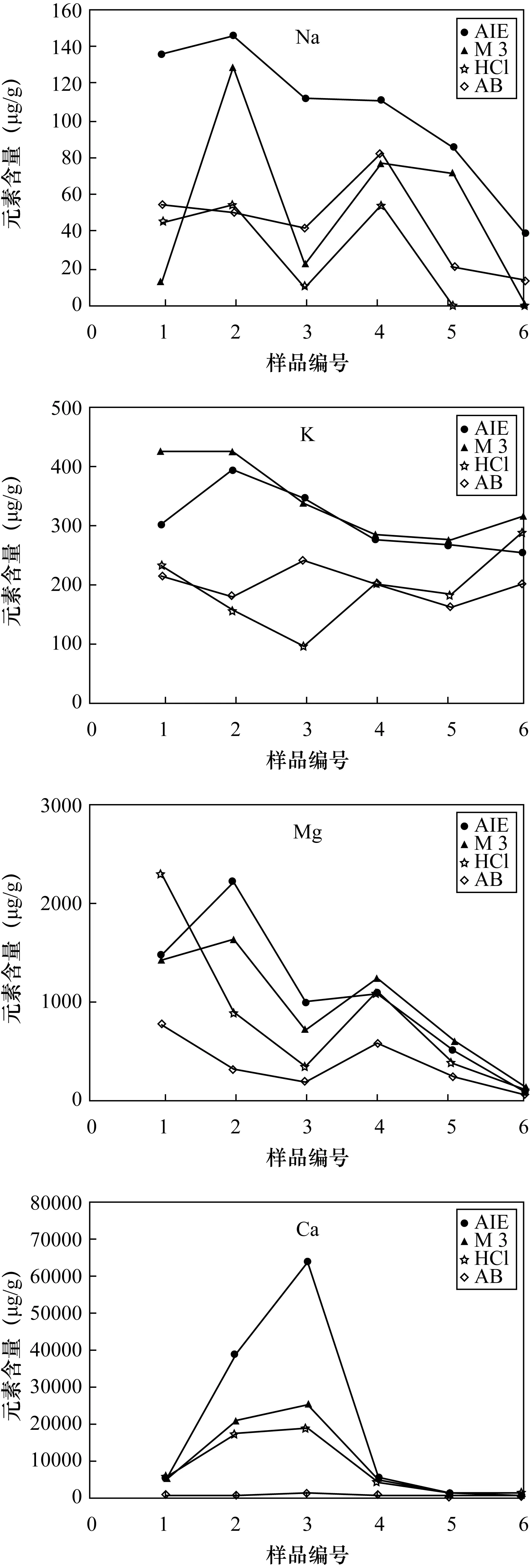
图2 四种提取液中盐基离子的含量
3.4.2 Fe、Mn、P
作图方法同3.4.1节,Fe、Mn提取量的变化如图3所示。AIE对土壤中Fe提取量的变化趋势与另外三种提取剂的变化趋势基本相同。1、4号样品显示,AIE对Fe的提取量为其他提取剂提取的2倍,是由于AIE中含有对苯二酚,增强了对活性(铁)锰氧化物的提取,符合设计理念。4、5、6号样品显示,四种提取剂对Mn的提取量接近,分别为53 μg/g、17 μg/g、11 μg/g左右,表明这三种土壤中缓效态Mn的含量较低。而对1、2、3号样品,AIE的提取量要高于其他三种提取剂,且在上述2.3节AIE与国家标准方法提取有效态Mn比较结果显示两者变化趋势一致。可以认为,AIE对土壤中活性Fe、Mn组分具有更好的提取效果。
Mehlich 3在设计提取元素时重点考虑了对P的提取,从图3可以看出Mehlich 3对P的提取量确实要高于其他提取剂。AIE对P的提取量与Mehlich 3相差不大,且对照上述2.3节国家标准方法提取有效态P的数值,AIE的数值与其更为接近。1、2、3号样品显示,盐酸和AB-DTPA对Mn的提取量较低,提取效果较差,尤其是盐酸对P的提取量偏低,提取效果差。总之,对于Fe、Mn、P元素,AIE的提取效果明显优于其他三种提取剂。
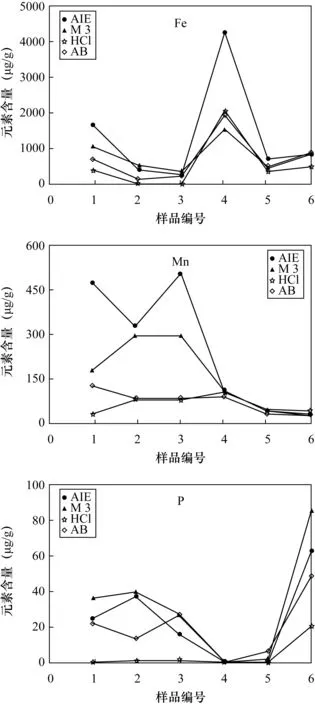
图3 四种提取液中Fe、Mn、P的含量
3.4.3 重金属元素
重金属元素对生物及环境危害较大。在土壤地球化学异常生态效应评价工作中,Hg、Cd、Pb、Cr、Co、Ni及 As等多种指标需要研究,但是这些指标的有效态并没有标准的提取和测试方法,更没有可以参考的标准值,因此缺乏判别试制提取剂对这些组分是否有效的直接证据。在这种情况下,本实验引进了国外相对成熟的两种提取剂(AB-DTPA、Mehlich 3),通过对比AIE和AB-DTPA、Mehlich 3、盐酸的提取效果来确定试制新型提取剂提取重金属组分的可行性。
已有研究表明,AB-DTPA提取剂主要针对的是P、K、Na、Fe、Mn、Zn、Cd、Pb等组分,除前面已经讨论的P、K、Fe、Mn、Zn、Na以外,此处可以对比的组分只有Cd和Pb。作图方法同3.4.1节,提取液中重金属元素含量的变化如图4所示。从图4可以看到,AIE对Cd的提取量明显高于或接近于AB-DTPA的提取量;对各样品中Pb、Cd提取量的变化趋势总体上与Mehlich 3相似,但是绝对提取量不同,以AIE的提取量较大;对Hg的提取,1、3、5号样品AIE的提取量与AB-DTPA提取量接近,2、4、6号样品相差较大;而2、4、6号样品AIE提取量与Mehlich 3提取量接近;对Cr的提取,除4号样品AIE提取量略低于Mehlich 3以外,其他样品的AIE提取量均高于AB-DTPA、Mehlich 3、盐酸。
由于对土壤中的重金属提取没有权威的判别标准,现将三种应用较多的提取剂的提取效果同研制的提取剂的提取效果进行比较。多数情况下各种提取剂的提取效果均具有一定的可比性。所有提取剂对供试的6件样品提取量总体的变化趋势相似,其中AIE的提取量多数高于其他提取剂,表现为既可提取有效态又可提取缓效态。因此可以认为AIE能够有效提取土壤的重金属活性组分,其提取结果均优于AB-DTPA和Mehlich 3、盐酸提取剂。
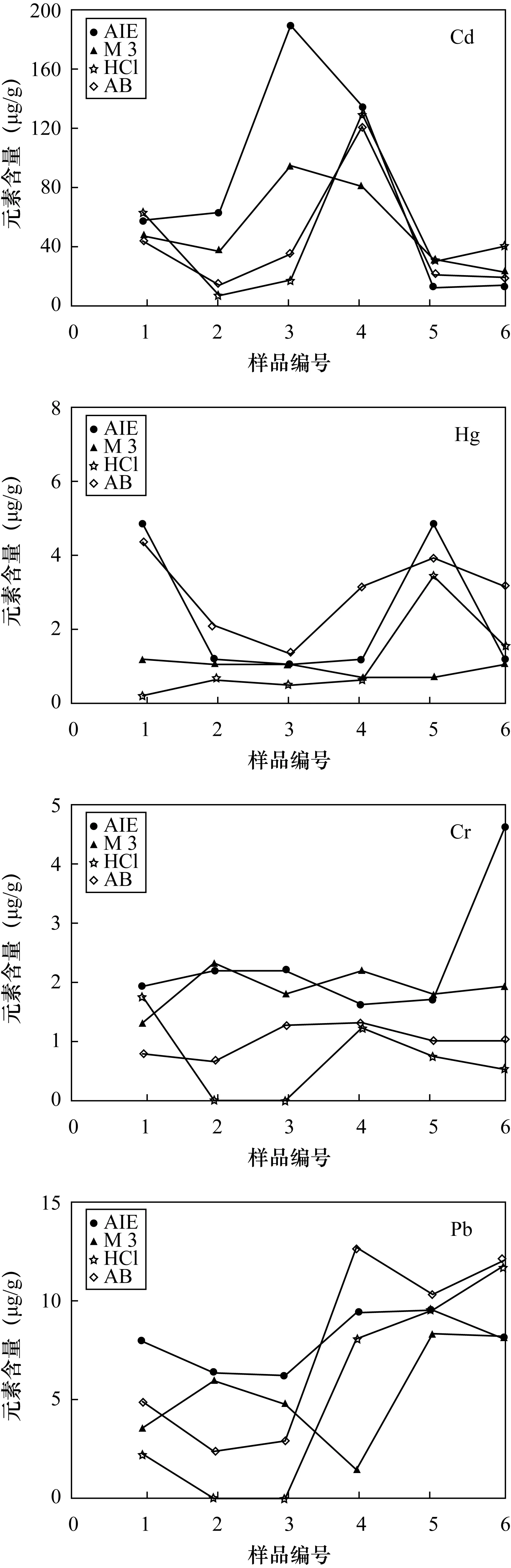
图4 四种提取液中重金属离子的含量
4 AIE提取剂的缓冲能力和重现性
土壤的pH值不同,对提取剂的提取量有较大影响。如果在提取前后提取液的pH值变化较小,可认为该提取剂具有缓冲性。如在具有很好的缓冲能力的前提下,保持提取液在弱酸性条件下,提取剂将增强离子交换态和吸附性的其他组态的提取。本实验记录了AIE、Mehlich 3、AB-DTPA浸泡前后溶液的pH值变化,考察AIE的缓冲效果。并对同一土壤进行多次提取测定,对结果进行重现性比较,考察其实际应用的稳定性。
4.1 AIE提取剂的缓冲能力
国内外相关研究可知,土壤理化性质对土壤重金属提取效果有很大影响,其中pH值影响尤为突出。王鹏新等[19]研究发现,pH对DTPA(0.005 mol/L)提取Ni有直接的正影响。贺建群等[20]研究发现,各提取剂提取灰钙土的Cd、Cu、Zn 量均与pH 值呈明显负相关。Mann等[21]试验结果表明,CaCl2(0.01 mol/L)、EDTA(0.005 mol/L)及盐酸(0.1 mol/L)对Cd的提取量分别与土壤pH呈显著负相关。因此,同一提取剂提取不同类型土壤中的元素时,pH值发生较大变化,重金属的提取率差异就大。
由于交换剂溶液的pH是影响阳离子交换量的重要因素,阳离子交换量是由土壤胶体表面的净负电荷量决定的。无机、有机胶体的官能团产生的正负电荷和数量则因溶液的pH和盐溶液浓度的改变而变动。实际上,提取剂的pH值及其缓冲能力对提取效果的影响是一个复杂的过程,本实验关注的只是提取剂对不同酸碱度土壤的通用性。
本实验中土壤样品pH值、提取剂pH值及加入提取剂后提取液的pH值列于表2。从表2可以看出,与AIE提取剂的pH值相比较,AIE提取液的pH值升高,而且碱性土壤提取液的pH值升高幅度较酸性土壤略大,但升高幅度(0.07~0.9)均未超过缓冲溶液的缓冲范围,保持在弱酸性环境。Mehlich 3提取液的pH值普遍较低,虽未超过缓冲溶液的缓冲范围,但对碱性土壤活性组分的提取会产生一定影响。AB-DTPA提取液的pH值受到原提取剂pH值的影响仍为碱性,不利于酸性土壤活性组分的提取。由此基本可以判定新型提取剂AIE的缓冲能力强,适用于酸性和碱性土壤,其通用性优于Mehlich 3和AB-DTPA提取剂。
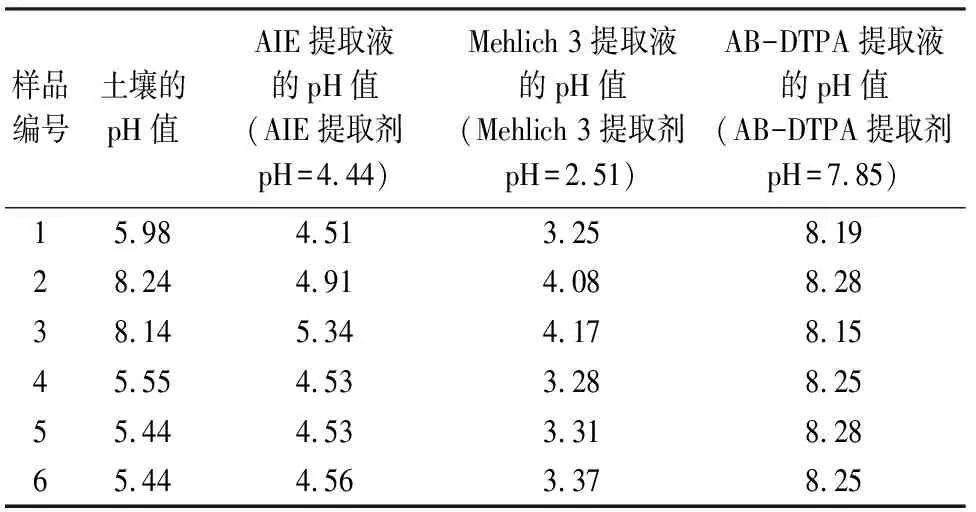
表2 土壤、提取剂及提取液的pH值
4.2 AIE提取剂的重现性
在已有相态分析和有效态分析中,存在的一个问题是样品重复分析的重现性普遍不好[22],从而在一定程度上限制了提取方法的实际应用。本次试验采用实际调查样品,对试制的AIE提取剂进行重现性检验,结果列于表3。在相同试验条件下,AIE提取剂对Cd、Cr、Cu、Pb、Hg、Mn等重金属元素及Ca、K、Mg、Na等常量组分提取结果的重现性均令人满意。表现在经重复分析的样品,除了Na以外,其他元素提取量测定结果的相对标准偏差均低于8%,各元素活性组分的含量差异不大,为实际应用奠定了基础。
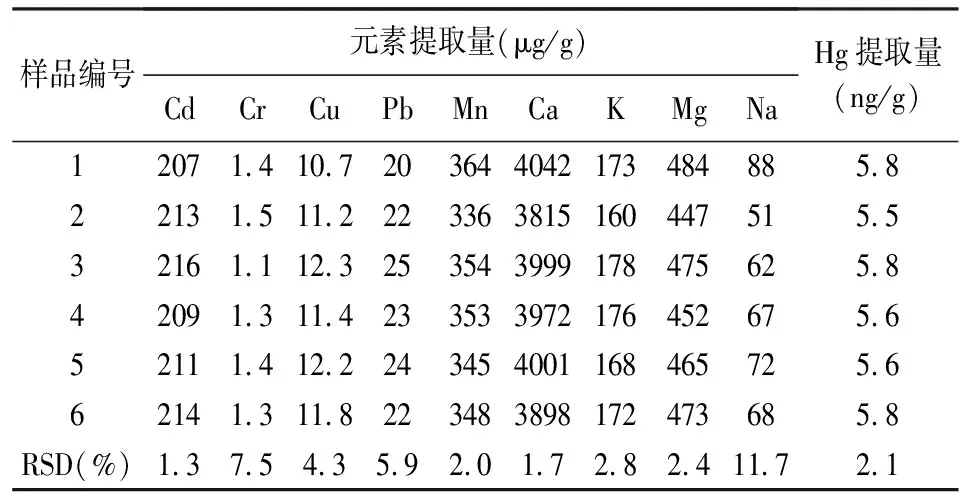
表3 试制提取剂重现性检验结果
5 结语
本研究充分借鉴了已有提取剂的化学组成特点及各组分在提取剂中的作用,综合考虑了土壤中农作物营养和环境评价指标的存在形式特点,同时重视提高提取剂的缓冲能力,研制了一种新型土壤活性组分提取剂——AIE。通过与国家标准方法和某些多元素提取剂(Mehlich 3、AB-DTPA和盐酸)提取效果的对比,AIE显示出对元素的提取没有受到土壤类型的影响,均表现很好的相关性,可以判定其通用性较好;且AIE的提取效果优于其他提取剂,表现为既可提取有效态又可提取缓效态。AIE具有广泛的适用性,缓冲能力强,适用于酸性和碱性土壤,也适用于营养组分和重金属元素,而且样品的前期处理和分析测试等环节大大简化。
AIE的重现性好,基本上能够满足土壤地球化学异常生态效应评价的需求。但由于土壤中的活性组分因提取剂的不同其提取量差异较大,因此不能单纯依据提取剂提取出的活性组分的量来确定提取剂对土壤地球化学异常生态效应评价工作的适用性,而需要结合农作物的生态效应等开展更深入的研究,这也正是本研究进一步的发展方向。
6 参考文献
[1] Ostatek B,Zofia A.Evaluation of Mehlich 3 as a universal nutrient extractant for Australian sugarcane soils[J].CommunicationsinSoilScience&PlantAnalysis,2012,43(4):623-630.
[2] Madurapperuma W S,Kumaragamage D.Evaluation of ammonium bicarbonate-diethylene triamine penta acetic acid as a multinutrient extractant for acidic lowland rice soils[J].CommunicationsinSoilScience&PlantAnalysis,2008,39(11/12):1773-1790.
[3] Alam M G M,Tokunaga S,Stagnitti F.Removal of arsenic from contaminated soils using different salt extractants[J].JournalofEnvironmentalScience&Health,2007,42(4):447-451.
[4] Mehlich A.Mehlich 3 soil test extractant:amodification of Mehlich 2 extractant[J].CommunicationsinSoilScience&PlantAnalysis,1984,15(12):1409-1416.
[5] Niaz A A,Waqar Z M H,Ranjha A M.Relative eff-iciency of different extractants for available boron estimation in alkaline calcareous soils[J].CommunicationsinSoilScience&PlantAnalysis,2011,42(16):1934-1944.
[6] Zarrabi M,Jalali M.Evaluation of extractants and qua-ntity intensity relationship for estimation of available potassium in some calcareous soils of Western Iran[J].CommunicationsinSoilScience&PlantAnalysis,2008,39(17):2663-2677.
[7] Haney R,Haney E,Hossner L,Arnold J.Development of a new soil extractant for simultaneous phosphorus,ammonium,and nitrate analysis[J].CommunicationsinSoilScience&PlantAnalysis,2006,37(11):1511-1523.
[8] Haney R L,Haney E B,Hossner L R.Modifications to the new soil extractant H3A-1: A multinutrient extractant[J].CommunicationsinSoilScience&PlantAnalysis,2010,41(12):1513-1523.
[9] Narayanaswamy C,Prakash N B.Evaluation of selected extractants for plant-available silicon in rice soils of Southern India[J].CommunicationsinSoilScience&PlantAnalysis,2010,41(8):977-989.
[10] Subirés-Muňoz J D,García-Rubio A,Vereda-Alonso C,Gómez-Lahoz C,Rodríguez-Maroto J M.Feasibility study of the use of different extractant agents in the remediation of a mercury contaminated soil from Almaden[J].Separation&PurificationTechnology,2011,79(2):151-156.
[11] Pauget B,Gimbert F,Scheifler R,Coeurdassier M.Soil parameters are key factors to predict metal bioavailability to snails based on chemical extractant data[J].ScienceoftheTotalEnvironment,2012,431(13):413-425.
[12] Giri P K,Bhattacharyya K,Sinha B,Mazumdar D.Study of the suitability of selected extractants for determination of plant-available arsenic in some inceptisols of West Bengal,India[J].CommunicationsinSoilScience&PlantAnalysis,2012,43(19):2449-2466.
[13] 马建军.褐土中有效态镍提取剂及提取条件的选择[J].河北农业技术师范学院学报,1999,13(2):10-14.
[14] 刘玉荣,党志,尚爱安.几种萃取剂对土壤中重金属生物有效部分的萃取效果[J].土壤与环境,2002,11(3):245-247.
[15] Tessier A,Campbell P G C,Bisson M.Sequential extra-ction procedure for the speciation of particulate trace metals[J].AnalyticalChemistry,1979,51(7):844-851.
[16] Marika K,Markku Y H.Use of sequential extraction to assess metal partitioning in soils[J].EnvironmentalPollution,2003,126(2):225-233.
[17] Speir T W,Schaik A P V,Percival H J.Heavy metals in soil,plants and groundwater following HIGH-RATE sewage sludge application to land[J].Water,Air,andSoilPollution,2003,150(1-4):319-358.
[18] Rodriguez-Suarez J A,Arias M,Lopez E,Soto B.Comparison of multi-element to single-element extractants for macro-and micronutrients in acid soils from Spain[J].CommunicationsinSoilScience&PlantAnalysis,2008,39(1/2):231-240.
[19] 王鹏新,曲尔复.嵝土中可给态镍浸提方法的研究[J].环境科学学报,1993,13(2):223-231.
[20] 贺建群,许嘉琳,杨居荣.土壤中有效态Cd、Cu、Zn、Pb提取剂的选择[J].农业环境保护,1994,13(6):246-251.
[21] Mann S S,Rate A W,Cilkes R J.Cadmium accumu-lation in agricultural soils in Western Australia[J].Water,Air,and Soil Pollution,2002,141(1-4):281-297.
[22] Huang Z Y,Chen T,Yu J,Zeng X C,Huang Y F.Labile Cd and Pb in vegetable-growing soils estimated with isotope dilution and chemical extractants[J].Gendarme,2011,160(3-4):400-407.
