松补力口服液总多酚及总多糖的测定
2014-07-14卢晓丽周晓英
刘 波,卢晓丽,周晓英
(新疆医科大学1中医学院,2药学院,乌鲁木齐 830011)
松补力口服液由甘松单味药组成。该方收载于《中华人民共和国卫生部药品标准·维吾尔药分册》,其具有养心、安神、增强胃功能的功效,用于治疗心悸、神经衰弱、腹痛、胃病等疾病的口服液体制剂[1]。
植物多酚类化合物在自然界分布广泛,具有抗氧化、清除自由基、与金属离子发生络合、与蛋白质形成多种生理学活性物质[2],是有效的肿瘤化学预防剂[3],有些多酚类化合物本身也具有抗肿瘤作用[4]。
在《中国药典》[5]2010版中仅对甘松药材进行了甘松新酮的薄层鉴别,原标准中没有对松补力口服液进行总多酚及总多糖的含量测定。为了完善该制剂质量标准,更好地控制该产品质量,本研究对松补力口服液中的总多酚及总多糖含量进行测定,建立测定方法,以控制其质量。
1 仪器与试药
1.1 仪器 U-3310紫外可见分光光度计(日本株式会社日立高新技术),KQ2200DE型数控超声波清洗器(昆山市超声仪器有限公司),AL204电子天平(梅特勒-托利多仪器有限公司)。
1.2 实验材料 原料:10批不同批号甘松制备的松补力口服液。试剂:5%亚硝酸钠溶液、10%硝酸铝溶液、4%氢氧化钠溶液、钨酸钠、钼酸钠、磷酸、浓盐酸、硫酸锂、双氧水、甲醇均为分析纯,实验用水为自制蒸馏水。没食子酸对照品(天津市光复精细化工研究所,含量99%),无水萄萄糖(上海实验试剂有限公司)。
2 方法与结果
2.1 试剂的制备 福林酚试剂的制备[6]:称取钨酸钠100.0g、钼酸钠25.0g,用700mL蒸馏水溶解于圆底烧瓶中,加入磷酸(≥85%)50mL和100mL浓盐酸充分混匀,小火加热回流12h,放冷,再加入150g硫酸锂、50mL蒸馏水及0.2mL双氧水,开口继续沸腾15min,使得双氧水完全挥发,冷却后用蒸馏水定容至1000mL,过滤,于棕色瓶中避光储存。试液应呈亮黄色,如放置后变为绿色,可加双氧水0.2mL,煮沸15min即可。
对照品储备溶液制备:精密称取葡萄糖标准品0.03004g置100mL容量瓶中,用蒸馏水定容,制成浓度为0.3mg/mL总多糖对照品储备溶液。精密称取0.0101g没食子酸对照品于100mL容量瓶中,用蒸馏水定容,制成浓度为0.101mg/mL总多酚对照品储备溶液。
2.2 供试品制备
2.2.1 总多酚供试品溶液制备 取口服液3mL用水稀释到100mL并定容。取2.0mL加4.0mL水,然后加0.5mL福林酚试剂,最后加1.5mL的20%Na2CO3混匀,加水定容,75℃加热10min,备用。
2.2.2 总多糖供试品溶液制备 取口服液10mL加30mL无水乙醇过夜,离心。分别用无水乙醇、丙酮洗3次,每次10mL。滤渣加适量水溶解,并定容到100mL,取5.0mL定容到10mL,备用。
2.3 最大吸收波长的确定 准确吸取2mL总多酚对照品储备溶液于25mL容量瓶中,分别加入18mL蒸馏水、福林酚试剂1.5mL,用20%Na2CO3定容,于75℃水浴加热10min,以蒸馏水为空白,在600~800nm波长处扫描其吸光度,结果表明没食子酸在760nm处有强吸收峰,故选择760nm作为总多酚的测定波长。
准确吸取葡萄糖标准溶液5mL,置25mL量瓶中,加水至刻度,摇匀,作为对照品稀释液。精密移取对照品稀释液1mL,置于具塞试管中,加入新鲜配制的0.2% 蒽酮-硫酸试液4mL,迅速浸于冰水浴中冷却后放入热水浴中,管口加盖玻璃塞,以防蒸发,准确煮沸10min取出,自来水冷却。室温放置10min,以试剂空白为参比,在400~800 nm波长范围内进行扫描。精密移取1mL供试品溶液置于10mL具塞试管中,按上法操作,在400~800nm波长范围内进行扫描。对照品溶液与供试品溶液均在610nm处有最大吸收。
2.4 绘制标准曲线
2.4.1 总多酚标准曲线的绘制 精密量取对照品溶液0.5、1、2、3、4、5mL,分别置10mL容量瓶中,各加水稀释至刻度。分别取上述溶液各2mL,置10mL容量瓶中,分别加4mL水、0.5mL福林酚试剂,摇匀,加1.5mL20%Na2CO3溶液,摇匀,加水稀释至刻度,75℃水浴加热10min,取出放冷。照紫外-可见光分光光度法(中国药典2010年版一部附录ⅤA),在760nm波长处测定吸收度,以浓度为横坐标,吸收度为纵坐标,绘制标准曲线。计算回归方程Y=0.1181 X+0.0208(r=0.9991),在线性范围0.913~9.130μg/mL范围内吸收度呈良好的线性关系。
2.4.2 总多糖标准曲线的绘制 取葡萄糖对照品储备溶液0.5、1、1.5、2、2.5、3、3.5mL分别置于10mL量瓶中,加水至刻度。分别取上述溶液1mL置10mL具塞试管中,各加0.2%蒽酮-硫酸试液4mL,摇匀后迅速浸于冰水浴中冷却,各管冷却后一起置沸水浴中加热10min取出,自来水冷却。室温放置10min,以试剂空白为参比。照紫外-可见光分光光度法(中国药典2010年版一部附录ⅤA),在610nm波长处测定吸收度,以浓度为横坐标,吸收度为纵坐标,绘制标准曲线。计算回归方程Y =7.2167 X+0.0719(r=0.999),在0.015~0.105mg/mL范围内吸收度呈良好的线性关系。
2.5 方法学考察
2.5.1 稳定性试验 精密取同一份供试品溶液,分别在0、10、20、40、80、160min按照“2.4.1”方法显色后测定吸光度值。计算得到松补力口服液总多酚的RSD为0.68%,表明供试品溶液在160min内显色稳定。精密取同一份供试品溶液,分别在0、10、20、40、80、160min按照“2.4.2”方法显色后测定吸光度值。计算得到松补力口服液总多糖的RSD为0.14%,表明供试品溶液在160min内显色稳定。
2.5.2 精密度试验 取6份总多酚对照品溶液,每份2mL,按照“2.4.1”方法显色后测定吸光度值,计算得到松补力口服液总多酚的RSD为0.76%,说明该方法测定松补力口服液总多酚精密度良好。取6份总多糖对照品溶液,每份1mL,按照“2.4.2”方法显色后测定吸光度值,计算得到松补力口服液总多糖的RSD为0.72%,说明该方法测定松补力口服液总多糖精密度良好。
2.5.3 重现性试验 取同一批松补力口服液样品6份,分别按照“2.2.1”方法制成总多酚供试品溶液,每份精密吸取2mL,按照“2.4.1”方法显色后测定吸光度值,计算得到RSD为1.05%,表明该方法测定松补力口服液中总多酚的含量重现性良好。取同一批松补力口服液样品6份,分别按照“2.2.2”方法制成总多糖供试品溶液,每份精密吸取1mL,按照“2.4.2”方法显色后测定吸光度值,计算得到RSD为1.28%,表明该方法测定松补力口服液中总多糖的含量重现性良好。
2.5.4 加样回收率试验 测定已知总多酚含量的松补力口服液6份,加没食子酸标准品适量,各取2mL,按照“2.4.1”方法显色后测定吸光度值,并计算平均回收率。平均加样回收率为98.2%,RSD为1.64%,结果见表1。测定已知总多糖含量的松补力口服液6份,加葡萄糖标准品适量,各取1mL,按照“2.4.2”方法显色后测定吸光度值,并计算平均回收率。平均回收率为96.62%,RSD为1.0%,结果见表2。
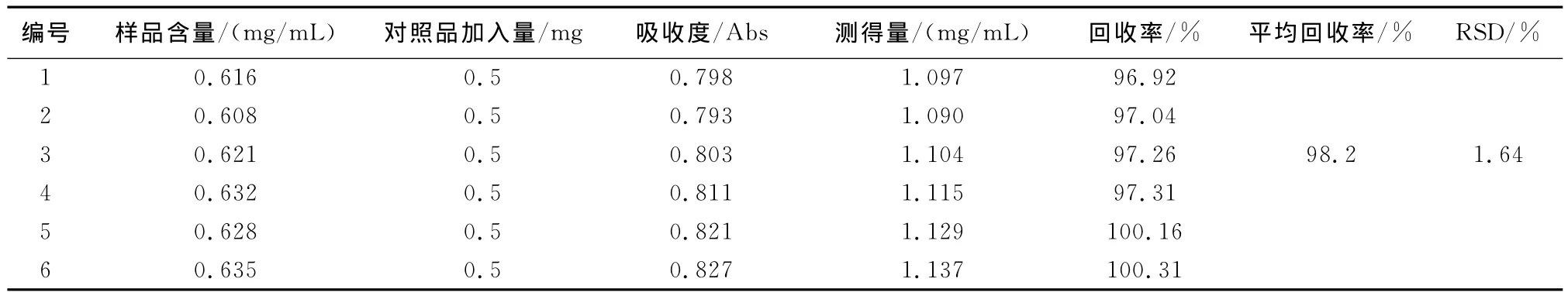
表1 松补力口服液中总多酚的回收率
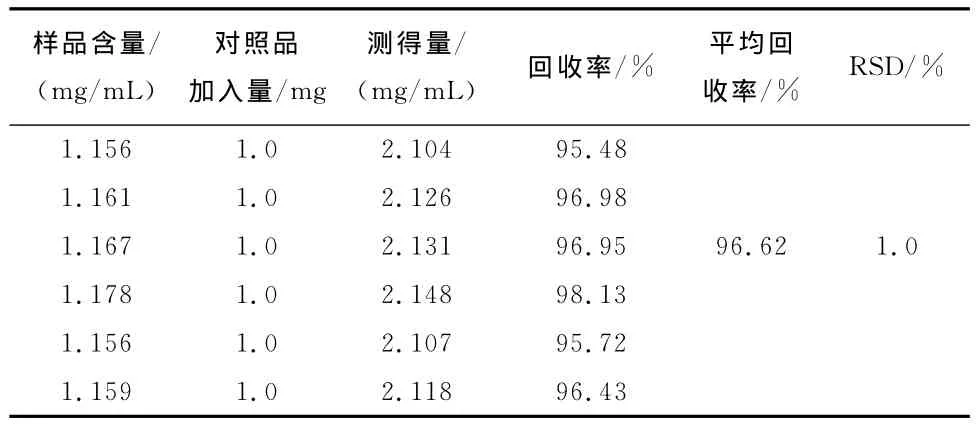
表2 松补力口服液中总多糖的回收率
2.6 样品测定
2.6.1 松补力口服液10批总多酚的含量测定 取松补力口服液各3份,每份取3mL用水稀释到
100mL并定容。按照“2.4.1”方法显色后在760 nm波长处测定吸光度值,计算松补力口服液中总多酚含量。10批松补力口服液总多酚的平均含量为0.617mg/mL。结果见表3。
2.6.2 松补力口服液10批总多糖的含量测定 取松补力口服液各3份,每份取10mL加30mL无水乙醇过夜,离心。分别用无水乙醇、丙酮洗3次,每次10mL。滤渣加适量水溶解,并定容到100mL,取5.0mL定容到10mL。按照“2.4.2”方法显色后在610nm波长处测定吸光度值,计算松补力口服液中总多酚含量。10批松补力口服液总多糖的平均含量为1.216mg/mL结果见表4。

表3 10批不同批次药材制成口服液总多酚含量(n=3)

表4 10批不同批次药材制成口服液总多糖含量
3 结论
本研究结果表明松补力口服液中总多酚、总多糖的含量较高。经查阅文献[6-12]确定采用本实验方法,简单易行,重现性好,结果可靠稳定,可作为松补力口服液总多酚和总多糖的检测方法。
本研究收集10批松补力口服液进行测定,总多糖含量相对于总多酚含量较高,但是总多糖含量测定方法没有总多酚的测定方法稳定,对于松补力口服液质量标准检测的提高还需进行相关的实验测定,以便建立科学的松补力口服液质量检测标准。
[1] 国家药典委员会.中华人民共和国卫生部药品标准·维吾尔药分册[M].乌鲁木齐:新疆科技卫生出版社,1999,WS3-BW-0151-98.
[2] Zi X,Grasso A W,Kung HJ,et al.A flavonoid antioxidant,silymarin,inhibits activation of erbB1signling and induces cyclin-dependent Kinase inhibitors,G1arrest,and anticarcinogenic effects in human prostate carcinoma DU145cells[J].Cancer Res,1998,58(9):1920-1929.
[3] 陈敏,刘晓芳,李秋娟,等.白黎芦醇对乳腺癌 MCF-7细胞的抗增殖作用[J].中国公共卫生,2004,20(11):1341-1342.
[4] Zi X,Feyes DK,Agarwal R,et al.Anticarcinogenic effect of a flavonoid antioxidant,silymarin,in human breast cancer MDAMB468:induction of G1arrest through an increase in Cpl/p21 concomitant with a decrease in kinase activity of cyclin-depent kinases and associated cyclins[J].Clin Cancer Res,1998,4(4):1055-1064.
[5] 国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:79.
[6] 田树革,魏玉龙,刘宏炳,等.Folin-Cioca lteu比色法测定石榴不同 部 位 总 多 酚 的 含 量 [J].光 谱 实 验 室,2009,26(2):341-343.
[7] 李鹏,魏晓霞,许建华,等.灵芝康葆胶囊中多糖的测定[J].西北药学杂 志,2008,24(4):249-250.
[8] 陈孝娟,顾政一,徐芳,等.不同产地的石榴皮总多酚的含量测定[J].时珍国医国药,2011,22(3):541-543.
[9] 刘硕谦,刘仲华,黄建安.紫外分光光度法检测水皂角总多酚的含量[J].食品工业科技,2003,(6):76-77.
[10] 张帆,刘宏炳,田树革,等.药桑中黄酮和多糖的超声提取与含量测定[J].西北药学杂志,2008,23(5):282-283.
[11] 李繁荣.至灵胶囊中多糖测定[J].中草药,2006,37(5):709-710.
[12] 陈平,陈新,王辉,等.硫酸-蒽酮法测定鄂产竹节参多糖含量[J].中国医院药学杂志,2007,27(12):1654-1656.
