椎体成形术后骨水泥渗漏分析
2014-07-07苏祥正毛克亚刘郑生
苏祥正,毛克亚,刘郑生,周 亮,史 腾
解放军总医院 骨科,北京,100853
椎体成形术后骨水泥渗漏分析
苏祥正,毛克亚,刘郑生,周 亮,史 腾
解放军总医院 骨科,北京,100853
目的 了解椎体成形术骨水泥渗漏的发生率、好发节段、椎体渗漏的位置等相关问题。方法 回顾性分析我院脊柱外科2012年6月- 2014年2月68例行椎体成形术患者的病历及影像学资料,分析术后腰背部疼痛症状缓解情况、骨水泥渗漏发生的节段、椎体渗漏的位置及相关并发症。结果 患者术后疼痛缓解率达94.2%,骨水泥渗漏发生率为52.7%,好发节段为胸12和腰1,椎体骨水泥渗漏的位置按发生率由高到低依次为:皮质骨渗漏(46.9%)、终板渗漏(30.6%)、椎旁血管渗漏(18.4%)、椎管内渗漏(4.1%)。1例患者发生肺栓塞。结论 椎体成形术骨水泥渗漏发生率相对较高,但其多数无临床症状,亦无需临床干预治疗。
椎体压缩骨折;椎体成形术;骨水泥;骨水泥渗漏;高黏度骨水泥
椎体压缩骨折(vertebral compression fractures,VCFs)已成为最常见的老年病之一。VCFs常导致腰背疼痛、持续进展的脊柱畸形、脊柱功能减低等,导致生活质量严重下降。椎体成形术是治疗VCFs的一项微创方法,效果已得到充分的证实和肯定。椎体成形术通过向密闭的已塌陷的椎体内注射液态聚甲基丙烯酸甲脂,从而达到稳定骨折及恢复椎体高度的目的。其广泛用于治疗由骨质疏松、溶骨性肿瘤、转移性肿瘤等原因引起的椎体压缩骨折[1]。而骨水泥渗漏是其最常见的严重并发症,可能引起神经组织的受压以及形成栓子等[2]。为了解椎体成形术骨水泥渗漏的好发节段、渗漏位置以及并发症的发生情况,对本院68例椎体成形术患者的临床病例进行了回顾性分析。
资料和方法
1 资料来源 2012年6月1日- 2014年2月10日本院脊柱病区椎体压缩骨折并行椎体成形术的患者。纳入标准:1)行电视透视下经皮椎体成形术的椎体压缩骨折患者;2)除椎体压缩骨折外既往无其他引起腰背部疼痛的相关疾病,如腰肌劳损、压缩骨折节段的椎间盘突出及椎管狭窄;3)脊柱肿瘤导致的椎体压缩骨折患者其肿瘤累及范围局限于椎体内,无椎弓根及其他附件累及;4)有术后CT检查资料。
2 手术方法 手术医师为本院脊柱病区4名主任医师。患者利多卡因局麻后于C壁引导下将穿刺针通过椎弓根送入骨折椎体,透视见位置良好后使用骨水泥枪注入骨水泥,每个椎体注入骨水泥3 ~5 ml。所有操作均按照经皮椎体成形术标准操作流程。使用器械及骨水泥均由史赛克公司提供。
3 测量方法及评估 所有患者术后常规行手术节段椎体正侧位X线片和CT平扫检查。骨水泥渗漏位置按椎体上骨水泥渗出部位分为椎体皮质渗漏、终板渗漏、椎旁血管渗漏及椎管内渗漏。统计患者术前、术后X线片、CT检查结果及其术后症状缓解情况,通过骨水泥渗漏长度结合术后并发症发生情况进行评估。测量X线片及术后CT片上骨水泥渗出最远端与椎体渗出处连线的长度,依其渗出长度及并发症发生情况分为4级:Ⅰ级为未观察到渗漏;Ⅱ级为可观察到1 ~ 2 mm的骨水泥的外渗,无需进一步的医学干预治疗;Ⅲ级为可观察到>3 mm的骨水泥的外渗,且骨水泥渗出对患者无风险或风险较小,不需要临床干预治疗;Ⅳ级为严重渗出,可以观察到明显的骨水泥外渗,可能需要临床干预治疗[2]。使用视觉模拟疼痛评分(visual analog score,VAS)法评估术后患者腰背痛缓解情况,同时观察记录相关术后并发症。
4 统计学方法 使用SPSS19.0软件进行统计分析,计数资料以率表示,组间采用χ2检验,以P<0.05为差异有统计学意义。
结 果
1 一般情况 共68例行椎体成形术的患者纳入研究,平均年龄71.3岁;其中男性23例(33.8%),年龄为46 ~ 85岁,平均66.22岁,女性45例(66.2%),年龄为54 ~ 86岁,平均73.96岁。单个椎体的椎体成形术49例,2个椎体的椎体成形术16例,3个椎体的椎体成形术2例,4个椎体的椎体成形术1例,共93个椎体;其中胸椎38(40.9%)个,腰椎55(59.1%)个。胸11-腰3手术节段最多,腰1最为常见。具体手术椎体分布见图1。
2 渗漏情况 共40个椎体发生骨水泥渗漏, 其中6个椎体发生两个部位的骨水泥渗漏,2个椎体发生3个部位的骨水泥渗漏(表1)。共49个位置发生渗漏,按发生骨水泥渗漏的位置计量,骨水泥渗漏的发生率为52.7%。胸椎与腰椎骨水泥渗漏率的差异无统计学意义。椎体皮质渗漏23例(46.9%) (图2),终板渗漏15例(30.6%),椎旁血管渗漏9例(18.4%),椎管内渗漏2例(4.1%)。所有发生渗漏的椎体中,Ⅳ级1例,继发肺栓塞;Ⅲ级7例(均为皮质骨渗漏);Ⅱ级24例(皮质骨渗漏12例,终板渗漏8例,椎旁血管4例);Ⅰ级17例。渗漏椎体均无特征,不需要处理。
3 术后疼痛缓解情况及并发症 患者术后均留院观察,无镇痛、抗炎等相关特殊治疗。术后第1天60例腰痛症状消失,术后第2天7例腰痛症状明显缓解,出院时疼痛缓解率高达94.2%。术后第1天4例发热,体温平均38.1℃,经物理降温后第2天均恢复正常体温。1例术后第3天并发肺栓塞,转至呼吸内科重症监护室接受进一步治疗。其余患者未发生相关并发症,亦无神经损伤、神经受压等症状。
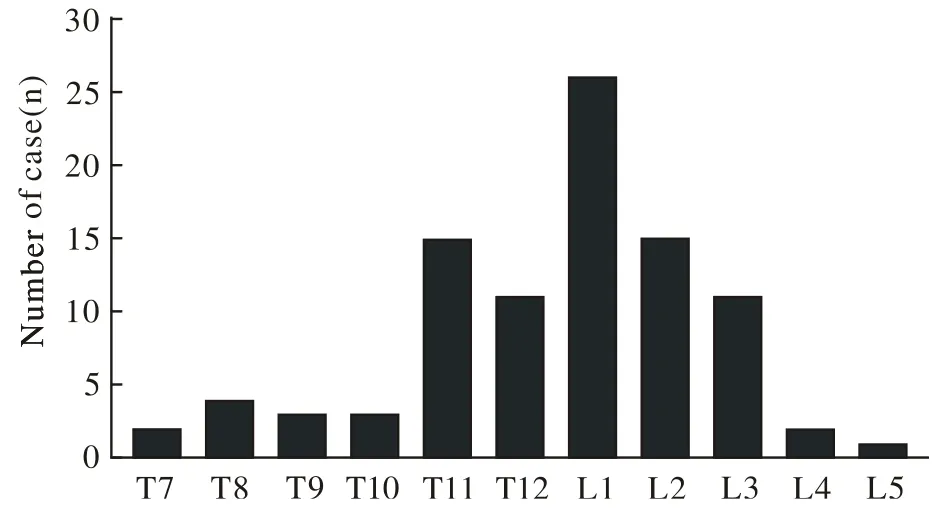
图 1 93个椎体成形术的分布情况Fig. 1 Distribution of vertebrae in 93 patients after vertebroplasty

图 2 行椎体成形术患者L1节段椎体皮质前侧及右侧可见骨水泥渗漏Fig. 2 Cement leakage in L1, anterior and right cortex of patients after vertebroplasty
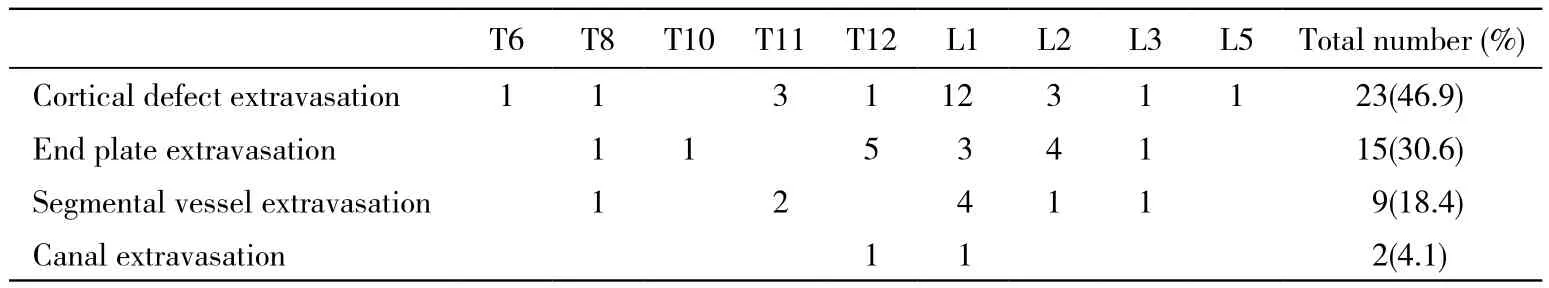
表1 骨水泥渗漏椎体分布表Tab. 1 Distribution of cement leakage in vertebrae
讨 论
椎体成形术是一项用来稳定骨折椎体的微创治疗方法。本组68例中,60例术后第1天疼痛缓解,7例术后第2天疼痛缓解,出院时疼痛缓解率高达94.2%,与以往文献报道椎体成形术能够立即缓解90%的腰背部疼痛一致[3]。虽然椎体成形术临床治疗效果令人满意,但其也存在一些风险,其中骨水泥渗漏是椎体成形术中的关键性安全问题[4]。骨水泥渗漏发生率较高,可能与骨折的严重性以及骨水泥注入的量相关[5]。骨水泥通过椎体骨折间隙或椎体静脉间隙发生渗漏。虽然大部分渗漏无临床症状,但有可能因压迫而出现神经症状甚至截瘫、肺栓塞、局部或者全身感染等严重并发症[6]。肺栓塞是骨水泥最严重的并发症,可能导致患者死亡,尤其是行椎体成形术的病理性椎体骨折患者出现呼吸急促症状时,则尤需提高警惕[7]。骨水泥渗漏发生率的文献报道结果不尽相同,报道最高为73%[8-11]。本组研究表明:骨水泥渗漏的发生率高达52.7%,与以往的一些文献报道(53.0%)相近[1]。
胸11-腰3节段处于胸弯与腰弯移行区,属于应力集中节段,且老年患者(尤其是老年女性)易患骨质疏松,故该节段压缩性骨折发生率较高。且本组数据表明,发生椎体压缩骨折患者中女性占多数,这可能与女性为骨质疏松高发人群有关。女性VCFs的发病率为10.7‰,男性为5.7‰,随着年龄的增加发病率明显增加。在75 ~ 79岁的女性患者中平均每年的发病率为29.3‰,男性为13.6‰[6]。
目前椎体成形术主要有两种,一种为常规椎体成形术,其直接通过骨水泥枪向椎体内注入骨水泥,该术式可恢复70%患者的椎体高度;另一种是球囊椎体成形术:通过特制球囊扩张骨折椎体并通过骨水泥枪向球囊内注入骨水泥,期望能够减少骨水泥渗漏。但与常规椎体成形术相比,其减少的骨水泥渗漏无统计学差异[12]。另有文献指出,如果在CT引导下将球囊准确地置于正确位置可使骨水泥渗漏减少76%[13-14]。这种理论认为常规椎体成形术骨水泥注入压力较大,而球囊椎体成形术则使骨水泥注入压力大大减小,从而减少骨水泥渗漏[15]。而大样本病例分析显示:常规、球囊椎体成形术二者骨水泥渗漏率无统计学差异[16]。此外,二种术式的椎体高度恢复、术后疼痛缓解情况及术后生活质量的提高情况都相近[17]。总之,两种椎体成形术其主要的并发症仍是骨水泥渗漏。本次研究病例均为常规椎体成形术。
近期有文献报道高黏度骨水泥可明显减少骨水泥渗漏[18]。高黏度骨水泥在混合后立刻成为稳定的糊状物(这点不同于低黏度骨水泥),并能保持持续的高黏度状态并在其凝固之前的8 ~ 10 min内持续可注射。高黏度骨水泥可以使用不同类型的针头进行注射。椎体压缩骨折模型研究显示:低黏度骨水泥的渗漏率较高,而高黏度骨水泥能够很好地充盈椎体且不伴渗漏[19]。
除骨水泥渗漏及术后近期的一些并发症以外,椎体成形术后相邻椎间盘发生退行性病变的风险增高,与手术后时间的长短、骨水泥的注入量密切相关[20]。因此,术前应充分考虑并评估术后长期存在的风险。
综上所述,椎体成形术仍是椎体压缩骨折的良好选择,其术后疼痛缓解率较高,且其并发症较开放性椎体钉棒系统内固定手术少,更为安全。其主要的并发症为骨水泥渗漏,发生率相对较高,尤其是椎体皮质渗漏和终板渗漏,但其多数无临床症状,亦无需临床干预治疗。总体来说,椎体成形术是较为安全、操作简单、患者痛苦少、临床效果好的一种手术方式。
1 Trumm CG, Jakobs TF, Stahl R, et al. CT fluoroscopy-guided vertebral augmentation with a radiofrequency-induced, highviscosity bone cement (StabiliT(®)): technical results and polymethylmethacrylate leakages in 25 patients[J]. Skeletal Radiol, 2013, 42(1):113-120.
2 Yeom JS, Kim WJ, Choy WS, et al. Leakage of cement in percutaneous transpedicular vertebroplasty for painful osteoporotic compression fractures[J]. J Bone Joint Surg Br, 2003, 85(1):83-89.
3 Baroud G, Crookshank M, Bohner M. High-viscosity cement significantly enhances uniformity of cement filling in vertebroplasty:an experimental model and study on cement leakage[J]. Spine (Phila Pa 1976), 2006, 31(22):2562-2568.
4 Habib M, Serhan H, Marchek C, et al. Cement leakage and filling pattern study of low viscous vertebroplastic versus high viscous confidence cement[J]. SAS J, 2010, 4(1): 26-33.
5 Chen HL, Wong CS, Ho ST, et al. A lethal pulmonary embolism during percutaneous vertebroplasty[J]. Anesth Analg, 2002, 95(4):1060-1062.
6 Robinson Y, Heyde CE, Försth P, et al. Kyphoplasty in osteoporotic vertebral compression fractures--guidelines and technical considerations[J]. J Orthop Surg Res, 2011, 6:43.
7 Kumar N, Malviya M, Meireles MD. It should not be here! A strange case of pulmonary cement embolism following balloon kyphoplasty[J/OL]. http://journal.publications.chestnet.org/article. aspx?articleID=1837477.
8 Fourney DR, Schomer DF, Nader R, et al. Percutaneous vertebroplasty and kyphoplasty for painful vertebral body fractures in cancer patients[J]. J Neurosurg, 2003, 98(1 Suppl):21-30.
9 Shapiro S, Abel T, Purvines S. Surgical removal of epidural and intradural polymethylmethacrylate extravasation complicating percutaneous vertebro-plasty for an osteoporotic lumbar compression fracture[J]. J Neurosurg, 2003, 98(1): 90-92.
10 Schmidt R, Cakir B, Mattes T, et al. Cement leakage during vertebroplasty: an underestimated problem?[J]. Eur Spine J,2005, 14(5): 466-473.
11 Machado R, Silva UX, Carneiro E, et al. Lack of correlation between tubular dentine cement penetration, adhesiveness and leakage in Roots filled with gutta percha and an endodontic cement based on epoxy amine resin[J]. J Appl Oral Sci, 2014, 22(1): 22-28.
12 La Maida GA, Giarratana LS, Acerbi A, et al. Cement leakage:safety of minimally invasive surgical techniques in the treatment of multiple myeloma vertebral lesions[J]. Eur Spine J, 2012, 21 Suppl 1:S61-S68.
13 Kang JD, An H, Boden S, et al. Cement augmentation of osteoporotic compression fractures and intraoperative navigation: summary statement[J]. Spine (Phila Pa 1976), 2003, 28(15 Suppl):S62-S63.
14 Ohnsorge JA, Siebert CH, Schkommodau E, et al. Minimallyinvasive computer-assisted fluoroscopic navigation for kyphoplasty[J]. Z Orthop Ihre Grenzgeb, 2005, 143(2):195-203.
15 Mathis JM, Ortiz AO, Zoarski GH. Vertebroplasty versus kyphoplasty: a comparison and contrast[J]. AJNR Am J Neuroradiol, 2004, 25(5):840-845.
16 Wang Y, Huang F, Chen L,et al. Clinical measurement of intravertebral pressure during vertebroplasty and kyphoplasty[J]. Pain Physician, 2013, 16(4):E411-E418.
17 Bozkurt M, Kahilogullari G, Ozdemir M, et al. Comparative analysis of vertebroplasty and kyphoplasty for osteoporotic vertebral compression fractures[J]. Asian Spine J, 2014, 8(1): 27-34.
18 Georgy BA. Clinical experience with High-Viscosity cements for percutaneous vertebral body augmentation: occurrence, degree, and location of cement leakage compared with kyphoplasty[J]. AJNR Am J Neuroradiol, 2010, 31(3): 504-508.
19 Anselmetti GC, Zoarski G, Manca A, et al. Percutaneous vertebroplasty and bone cement leakage: clinical experience with a new high-viscosity bone cement and delivery system for vertebral augmentation in benign and malignant compression fractures[J]. Cardiovasc Intervent Radiol, 2008, 31(5): 937-947.
20 Zhao H, Ni CF, Huang J, et al. Effects of bone cement on intervertebral disc degeneration[J]. Exp Ther Med, 2014, 7(4):963-969.
Cement leakage after vertebroplasty
SU Xiang-zheng, MAO Ke-ya, LIU Zheng-sheng, ZHOU Liang, SHI Teng
Department of Orthopedics, Chinese PLA General Hospital, Beijing 100853, China
MAO Ke-ya. Email: maokeyeya@sina.com
Objective To study the incidence and predilection site of cement leakage and vertebral leakage after vertebroplasty. Methods Imaging data about 68 patients who underwent vertebroplasty in our hospital from June 2012 to February 2014 were retrospectively analyzed, including alleviated symptoms of lumbar and back pain, cement leakage site, vertebral leakage site and related complications. Results The pain relief rate was 94.2%, the incidence of cement leakage, cortical leakage, termatic leakage, paravertebral vascular leakage, intravertebral leakage was 52.7%, 46.9%, 30.6%, 18.4%, 4.1%, respectively. The 12th thoracic vertebrae and the 1st lumbar vertebrae were the predilection sites of cement leakage. Pulmonary embolism occurred in 1 patient. Conclusion Although the incidence of cement leakage is relatively high after vertebroplasty, most patients have no clinical symptoms and do not need clinical intervention.
vertebral compression fracture; vertebroplasty; bone cement; cement leakage; high viscosity cement
R 683.2
A
2095-5227(2014)10-0987-04
10.3969/j.issn.2095-5227.2014.10.003
时间:2014-05-09 09:58
http://www.cnki.net/kcms/detail/11.3275.R.20140509.0958.001.html
2014-03-05
国家自然科学基金项目(51372276)
Supported by the National Natural Science Foundation of China(51372276)
苏祥正,男,在读硕士。Email: 838624789@qq.com
毛克亚,男,博士,主任医师。Email: maokeya@sina.com
