超声微波协同水蒸气蒸馏-GC-MS分析南、北五味子挥发油化 学成分
2014-06-21高正德李祖光邓丰涛吴先伟
李 昕,聂 晶,高正德,李祖光,*,邓丰涛,吴先伟
(1.浙江工业大学化学工程学院,浙江 杭州 310014;2.聚光科技(杭州)股份有限公司,浙江 杭州 310052)
五味子为木兰科多年生落叶木质藤本植物,《中华人民共和国药典》收录有两种五味子药材,分别为北五味子(Schisandra chinensis(Turcz.)Baill)和南五味子(华中五味子)(Schisandra sphenanthera Rehd. et Wils.)的成熟果实,尤以北五味子质量最佳[1-2]。《神农本草经》将五味子列为上品,它具有收敛固涩、益气生津、补肾宁心的功效,用于久咳虚喘、久泻不止、自汗、盗汗、津伤口渴、短气脉虚、心悸失眠等症。现代科学研究证明,五味子中含有挥发油、有机酸、维生素、木脂素、三萜、倍半萜及多糖等多种化学成分。五味子挥发油中含有单萜类、含氧单萜类、倍半萜类、含氧倍半萜类和少量醇、酸等含氧化合物,其中以倍半萜类为主[3]。超声微波协同萃取是将微波与超声波有机结合,充分利用超声波的空化作用和微波的高能作用,将超声波振动能和通过波导管引出的微波能直接或定向聚焦于样品或物料[4-6]。超声微波协同萃取是一种新型萃取方法,超声萃取不改变萃取对象的化学结构,提取温度低[7],与微波联用,和传统的萃取方法相比具有操作简单、节约时间和降低能耗等特点。1999年,Lagha等[8]首次将微波与超声波结合,用于生物和化学样品的前处理。目前,超声微波协同萃取已被用于靖安椪柑鲜果皮中的精油提取[9]、大黄叶柄的蒽醌类物质[10]、土壤样品中多环芳烃[11]、坚果中脂肪酸[12]、西红柿中番茄红素[13]、烟草中的有机氯类农药[14]、酚醛树脂[15]的提取等方面研究,该方法具有萃取时间短、萃取效率高等特点。
目前,关于五味子挥发油的研究主要采用水蒸气蒸馏[16]、离子液体结合微波辅助萃取[17]、微波辅助无溶剂萃取[18]、超临界流体萃取[19]、索氏提取[19],超声辅助萃取[19]。五味子中挥发油成分对于中枢神经系统具有调节作用,它能够增强机体对于非特异性刺激的预防和防御能力,可以显著地缩短戊巴比妥钠引起的小鼠睡眠时间[20];五味子挥发油中还具有较强的抗纤溶酶原激活物抑制剂活性[21]。因此,开展五味子挥发油的研究具有重要研究意义。目前未见采用超声微波协同水蒸气蒸馏法提取五味子挥发油的报道,且目前关于南、北五味子挥发油差异比较的研究也较少。本实验采用超声微波协同水蒸气蒸馏(ultrasonic-microwave assisted steam distillation,UMASD)和水蒸气蒸馏法(steam distillation,SD)法分别提取南五味子和北五味子中的挥发油成分,用气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)联用技术分析鉴定,分析不同方法所得挥发油差异以及不同品种的五味子挥发油的异同,为不同品种五味子的鉴别和开发利用提供科学依据。
1 材料与方法
1.1 材料、试剂与仪器
南五味子和北五味子 杭州九州大药房;超纯水。
GC2000/MS6100气相色谱-质谱联用仪 聚光科技股份有限公司;XH-100A型微波催化合成/萃取仪 北京祥鹄科技发展有限公司;AL204电子分析天平 梅特勒-托利多仪器(上海)有限公司。
1.2 方法
1.2.1 超声微波协同水蒸气蒸馏萃取南(北)五味子挥发油
使用绞碎机将南(北)五味子打碎,准确称取35 g已切碎的南(北)五味子于500 mL的三口烧瓶中,加入300 mL超纯水,浸泡过夜。将浸泡过的样品置于微波催化合成/萃取仪中,调整微波萃取温度为103 ℃,设定微波功率400 W、时间60 min,同时设定超声功率600 W,时间60 min[22]。实验装置如图1所示。收集南(北)五味子挥发油于样品瓶中,密封后保存于冰箱中待分析。
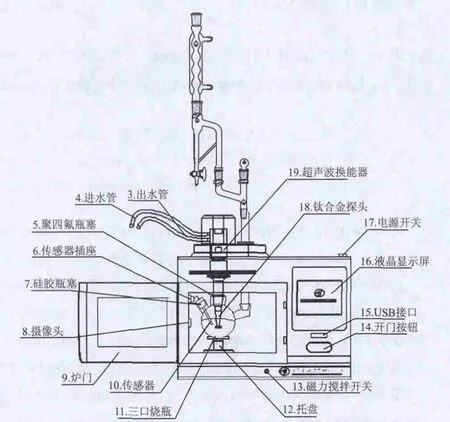
图 1 实验装置Fig.1 Experimental set-up for the extraction of volatile oil
1.2.2 传统水蒸气蒸馏萃取南(北)五味子挥发油
准确称取35 g已切碎的南(北)五味子于500 mL的圆底烧瓶中,加入300 mL超纯水,浸泡过夜。将浸泡过的样品使用传统水蒸气蒸馏6 h,收集南(北)五味子挥发油于样品瓶中,密封后保存于冰箱中待分析。
1.2.3 挥发油处理步骤
准确移取1 μL的五味子挥发油于1 mL PCR小管中,用乙醚稀释至1 mL;准确移取25 μL上述溶液于1 mL PCR小管中,用乙醚稀释至0.5 mL,加入无水硫酸钠除水,取1 μL进行GC-MS分析。
1.2.4 GC-MS分析条件
色谱条件:J&W D B-5石英毛细管柱(30 m×0.25 mm,0.25 μm);进样口温度250 ℃;升温程序:40 ℃保持3 min,以5 ℃/min升温至90 ℃,保持1 min,再以3 ℃/min升温至250 ℃,保持5 min;载气为氦气(99.99%),流速0.8 mL/min;进样量1 μL;分流比10∶1。
质谱条件:电子电离(electron ionization,EI)源;电子能量70 eV;离子阱温度150 ℃;歧管温度50 ℃;传输线温度280 ℃;质量扫描范围m/z 40~600;扫描速率3 scan/s;溶剂延迟5 min。
1.2.5 定性和定量分析
以EI为电离源,进行GC-MS联用分析,采集得到的总离子流图中各质谱图,利用NIST库检索,同时采用保留指数和参考文献来辅助质谱检索定性;定量分析结果依据总离子流色谱峰的峰面积归一化法来计算各组分的相对含量。用于测定保留指数的正构烷烃系列标准样品为C8~C16,计算公式为:
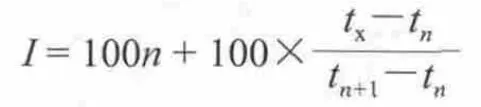
式中:I为待测物的程序升温保留指数;tn和tn+1分别为含n、n+1个碳的正构烷烃的保留时间;tx为待测物的保留时间。
2 结果与分析
2.1 两种不同提取方法的得油率比较
采用传统SD和UMASD两种不同的方法分别提取南、北五味子中的挥发油成分,得到的挥发油性状和收率见表1。

表 1 不同提取方式对南、北五味子挥发油影响Table 1 Impact of different extraction methods on the recoveries Table 1 Impact of different extraction methods on the recoveries of essential oil from fruits ofSchisandra chinensis d Schisandra sphenanthera (Turcz.) Baill an Rehd. et Wils s提取方式 样品种类 提取耗费时间/h 精油外观 精油收率/%SD 南五味子 6 淡黄色透明 1.2北五味子 淡黄色透明 1.3 U MASD 南五味子 1 淡黄色透明 1.4北五味子 淡黄色透明 1.8
由表1可以看出:不同提取方式对五味子挥发油收率有一定的影响,不同提取方式下五味子挥发油收率有一定差异,UMASD所得精油收率较传统SD有所提高;不同品种五味子的挥发油收率也有差异,北五味子的精油收率较南五味子的收率高;根据分水器中挥发油的量是否不再增加为止来判断提取终点,UMASD整个过程仅需1 h,而SD需要6 h,UMASD大大缩短了提取时间,降低了提取过程中的能量消耗。
2.2 五味子挥发油成分分析
按上述实验条件对南北五味子的化学成分进行测定分析,得到总离子流色谱图,如图2、3所示。采用质谱检索和保留指数结合的二维定性法,定性结果及相对含量见表2、3。其中相对百分含量由面积归一化法计算所得。
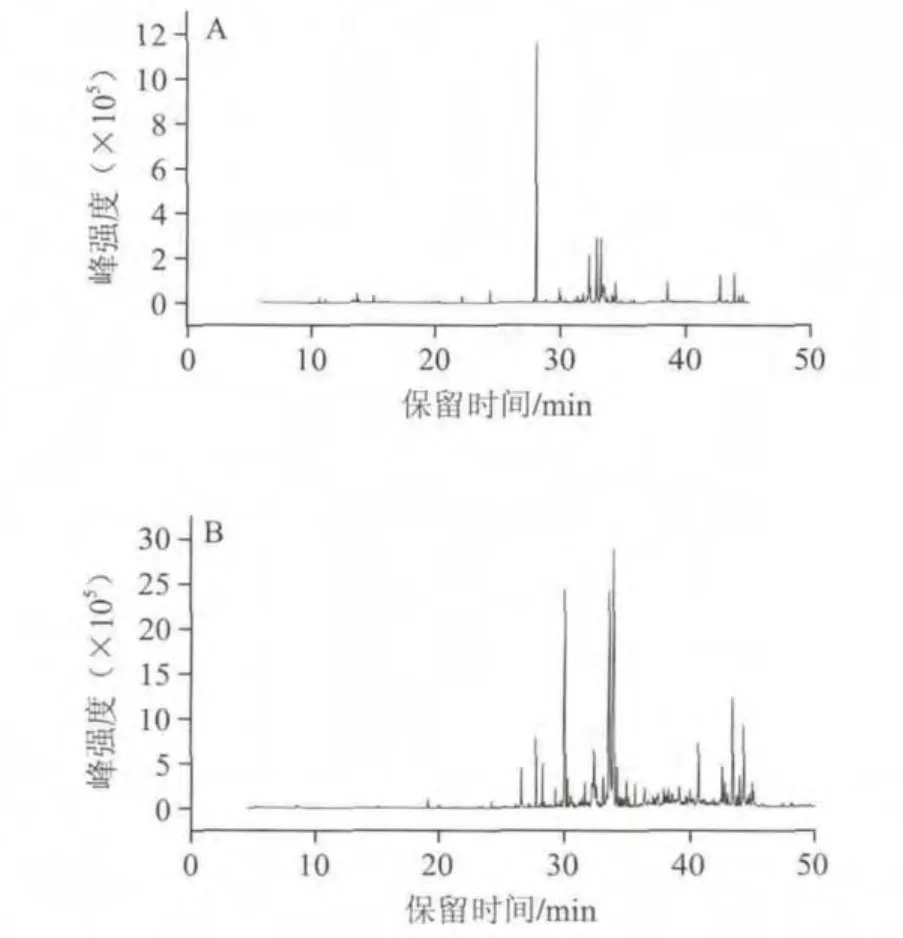
图 2 SD法提取北五味子(A)和南五味子(B)挥发油总离子流色谱图Fig.2 TIC of essential oil extracted by SD from fruits of Schisandra chinensis (Turcz.) Baill (A) and Schisandra sphenanthera Rehd. et Wils (B)
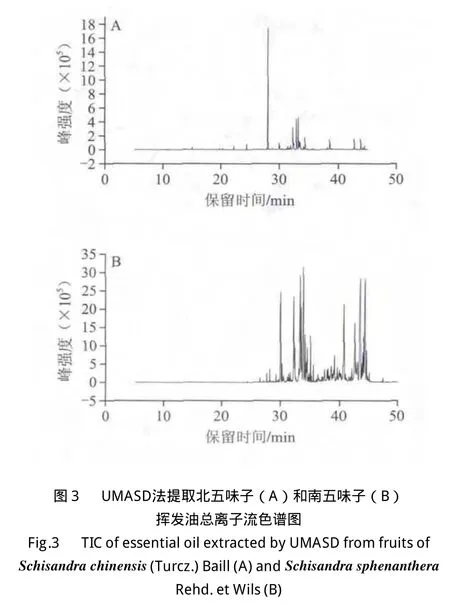

表 2 南五味子挥发油中化学成分的GC-MS鉴定结果及各化合物的相对含量Table 2 Identification of main chemical components from essential oils Table 2 Identification of main chemical components from essential oils of of Schisandra sphenantherahera Rehd. et Wils fruits序号 保留时间/min 名称 分子式 CAS号 保留指数(文献值)相对含量/%SD UMASD 1 7.34 2-furaldehyde 2-糠醛 C5H4O2 98-01-1 828(829) — 0.01 2 8.47 p-xylene 对二甲苯 C8H10 106-42-3 860(862) 0.17 —3 11.13 camphene 莰烯 C10H16 79-92-5 934(934) — 0.01 4 11.62 5-methyl-2-furfural 5-甲基-2-糠醛 C6H6O2 620-02-0 947(946) — 0.01 5 12.55 β-pinene β-蒎烯 C10H16 127-91-3 972(973) — 0.02 6 13.66 o-cymene 邻-异丙基苯 C10H14 527-84-4 1002(1006) — 0.01 7 13.88 3-carene 3-蒈烯 C10H16 13466-78-9 1007(1008) 0.02 0.01 8 14.35 benzeneacetaldehyde 苯乙醛 C8H8O 122-78-1 1018(1019) — 0.01 9 14.95 crithmene 海茴香烯 C10H16 99-85-4 1032(1035) 0.19 0.01 10 15.53 cis-linalool oxide 顺式-氧化芳樟醇 C10H18O2 5989-33-3 1047(1047) 0.01 0.01 11 16.11 ocimene 罗勒烯 C10H16 502-99-8 1061(1056) — 0.01 12 18.37 limonene oxide 氧化宁烯 C10H16O 1195-92-2 1114(1116) — 0.01 13 19.27 borneol 冰片 C10H18O 507-70-0 1134(1130) 0.02 0.02 14 19.75 4-terpineol 4-松油醇 C10H18O 562-74-3 1144(1148) — 0.02 15 20.02 prehnitene 连四甲苯 C10H14 488-23-3 1150(1150) — 0.01 16 20.72 3-methylundecane 3-甲基十一烷 C12H26 1002-43-3 1166(1169) 0.11 —17 22.39 myrtenol 桃金娘烯醇 C10H16O 515-00-4 1203(1201) 0.04 —18 24.36 bornyl acetate 乙酸龙脑酯 C12H20O2 76-49-3 1246(1242) 0.11 0.07 19 28.10 ylangene 依兰烯 C15H24 14912-44-8 1329(1328) 3.15 1.25 20 28.37 倍半萜烯类化合物 C15H24 N/A 1335 0.44 —21 28.54 β-bourbonene β-波旁烯 C15H24 5208-59-3 1339(1337) 0.17 0.04 22 28.73 α-cubebene α-荜澄茄油烯 C15H24 17699-14-8 1343(1343) 0.16 0.06 23 29.25 isoledene 异喇叭烯 C15H24 N/A 1355(1353) 1.29 0.65 24 29.44 α-longipinene α-长叶蒎烯 C15H24 5989-08-2 1359(1357) 0.06 0.02 25 29.53 β-cubebene β-荜澄茄油烯 C15H24 13744-15-5 1361(1361) 0.15 0.07 26 29.69 copaene 古巴烯 C15H24 3856-25-5 1364(1367) 0.49 0.18 27 30.08 longicyclene 长叶蒎烯 C15H24 1137-12-8 1373(1371) 23.45 13.87 28 30.26 β-patchoulene β-藿香萜烯 C15H24 514-51-2 1377(1377) 1.93 1.37 29 30.48 di-epi-α-cedrene C15H24 N/A 1382(1381) 1.35 0.88 30 31.17 cyperene 香附烯 C15H24 2387-78-2 1397(1398) 0.31 0.37 31 31.35 β-elemene 榄香烯 C15H24 515-13-9 1401(1403) 0.41 0.50 32 31.53 caryophyllene 石竹烯 C15H24 87-44-5 1406(1406) 1.89 0.91 33 31.90 α-cedrene α-柏木烯 C15H24 469-61-4 1414(1414) 0.26 —34 32.24 τ-gurjunene τ-古芸烯 C15H24 22567-17-5 1422(1424) 2.25 11.70 35 32.38 chamigrene 花柏烯 C15H24 18431-82-8 1425(1428) 6.38 2.93 36 32.69 α-amorphene α-紫穗槐烯 C15H24 483-75-0 1432(1433) 0.39 —37 33.08 β-gurjunene β-古芸烯 C15H24 17334-55-3 1441(1441) 2.62 1.45 38 33.32 aristolene 马兜铃烯 C15H24 N/A 1446(1450) 1.48 —39 33.35 thujopsene 罗汉柏烯 C15H24 470-40-6 1447(1450) — 16.61 40 33.62 α-himachalene α-雪松烯 C15H24 3853-83-6 1453(1451) 0.41 0.45 41 33.91 τ-muurolene τ-依兰油烯 C15H24 30021-74-0 1460(1462) 32.21 18.50 42 34.18 alloaromadendrene 别香树烯 C15H24 25246-27-9 1466(1466) 0.40 4.90 43 34.39 varidiflorene 喇叭烯 C15H24 21747-46-6 1471(1470) 0.67 1.88 44 34.52 倍半萜烯类化合物 C15H24 N/A 1474 0.65 3.07 45 34.68 α-muurolene α-依兰油烯 C15H24 31983-22-9 1477(1479) 0.81 0.42 46 34.84 β-eudesmene β-桉叶烯 C15H24 17066-67-0 1481(1482) — 0.98 47 34.92 trans-β-ionone 反-β-紫罗兰酮 C15H24 79-77-6 1483(1482) 2.38 —48 35.08 valencene 朱栾倍半萜 C15H24 4630-07-3 1487(1485) 0.64 4.12 49 35.62 α-selinene α-芹子烯 C15H24 473-13-2 1499(1498) 0.42 1.39 50 36.18 δ-cadinene δ-杜松烯 C15H24 483-76-1 1512(1513) 0.05 0.22 51 37.10 spathulenol 斯巴醇 C15H24 6750-60-3 1535(1537) 0.82 0.44 52 37.24 isolongifolene, 7,8-dehydro-8a-hydroxy-异长叶烯,7,8-氧脱氢-8a-羟基- C15H24O N/A 1538(1537) 0.3 0.31
续表2
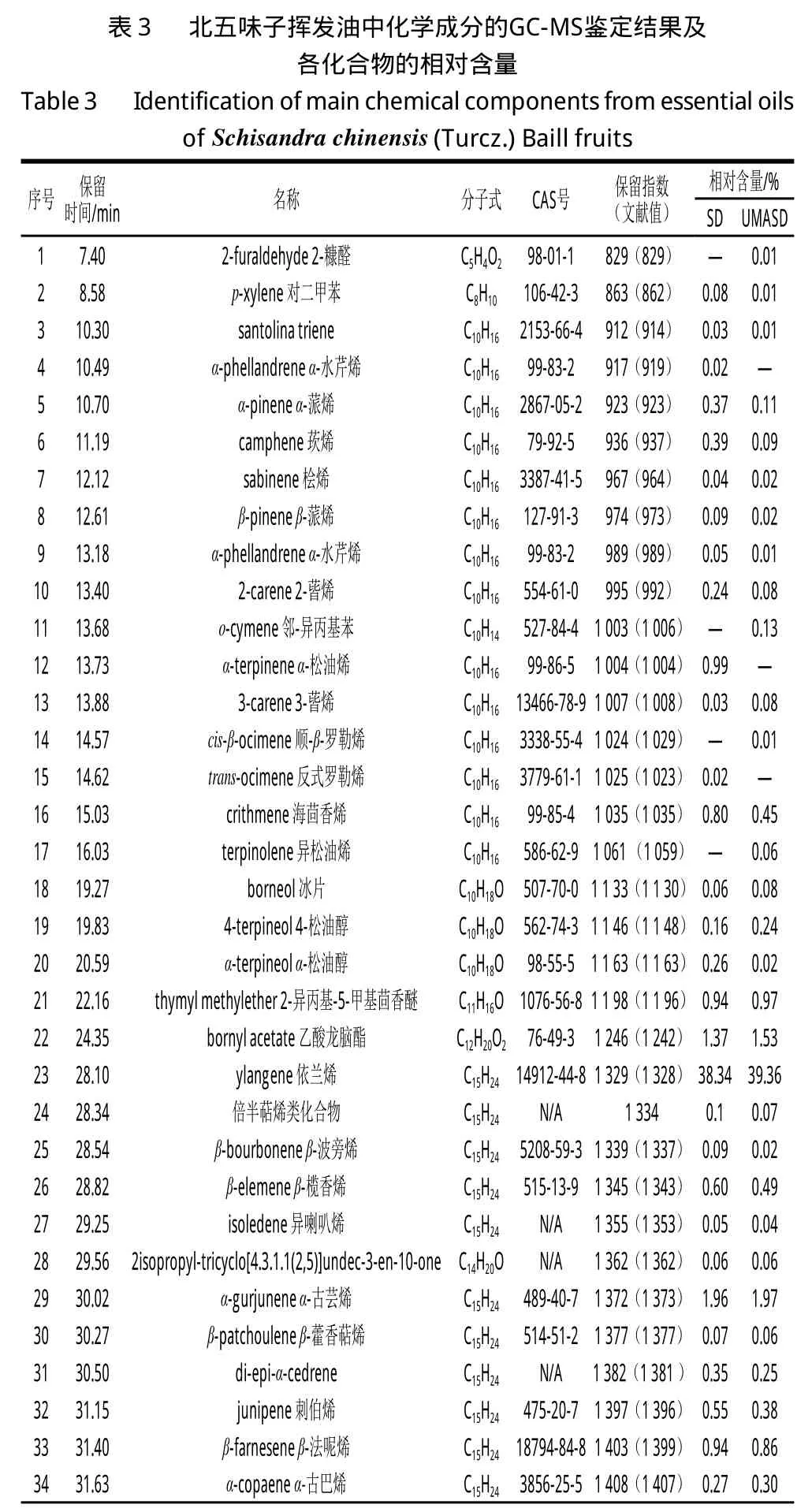
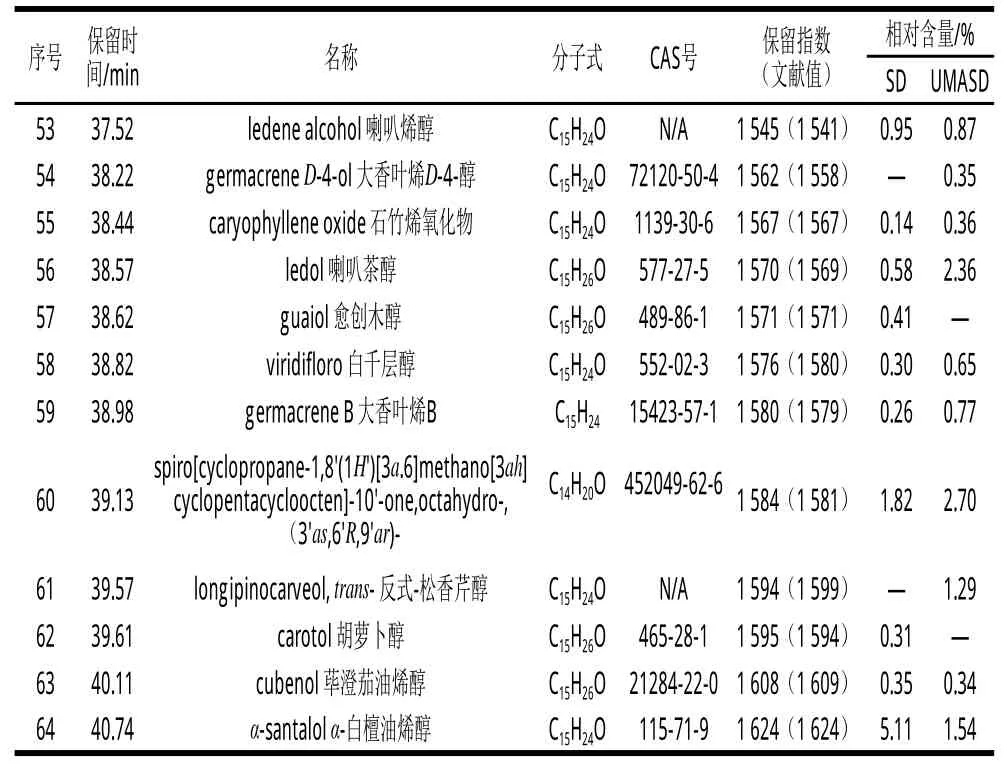
表 3 北五味子挥发油中化学成分的GC-MS鉴定结果及各化合物的相对含量Table 3 Identification of main chemical components from essential oils Table 3 Identification of main chemical components from essential oils ofof Schisandra chinensis sis (Turcz.) Baill fruitss序号 保留时间/min 名称 分子式 CAS号 保留指数(文献值)相对含量/%SD UMASD 1 7.40 2-furaldehyde 2-糠醛 C5H4O2 98-01-1 829(829) — 0.01 2 8.58 p-xylene 对二甲苯 C8H10 106-42-3 863(862) 0.08 0.01 3 10.30 santolina triene C10H16 2153-66-4 912(914) 0.03 0.01 4 10.49 α-phellandrene α-水芹烯 C10H16 99-83-2 917(919) 0.02 —5 10.70 α-pinene α-蒎烯 C10H16 2867-05-2 923(923) 0.37 0.11 6 11.19 camphene 莰烯 C10H16 79-92-5 936(937) 0.39 0.09 7 12.12 sabinene 桧烯 C10H16 3387-41-5 967(964) 0.04 0.02 8 12.61 β-pinene β-蒎烯 C10H16 127-91-3 974(973) 0.09 0.02 9 13.18 α-phellandrene α-水芹烯 C10H16 99-83-2 989(989) 0.05 0.01 10 13.40 2-carene 2-蒈烯 C10H16 554-61-0 995(992) 0.24 0.08 11 13.68 o-cymene 邻-异丙基苯 C10H14 527-84-4 1 003(1 006) — 0.13 12 13.73 α-terpinene α-松油烯 C10H16 99-86-5 1 004(1 004) 0.99 —13 13.88 3-carene 3-蒈烯 C10H16 13466-78-9 1 007(1 008) 0.03 0.08 14 14.57 cis-β-ocimene 顺-β-罗勒烯 C10H16 3338-55-4 1 024(1 029) — 0.01 15 14.62 trans-ocimene 反式罗勒烯 C10H16 3779-61-1 1 025(1 023) 0.02 —16 15.03 crithmene 海茴香烯 C10H16 99-85-4 1 035(1 035) 0.80 0.45 17 16.03 terpinolene 异松油烯 C10H16 586-62-9 1 061 (1 059) — 0.06 18 19.27 borneol 冰片 C10H18O 507-70-0 1 1 33(1 1 30) 0.06 0.08 19 19.83 4-terpineol 4-松油醇 C10H18O 562-74-3 1 1 46(1 1 48) 0.16 0.24 20 20.59 α-terpineol α-松油醇 C10H18O 98-55-5 1 1 63(1 1 63) 0.26 0.02 21 22.16 thymyl methylether 2-异丙基-5-甲基茴香醚 C11H16O 1076-56-8 1 1 98(1 1 96) 0.94 0.97 22 24.35 bornyl acetate 乙酸龙脑酯 C12H20O2 76-49-3 1 246(1 242) 1.37 1.53 23 28.10 ylangene 依兰烯 C15H24 14912-44-8 1 329(1 328) 38.34 39.36 24 28.34 倍半萜烯类化合物 C15H24 N/A 1 334 0.1 0.07 25 28.54 β-bourbonene β-波旁烯 C15H24 5208-59-3 1 339(1 337) 0.09 0.02 26 28.82 β-elemene β-榄香烯 C15H24 515-13-9 1 345(1 343) 0.60 0.49 27 29.25 isoledene 异喇叭烯 C15H24 N/A 1 355(1 353) 0.05 0.04 28 29.56 2isopropyl-tricyclo[4.3.1.1(2,5)]undec-3-en-10-one C14H20O N/A 1 362(1 362) 0.06 0.06 29 30.02 α-gurjunene α-古芸烯 C15H24 489-40-7 1 372(1 373) 1.96 1.97 30 30.27 β-patchoulene β-藿香萜烯 C15H24 514-51-2 1 377(1 377) 0.07 0.06 31 30.50 di-epi-α-cedrene C15H24 N/A 1 382(1 381 ) 0.35 0.25 32 31.15 junipene 刺伯烯 C15H24 475-20-7 1 397(1 396) 0.55 0.38 33 31.40 β-farnesene β-法呢烯 C15H2418794-84-8 1 403(1 399) 0.94 0.86 34 31.63 α-copaene α-古巴烯 C15H24 3856-25-5 1 408(1 407) 0.27 0.30

续表3
用SD法和UMASD法鉴定出的南五味子挥发油化合物数目为50、54 种,其中共有成分40 种;北五味子挥发油化合物数目分别为54、55 种,其中共有成分42 种。上述两种不同提取方法得到的南五味子挥发油的主要化学成分(相对含量)为τ-依兰油烯(32.21%、18.50%)、长叶蒎烯(23.45%、13.87%)、τ-古芸烯(2.25%、11.70%)、花柏烯(6.38%、2.93%)、依兰烯(3.15%、1.25%)等;其中醛类分别有0、3 个(占总量的5.56%),烯类33 种(占总量66%)、35 种(占总量64.8%),醇类10 个(占总量的20.0%)、10个(占总量的18.5%),酯类1 个(占总量的2.0%)、1 个(占总量的1.85%),其他为6 个(占总量的12.0%)、5 个(占总量的9.26%)。北五味子挥发油的主要化学成分(相对含量)为依兰烯(38.34%、39.36%)、α-香柠檬烯(10.00%、9.28%)、柏木烯(9.46%、9.73%)、τ-古芸烯(7.07%、6.85%)、花柏烯(2.20%、2.52%)等;其中醛类分别有0、1 个(占总量的1.82%),烯类43 种(占总量79.63%)、41 种(占总量74.55%),醇类7 个(占总量的12.96%)、6 个(占总量的10.91%),酯类1 个(占总量的1.85%)、1 个(占总量的1.82%),其他为3 个(占总量的5.56%)、6 个(占总量的10.91%)。
2.3 南五味子和北五味子挥发油成分的比较
五味子中挥发油成分主要为各种萜类化合物。单萜类如莰烯、蒎烯、水芹烯、罗勒烯等相对分子质量为136的物质;倍半萜类如榄香烯、石竹烯、古芸烯、依兰烯、柏木烯等相对分子质量为204的物质。此外,挥发油中还有少量的醇、酯、醛、酮以及苯的衍生物等。结果表明:SD法和UMASD法提取得到的南、北五味子挥发油成分中共有成分均约90%,说明超声波没有改变提取对象的化学结构。从提取时间来看,UMASD大大缩短了提取时间,具有快速、高效、节能等优点。UMASD法所得到的低沸点物质较SD法多,表明UMASD法利于获得挥发油中低沸点物质;南五味子和北五味子中挥发油共有成分20 个,北五味子中依兰烯的含量远远高于南五味子。朱凤妹等[23]采用气相色谱-质谱联用方法从北五味子挥发油中分离并鉴定出39 种成分,主要为依兰烯(14.34%)、2,6-二甲基-双环[3.1.1]庚-2-烯(10.38%)等;毛日文等[24]采用超临界流体CO2提取法和水蒸气蒸馏法提取南五味子挥发油成分,SFE-CO2提取南五味子挥发油鉴定出16 个成分,南五味子水蒸汽蒸馏的挥发油鉴定出24 个成分。主要成分分别为依兰烯(19.03%、20.5%)、α-铅笔柏油烯(9.7%、10.05%)、花柏烯(1.64%、1.44%)等。南五味子和北五味子的主要化学成分(如依兰烯等)与文献[23-24]报道的挥发油的主要化学成分基本一致,但也存在一定的差异,这可能是因为不同的产地,气候等因素对南五味子和北五味子的化学成分有一定的影响。
3 结3 论
运用UMASD、SD结合GC-MS技术分析了南五味子和北五味子挥发油中的化学成分,实验过程中两种方法均采用水作为溶剂,对操作者身体无伤害,具有绿色、环保等优点。采用两种方法对不同品种的五味子进行挥发油提取,所得到的挥发油外观性状均为淡黄色透明液体,且UMASD法精油收率略高于SD法,北五味子的精油收率较南五味子的收率高;两种方法提取得到的同种五味子的挥发油成分和含量也有一定的差异,且UMASD法更有利于低沸点挥发油成分的提取;南五味子和北五味子中挥发油成分和含量差异较大。UMASD整个过程仅需1 h,而SD需6 h,UMASD大大缩短了提取时间,降低了提取过程的能量消耗,且分离和鉴定出的化学成分略多于其他方法。超声微波协同萃取技术具有装置简单、操作方便和节约时间等优点,是提取植物挥发油成分的一种快速可行的方法。
[1]王文燕, 陈建光. 五味子的药理作用及开发研究[J]. 北华大学学报,2007, 8(2): 128-133.
[2]齐治, 崔景荣, 田建柱, 等. 五味子果实挥发油对中枢神经系统的药理作用研究[J]. 北京医科大学学报, 1988, 20(6): 157-158.
[3]胡双丰, 杨志芬. 北五味子与南五味子的鉴别[J]. 中医学报, 2010,25(6): 1149-1150.
[4]LOU Zaixiang, WANG Hongxing, ZHU Song, et al. Ionic liquids based simultaneous ultrasonic and microwave assisted extraction of phenolic compounds from burdock leaves[J]. Analytica Chimica Acta,2011, 716: 28-33.
[5]CHENG Xiaolan, WAN Jinyi, LI Ping, et al. Ultrasonic/microwave assisted extraction and diagnostic ion filtering strategy by liquid chromatography-quadrupole time-of-flight mass spectrometry for rapid characterization of flavonoids in Spatholobus suberectus[J]. Journal of Chromatography A, 2011, 1218(34): 5774-5786.
[6]CHAN C, YUSOFFA R, NGOH G, et al. Microwave-assisted extractions of active ingredients from plants[J]. Journal of Chromatography A, 2011, 1218(37): 6213-6225.
[7]张斌, 许莉勇. 超声萃取技术研究与应用进展[J]. 浙江工业大学学报, 2008, 36(5): 558-561.
[8]LAGHA A, CHEMAT S, BARTELS P V, et al. Microwave-ultrasound combined reactor suitable for atmospheric sample preparation procedure of biological and chemical products[J]. Analusis, 1999,27(5): 452-457.
[9]胡吾居, 李雄辉, 熊伟, 等. 椪柑果皮精油集成提取新技术研究[J].食品工业, 2012(1): 42-45.
[10]LU Chunxia, WANG Hongxin, L Wengpin, et al. Ionic liquid-based ultrasonic/microwave-assisted extraction combined with UPLC for the determination of anthraquinones in rhubarb[J]. Chromatographia,2011, 74(1): 139-144.
[11]刘春娟, 邹世春. 超声-微波协同萃取分离、气相色谱-质谱联用测定土壤中多环芳烃[J]. 理化检验: 化学分册, 2008, 44(5): 421-426.
[12]LIU Ruilin, SONG Shuanghong, WU Wei, et al. Rapid analysis of fatty acid profiles in raw and seeds by microwave-ultrasonic synergistic in situ extraction-deriatisation and gas chromatographymass spectrometry[J]. Food Chemistry, 2013, 141(4): 4269-4277.
[13]ZHANG Lianfu, LIU Zelong. Optimization and comparison of ultrasound/microwave assisted extraction (UMAE) and ultrasonic assisted extraction (UAE) of lycopene from tomatoes[J]. Ultrasonics Sonochemistry, 2007, 15(5): 731-737.
[14]ZHOU Ting, XIAO Xiaohua, LI Gongke. Hybrid field-assisted solid-liquid-solid dispersive extraction for the determination of organochlorine pesticides in tobacco with gas chromatography[J].Analytical Chemistry, 2012, 84(1): 420-427.
[15]LOU Zaixiang, WANG Hongxing, ZHU Song, et al. Improved extraction and identification by ultra performance liquid chromatography tandem mass spectrometry of phenolic compounds in burdock leaves[J]. Journal of Chromatography A, 2010, 1217(16): 2441-2446.
[16]李桂军, 张艳婷, 李良. 南五味子挥发油化学成分分析[J]. 河北化工,2008, 38(10): 66-68.
[17]MA Chunhui, LIU Tingting, YANG Lei, et al. Ionic liquidbased microwave-assisted extraction of essential oil and biphenyl cyclooctene lignans from Schisandra chinensis Baill fruits[J]. Journal of Chromatography A, 2011, 1218(48): 8573-8580.
[18]MA Chunhui, YANG Lei, ZU Yuangang, et al. Optimization of conditions of solvent-free microwave extraction and study on antioxidant capacity of essential oil from Schisandra chinensis (Turcz.)Baill[J]. Food Chemistry, 2012, 134(4): 2532-2539.
[19]WANG Longhu, CHEN Yangsheng, SONG Yanting, et al. GC-MS of volatile components of Schisandra chinensis obtained by supercritical fluid and conventional extraction[J]. Journal of Separation Science,2008, 31(18): 3238-3245.
[20]应国清, 余志明, 单剑锋, 等. 北五味子有效组分的研究进展[J]. 河南中医, 2005, 25(6): 85-87.
[21]戴好富, 余志明, 单剑锋, 等. 北五味子挥发性化学成分的研究[J].中草药, 2006, 6(9): 1309-1310.
[22]李祖光, 孟微微, 王芳, 等. 超声微波协同水蒸气蒸馏-GC/MS分析生姜挥发油化学成分[J]. 浙江工业大学学报, 2013, 41(6): 614-619.
[23]朱凤妹, 杜彬, 李军, 等. 气相色谱- 质谱法测定北五味子中挥发油成分[J]. 食品与发酵工业, 2008, 34(8): 149-152.
[24]毛日文, 张敏, 徐佐旗, 等. 超临界流体CO2提取法和水蒸气蒸馏法提取南五味子挥发油的成分比较[J]. 食品与药品, 2011, 13(5): 189-191.
