α-硫辛酸对糖尿病周围神经病变的疗效及氧化应激的影响
2014-06-05陈若平徐将林海燕陈国平鲍溪荷荆春艳叶山东
陈若平,徐将,林海燕,陈国平,鲍溪荷,荆春艳,叶山东
(1.安徽医科大学附属省立医院、安徽省立医院内分泌科,合肥 230001;2.安徽省疾病预防控制中心急性传染病防治科)
α-硫辛酸对糖尿病周围神经病变的疗效及氧化应激的影响
陈若平1,徐将1,林海燕1,陈国平2,鲍溪荷1,荆春艳1,叶山东1
(1.安徽医科大学附属省立医院、安徽省立医院内分泌科,合肥 230001;2.安徽省疾病预防控制中心急性传染病防治科)
目的观察α-硫辛酸(ALA)对2型糖尿病患者糖尿病周围神经病变(DPN)的临床疗效,并观察其对氧化应激的影响。方法48例DPN患者用随机数字表法分为两组,对照组24例予以甲钴胺口服治疗,观察组24例予以ALA口服治疗,疗程6个月,比较两组治疗前后神经病变自觉症状问卷(TSS)评分,运动神经传导速度(MNCV)和感觉神经传导速度(SNCV),血清丙二醛(MDA)、超氧化物歧化酶(SOD)和谷胱甘肽过氧化物酶(GSH-Px)水平。结果两组患者治疗后均较同组治疗前TSS评分降低(P<0.01)及神经传导速度加快(P<0.05);观察组治疗前后TSS评分降低及神经传导速度变化增加均较对照组显著(P<0.05)。观察组治疗后较治疗前血清MDA水平显著降低(P<0.05),SOD和GSH-Px活性显著增加(P<0.05),而对照组治疗前后差异无统计学意义(P>0.05),观察组血清MDA、SOD和GSH-Px前后变化较对照组显著(P<0.05)。结论ALA可显著改善患者临床症状,提高神经传导速度,减轻机体氧化应激,其疗效优于甲钴胺。
糖尿病神经病变;硫辛酸;氧化性应激;神经传导
糖尿病周围神经病变(DPN)是糖尿病最常见 的慢性并发症之一,其发生率占糖尿病患者50%以上,是糖尿病患者高致死致残率的重要危险因素。DPN发病机制复杂,临床表现多样,临床尚缺乏十分有效的防治措施。近来研究认为氧化应激是糖尿病慢性并发症发生发展的中心环节,包括DPN,抗氧化应激成为临床防治DNP的热点。α-硫辛酸(ALA)属于维生素B类化合物,有研究提示其可有效改善DPN症状体征[1-2]。本研究通过临床试验旨在观察ALA对2型糖尿病(T2DM)并发DPN患者的临床疗效和抗氧化作用,并与甲钴胺进行比较。
1 对象与方法
1.1 研究对象 选取2009年6月至2010年9月在安徽省立医院内分泌门诊确诊2型糖尿病并有明显自发性疼痛和(或)麻木等神经病变症状的患者48例,男27例,女21例;年龄32~68岁,平均年龄(58.3±9.2)岁;用随机数字表法将受试者分为对照组和观察组,每组24例患者。所有患者均排除继发性糖尿病,其他严重肾脏疾病、肝胆疾病,尿路感染和恶性肿瘤等。对照组和观察组年龄、体质量指数(BMI)、血压、空腹血糖(FPG)、餐后2h血糖(PPG)、血肌酐(Cr)及糖化血红蛋白(HbA1c)比较均差异无统计学意义(P>0.05)。
1.2 方法
1.2.1 治疗方法 所有T2DM患者均糖尿病饮食、运动基础上,予以口服降糖药物或胰岛素治疗,将血糖控制在FPG<8.0 mmol/L,PPG<10 mmol/L。对照组每天口服甲钴胺1.5 mg(山东鲁抗辰欣药业有限公司产),观察组每天口服ALA 600 mg(山东烟台只楚药业有限公司产),疗程均为6个月。患者均签署知情同意书,治疗方案经医院伦理学会批准。
1.2.2 观察指标 记录研究对象性别、年龄、病程、BMI、收缩压(SBP)、舒张压(DBP)、症状和体征;采用葡萄糖氧化酶法测定FPG和PPG;采用离子交换层析法测定HbA1c;全自动生化分析仪测定血Cr和尿Cr,放射免疫法测定尿白蛋白;黄嘌呤氧化酶法测定血清丙二醛(MDA),硫代巴比妥酸法测定超氧化物歧化酶(SOD),DTNB显色法测定谷胱甘肽过氧化物酶(GSH-PX)。
患者神经病变症状采用“神经病变主觉症状问卷(TSS)”对患者对下肢及足部疼痛、灼热感、感觉异常、麻木4项症状的程度和频率进行评分和汇总评估。运动神经传导速度(MNCV)和感觉神经传导速度(SNCV)采用丹麦Dantec Keypoint神经肌电图仪测定,数据取双侧肢体传导速度的平均值。
1.3 统计学处理 采用SPSS 13.0统计软件,组间数据分析采用独立样本t检验,组内治疗前后差异分析采用配对t检验。
2 结果
2.1 两组治疗前后TSS评分比较 治疗前两组患者TSS评分比较差异无统计学意义(P>0.05);两组患者治疗后与治疗前相比较,TSS总评分均明显减少,观察组疼痛、麻木、灼热感及感觉异常4项阳性症状评分较前均明显改善(P<0.01),对照组除疼痛症状评分无显著变化外(P>0.05),余麻木、灼热感及感觉异常症状均较治疗前显著改善(P<0.01);治疗后观察组疼痛、麻木和灼热感症状评分及TSS总评分下降率较对照组明显,差异有统计学意义(P<0.01),见表1。
2.2 两组治疗前后神经传导速度比较 两组患者治疗前神经传导速度比较均差异无统计学意义(P>0.05)。治疗6月后,两组患者SNCV及MNCV均较治疗前明显增快(P<0.05),但对照组治疗前后腓总神经传导速度比较差异无统计学意义(P>0.05)。治疗后观察组腓总神经和胫神经的SNCV传导速度增加率较对照组明显,差异有统计学意义(P<0.05);两组MNCV传导速度增加率差异无统计学意义(P>0.05),见表2。
表1 两组患者治疗前后TSS评分比较(±s,分)

表1 两组患者治疗前后TSS评分比较(±s,分)
注:与同组治疗前比较,aP<0.01;与对照组治疗后比较,bP<0.01
组别 例数 疼痛治疗前 治疗后麻木治疗前 治疗后灼热感治疗前 治疗后感觉异常治疗前 治疗后总评分治疗前 治疗后对照组 24 1.42±1.02 1.25±0.74 2.04±1.00 1.08±0.78a1.54±1.10 0.88±0.99a2.04±1.20 1.17±1.09a7.04±3.03 4.38±2.37a观察组 24 1.50±0.98 0.88±0.85ab2.33±0.76 0.96±0.95ab1.38±0.88 0.42±0.78ab1.79±1.78 0.96±0.91a7.04±2.69 3.29±1.83ab
表2 两组患者治疗前后神经传导速度比较(±s,m/s)

表2 两组患者治疗前后神经传导速度比较(±s,m/s)
注:与同组治疗前比较,aP<0.05;与对照组治疗后比较,bP<0.05
组别 例数 正中神经的SNCV治疗前 治疗后腓总神经的SNCV治疗前 治疗后胫神经的SNCV治疗前 治疗后腓总神经的SNCV治疗前 治疗后胫神经的SNCV治疗前 治疗后对照组 24 45.08±6.13 48.85±4.97a45.04±6.29 46.46±6.89 33.38±4.45 35.71±4.33a43.88±3.01 45.65±3.44a41.87±2.76 44.29±3.21a观察组 24 46.40±6.38 48.73±5.30a45.19±5.03 47.96±4.69ab33.80±5.85 37.51±5.77ab42.90±5.11 44.68±5.51a42.90±4.63 45.41±3.91a
表3 两组患者治疗前后氧化应激指标比较(±s)
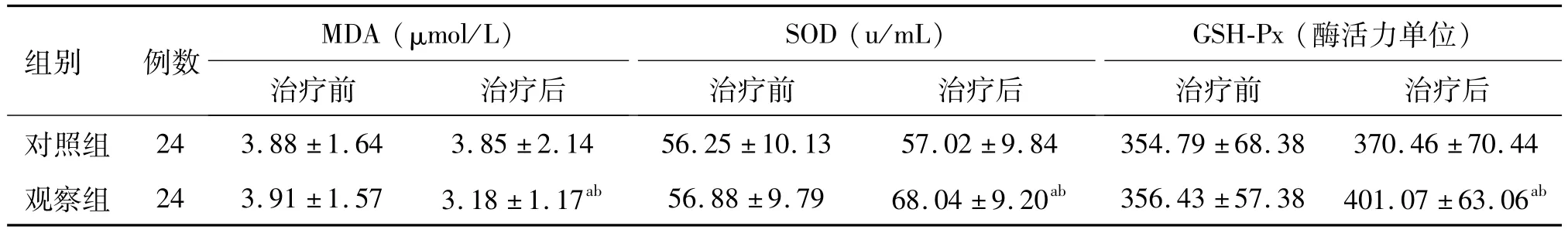
表3 两组患者治疗前后氧化应激指标比较(±s)
注:与同组治疗前比较,aP<0.05;与对照组治疗后比较,bP<0.05
组别 例数 MDA(μmol/L)治疗前 治疗后SOD(u/mL)治疗前 治疗后GSH-Px(酶活力单位)治疗前 治疗后对照组 24 3.88±1.64 3.85±2.14 56.25±10.13 57.02±9.84 354.79±68.38 370.46±70.44观察组 24 3.91±1.57 3.18±1.17ab 56.88±9.79 68.04±9.20ab356.43±57.38 401.07±63.06ab
2.3 两组治疗前后氧化应激指标变化 两组患者治疗前氧化应激指标MDA、SOD及GSH-Px水平差异无统计学意义(P>0.05)。两组分别采用甲钴胺或ALA治疗6月后,观察组患者较治疗前SOD活力显著升高,MDA含量显著降低,GSH-Px活力显著升高,差异均有统计学意义(P<0.05);但对照组治疗前后MDA、SOD及GSH-Px水平变化差异无统计学意义。两组患者治疗后氧化应激指标MDA、SOD及GSH-Px水平差异有统计学意义(P<0.05),见表3。
3 讨论
近年来,细胞线粒体电子呼吸链超氧化物产生过多导致氧化应激损伤被认为是包括DPN在内的糖尿病慢性并发症的共同机制[3]。长期高血糖通过机体氧化应激增加,脂质过氧化物和活性氧产生增多,使糖基化终末产物异常增加,微血管内皮损伤、滋养神经微血管缺血缺氧,导致神经营养障碍,多元醇代谢紊乱、神经因子减少、肌醇减少,进而周围神经轴突萎缩变性、髓鞘节段性或弥散性皱缩或脱髓鞘病变[4-5]。甲钴胺是甲基转移酶辅酶,是目前临床常用治疗DPN药物,其可直接转入神经细胞、促进轴索内蛋白质合成,促进神经髓鞘主要结构磷脂酰胆碱的合成,提高髓鞘的形成,加快损伤神经修复[6-7]。本研究对照组表明口服甲钴胺治疗可降低患者TSS评分,加快除腓总神经外多个感觉与运动神经传导速度。ALA是一种强抗氧化剂,多项研究证实其可改善DPN临床症状;本研究观察组我们严格控制血糖基础上连续口服应用ALA治疗6月也证实其显著提高感觉神经和运动神经传导速度,明显改善T2DM患者疼痛、麻木、灼热感和感觉异常症状,其临床疗效优于甲钴胺,与国内外研究相一致[2-3,8-10]。
ALA是线粒体酶系复合物的辅助因子,其在体内可转化为还原型二氢硫辛酸(DHLA),两者均为强抗氧化剂[11-12]。ALA与DHLA在体内可直接清除以超氧阴离子为代表自由基和活性氧;并可还原再生谷胱甘肽(GSH)、维生素C、维生素E等维持机体内抗氧化剂水平,减轻脂质过氧化[5]。SOD能清除超氧阴离子保护细胞免受损伤,对机体氧化与抗氧化平衡具有重要作用;MDA是脂质过氧化物产物,可反映体内脂质过氧化程度;GSH-Px可清除活性氧和自由基诱发的脂质过氧化,促进过氧化氢与还原型GSH反应生成氧化型GSH,保护细胞膜结构和功能的完整性。本研究显示ALA治疗后患者患者神经传导速度加快同时患者血清SOD活力、GSH-Px水平显著提高,血清MDA含量较前明显减少,提示ALA可有效提高机体抗氧化应激能力,抑制脂质过氧化,表明ALA对DPN的临床疗效与改善机体氧化应激相关。
因此,在严格控制血糖基础上予以ALA长期治疗可显著提高机体抗氧化应激能力,显著改善周围神经的临床症状,提高神经传导速度,保护DPN的神经损伤,对改善糖尿病患者生活质量有益。
[1] Ametov AS,Barinov A,Dyck PJ,et al.The sensory symptoms of diabetic polyneuropathy are improved with alphalipoic acid:the SYDNEY trial[J].Diabetes Care,2003,26(3):770-776.
[2] Ziegler D,Nowak H,Kempler P,etal.Treatmentof symptomatic diabetic polyneuropathy with the antioxidant alpha-lipoic acid:ameta-analysis[J].DiabetMed,2004,21(2):114-121.
[3] Brownlee M.Biochemistry and molecular cell biology of diabetic complications[J].Ature,2001,414(6865):813-820.
[4] Kubo E,Urakami T,Fatma N,et al.Polyol pathway-dependent osmotic and oxidative stresses in aldose reductase-mediated apoptosis in human lens epithelial cells:role of AOP2[J].Biochem Biophys Res Commun,2004,314(4):1050-1056.
[5] 章晓燕,刘芳,贾伟平.硫辛酸与糖尿病周围神经病变[J].国外医学:内分泌学分册,2005,25(4):262-264.
[6] Zin CS,Nissen LM,Smith MT,et al.An update on the pharmacological management of post-herpetic neuralgia and painful diabetic neuropathy[J].CNSDrugs,2008,22(5):417-442.
[7] 赵凡,区转焕,郭翼华.甲钴胺对糖尿病冠心病患者的血浆同型半胱氨酸的干预研究[J].中国临床保健杂志,2006,9(2):154-155.
[8] 刘芳,张扬,杨明,等.α-硫辛酸对糖尿病患者周围神经病变的治疗作用[J].中华医学杂志,2007,87(38):2706-2709.
[9] 宋利格,李颖,周筠,等.α-硫辛酸对糖尿病周围神经病变的疗效[J].中华内分泌代谢杂志,2007,23(2):166-167.
[10]唐奇志,陈聪,张燕华.α-硫辛酸治疗2型糖尿病周围神经病变的临床研究[J].中国糖尿病杂志,2011,19(6):444-446.
[11]黄海,祝开思,王平,等.α-硫辛酸联合前列腺素E1治疗糖尿病性单一神经病变疗效观察[J].中国临床保健杂志,2009,12(1):74.
[12]林海燕,徐将,叶山东.硫辛酸对2型糖尿病患者尿8-羟基脱氧鸟苷排泄的影响[J].中国临床保健杂志,2013,16(1):16-18.
Efficacy of alpha-lipoic acid in treating diabetic peripheral neuropathy and its influence on the oxidative stress
CHEN Ruoping*,XU Jiang,LIN Haiyan,CHEN Guoping,BAO Xihe,JINGChunyan,YE Shandong(*Depart-ment of Endocrinology,the Affiliated Provincal Hospital of Anhui Medical University,Hefei230001,China)
YE Shandong,Email:ysd196406@163.com
ObjectiveTo investigate the effect of alpha-lipoic acid(ALA)in the treatment of diabetic peripheral neuropathy(DPN)and its influence on the oxidative stress.Methods48 patients with DPN were randomly divided into control group and observation group with each group of24 cases,the control group was given oral therapy withmecobalamin and the observation group was given oral therapy with ALA for6 months.The total symptoms scores(TSS),the nerve conduction velocity,the serum levels ofmalonaldehyde(MDA),superoxide dismutase(SOD)and glutathione peroxidase(GSH-Px)were compared before and after treatment in both groups.Resu lts Compared with before treatment,the TSSwas decreased(P<0.01)and nerve conduction velocity was accelerated significantly(P<0.05)after 6 months of treatment in both groups.Compared with before treatment,the serum level of MDA was decreased significantly(P<0.05),the serum levels of SOD and GSH-Px were increased significantly(P<0.05)in observation group,while slightly in control group(P>0.05).Comepared with the control group,the TSSdecrease,the nerve conduction velocity accelerated degree and the level changes of MDA,SOD and GSH-Px of the observation group weremore obvious after treatment(P<0.05).ConclusionALA can effectively improve the clinical symptoms,accelerate the nerve conduction velocity and inhibit the oxidative stress of DPN patients.
Diabetic Neuropathies;Thioctic acid;Neural Conduction
R587.25
A
10.3969/J.issn.1672-6790.2014.06.003
2014-09-12)
安徽高校省级自然科学研究项目(KJ2011A157);安徽医科大学科研基金项目(2011xkj068)
陈若平,副主任医师,Email:chrp2009@163.com
叶山东,博士,教授,博士生导师,Email:ysd196406@163.com
