表面活性剂辅助抗溶剂法制备缬沙坦超微粉体
2014-05-11于世华程振玉
于世华,王 洁,陈 萍,程振玉,张 俭
(吉林化工学院化学与制药工程学院,吉林 吉林 132022)
表面活性剂辅助抗溶剂法制备缬沙坦超微粉体
于世华,王 洁,陈 萍,程振玉,张 俭
(吉林化工学院化学与制药工程学院,吉林 吉林 132022)
采用表面活性剂辅助,抗溶剂沉淀法制备了缬沙坦药物微粉,以 丙酮为溶剂,水为抗溶剂,考察了表面活性剂种类、浓度、溶剂-抗溶剂体积比对缬沙坦形貌和大小的影响。分别利用扫描电镜(SEM)、X射线衍射(XRD)、红外光谱( FT-IR)等分析方法对原料及微粉化的产品进行了表 征。
缬沙坦;抗溶剂沉淀法;微粉化
缬沙坦,化学名为N-(1-戊酰基)-N-[4-[2-(1H-四氮唑-5-基)苯基]苄基]-L-缬氨酸,是一种非肽类血管紧张肽受体拮抗药[1]。药物微粉化是一种快速有效的改善药物溶出度,提高生物利用度的技术[2]。药物微粉化可以增加药物的比表面积,增大药物的溶出速率,提高吸收速率,从而提高生物利用度 。常用的药物微粉化技术有超临界萃取法[3]、高压均质法[4]和反应结晶法[5]等。超临界萃取和高压均质技术设备投资高,操作条件要求苛刻,得到的微粉粒径分散不均匀。反应结晶法仅适用于含有羟基和羧基的药物粉体的制备。反溶剂重结晶法通过加入药物的不良溶剂改变其饱和溶解度而使药物颗粒重新结晶析出,故成为制备微粉化药物的又一种重要方法[6]。
1 实验部分
1.1 试剂与仪器
缬沙坦(纯度99.9%),丙酮(分析纯),乙醇(分析纯),羟丙甲纤维素(分析纯),β-环糊精(99%分析纯),十二烷基硫酸钠(化学纯),聚乙烯吡咯烷酮K30,蒸馏水(实验室自制)。
JSM-6490LV扫描电镜,UV-2550紫外可见分光光度计,D8 FOCUS X射线衍射仪,Nicolet6700傅里叶红外光谱仪。
1.2 缬沙坦药物微粉的制备
采用丙酮为溶剂,蒸馏水为反溶剂探讨了各个条件对产品形貌及粒径的影响,主要包括表面活性剂种类、质量浓度、溶剂-抗溶剂体积比。对所制得的微粉分别采用扫描电镜(SEM)、X射线衍射(XRD)、红外光谱分析( FT-IR)等方法对原料及产品的性质进行表征。
2 结果与讨论
2.1 不同实验条件对颗粒形貌和大小的影响
2.1.1 表面活性剂种类及浓度的影响
实验分别考察了羟丙基甲基纤维素、β-环糊精、十二烷基硫酸钠、聚乙烯吡咯烷酮4种表面活性剂的影响。药物和表面活性剂的比例为1∶1。药物溶液通过恒温磁力搅拌慢慢加入到水相中,最终得到缬沙坦药物的悬浮液。将4种悬浮液静止沉积大约15h左右,羟丙基甲基纤维素为沉淀、乳白色透明液体,β-环糊精为完全沉淀、溶液澄清透明,十二烷基硫酸钠钠为完全沉淀、溶液澄清透明,聚乙烯吡咯烷酮为微量沉淀、溶液呈悬浮液。根据Noyese-Whitney方程[8]可知,颗粒直径与沉降速度成反比。综上所述最佳表面活性剂为聚乙烯吡咯烷酮。在丙酮作为溶剂,蒸馏水作为反溶剂的条件下,抗溶剂-溶剂比为15,磁力搅拌转速为1000r·min-1且搅拌30s条件下,分别考察了0.05%、0.1%、0.2%、0.4%这4个质量浓度对颗粒大小的影响。表面活性剂浓度与颗粒大小的关系如图1所示。
从图1可以看出,聚乙烯吡咯烷酮质量浓度为0~0.05%时,部分颗粒有团聚现象;当聚乙烯吡咯烷酮质量浓度为0.2%~0.4%时,产物颗粒分散较好,但形貌不规则;当聚乙烯吡咯烷酮质量浓度为0.1%时,颗粒分散又趋于良好且形貌规则。综上分析,确定的聚乙烯吡咯烷酮的质量浓度为0.1%。

图1 表面活性剂浓度对颗粒大小的影响
2.1.2 抗溶剂-溶剂体积比的影响
过饱和度是沉淀过程的推动力,而抗溶剂-溶剂体积比是影响体系过饱和度的重要因素。在丙酮作为溶剂,蒸馏水作为抗溶剂,药物浓度为80mg·mL-1,聚乙烯吡咯烷酮质量浓度为0.1%,磁力搅拌强度为1000r·min-1且搅拌30s的条件下,分别考察了10、15、20、25这4组抗溶剂-溶剂体积比对颗粒大小的影响,实验结果如图2所示。

图2 抗溶剂-溶剂体积比对颗粒大小的影响
在一定温度下,增大抗溶剂-溶剂体积比,可以降低缬沙坦在体系中的溶解度,从而增大体系的过饱和度,得到粒度分布窄的颗粒。但是当溶剂与反溶剂比例达到一定值时,增大溶剂的用量对晶体的成核和生长过程影响不大,所以选取抗溶剂与溶剂体积比为15。
2.2 缬沙坦药物微粉的表征
2.2.1 FT-IR分析
图3为缬沙坦原料及微粉化的FT-IR谱图。通过对比可以看出,微粉化前后吸收峰位置和强度几乎未发生变化,由此可见,微粉化前后缬沙坦的化学结构并未发生改变。
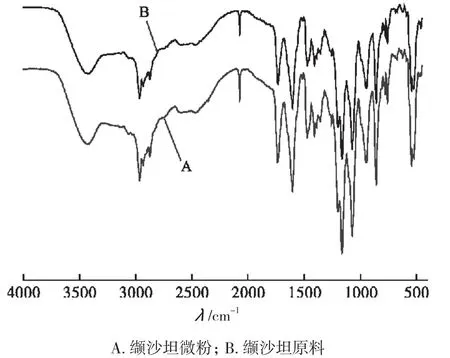
图3 缬沙坦FT-IR谱图
2.2.2 X-射线衍射分析(XRD)
图4为缬沙坦原粉及微粉的XRD谱图。从图4可以看出,微粉化以后缬沙坦衍射峰的强度降低,说明微粉化前后药物的结晶度明显下降,且微粉化以后半高宽变大,说明微粉化以后粒度减小。
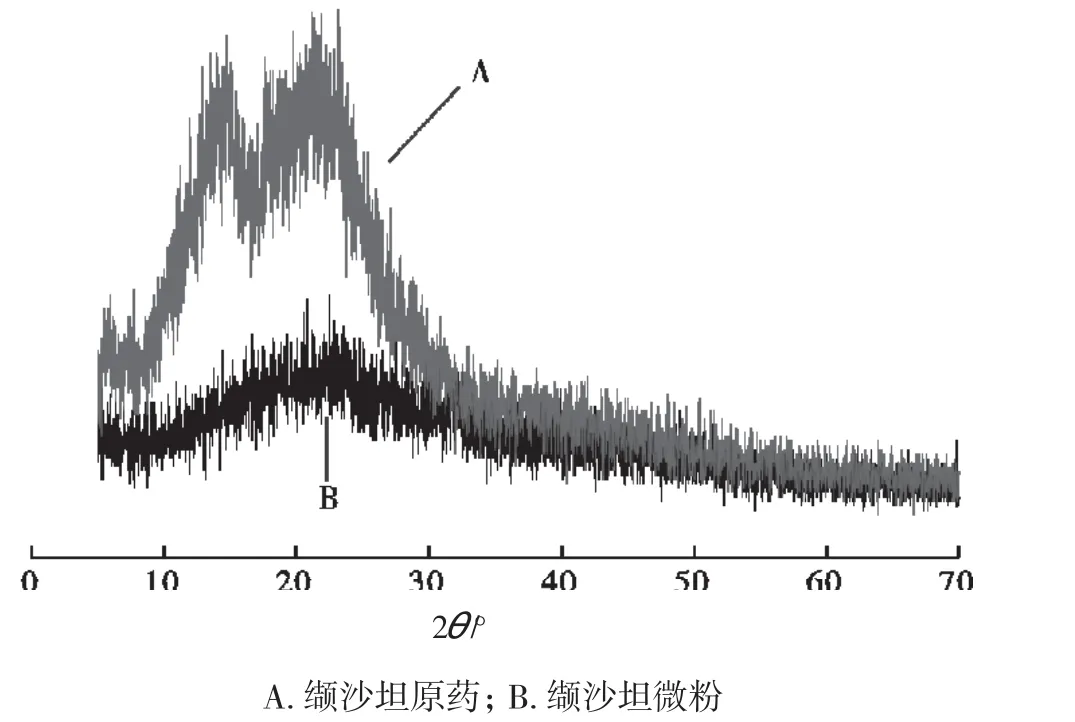
图4 缬沙坦XRD谱图
3 结论
以丙酮作为溶剂,蒸馏水作为抗溶剂,主要考察了表面活性剂种类、浓度、溶剂-抗溶剂体积比对缬沙坦的颗粒形貌和大小的影响,结果表明,在溶液中缬沙坦的浓度80mg·mL-1,溶剂与反溶剂体积比1∶15,表面活性剂聚乙烯吡咯烷酮的质量浓度为0.1%,磁力搅拌转速1000 r·min-1时,可得到粒径约为0.36μm且形貌规则、粒度分布较窄的缬沙坦药物微粉。
[1] 刘红梅,刘艳,程彦文,等.国产和进口缬沙坦胶囊的人体生物利用度[J].中国医院药学杂志,2001,21(12):724-726.
[2] 平其能.纳米药物和纳米载体系统[J].中国新药杂志,2002,11(1):42-45.
[3] Imsanguan P, Pongamphai S, Douglas S, et al. Supercritical antisolvent precipitation of andrographolide from Andrographis paniculata extracts:Effect of pressure,temperature and CO2flow rate[J].Original Research Article Powder Technology, 2010, 200(3): 246-253.
[4] Müller R H, Jacob C, Kayser O. Nanosuspensions as particulate drug formulations in therapy:rationale for development and what we can expect for the future[J].Advanced Drug Delivery Reviews, 2001, 47(1): 3-19.
[5] 杨芳,沈志刚,陈建峰.反应结晶法制备萘普生超细微粒[J].北京化工大学学报,2006,33(3):16-18.
[6] T.O’Ciardha C, Patrick J. Frawley N A.Mitchell.Estimation of the nucleation kinetics for the anti-solvent crystallisation of paracetamol in methanol/water solutions[J].Journal of Crystal Growth, 2011(328): 50-57.
[7] Date A A, Patravale V B.Current strategies for engineering drug nanoparticles[J].Current Opinion in Colloid & Interface Science, 2004(9):222-235.
Preparation of Valsartan Nanoparticles by Antisolvent Precipitation with Surfactants
YU Shi-hua, ZHANG Jian, CHENG Zhen-yu, CHEN Ping
(College of Chemical & Pharmaceutical Engineering, Jilin Institute of Chemical Technology, Ji lin 132002, China)
Valsartan nanoparticles were suc cessfully prepared by a ant isolvent precipitation method in presence of surfactants. The effects of various experimental variables (the types, concentrations of surfacta nts and the anti-solvent/solvent (AS/S) vol ume ratio) on the particle size of valsartan were investigated in the acetone-deionized water system.The as-prepared particles were characterized by SEM, XRD FT-IR techniques.
valsartan; anti-solvent deposition; micronization
TQ 423
A
1671-9905(2014)12-0020-02
于世华(1984-),助教,硕士研究生,研究方向为药物微粉制备及水溶性研究,E-mail:ysh@jlict.edu.cn
2014-11-03
