氯诺昔康-铜(Ⅱ)-牛血清白蛋白三元配合物的荧光光谱法研究
2014-05-10王晓霞张文宁王正德刘云颖
王晓霞,张文宁,王正德,刘云颖,闫 慧
(内蒙古科技大学化学与化工学院,内蒙古 包头 014010)
氯诺昔康-铜(Ⅱ)-牛血清白蛋白三元配合物的荧光光谱法研究
王晓霞,张文宁,王正德,刘云颖,闫 慧
(内蒙古科技大学化学与化工学院,内蒙古 包头 014010)
在生理条件下,用荧光光谱法研究了氯诺昔康对牛血清白蛋白,铜(Ⅱ)对牛血清白蛋白以及铜(Ⅱ)对氯诺昔康和牛血清白蛋白荧光光谱特性的影响。铜(Ⅱ)和氯诺昔康均可使牛血清白蛋白的荧光强度发生猝灭,在铜(Ⅱ)存在下,氯诺昔康对牛血清白蛋白的荧光猝灭作用显著增强。根据荧光猝灭双倒数图计算氯诺昔康和牛血清白蛋白之间的结合常数是5.43×105,结合位点数是1.14。铜(Ⅱ)和牛血清白蛋白之间的结合常数是2.10×105,结合位点数是0.78。
荧光光谱法;牛血清白蛋白(BSA);铜(Ⅱ);氯诺昔康;三元配合物
氯诺昔康为非甾体类消炎镇痛药,系噻嗪类衍生物。它通过抑制环氧合酶(COX)的活性来抑制前列腺素合成,具有较强的镇痛和抗炎作用[1]。
铜是生命元素之一,人体缺铜会导致失眠,血液中胆固醇增高,引起冠心病,心血管功能降低,会出现记忆减退,思维混乱,反应迟钝等症状[2]。
血浆中含量最丰富的载体蛋白是血清白蛋白,许多内源化合物及其药物与它的相互作用已广泛被研究[3-4]。文献中对氯诺昔康、血清白蛋白和金属离子三元配合物体系的研究较少。本文通过荧光光谱法研究了氯诺昔康、牛血清白蛋白和铜(Ⅱ)三元配合物的荧光特性,并且确定了结合反应的结合常数和结合位点数。
1 实验部分
1.1 仪器与试剂
F-4600型荧光分光光度仪,HH-S型数显恒温水浴锅。
牛血清白蛋白(BSA),氯诺昔康,三羟甲基氨基甲烷(Tris),盐酸,氯化钠,氯化铜(均为分析纯)。实验用水为去离子二次蒸馏水,无荧光杂质。
BSA溶液:以pH=7.0,0.05mol·L-1的Tris-HCl溶液配制成浓度为1.0×10-5mol·L-1,以0.1mol·L-1NaCl维持离子强度。
氯诺昔康溶液:以pH=7.0,0.1 mol·L-1的Tris-HCl溶液配制成浓度为1.0×10-5mol·L-1,以0.1mol·L-1NaCl维持离子强度。
CuCl2溶液:1×10-2mol·L-1,1×10-3mol·L-1,1×10-4mol·L-1pH=7的Tris-HCl缓冲溶液。
1.2 试验方法
(1) 分别取一定量的BSA(1.0×10-5mol·L-1),[BSA]∶[1×10-4mol·L-1Cu2+]=1∶1的混合物,BSA与氯诺昔康(浓度1∶1),Cu2+和BSA-氯诺昔康(1∶1)以及氯诺昔康(1.0×10-5mol·L-1)于1cm比色皿中,以荧光激发波长为280nm,发射波长狭缝宽度为5nm,测定346nm处的荧光发射光谱强度(图1)。
(2)取1mL 1.0×10-5mol·L-1BSA溶液分别加入到9个相同的10mL比色管中,再逐次加入0、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0mL 1.0×10-5mol·L-1的氯诺昔康,二次水定容至刻度,摇匀,以相同的参数分别测定该系列荧光发射强度,结果见表1。
(3)取1mL 1.0×10-5mol·L-1BSA溶液分别加入到9个相同的10mL比色管中,逐次加入0、0.5、1.0、1.5、2.0、2.5、3.0、3.5 mL 1.0×10-4mol·L-1的Cu2+,二次水定容至刻度,充分摇匀,以相同的参数分别测定该系列荧光发射强度,结果见表2。
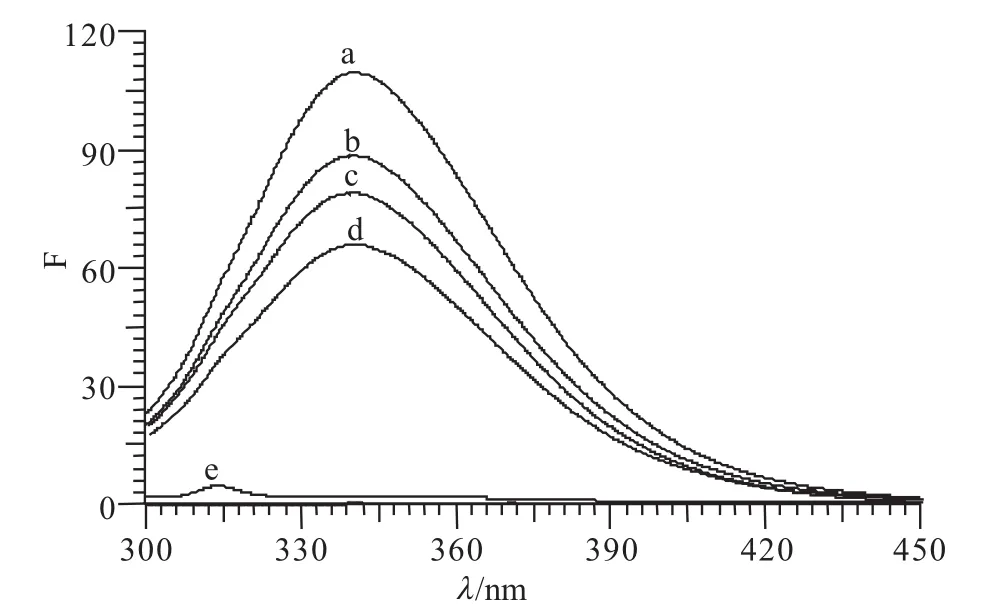
图1 荧光发射光谱Fig.1 Emission spectra of samples spectrum
(4)在(2)中的比色管中分别加入1×10-2mol·L-1的Cu2+1mL和1×10-3mol·L-1的Cu2+1mL,水定容至刻度,摇匀,放置10min后用激发波长283 nm测定其荧光发射光谱(图2、图3)并得出荧光强度结果(表3)。
2 结果与讨论
2.1 氯诺昔康和铜(Ⅱ)对BSA的猝灭作用
由于蛋白质中色氨酸和酪氨酸的存在使其具有内源荧光,以283nm激发波长为,在300~500 nm的范围内,氯诺昔康在314nm处(图1e)有最大发射峰,而BSA的最大发射波长为341nm(图1a),在BSA中分别加入Cu2+和氯诺昔康后,BSA的最大发射峰位置不变,但荧光强度明显降低(图1b,图1c),当氯诺昔康和Cu2+同时加入时BSA的荧光强度又进一步降低,这说明BSA和Cu2+之间,BSA和氯诺昔康之间以及三者都存在时它们产生了作用,发生了能量转移,可见Cu2+和氯诺昔康对BSA的荧光产生猝灭作用。
2.2 氯诺昔康对BSA的猝灭作用
荧光猝灭分为静态猝灭和动态猝灭。在动态猝灭过程中,用KSV(动态猝灭常数)来描述猝灭剂与荧光体荧光强度之间的相互作用关系,以动态猝灭的Stern-Volmer方程[5]处理,即:
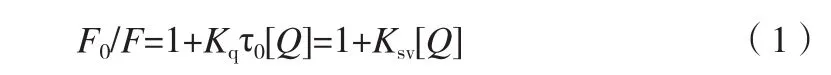
式中F0是没有加入氯诺昔康时BSA的荧光强度,F是加入一定量氯诺昔康时BSA的荧光强度,Kq是双分子猝灭过程速率常数,τ0是猝灭剂不存在时生物大分子的平均寿命,生物大分子的荧光寿命约为10-9s,[Q]为猝灭剂即氯诺昔康的浓度。由表1可知,随着氯诺昔康浓度的增大BSA的最大荧光发射峰强度逐渐降低,这表明氯诺昔康加入后对BSA产生了荧光猝灭作用。
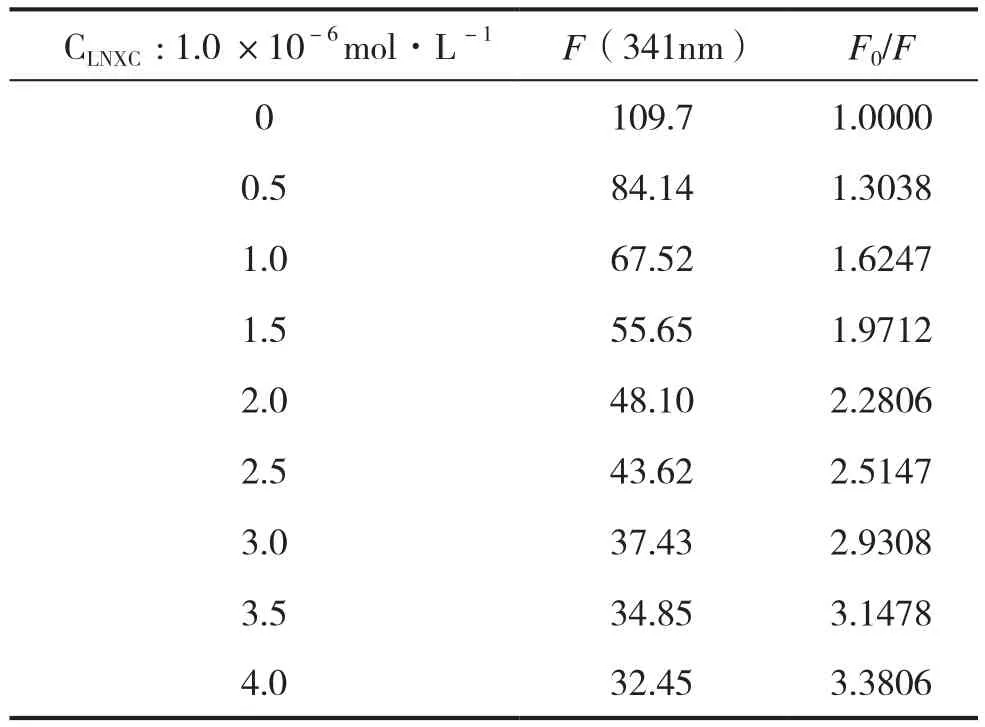
表1 氯诺昔康对BSA的荧光光谱影响Tab.1 Effect of LNXC concentration on fluorescence spectrum of BSA

温度对BSA的影响,可由公式:得Ksv(25℃)=4.839×105L·mol-1,Ksv(35℃)=4.249× 105L·mol-1,Ksv(45℃)=3.615×105L·mol-1,可知随温度的升高Ksv减小,从而初步表明猝灭过程为静态猝灭。以F0/F对CLNXC作出氯诺昔康对BSA的荧光猝灭图Stern-Voimer(图2),图2中曲线有较为良好的线性关系, 根据实验及公式(2)所得Ksv=6.07× 105L·mol-1代入公式(1)得Kq=6.07×1013L·mol-1·s-1,远大于各类猝灭剂对生物大分子的最大扩散碰撞猝灭常数2.0×1010L·mol-1·s-1,所以氯诺昔康对BSA的猝灭是静态猝灭。根据静态猝灭方程:
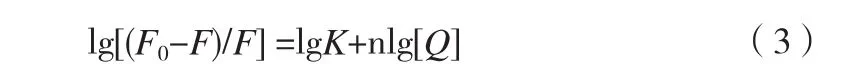
式中K为白蛋白分子与药物的结合常数,n为结合位点数。以lg[(F0-F)/F]对lg[Q]作图(图3)。
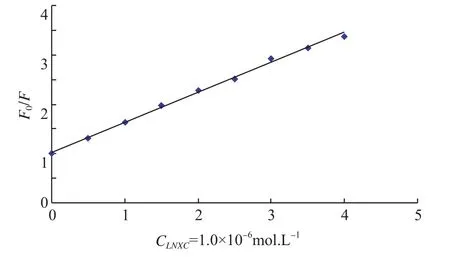
图2 LNXC浓度对F0/F方程图Fig.2 plot ofF0/Fversus concentration of LNXC
由直线的斜率和截距得结合常数K=6.54×105,结合位点数n=1.23,可见二者之间的结合作用很强,且可形成一个结合位点。
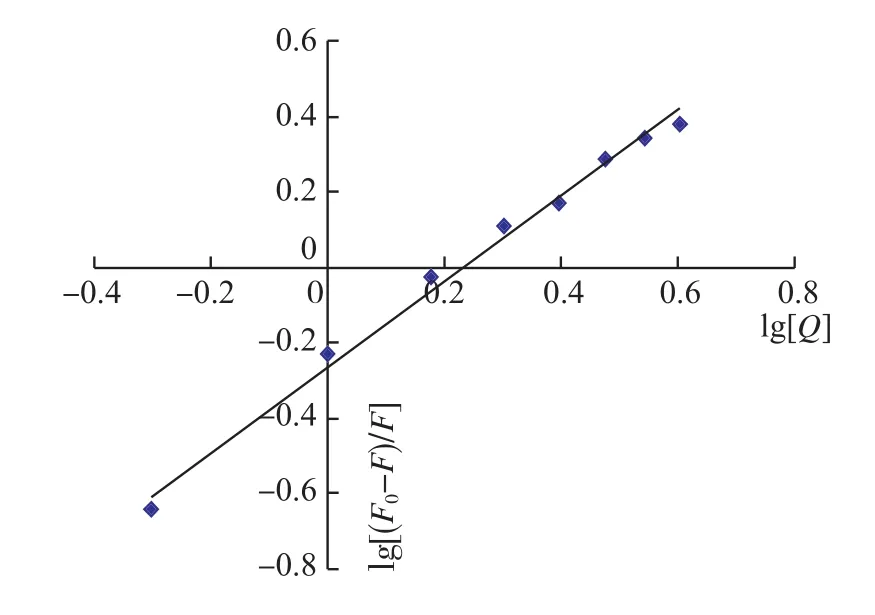
图3 lg[(F0-F)/F]对lg[Q]作图Fig.3 Plot of lg[(F0-F)/F] versusconcentration of LNXC
2.3 铜(Ⅱ)对BSA的猝灭作用
由实验可知,随着Cu2+浓度增大BSA的最大荧光发射峰也降低了(表2),这说明Cu2+对BSA也有荧光猝灭作用。同样的用动态猝灭的Stern-Volmer方程 处理,用表2的F0/F对CCu2+做Cu2+对BSA的荧光猝灭图Stern-Voimer,所得结果见图4。图4中曲线也有很好的线性关系, 根据实验及公式(2)所得Ksv=1.51×105L·mol-1代入公式(1)得Kq=1.51×1013L·mol-1·s-1,也远大于各类猝灭剂对生物大分子的最大扩散碰撞猝灭常数2.0×1010L·mol-1·s-1,所以Cu2+对BSA的猝灭也是静态猝灭。
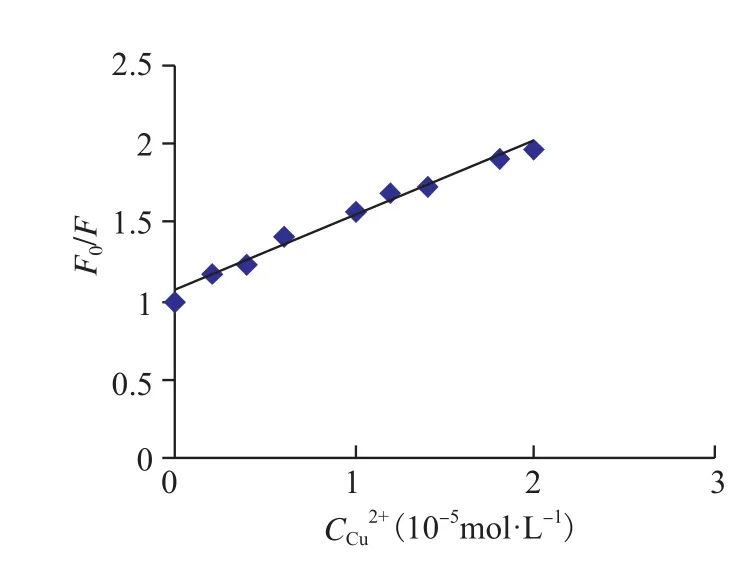
图4 Cu(Ⅱ)浓度对F0/F方程图Fig.4 plot of F0/F versus concentration of Cu(II)
以lg[(F0-F)/F]对lg[Cu2+]作图(图5),得一直线方程为y= 0.7664x-0.6775,r=0.9984,由截距和斜率得结合常数K=2.1×105,结合位点数n=0.77,可见结合常数也比较大,说明二者之间也具有很强的结合作用,说明[Cu2+]的存在可能会对氯诺昔康与BSA体系产生不可忽略的影响。
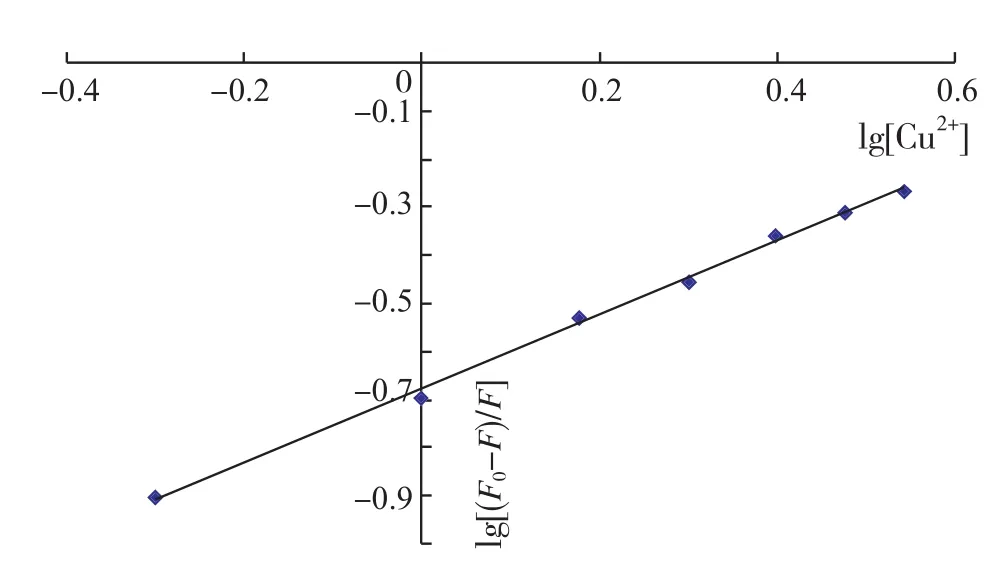
图5 lg[(F0-F)/F]对lg[Cu2+]作图Fig.5 Plot of lg[(F0-F)/F] versusconcentration of[Cu2+]
2.4 氯诺昔康与BSA作用的热力学参数和作用力类型的确定
实验中研究了不同温度下氯诺昔康与血清白蛋白的相互作用,并根据热力学常数确定了氯诺昔康-BSA体系的作用力类型。通常△S>0为疏水作用力的表现;△H<0,△S>0为静电作用力的特征;△H<0,△S<0为氢键和笵德华力的特点[6-7]。
由以下公式:
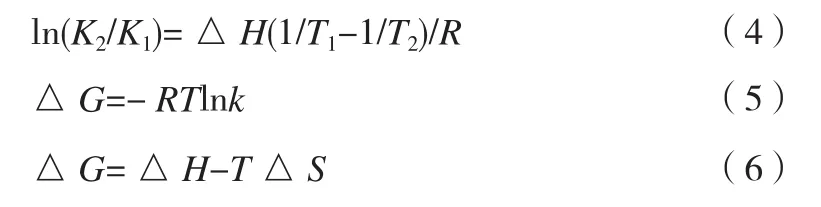
在体系氯诺昔康-BSA中,依据不同温度下的结合常数K求得:△H均为-9.93kJ·mol-1,△S25℃=76.44J·mol-1·K-1;△S35℃=76.42J·mol-1·K-1;△S45℃=76.10J·mol-1·K-1,从而证明氯诺昔康与BSA的相互作用力为静电作用力。
2.5 铜(Ⅱ)对BSA与氯诺昔康结合作用的影响
表2列出了不同浓度的Cu2+对BSA与氯诺昔康的荧光光谱的影响。
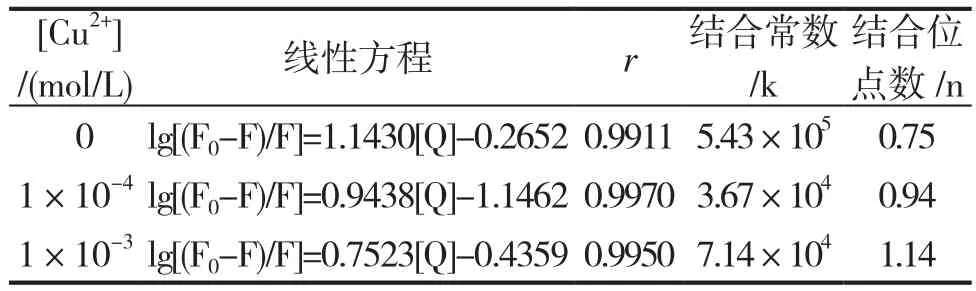
表2 不同Cu (Ⅱ)浓度下BSA和LNXC的结合常数和结合位点数Table 2 Binding constant Kand the number of binding siten between BSA and LNXC in the presence of different concentration of Cu (Ⅱ)
表2表明,随着Cu(Ⅱ)浓度的增大,BSA与LNXC结合作用增强,提高了结合常数,表明Cu (Ⅱ)、BSA与LNXC之间形成了三元配合物。
3 结论
研究了不同温度下氯诺昔康与牛血清白蛋白作用的荧光特性,证明氯诺昔康与BSA的相互作用力为静电作用力,同时也证实了氯诺昔康对BSA的猝灭是静态猝灭。比较不同浓度铜离子存在下BSA与LNXC的结合常数和结合位点,结果表明,随着Cu(Ⅱ)浓度的增大,BSA与LNXC结合作用增强,提高了结合常数,表明Cu (Ⅱ) 、BSA与LNXC之间形成了三元配合物。
[1] 王亚南,王洪权.2-羟丙基-β-环糊精对氯诺昔康的增溶作用[J].解放军药学学报,2006,22(2):146-148.
[2] 陈晓波,李崧.铜.钠和钼离子与牛血清白蛋白作用的荧光光谱研究[J].光谱学与光谱分析,2006,26(2):309-312.
[3] 何华,李杉杉,芦金荣,等. 荧光光谱法研究G3.0 PAMAM树状大分子与牛血清白蛋白的相互作用[J].光谱学与光谱分析,2009,29(10):2782-2786.
[4] 王晓霞,敖登高娃,阿娟.美洛昔康-Cu(Ⅱ)-牛血清白蛋白三元配合物的荧光光谱法研究[J].分析试验室,2009,28(12):51-54.
[5] 于岚岚,杨冉,陈晓英,等.光谱法研究喜树碱与牛血清白蛋白的相互作用[J].分析试验室,2012,31(1):42-46.
[6] Ross PD, Subramanian S. Thermodynamics of protein association reactions: forces contributing to stability[J]. Biochemistry, 1981, 20(11):3096-3099.
[7] 李俊芬,许志成,董川.隐丹参酮与环糊精包结物的制备与光谱研究[J].分析科学学报,2004,20(3):299-232.
Study on Ternary Complex of Lornoxicam, Copper(Ⅱ)and BSA by Method of Fluorescence
WANG Xiao-xia, WANG Zheng-de, LIU Yun-ying
(College of Chemistry and Chemical Engineering, Inner Mongolia University of Science and Technology, Baotou 014010, China)
Under the physiological conditions, fluorescence spectrometry was used to study bovine serum albumin, copper (Ⅱ ) of bovine serum albumin and copper (Ⅱ ) on bovine serum albumin fluorescence spectrum characteristics. Copper (Ⅱ ) and lornoxicam could both cause bovine serum albumin fluorescence quenched. Under the existence of copper (Ⅱ ), lornoxicam enhanced the fluorescence quenching effect of bovine serum albumin. According to lineweaver-burk plot calculation, the combining constant between lornoxicam and bovine serum albumin was 5.43×105, position points were 1.14. The combining constant between Copper (Ⅱ) and bovine serum albumin was 2.10×105, position points were 0.78.
fluorescence spectroscopy;bovine serum albumin (BSA);copper (Ⅱ);lornoxicam;ternary complexes;
O 657.3
A
1671-9905(2014)04-0015-04
教育部“春晖计划”基金资助项目(2009-1-01040);内蒙古教育厅高校科研基金项目(NJZY11145);内蒙古科技大学创新基金资助项目(2012NCL034);内蒙古科技大学大学生创新基金项目
王晓霞(1984-),女,内蒙古包头市人,讲师,硕士,研究方向:药物化学,电话:(0472)5951561,E-mail:wxx572369@163.com
2014-02-19
