光学超分辨荧光显微成像
——2014年诺贝尔化学奖解析
2014-05-09纪伟徐涛刘贝
纪 伟 徐 涛 刘 贝
①副研究员,②研究员,③博士研究生,中国科学院生物物理研究所,北京 100101
光学超分辨荧光显微成像
——2014年诺贝尔化学奖解析
纪 伟①徐 涛②刘 贝③
①副研究员,②研究员,③博士研究生,中国科学院生物物理研究所,北京 100101
超分辨成像;受激发射损耗显微镜;光敏定位显微镜
超分辨成像显微镜的出现为现代生物医学研究提供了新的强有力的工具,将荧光显微镜的应用推到了新的高度。2014年诺贝尔化学奖授予了Eric Betzig、Stefan Hell以及William Moerner三位科学家,以表彰他们在“发展超高分辨荧光显微镜”上的贡献。他们的获奖肯定了化学生物物理多学科交叉对于当今前沿科技发展的重要性。本文主要介绍了超分辨荧光显微成像诞生的历史背景,以及各成像技术的发生发展过程,最后对此技术的未来发展做了展望。

图1 从左至右依次为Eric Betzig、Stefan Hell以及William Moerner(图片摘自http://www.nobelprize.org/nobel_prizes/chemistry/laureates/2014/)
近日瑞典皇家科学院宣布将2014年诺贝尔化学奖颁给美国霍华德•休斯医学研究所的Eric Betzig、德国马普生物物理化学研究所的Stefan Hell以及美国斯坦福大学的William Moerner (图1),以表彰他们在“发展超高分辨荧光显微镜”上的贡献。历史上,诺贝尔奖已经多次颁发给了与生物医学成像相关的研究,包括电子显微成像、CT成像、核磁共振成像等等,但是像光学超分辨荧光成像这样从理论证实、实验证明再到推广,仅仅过去十多年时间便获得诺贝尔奖青睐的实属少见,这也足见此项技术的重要性。
在过去的一百多年间,德国物理学家Ernst Abbe的发现都坚不可摧,即:受光学衍射限制,显微镜无法分辨两个相距小于发射波长一半的物体[1]。由于衍射,一个点光源在通过透镜系统后,都会以艾里斑的形式存在(图2(a))。具体来讲,显微镜的分辨率可由公式d=λ/(2NA)表征,λ表示发射光波长,NA表示物镜的数值孔径(图2(b))。这一理论终于在20世纪末受到了前所未有的挑战并被打破,形成了现今在生物成像领域广泛应用的三类超分辨荧光成像技术,包括受激发射损耗(stimulated emission depletion, STED)技术[2-4]、结构光照明显微镜(structured illumination microscopy, SIM)技术[5-6]以及基于单分子定位的超分辨成像技术——光激活定位显微镜(photo-activation localization microscopy, PALM)[7]和随机光学重构显微镜(stochastic optical reconstruction microscopy, STORM)[8]。STED技术和SIM技术通过不同方法调制系统的点扩散函数(point spread function, PSF)实现了超分辨成像,而PALM/STORM技术则是采用牺牲时间换取空间频率的策略利用单分子成像加上图像重构算法实现分辨率的提升。本次获奖的Stefan Hell教授是STED技术的发明人,他于1994年提出利用量子光学中的受激辐射耗竭理论能够突破衍射极限。Eric Betzig与William Moerner则是基于单分子定位实现超分辨成像技术的奠基者,前者于1995年提出了单分子定位的概念[9],并在2006年实现了PALM显微镜[7];后者则是开创了单分子光谱学[10],并首次在单分子尺度上观测了荧光蛋白的光激活和光闪烁性质[11],为PALM/STORM技术的实现奠定了基础。
遗憾的是,另外一个目前广泛应用的超分辨光学成像技术——SIM的发明人Mats Gustafsson博士于2011年英年早逝,与此次诺贝尔奖失之交臂。
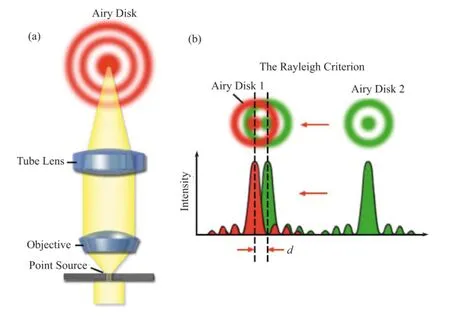
图2 (a)光学衍射和艾里斑;(b)受瑞利准则的约束,普通显微镜的分辨率只能达到d=0.61λ/NA,假设光波长500 nm,数值孔径为1,则分辨率约为300 nm(图片摘自http://zeiss-campus.magnet.fsu.edu/articles/basics/resolution.html)
1 受激发射损耗显微镜
机遇总是会留给有准备的人。Stefan Hell博士一直是一位勇于挑战权威的人,他很早就意识到光学极限迟早是要被打破的,而他最初只是脑海中有粗略的概念却缺乏具体实现的理论支持。他在博士及博士后期间对4Pi显微镜的研究,算是其向突破衍射极限迈出的第一步,或许那时的他已清楚明白通过调制系统的点扩散函数的方法能够逼近甚至突破衍射极限。他思考并尝试了无数种突破衍射极限的方法,最终量子光学中“受激发射”现象吸引了Hell的注意。我们知道荧光是指处于基态的荧光基团吸收光子后跃迁到激发态,并在弛豫一段时间后以发光的形式放出热量回到基态;而“受激发射”是指那些受到激发的准备发荧光的荧光基团能够暂时性的被转化到关闭态(图3(a))。Hell博士迅速地构建了基于受激发射理论的显微镜原理图(图3(b)),并且意识到有可能将分辨率推进到30 nm——传统共聚焦显微镜分辨率的1/10,而计算机模拟的结果同样支持他的构想。遗憾的是,Hell的工作起初并没有引起科研界的重视,尤其是在生物成像领域,STED的发展也因此沉寂了数年之久。直到2000年,Hell在《美国科学院院刊》上发表文章,第一次实现了基于STED技术的显微镜,并得到了纳米级的荧光图像,至此STED技术才引起科研界重视,而STED技术的发展也进入了快车道。从技术层面讲:双色STED的出现扩展了STED显微镜的应用范围[12];采用连续光激光器极大降低了STED显微镜的成本[13];高速STED技术使得科研人员能够在高分辨率下观察细胞动态过程[14];RESOLFT将STED的概念拓展到更普适的高度[15]。Hell对于突破衍射极限的执着追求造就了STED技术的问世,而后引领的STED技术的发展和推广热潮成就了STED技术在超分辨成像领域的一席之地。

图3 (a)荧光基团实现饱和光转化的能级示意图;(b) STED原理示意图:激发光和STED光经过准直耦合后同时照在样品上,STED光束所产生的saturated depletion效应将激发区域限制在非常小的区域,从而实现超分辨成像(图片摘自http://www. nobelprize.org/nobel_prizes/chemistry/laureates/2014/advanced.html)[16]
2 基于单分子定位的超分辨显微镜
物理学出身的Betzig一直痴迷于新型成像技术的开发,突破衍射极限同样也是他的终极目标。早在贝尔实验室工作期间,他就发明了近场扫描光学显微镜(near-field scanning optical microscopy, NSOM)[16],并且利用它观察到了单分子荧光[17]。虽然从原理上讲NSOM也突破了传统的光学衍射极限,但是近场成像分辨率依赖于探针与样品间的距离,所以仅能进行表面成像,应用非常局限。1995年,Betzig于《光学快报》上的一篇文章中首次提及了利用单分子定位的概念(图4(a))理论上能够达到近似分子精度的分辨率水平[9]。2002年Jennifer Lippincott-Schwartz首次报道了具有光激活性质的荧光蛋白PA-GFP[18]。科学家的嗅觉使得Eric迅速意识到PA-GFP是实现超分辨成像的前提要素。于是供职于工业界顶级实验室的Betzig再也按捺不住,在Hess教授的帮助下再次回到科研界,并于2006年在《Science》杂志上发表文章正式提出了光激活定位超分辨显微镜[7],至此开启了通往超分辨成像的另外一扇大门。几乎与此同时,华人科学家庄小威利用类似原理,在《Nature Methods》杂志上提出了STORM的概念[8]。PALM/STORM均是通过对荧光分子的激活—定位—漂白三个步骤加之数万次的循环最终重构出超分辨图像(图4(b))。相比于STED技术,PALM/STORM在实现上更简单且成本更低,多色PALM成像、三维PALM成像、活细胞PALM成像以及厚样本PALM成像相继诞生,并且在生物学研究中迅速普及开来。Betzig开启了单分子超分辨成像的先河,却没有将视野局限于此。传统的PALM技术利用全内反射照明样品,成像深度很浅,而片层光照明(light sheet illumination)技术拥有光毒性小、低背景噪声和兼容厚组织成像等诸多优势。Betzig在片层光照明的概念下先后发展了Bessel光照明技术[19]和Lattice light-sheet照明技术[20],并且在世界顶级杂志《Nature Methods》和《Science》上先后发表文章阐述其实现方法和应用,后者更是在组织细胞上实现了PALM成像。
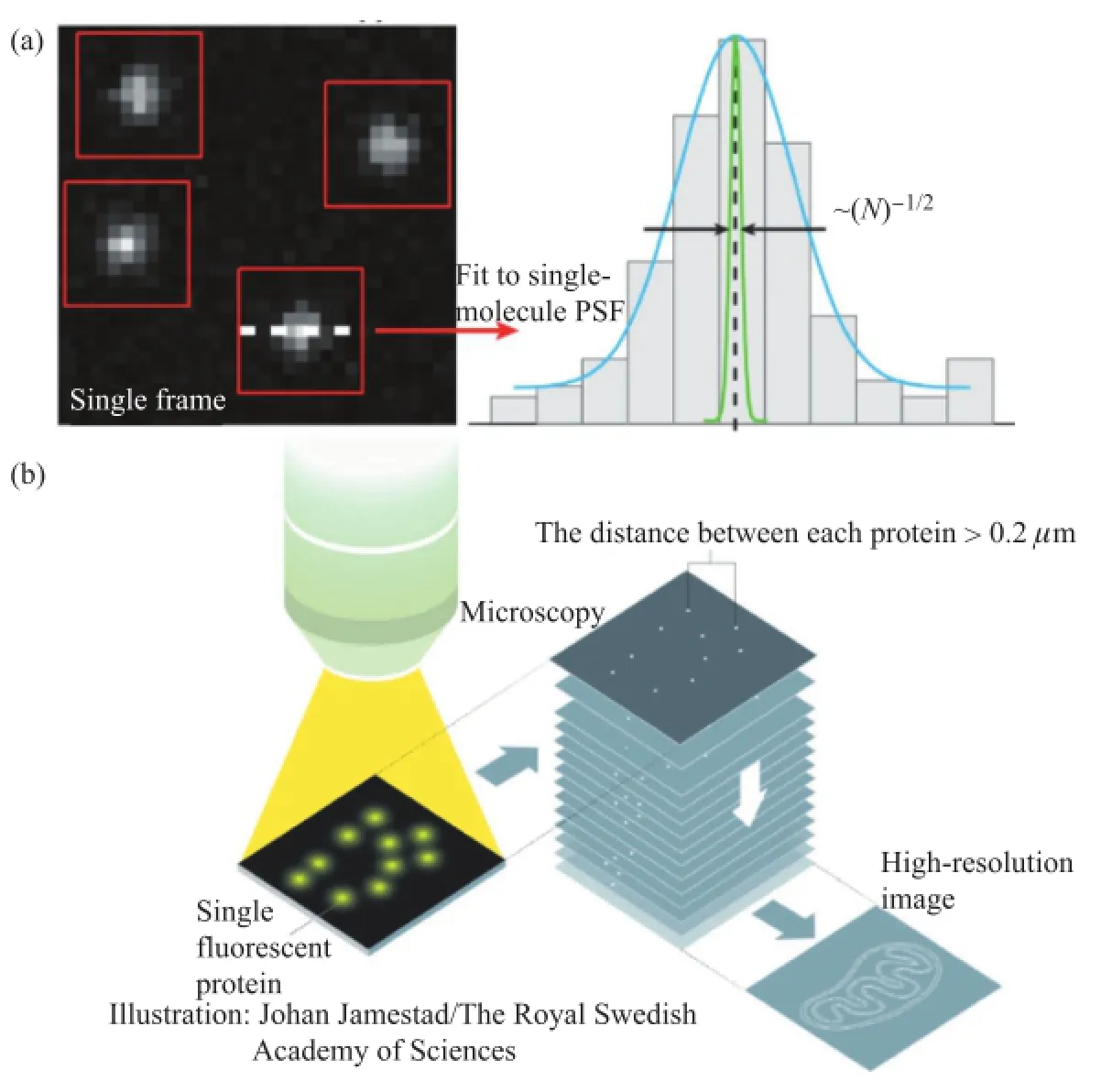
图4 (a)单分子定位的原理:单分子信号可以通过高斯拟合的方法进行精确定位,其定位精度取决于每个单分子发出的光子数(N);(b)基于单分子定位的超分辨成像的流程图:采用高灵敏度的CCD/sCMOS记录下稀疏的单分子信号,通过图像识别算法分割出每个单分子,再通过拟合算法精确定位出每个单分子的位置,最终重构出超分辨图像。(图片摘自http://www.nobelprize.org/nobel_prizes/chemistry/laureates/2014/advanced.html)
Moerner教授虽然没有直接提出超分辨成像的概念,却是第一个观察到单分子并对单分子性质进行详细测量的科学家。长久以来,科学家们通过化学方法来进行测量吸收或者荧光,都是研究的数百万分子的平均效应。1989年,还在IBM工作的Moerner教授第一次在超低温下(4 K)观测到了单个分子的吸收光谱[10]。这项先驱性的工作开启一个全新的科研领域——单分子光谱学,同时也启发了无数科学家将更多的注意力转向了单分子研究,而这其中最著名的一个或许就是Eric Betzig了。1997年,Moerner加入加州大学San Diego分校,在那里他结识了后来同样是诺贝尔奖得主的钱永健并了解了刚开始广泛应用的GFP蛋白[21]。Moerner发现GFP的一个变种的荧光状态能够被不同波长的光调制,即:当用488 nm的激光激发蛋白时,GFP开始发光紧接着被淬灭;而在被紫外光照射后,GFP又能重新回到能够发光的状态。Moerner阐明了一种利用光来控制单分子荧光的方法,这也解决了Eric Betzig在两年前已经用公式证明了的一种成像方法的实现上的难题。Moerner同时发现GFP分子自身能够在on态和off态之间转换(blinking),这种blinking现象同样也是通往超分辨成像的途径之一[11]。
3 展望
超分辨显微成像技术在问世十多年之后便迅速获得了诺贝尔奖,足见其对化学领域尤其是生物学领域的重大影响。时至今日,三大超分辨成像技术的理论基础已比较完备,但是其应用范围与普通共聚焦显微镜相比还有很大差距,因此此次诺贝尔奖的颁发势必会引起更多化学家、生物学家的重视,将更多的科研兴趣和研究重点投入超分辨显微成像技术上来。高昂的装备和维护费用也是影响超分辨成像技术推广的重要制约因素。综上所述,笔者认为今后新的突破势必将会集中在:
(1) 上游新型荧光标签的改造;
(2) 针对原有技术的多模态扩展;
(3) 针对最前沿生物学、医学问题的有效应用;
(4) 成像流程和图像分析技术的普及和简化,系统成本的降低。
(2014年11月16日收稿)
[1] ABBE E. BEITRÄGE ZUR theorie des mikroskops und der mikroskopischen wahrnehmung [J]. Archiv für mikroskopische Anatomie, 1873, 9 (1): 413-418.
[2] HELL S, WICHMANN J. Breaking the diffraction resolution limit by stimulated emission [J]. Opt Lett, 1994, 19 (11): 780-782.
[3] HELL S W, KROUG M. Ground-state-depletion fluorscence microscopy: a concept for breaking the diffraction resolution limit [J]. Applied Physics B, 1995, 60 (5): 495-497.
[4] KLAR T A, JAKOBS S, DYBA M, et al. Fluorescence microscopy with diffraction resolution barrier broken by stimulated emission [J]. Proc Natl Acad Sci, 2000, 97 (15): 8206-8210.
[5] GUSTAFSSON M G. Surpassing the lateral resolution limit by a factor of two using structured illumination microscopy [J]. J Microsc, 2000, 198 (2): 82-87.
[6] GUSTAFSSON M G. Nonlinear structured-illumination microscopy: wide-field fluorescence imaging with theoretically unlimited resolution [J]. Proceedings of the National Academy of Sciences of the United States of America, 2005, 102 (37): 13081-13086.
[7] BETZIG E, PATTERSON G H, SOUGRAT R, et al. Imaging intracellular fluorescent proteins at nanometer resolution [J]. Science, 2006, 313 (5793): 1642-1645.
[8] RUST M J, BATES M, ZHUANG X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM) [J]. Nature Methods, 2006, 3 (10): 793-796.
[9] BETZIGE. Proposed method for molecular optical imaging [J]. Opt Lett, 1995, 20 (3): 237-239.
[10] MOERNER W, KADOR L. Optical detection and spectroscopy of single molecules in a solid [J]. Phys Rev Lett, 1989, 62 (21): 2535.
[11] DICKSON R M, CUBITT A B, TSIEN R Y, et al. On/off blinking and switching behaviour of single molecules of green fluorescent protein [J]. Nature, 1997, 388 (6640): 355-358.
[12] DONNERT G, KELLER J, WURM C A, et al. Two-color far-field fluorescence nanoscopy [J]. Biophys J, 2007, 92 (8): L67-L69.
[13] WILLIG K I, HARKE B, MEDDA R, et al. STED microscopy with continuous wave beams [J]. Nature Methods, 2007, 4 (11): 915-918.
[14] NÄGERL U V, WILLIG K I, HEIN B, et al. Live-cell imaging of dendritic spines by STED microscopy [J]. Proc Natl Acad Sci, 2008, 105 (48): 18982-18987.
[15] HOFMANN M, EGGELING C, JAKOBS S, et al. Breaking the diffraction barrier in fluorescence microscopy at low light intensities by using reversibly photoswitchable proteins [J]. Proceedings of the National Academy of Sciences USA, 2005, 102 (49): 17565-17569.
[16] BETZIG E, TRAUTMAN J K. Near-field optics: microscopy, spectroscopy, and surface modification beyond the diffraction limit [J]. Science, 1992, 257 (5067): 189-195.
[17] BETZIG E, CHICHESTER R J. Single molecules observed by nearfield scanning optical microscopy [J]. Science, 1993, 262 (5138): 1422-1425.
[18] PATTERSON G H, LIPPINCOTT-SCHWARTZ J. A photoactivatable GFP for selective photolabeling of proteins and cells [J]. Science, 2002, 297 (5588): 1873-1877.
[19] PLANCHON T A, GAO L, MILKIE D E, et al. Rapid threedimensional isotropic imaging of living cells using Bessel beam plane illumination [J]. Nature Methods, 2011, 8 (5): 417-423.
[20] CHEN B C, LEGANT W R, WANG K, et al. Lattice light-sheet microscopy: imaging molecules to embryos at high spatiotemporal resolution [J]. Science, 2014, 346 (6208): 1257998.
[21] TSIEN R Y. The green fluorescent protein [J]. Annu Rev Biochem, 1998, 67 (1): 509-544.
Super-resolution fluorescent microscopy: A brief introduction to the Nobel Prize in Chemistry 2014
JI Wei①, XU Tao②, LIU Bei③
①Associate Professor, ②Professor, ③Ph. D. Candidate, Institute of Biophysics, Chinese Academy of Sciences, Beijing 100101
Super-resolution fluorescent microscopy becomes a powerful tool for biomedical research, and extent the application of fluorescent microscopy to a brand new level. The Royal Swedish Academy of Sciences decided to award Erik Betzig, Stefan W. Hell and W. E. Moerner the Nobel Prize in Chemistry 2014 for the development of super-resolution fluorescence microscopy. Their award proved the importance of this multidisciplinary field consist of chemistry, biology and physics. In this article, we briefly introduced the historical background of super-resolution imaging, and dissect the born and development of each techniques. Finally, the current problems and the challenges for future research were presented.
super-resolution imaging, stimulate emission depletion, photoactivated localization microscopy
(编辑:段艳芳)
10.3969/j.issn.0253-9608.2014.06.003
