小兴凯湖表层底泥磷吸附容量及潜在释放风险
2014-05-09于淑玲李晓宇张继涛陈国双李秀军
于淑玲,李晓宇,张继涛,陈国双,李秀军*
(1.中国科学院湿地生态与环境重点实验室,中国科学院东北地理与农业生态研究所,吉林 长春130102;2.中国科学院大学,北京100049)
小兴凯湖表层底泥磷吸附容量及潜在释放风险
于淑玲1,2,李晓宇1,张继涛1,陈国双1,李秀军1*
(1.中国科学院湿地生态与环境重点实验室,中国科学院东北地理与农业生态研究所,吉林 长春130102;2.中国科学院大学,北京100049)
利用沉积物磷吸附指数(PSI)和磷吸附饱和度(DPS)研究了小兴凯湖表层沉积物的磷吸附容量,分析了沉积物中磷的吸附饱和度(DPS)与其他指标的相关关系,并讨论了不同采样点湖泊沉积物中磷的潜在释放风险.结果表明:13个采样点的表层沉积物的 PSI为9.78~197.53(mg·L)/(100g·µmol),平均值为59.77(mg·L)/(100g·µmol);DPS为9.95%~24.47%,平均值为15.41%.PSI与草酸铵提取的磷(Pox)极显著正相关,与草酸铵提取的铁、铝(Feox,Alox)显著正相关,草酸铵提取的铁是影响PSI的主导因素;DPS主要受沉积物中原有吸附态磷的影响.此外,磷释放风险指数(ERI)8.99%~129.94%的计算结果表明:小兴凯湖表层沉积物中磷释放诱发富营养化的风险处于高度风险范围,其中,受农业面源污染影响较大的北岸区域相比其他区域发生富营养化的风险更高.
磷吸附指数;磷吸附饱和度;富营养化风险;铁铝氧化物;小兴凯湖
兴凯湖是黑龙江流域最大的湖泊[1-4],位于黑龙江省东南部和俄罗斯远东滨湖边区,为中俄界湖.兴凯湖分为大、小兴凯湖,都是造山运动地壳陷落而形成的构造湖,小湖与大湖仅一岗之隔,由两个泄洪闸连通.小兴凯湖地理坐标为 N45°16′~45°24′,E132°20'~132°50',总水面积176km2[5],北接穆棱河,南通大兴凯湖,其所在区域为国家地质公园,拥有湖滨浴场、西泡子野生垂钓场、大型观鸟台及养鱼场,是一座集防洪蓄水、排涝灌溉、养殖及旅游等多功能的天然水体.2012中国环境状况公报[6]显示小兴凯湖为轻度富营养状态.近年来,随着对小兴凯湖开发力度的逐年加大,尤其是旅游业的发展和人口增多,农业退水和生活污水等未经处理就直接排入湖中,使小兴凯湖富营养化程度有加剧的趋势.湖泊沉积物是湖泊营养物质的主要归宿[7],其中磷被视为限制湖泊中藻类生长的主要限制性营养因子[8],外部输入湖泊中的磷以可溶性和不溶性的混合物进入水体,被动植物吸收利用或通过吸附、沉积作用转移到沉积物中,当与沉积物所接触的水体中磷浓度大于沉积物-水界面磷动态平衡浓度时,沉积物会吸附水体中的磷,相反,沉积物中的磷又可作为内源污染释放到上覆水体中[9-11].Bache和Williams提出了磷吸附指数(PSI)和磷吸附饱和度(DPS)来表征土壤磷吸附容量[12-15];黄清辉等[16]则以基于PSI和DPS的磷释放风险指数(ERI)评估了太湖表层沉积物磷的富营养化风险,较好地反映了太湖的富营养化状况.小兴凯湖是我国重要淡水湖泊之一,目前对兴凯湖富营养化的研究多集中于大兴凯湖[17-18],关于小兴凯湖富营养化的研究较少,而小兴凯湖与大兴凯湖具有水力联系,小兴凯湖的富营养化状况将会影响大兴凯湖的水环境.因此,本文采用磷吸附指数和磷吸附饱和度探讨了该湖表层沉积物中磷的吸附容量及潜在释放能力,并用磷释放风险指数预测了该湖表层沉积物磷释放诱发富营养化的风险,为小兴凯湖的污染防治工作提供基础数据.
1 材料与方法
1.1 样品采集及处理
2013年7月在小兴凯湖实施现场观测与采样,13个采样点地理位置如图1、表1所示.在每个采样位置用柱状采泥器(德国HYDRO-BIOS公司)采集10cm的表层沉积物,每个位置均取3个平行样品,混合均匀,并在相应采样点从水面以下0.5m处采集3个上覆水水样,再混合均匀成混合水样,移入预先洗净的500mL聚乙烯瓶中,上覆水理化指标,包括pH、DO、EC、TDS及SD,在现场用YSI水质分析仪测定,SD用透明度盘测定,其他指标低温保存带回实验室分析.底泥样品采集后当天冷藏保存带回实验室,待沉积物自然风干后,去除样品中贝壳、杂草、沙粒等杂物,经研磨、过筛(100目)后,保存于密封袋中,置于冰箱内待用.
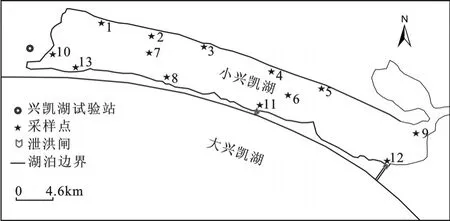
图1 小兴凯湖采样点位示意Fig.1 Samping sites of Lake Xiaoxingkai
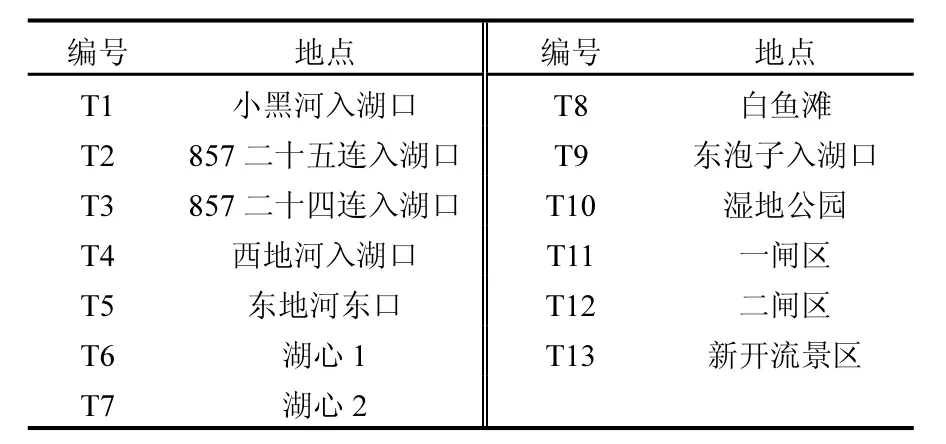
表1 取样点地理位置Table1 Geographic position of sampling sites
1.2 实验方法
1.2.1 PSI的测定[16]每份沉积物分别称取4份1.000g样品,于50mL聚乙烯离心管中,其中1个离心管中加入20mL0.01mol/L CaCl2溶液,作为空白平行,其余3个离心管中分别加入20mL75mg/L KH2PO4溶液(配制在0.01mol/L CaCl2溶液中),为实验平行.分别加2滴氯仿抑制微生物活动,20℃下振荡24h后,以3000r/min离心20min,上清液过0.45μm孔径滤膜后,用钼锑抗比色法测定磷浓度,由反应初始磷浓度与反应后滤液中磷浓度的差值可计算出1.000g沉积物吸附磷的量,以100g沉积物吸附磷的量值为X,磷吸附指数PSI=X/lgC, C为滤液中溶解磷浓度, μmol/L; X的单位为 mgP/100g, PSI的单位为(mg·L)/ (100g·μmol).
1.2.2 DPS的测定[16]每份沉积物分别称取3份2.500g样品,置于100mL聚乙烯瓶中,分别加50mL草酸铵提取剂(pH=3),准备3个空白.在暗室内180r/min振荡2h(20℃).先后用无灰分定量细滤纸和0.45μm孔径滤膜过滤提取液.弃去最初通过的滤液,余下的用100mL的聚乙烯瓶收集.移取10mL滤液于50mL离心管中,加入40mL0.01mol/L盐酸,混合均匀.配置系列标准溶液,分别含0,1.25,5.0,12.5,25.0mg/L P以及0,2.5,10.0,25.0,50.0mg/L Al和Fe.在1周内,用ICP-AES测定磷、铝和铁的含量.重复上述过程,即2次平行实验.沉积物的DPS可估算为草酸铵提取的磷量(Pox,mmol/kg)与提取的铝(Alox, mmol/kg)和铁(Feox,mmol/kg)总量之一半的摩尔百分比值,即DPS(%)=100Pox/[0.5(Alox+ Feox)].
1.3 ERI评估方法
用黄清辉等[16]提出的以沉积物PSI和DPS这两个指标构成的 ERI来评估湖泊表层沉积物中磷的释放风险的方法.

式中: ERI为磷释放风险指数,%; DPS为磷吸附饱和度,%; PSI为磷吸附指数,(mg·L)/(100g·μmol).
1.4 其他指标的测定
测定样品湿度(105℃下烘干8h), PSI和DPS实验结果都经过湿度校正,以炉温干重表达;沉积物中有机质含量(OM)通过重铬酸钾容量法测定[19],沉积物中总磷(TP)测定采用 HClO4-H2SO4高温消煮后用钼锑抗比色法测定[19].硫酸-连续流动分析仪测定各土样中的总氮(TN)[19].采集的水样带回实验室后,立即对水样中的总氮(TN)、总磷(TP)、高锰酸钾指数(CODMn)和叶绿素 a(chla)等进行分析和测定,相关指标的测定方法参照《水和废水监测分析方法》[20].各分析指标以每个样品的3个平行样的平均值作为实验结果.
1.5 数据处理
数据处理及其相关分析采用SPSS17.0软件,多元回归分析采用origin8.0软件.
2 结果与讨论
2.1 小兴凯湖水体的理化特征
小兴凯湖7月湖水的pH值为6.59~8.47,呈中性偏碱,湖心区域的pH值相对较大.浊度(TDS)值为126.10~174.80mg/L,较大值点多位于水流较大的河流入湖口(小黑河入湖口、857二十五连入湖口)、大湖与小湖的连通口(二闸)以及旅游区域(湿地公园和新开流风景区),这可能与水流流速较大及人为扰动等引起的湖水的扰动较大有关.小兴凯湖水体的溶解氧含量为1.94~8.96mg/L,含量偏低,最低值点位于东泡子入湖口附近区域,这可能是由于该片区域腐殖质较多,耗氧量大.小兴凯湖水体的叶绿素a含量为1.31~13.77μg/L,最大值点位于湿地公园和白鱼滩附近,这些区域的人为扰动较大,水质较差,浮游植物较多,初级生产能力较高.小兴凯湖水体中 CODMn为2.24~9.01mg/L,平均值为5.13mg/L,在地表水环境质量标准(GB3838-2002)[21]Ⅱ类~Ⅲ类标准之间.
氮是构成水生生态系统中最主要的营养元素之一,以多种形式参与水体中的生物过程而成为水体初级生产力的潜在限制性因素之一[22].小兴凯湖7月水体中 TN 的含量分别为0.69~3.12mg/L.各个取样点之间差别比较大(P<0.05),TN含量的最大值主要分布在北岸河流入湖口的几个采样点.其原因可能在于7月雨水较多,小兴凯湖周围以及主要入湖河流流域的面源污染中的营养盐随着地表径流进入水体,这也说明小兴凯湖中的总氮可能主要来源于面源污染.磷是水体浮游藻类生长和造成湖泊水体富营养化的最重要控制因子之一[23-26],在富营养化过程中起着十分重要的作用.小兴凯湖7月水体中TP的含量分别为0.05~0.11mg/L,从表2可以看出,小兴凯湖湖心区域水体的总磷浓度要高于河流入湖口湖水中的总磷浓度,分析其原因可能是由于:一方面,河流入湖口附近多为芦苇生长区,农田退水入湖时要先经过芦苇带,芦苇对水体中的总磷具有一定的净化作用[27-29];另一方面,由于风浪较大,岸边进行气体交换的强度大于湖心区域,溶解氧含量比湖心的高,进而使 Fe2+被氧化为Fe3+,使磷沉淀增多,因而导致岸边水体中的磷浓度小于湖心中的磷浓度.并且可以看出受人为扰动较大的白鱼滩和旅游区域的总磷含量较高.从国内外已有的研究成果中可知,能比较直接地反映湖泊富营养化的主要特征是湖泊中浮游植物生长量的大小.根据Liebig最小值定律,浮游植物的最大生长量由所需的营养盐中总物质量最少的那种营养盐所控制,这种营养盐称为限制性营养盐.由藻体中所含碳、氮、磷的原子比率(C:N:P=106:16:1)分析,在藻类生长期,当所测定的湖泊中可被植物吸收的氮和磷的浓度比小于7(N:P<7)时,氮是可能的限制性营养盐;大于7,则磷是可能的限制性营养盐;接近7时,二者均可能是限制性营养盐[30-31].小兴凯湖7月湖水体中的氮磷比(N:P)为6.66~63.57,平均为17.90.由此可见小兴凯湖7月湖水中的总氮浓度超过总磷浓度7倍以上,这说明小兴凯湖7月为磷营养限制性湖泊.

表2 小兴凯湖水质监测结果Table2 Results of water quality of Lake Xiaoxingkai
2.2 小兴凯湖表层沉积物的氮、磷分布特征
研究小兴凯湖表层沉积物的主要理化特征是探讨表层沉积物磷吸附容量及沉积物中磷的潜在释放的基础.主要理化特征测得结果(以平均值表示)见表3.
在沉积物的沉积过程中,细小颗粒吸附的铁、铝氢氧化物易与比重较轻的有机物聚合产生共沉淀,而铁、铝氧化物与磷有很强的亲和力,因而容易形成富含有机磷和铁磷的沉积层.由表3可看出,小兴凯湖沉积物有机质所占比例变化范围为0.27%~9.48%,平均值为5.16%.有机质在空间分布差异比较大,这主要是与湖泊的不同区域的污染程度不同有关.
沉积物中总氮(TN)含量的变化范围为188.73~3224.79mg/kg,平均含量为1676.54mg/kg,由表3可知,除小黑河入湖口、857二十五连入湖口外,其余各采样点的总氮含量均比较高.
沉积物是湖泊中磷的重要蓄积库,从流域中进入湖泊的磷、湖泊水生生物的组成物质以及生活污水,都会进入到沉积物中,致使沉积物的磷逐渐积累起来.近年来随着经济的发展,人类污染排入不断增加,许多湖泊沉积物中磷的含量都达到了相当高的水平,尤其是人为扰动较大区域的表层沉积物.
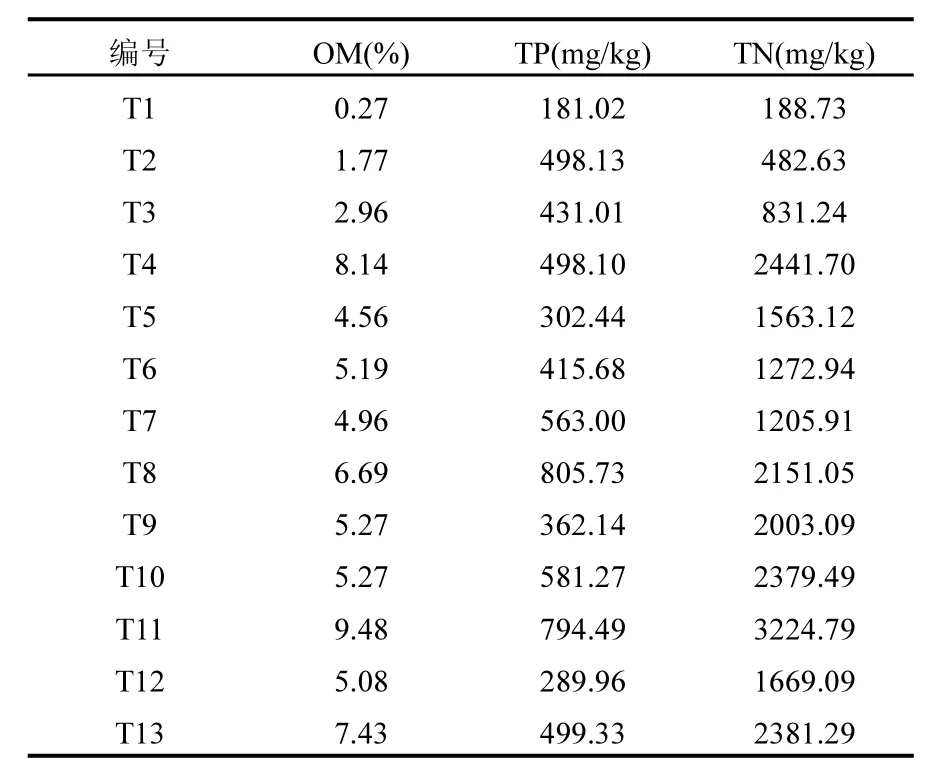
表3 小兴凯湖表层沉积物理化特征Table3 The physicochemical parameters of surfical sediment in Lake Xiaoxingkai
表层沉积物中总磷含量分析结果(以平均值表示)见表3.小兴凯湖表层沉积物中的 TP含量为181.02~805.73mg/kg,平均含量为478.64mg/kg.小兴凯湖表层沉积物中TP含量的空间差异性较大,其中白鱼滩采样点的 TP含量高于其他采样点,这可能是由于该区域为捕鱼村,人为扰动较大,并且附近含磷生活污水的排放使磷在沉积物中累积较多造成的.
2.3 表层沉积物中Pox、Alox、Feox的分布特征
沉积物中无定形态的铁、铝水合氧化物的含量影响着沉积物对磷的吸附容量[32].如图2所示,小兴凯湖表层沉积物中草酸铵提取的铁(活性铁)含量变化范围为7.89~35.88mmol/kg,平均含量为20.31mmol/kg,在 T8(白鱼滩)采样点处最大, T2(857二十五连入湖口)、T4(西地河入湖口)采样点处的 Feox含量也较大.草酸铵提取的铝(活性铝)含量范围为1.61~9.86mmol/kg,平均含量为6.31mmol/kg,它与提取出的铁含量相比,变化幅度不大,最大值出现在 T13(新开流景区)采样点.草酸铵提取的磷含量变化范围为 0.60~3.94mmol/kg,平均含量为2.04mmol/kg,最大值出现于T8(白鱼滩)采样点.T8(白鱼滩)采样点处
沉积物中草酸铵提取的铁、磷含量均为各处中的最大值,这可能是因为活性铁的含量在一定程度上与人类干扰相关[33],该处为捕鱼村,渔民使用的多为铁制船只,渔民的生活污水多直接倾倒于小兴凯湖中,常年的人为干扰活动大于其他采样点.
研究表明,小兴凯湖表层沉积物中草酸铵提取的铁、铝、磷的含量均小于太湖[16]和巢湖[34]中的相应含量,由2012中国环境状况公报[6]可知小兴凯湖的水体富营养状况比太湖、巢湖的轻,由此表明湖泊富营养状况与表层沉积物中草酸铵可提取的铁、磷含量有同步的变化关系,这与邢友华等[35]的研究结果相一致.

图2 表层沉积物中草酸铵提取的Pox,Alox,Feox含量Fig.2 Concentration of Pox, Alox, Feox extracted fromsediment by ammonium oxalate
小兴凯湖沉积物中草酸铵提取的铁、铝、磷的含量之间有较好的相关性(表4),尤其是沉积物中草酸铵提取的磷与活性铝、铁之间为极显著正相关,表明草酸铵提取的无定形的铁和铝是息息相关的,对沉积物吸附磷起着重要的作用.同时小兴凯湖沉积物中草酸铵提取的磷与沉积物中总磷含量极显著相关(r=0.983, n=13),而总磷与沉积物有机质含量也有较好的相关性(r=0.658, n=13).
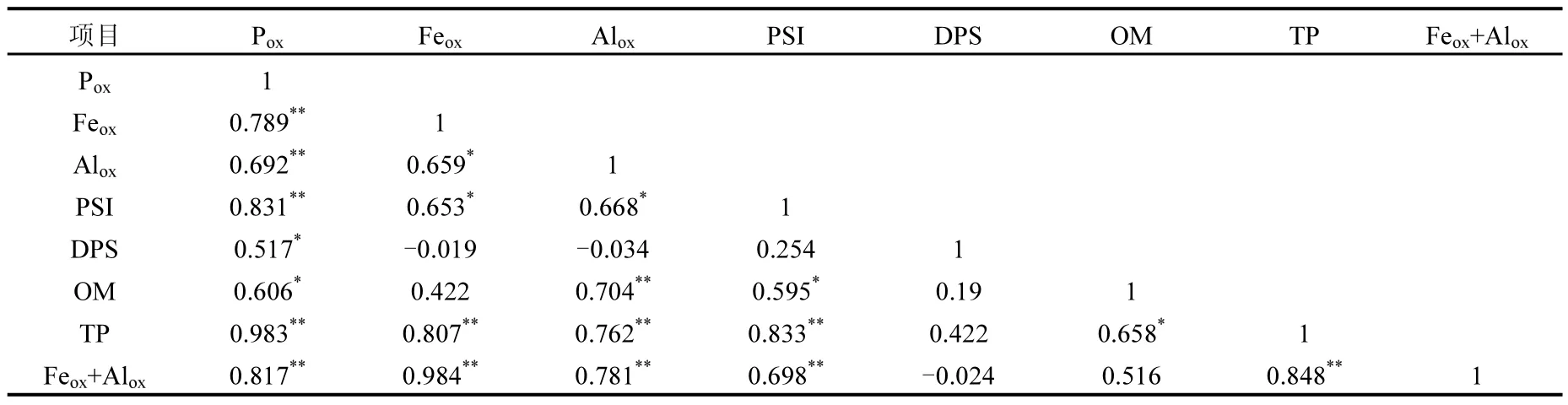
表4 小兴凯湖沉积物样品中理化参数间的相关性(n=13)Table4 Correlation of physicochemical parameters of sediment in Lake Xiaoxingkai (n=13)
2.4 表层沉积物磷吸附指数(PSI)特征分析
PSI表示土壤颗粒对溶解性磷盐固定能力的强弱.因湖泊沉积物长期处于淹水状态下且颗粒粒径较细,其PSI值常大于土壤中的测定值[36].
小兴凯湖表层沉积物的磷吸附指数(PSI)变化范围为9.78~197.53(mg·L)/(100g·μmol),平均值为59.77(mg·L)/(100g·μmol).PSI整体表现出南高北低,西高东低的分布特征,根据 PSI 的定义可知,PSI 值低的土壤对磷具有较弱的缓冲能力,磷释放进入水体的风险较高[37],由此表明小兴凯湖北岸、湖东区域可能具有较高的磷释放风险;而磷吸附饱和度(DPS)分布恰恰与磷吸附指数有着相反的特征(尽管两者的相关性较差,表4)[16],在PSI较高的区域(如T8采样点),相应的DPS较低.
PSI与Pox极显著正相关(r=0.831,n=13,表4)与 Alox(r=0.653,n=13,表4)、Feox(r=0.668,n=13,表4)显著正相关,当无定形的铁、铝氧化物含量增大时,磷的可吸附位增多,沉积物对磷具有更强的缓冲能力,这表明活性铁和铝是小兴凯湖表层沉积物中对磷持留能力的主要影响因素,而小兴凯湖表层沉积物中活性铁的量大约是活性铝的3倍,表明小兴凯湖表层沉积物中活性铁可能对磷起主要的持留作用,如果 Feox含量升高势必会使PSI升高. T8(白鱼滩)采样点的PSI最大(图2),说明 T8(白鱼滩)采样点表层沉积物的磷吸附能力最强,因 T8(白鱼滩) 采样点的 Feox含量最高,铁氧化物为磷提供了更多吸附点位,导致无定形铁成为主要基. PSI与表层沉积物中Pox含量呈正相关,即Pox含量高则吸附能力也强.
2.5 表层沉积物的磷吸附饱和度(DPS)特征分析
小兴凯湖表层沉积物的 DPS变化范围为9.95%~24.47%,平均值15.41%.由DPS的多元回归方程(Ⅲ和Ⅳ)显示(表5),小兴凯湖沉积物磷吸附饱和度主要受到草酸铵提取的磷含量的控制,但是如果活性铁、铝含量和有机质含量升高,势必会扩大沉积物磷的吸附容量[38],进而导致磷吸附饱和度的降低. DPS的大小在很大程度上决定了沉积物汇总的磷向水体释磷量,可以作为衡量沉积物含磷水平和评估沉积物对磷吸附容量的可靠指标[36,39],DPS越高,则磷越容易从沉积物表面迁移到水体,即磷释放到上覆水体中的风险也越大.当磷成为富营养化发生限制因素时,随上覆水体中的供磷量增加,富营养化的程度将加重.表5对沉积物TP含量与草酸铵提取的铝、铁、磷以及沉积物有机质含量进行了多元回归拟合,拟合出方程(Ⅰ)和方程(Ⅱ),相关系数均在0.98以上,表明无定形的铝、铁、磷以及沉积物有机质对总磷可能起着重要的贡献作用,这与黄清辉等[16]对太湖的研究结果一致.

表5 沉积物中磷的吸附参数与草酸铵提取的铝、铁、磷及有机质间的多元回归方程(n=13)Table5 Mutipule regression equations of P sorption on Pox, Alox, Feox and OM(n=13)
2.6 磷释放风险评估
结合2012中国环境状况公报[6]小兴凯湖富营养化状况以及黄清辉等[16]对太湖表层沉积物磷释放诱发富营养化风险的评价体系,将小兴凯湖表层沉积物磷释放诱发富营养化风险评价等级分成高度风险(ERI>25),较高风险(20 表6 小兴凯湖富营养化风险评价Table6 Eutrophication risk assessment of Lake Xiaoxingkai 黄清辉等[16,34]对太湖和巢湖表层沉积物磷释放诱发富营养化风险研究发现,太湖紧邻城区和工业区的梅梁湾北部至五里湖一带、竺山湖北部湖区属于高度风险区,其余区域风险相对较低,巢湖处于较高风险至高度风险状态,并发现对太湖和巢湖富营养化风险的预测和实际的富营养化发生情况基本相符,并且高度风险区多位于受人为因素影响较大的区域.此外,卢少勇等[40]也对北京六湖泊表层底泥磷释放诱发富营养化风险进行研究,发现六湖中以娱乐为主的景观湖泊和受人为因素影响大的四个湖区处于高度风险,城市地表径流是导致其污染的主要原因.因此,小兴凯湖和北京六湖泊中的四湖表层沉积物磷释放诱发富营养化的高度风险区都是受地表径流影响较大的区域. 3.1 小兴凯湖表层沉积物的PSI与沉积物中活性铁(Feox)含量呈极显著正相关,与铁铝总量呈显著正相关,DPS与沉积物中草酸铵提取的磷(Pox)含量呈显著正相关.小兴凯湖表层沉积物中活性铁、铝的含量影响着沉积物的磷吸附容量,其中,表层沉积物中活性铁可能对磷起主要的持留作用.小兴凯湖沉积物磷的吸附容量具有一定的空间差异,主要是由无定形的铁、铝氧化物及有机质等沉积物内在属性的空间差异决定,但在一定程度上也取决于受人类活动等外在因素干扰的程度. 3.2 利用磷释放风险指数(ERI)对小兴凯湖表层沉积物中的磷的潜在释放风险进行评估,结果表明:小兴凯湖表层沉积物中磷释放诱发富营养化的风险处于高度风险范围,其中,受农业面源污染较大的北岸区域相比其他区域发生富营养化的风险更高. [1] 王彦明.兴凯湖自然保护区 [J]. 黑龙江环境通报,1998,22(1):60-62. [2] 姬忠光,吴明官.国境界湖兴凯湖水资源可利用量初探[J]. 黑龙江水利科技,2006,34(2):47-49. [3] 刘正茂,吕宪国,武海涛,等.兴凯湖最低生态安全水位 [J]. 水利水电技术,2006,39(2):8-9. [4] 孙 冬,孙晓俊.兴凯湖水文特性 [J]. 东北水利水电,2006,24(2):21-27. [5] 刘凤林,张海洋,刘建清,等.小兴凯湖水生高度植物区系组成及其特点 [J]. 黑龙江八一农垦大学学报,1991,2:37-46. [6] 环境保护部.2012年中国环境状况公报 [R]. 北京,2012. [7] 余 辉,张文斌,卢少勇,等.洪泽湖表层底质营养盐的形态分布特征与评价 [J]. 环境科学,2010,31(4):961-968. [8] 袁和忠,沈 吉,刘恩峰.太湖不同湖区沉积物磷形态变化分析[J]. 中国环境科学,2010,30(11):1522-1528. [9] Gonsiorczyk T, Casper P, Koschel R. Phosphorus binding forms in the sediment of an oligotrophic and an eutrophic hardwater lake of the baltic district (Germany) [J]. Water Science and Technology,1998,37(3):51-58. [10] 金相灿,庞 燕,王圣瑞,等.长江中下游浅水湖沉积物磷形态及其分布特征研究 [J]. 农业环境科学学报,2008,27(1):279-285. [11] 吕昌伟,何 江,孙惠民,等.乌梁素海沉积物中磷的形态分布特征 [J]. 农业环境科学学报,2007,26(3):878-885. [12] Bache B W, Williams E G. A phosphate sorption index for soils [J]. Journal of Soil Science,1971,22(3):289-301. [13] Chen C R, Sinaj S, Condron L M, et al. Characterization ofphosphorus availability in selected New Zealand grassland soils [J]. Nutrient Cycling in Agroeco Systems,2003,65:89-100. [14] Pan G, KromM D, Herut B. Adsorption-desorption of phosphate on airborne dust and riverborne particulates in east Mediterranean sea water [J]. Environ. Sci. Technol.,2002,36:3519-3524. [15] McDowell R W, Sharpley A N. Phosphorus solubility and release kinetics as a function of soil test P concentration [J]. Geoderma,2003,112(1):143-154. [16] 黄清辉,王子健,王东红,等.太湖表层沉积物磷的吸附容量及其释放风险评估 [J]. 湖泊科学,2004,16(2):97-104. [17] 朴德雄,王凤昆.兴凯湖水环境状况及其保护对策 [J]. 湖泊科学,2011,23(2):196-202. [18] 卢 玲,赵彩霞,陈中祥,等.兴凯湖水域水体氮、磷含量特征及潜在性富营养化评价 [J]. 黑龙江科学,2011,2(3):1-3. [19] 中国土壤学会.土壤农业化学分析方法 [M]. 北京:中国农业科技出版社,1999:22-26. [20] 国家环境保护总局《水和废水监测分析方法》编委会.水和废水监测分析方法 [M]. 北京:中国环境科学出版社,2002. [21] GB3838-2002 地表水环境质量标准 [S]. [22] Smith V H, Tilman G D, Nekola J C. Eutrophication: impacts of excess nutrient inputs on freshwater, marine and terrestrial ecosystems [J]. Environment and Pollution,1999,100:179-196. [23] 隋少峰,罗启芳.武汉东湖底泥释磷特点 [J]. 环境科学,2001,22(l):102-105. [24] 王雨春,万国江,黄荣贵,等.湖泊现代化沉积物中磷的地球化学作用及环境效应 [J]. 重庆环境科学,2000,22(4):39-41. [25] Correll D L. The role of phosphorus in the eutrophication of receiving waters: A review [J]. Journal of Environmental Quality,1998,27(2):261-266. [26] Hudson J J, Taylor W D, Schindler D W. Phosphate concentrations in lakes [J]. Nature,2000,406(6791):54-56. [27] 周莉荫,任 琼,严员英,等.水生植物污水净化概述—以芦苇为例 [J]. 江西林业科技,2011,3:46-48. [28] Białowiec A, Janczukowicz W, Randerson P F. Nitrogen removal from wastewater in vertical flow constructed wetlands containing LWA/gravel layers and reed vegetation [J]. Ecological Engineering,2011,37(6):897-902. [29] Wang Y, Zhang J, Kong H, et al. A simulation model of nitrogen transformation in reed constructed wetlands [J]. Desalination,2009,235(1):93-101. [30] Bulgakov N G, Levich A P. The nitrogen: Phosphorus ratio as a factor regulating phytoplankton community structure: Nutrient ratios [J]. Archiv für Hydrobiologie,1999,146(1):3-22. [31] Xie L, Xie P, Li S, et al. The low TN: TP ratio, a cause or a result of Microcystis blooms [J]. Water Research,2003,37(9):2073-2080. [32] Lopez P, Lluch X, Morguí J A. Adsorption of phosphoruson sediments of the balearic islands related to their composition [J]. Estuarine, Coastal and Shelf Science,1996,42:185-196. [33] Ruban V, Brigault S, Demare D, et al. An investigation of the origin and mobility of phosphorus in freshwater sediments from Bort -Les -Orgues Reservoir, France [J]. Journal of Environmental Monitoring,1999,1(4):403-407. [34] 黄清辉.浅水湖泊内源磷释放及其生物有效性 [D]. 北京:中国科学院研究生院,2005. [35] 邢友华,董 洁,等.东平湖表层沉积物中磷的吸附容量及潜在释放风险分析 [J]. 农业环境科学学报,2010,29(4):746-751. [36] 邵兴华,章永松,林咸永,等.三种铁氧化物的磷吸附解吸特性以及与磷吸附饱和度的关系 [J]. 植物营养与肥料学报,2006,12(2):208-212. [37] 张 静.鄱阳湖南矶山湿地土壤对磷的吸附与释放特性的研究[D]. 南昌:南昌大学,2006. [38] 范成新,刘元波,陈荷生.太湖底泥蓄积量估算及分布特征探讨[J]. 上海环境科学,2000,19(2):72-75. [39] Nair V D, Graetz D A. Phosphorus saturation in Spodosols impacted by manure [J]. Journal of environmental quality,2002,31(4):1279-1285. [40] 卢少勇,王 佩,王殿武,等.北京六湖泊表层底泥磷吸附容量及潜在释放风险 [J]. 中国环境科学,2011,31(11):1836-1841. Phsophorus sorption capacity of surface sediments and risk assessment of potential phosphorus release in Lake Xiaoxingkai, China. YU Shu-ling1,2, LI Xiao-yu1, ZHANG Ji-tao1, CHEN Guo-shuang1, LI Xiu-jun1* Phosphorus sorption capacity of surface sediments are estimated by phosphorus sorption index (PSI) of sediments and degree of phosphorus saturation (DPS) in Lake Xiaoxingkai, China. The relationship between DPS and other indicators were analyzed, and the risk of potential phosphorus release were discussed by calculating phosphorus release risk index (ERI). The results showed that PSI ranged from9.78 to197.53 (mg·L)/(100g·µmol), with an average of59.77 (mg·L)/(100g·µmol). DPS ranged from9.95% to24.47%, with an average of15.41%. PSI was significantly and positively correlated to phosphorus (Pox), iron (Feox) and aluminum (Alox) extracted from sediment by ammonium oxalate. Rion extracted from sediment by ammonium oxalate might be the main factor to affect PSI. DPS was influenced mainly by original adsorbed phosphorus of sediments (or Pox). In addition, ERI ranged from8.99% to129.94%, which indicated that the Lake Xiaoxingkai might be in high potential eutrophication risk due to the release of phosphorus from surface sediments. Compared to the different sample points, the north area polluted by agricultural non-point source pollution has higher potential eutrophication risk than other areas. t:phosphorus sorption index (PSI);degree of phosphorus saturation (DPS);phosphorus release risk index;amorphous Fe and Al oxides;Lake Xiaoxingkai X524,X142 :A :1000-6923(2014)08-2078-08 于淑玲(1988-),女,黑龙江绥化人,硕士研究生,主要从事湿地生态恢复及湿地评价研究. 2013-11-30 国家重大科学研究计划资助(2012CB956100) * 责任作者, 研究员, lixiujun@neigae.ac.cn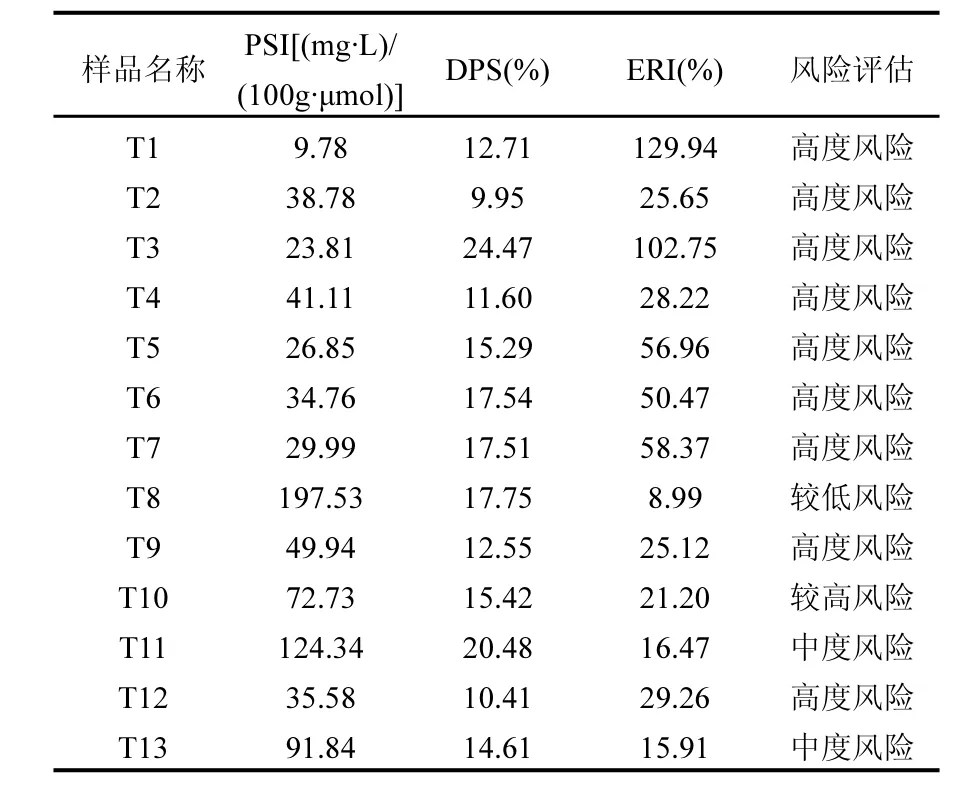
3 结论
(1.Key Laboratory of Wetland Ecology and Environment, Northeast Institute of Geography and Agroecology, Chinese Academy of Sciences, Changchun130102, China;2.University of Chinese Academy of Sciences, Beijing100049, China). China Environmental Science,2014,34(8):2078~2085
