柠檬醛合成紫罗兰酮的工艺优化
2014-05-03皮少锋孙汉洲黎继烈
胡 铁 王 烨 皮少锋 孙汉洲 黎继烈
HU Tie 1 WANG Ye 2 PI Shao-feng 2 SUN Han-zhou 2 LI Ji-lie 2
(1.广州航海学院,广东 广州 410208;2.经济林培育与保护省部共建教育部重点实验室(中南林业科技大学),湖南 长沙 410004)
(1.Guangzhou Maritime Institute,Guangzhou,Guangdong 510725,China;2.Key Laboratory of Cultivation and Protection for Non-Wood Forest Trees (Central South University of Forestry and Technology),Ministry of Education,Changsha,Hunan 410004,China)
紫罗兰酮是极其重要的调香原料,又名香堇酮,分子式为C13H20O[1],它存在于高茎当归、合金欢大柱波罗尼花、西红柿指甲花等多种植物中,因双键位置不同而有α、β、γ3种同分异构体,自然界多以α体,β体这两种异构的混合形式存在,γ-体较为少见。其中以α-紫罗兰酮最具有紫罗兰酮花香特性,香气柔和淳厚,最为人们所喜爱,销售价格也较高[2];β-紫罗兰酮则是医药工业上合成维生素A的重要原料,也用于高档级精细日用化妆品的调香剂和增香剂[3]。在食品行业中紫罗兰酮常用作高档食品、饮料的增香剂,是中国GB 2760-2011规定允许使用的食用香料,主要用以配制龙眼、树莓、黑莓、樱桃、柑橘等型香精。
紫罗兰酮制备工艺多数是以柠檬醛或假紫罗兰酮为关键中间体合成紫罗兰酮[4-7],其合成工艺根据环化时不同催化剂的选择,归纳起来主要可以分为2种:① 无机酸催化环化法[8],② 固体酸催化环化法[9,10],这2种方法的紫罗兰酮收率不高(为54%~70%[8-10]),且α-紫罗兰酮含量较低,尚有很大的提升空间。因此本研究拟以氢氧化钠为催化剂,通过柠檬醛与丙酮进行羟醛缩合合成假紫罗兰酮,再用磷酸催化环化得到紫罗兰酮,旨在通过优化合成反应工艺条件,简化处理过程,提高紫罗兰酮收率和α-紫罗兰酮选择性。
1 材料与方法
1.1 材料和试剂
柠檬醛:97%,湖南湘农山香油脂香料有限责任公司;
丙酮、氢氧化钠、冰醋酸、磷酸、碳酸氢钠、甲苯:均为国产分析纯试剂。
1.2 主要仪器
气相色谱仪:Agilent 6890N型,美国安捷伦科技有限公司;
气相色谱-质谱联用仪:HP7890-HP 5975C型,美国安捷伦科技有限公司;
核磁共振波谱仪:Bruker Avance DRX 500型,德国布鲁克公司。
1.3 试验方法
1.3.1 样品定量检测 采用气相色谱检测,测式条件:HP-5石英毛细管柱(30 m×0.25 mm×0.25μm),程序升温:柱初始温度70℃,保持2 min,升温速率3℃/min,升温至180℃,升温速率改为10℃/min,升温至250℃,保持5 min,载气为氮气,流速25 m L/min,分流比50∶1,气化室温度250℃(FID)。
定量数据用峰面积归一化法进行计算,即:

式中:
Pi—— 组分i的质量分数,%;
Ai—— 组分i的峰面积;
∑A——馏出峰的总面积。
1.3.2 样品定性检测 采用气相色谱-质谱联用法,测式条件:HP-5石英毛细管柱(30 m×0.25 mm×0.25μm),程序升温:柱初始温度70℃,保持2 min,升温速率3℃/min,升温至180℃,升温速率改为10℃/min,升温至250℃。质谱EI源:70 eV,倍增器电压:1 500 V,扫描范围:33~500 m/z,全扫描方式。
1.3.3 样品结构鉴定 样品结构鉴定采用核磁共振检测方法。核 磁 共 振 条 件 为1H NMR (500 MHz,CDCl3),13C NMR(125 MHz,CDCl3),以氘代三氯甲烷为溶剂,三甲基硅烷(TMS)为内标进行测定,将样品用氘代三氯甲烷溶解于核磁样品管中,置于仪器中进行扫描。
1.3.4 假紫罗兰酮的合成 在1 000 m L的四口烧瓶中,按设定比例加入丙酮、NaOH和柠檬醛(柠檬醛30 min内滴加完毕)。反应完全后,反应液用36%的冰醋酸溶液中和至p H=6~7,回收丙酮,有机层用60 m L饱和食盐水洗涤后减压蒸馏,收集沸点为110~120℃(760 Pa)的馏分,得到假紫罗兰酮样品,定量定性分析试验结果。
1.3.5 紫罗兰酮的合成 在1 000 m L的四口烧瓶中,按设定比例加入假紫罗兰酮、甲苯和85%H3PO4(H3PO4在60 min内滴加完毕),控制反应温度反应2 h。反应完全后,冷却至室温,分出磷酸层,有机层用15%的Na HCO3溶液中和至p H=6~7,再用60 m L饱和食盐水洗涤,回收甲苯后,减压蒸馏,收集沸点为121~129℃(1 330 Pa)的馏分,得到紫罗兰酮样品,定量定性分析试验结果。
2 结果与分析
2.1 假紫罗兰酮的合成
2.1.1 反应温度对假紫罗兰酮收率的影响 按1.3.4的合成方法,考察反应温度对假紫罗兰酮收率的影响,结果见图1。当反应温度低于40℃时,假紫罗兰酮收率降低,因为反应温度较低时,催化剂的活性较低,反应进行得不完全。当反应温度高于45℃时,由于反应体系中反应温度过高,副反应加剧,假紫罗兰酮的收率降低。因此适宜的反应温度为40~45℃。
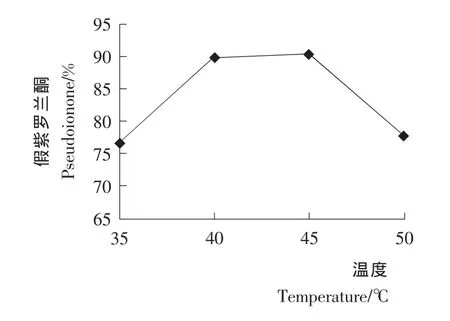
图1 反应温度对假紫罗兰酮收率的影响Figure 1 Effects of reaction temperature on the yield of pseudoionone
2.1.2 催化剂用量对假紫罗兰酮收率的影响 按1.3.4的合成方法,考察催化剂用量对假紫罗兰酮收率的影响,结果见图2。当NaOH用量为1%~3%时,假紫罗兰酮收率随催化剂用量的增加而增大。而当NaOH用量高于3%时,碱浓度过高,导致假紫罗兰酮进一步缩合或发生其他副反应产生高沸物,反应收率降低。所以适宜的NaOH用量为3%。
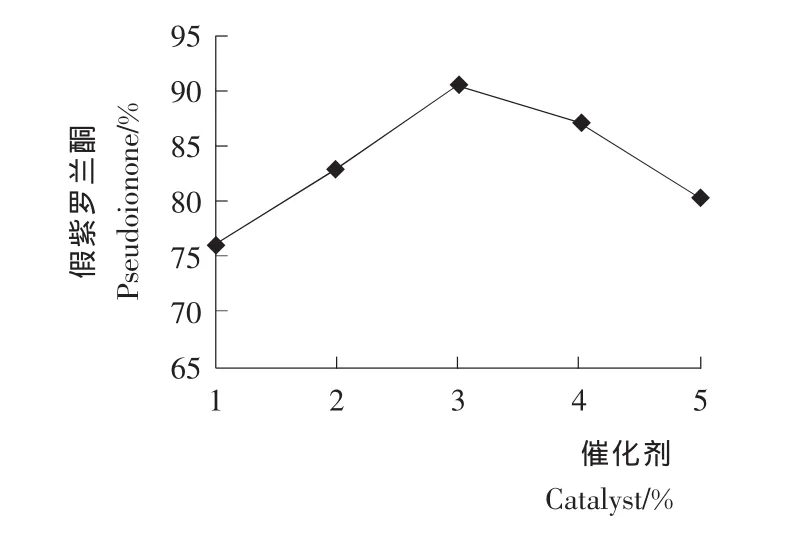
图2 催化剂用量对假紫罗兰酮收率的影响Figure 2 Effects of catalyst dosage on the yield of pseudoionone
2.1.3 物料比n丙酮∶n柠檬醛对假紫罗兰酮收率的影响 按1.3.4的合成方法,考察物料比对假紫罗兰酮收率的影响,结果见图3。当n丙酮∶n柠檬醛(丙酮∶柠檬醛摩尔比)<6时,假紫罗兰酮收率降低,因为丙酮量少不足时,导致柠檬烯基柠檬酮、二柠檬烯基酮等副产物生成。此后再增加丙酮的用量,反应收率基本保持不变。所以适宜的物料比n丙酮∶n柠檬醛为6∶1。
2.1.4 反应时间对假紫罗兰酮收率的影响 按1.3.4的合成方法,考察反应时间对假紫罗兰酮收率的影响,结果见图4。假紫罗兰酮的收率在3 h以内,随反应时间的延长明显增加,反应3 h时,假紫罗兰酮的收率达到最大值90.6%。继续延长反应时间,反应收率开始降低。因此适宜的反应时间为3 h。
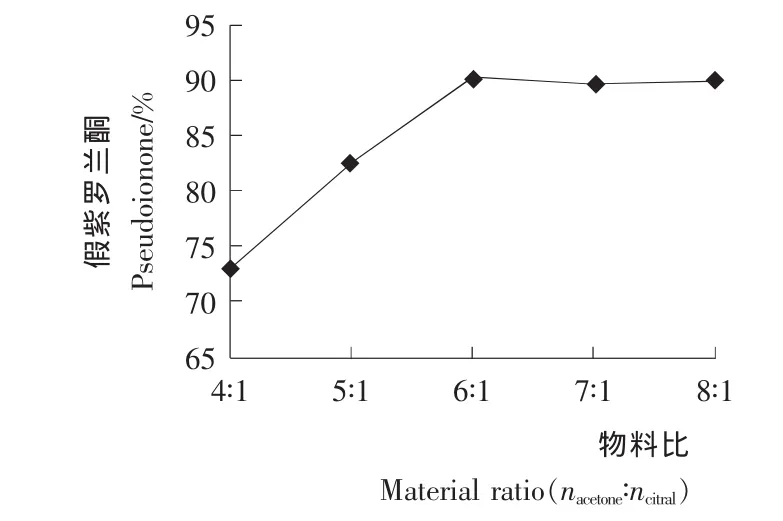
图3 物料比对假紫罗兰酮收率的影响Figure 3 Effects of material ratio on the yield of pseudoionone
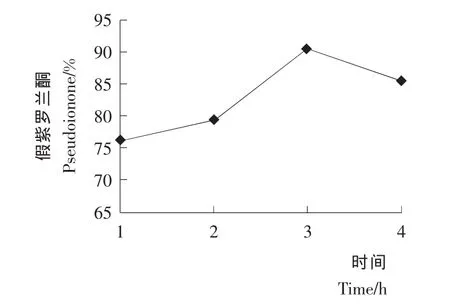
图4 反应时间对假紫罗兰酮收率的影响Figure 4 Effects of reaction time on the yield of pseudoionone
2.1.5 假紫罗兰酮样品结构鉴定 采用核磁共振波谱仪和气-质联用仪对所得的假紫罗兰酮样品进行结构鉴定。样品为淡黄色液体,1H NMR (500 MHz,CDCl3)δ:7.44~7.26(m,1H),6.08~6.05 (dd,J =15 Hz,1 H),6.02~6.98(d,J =7.5 Hz,1H),5.10~5.06 (m,1H),2.32~2.29(d,J=7.5 Hz,1H),2.26~2.25(dd,J=5Hz,3H),2.15~2.12 (d,J =9 Hz,4H),1.99~1.88 (dd,J =7 Hz,3H),1.67~1.66 (d,J = 4.5 Hz,3H),1.60 (s,3H);13C NMR (125 MHz,CDCl3)δ:151.23 (s,1C),151.17(s,1C),139.64 (s,1C),139.49 (s,1C),132.67 (s,1C),132.68 (s,1C),132.68 (s,1C),128.34 (s,1C),128.17(s,1C),124.57 (s,1C),123.65 (s,1C),123.17 (s,1C),123.09(s,1C),77.25(s,1C),77.00(s,1C),76.75(s,1C),40.38 (s,1C),32.94 (s,1C),27.45 (s,1C),27.30 (s,1C),26.79 (s,1C),26.23 (s,1C),25.64 (s,1C),24.58 (s,1C),17.66(s,1C),17.48 (s,1C);GC-MS(E1,70 e V,m/z,图5,图6):192(M+,5),55(70),69(100),109(66)。样品经1H-NMR、13C NMR以及GC-MS确证该产物即为目标产物假紫罗兰酮。
2.1.6 假紫罗兰酮组分分析 采用GC-MS法对假紫罗兰酮试验样品的组分进行分析,结果见图5和图6,假紫罗兰酮样品中主要组分为α-假紫罗兰酮和β-假紫罗兰酮,柠檬醛合成假紫罗兰酮反应的收率为90.6%。
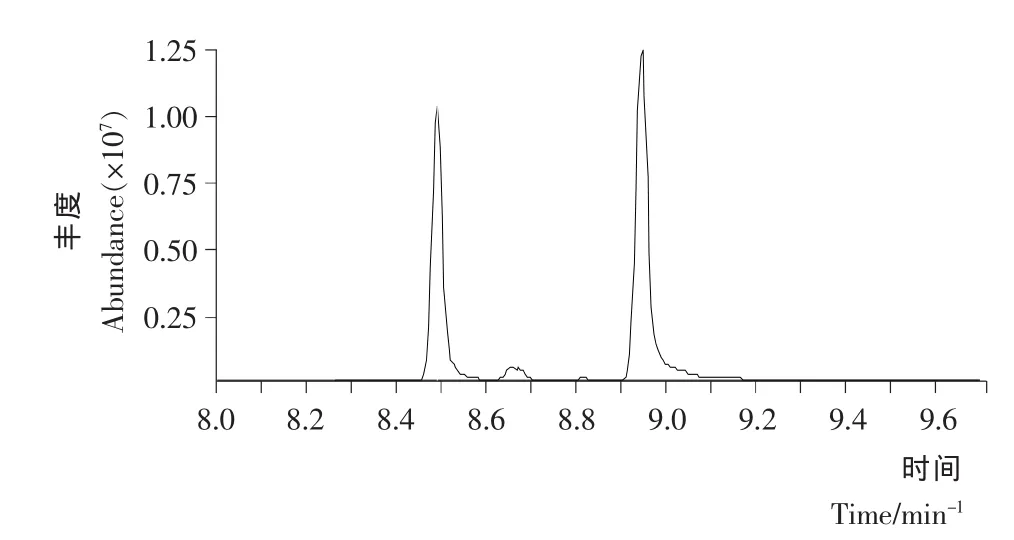
图5 假紫罗兰酮的GC谱图Figure 5 GC chromatograms of Pseudoionone
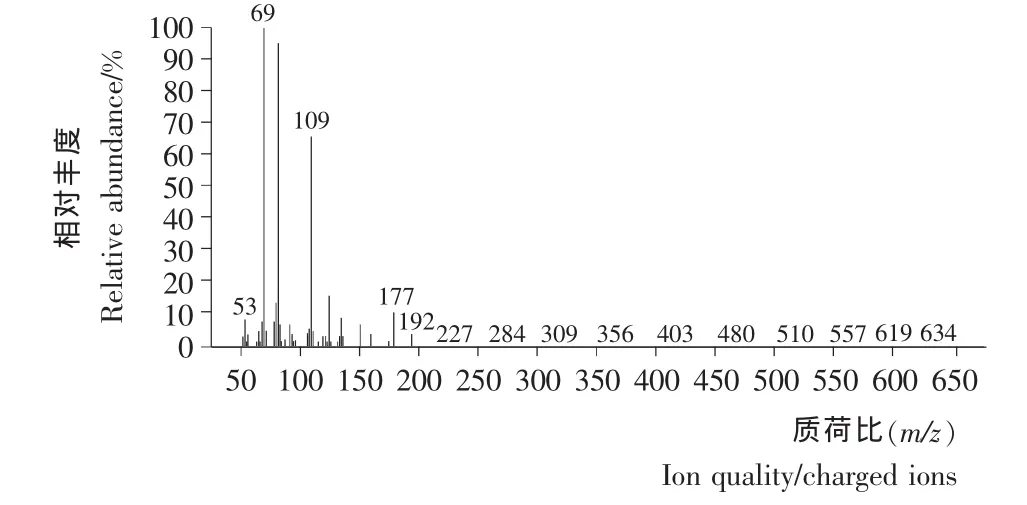
图6 假紫罗兰酮的质谱图Figure 6 MS chromatograms of Pseudoionone
2.2 紫罗兰酮的合成
2.2.1 反应温度对紫罗兰酮收率和α-紫罗兰酮选择性的影响 按1.3.5合成方法,考察反应温度对紫罗兰酮收率的影响,结果见图7。当反应温度低于50℃时,紫罗兰酮收率和α-紫罗兰酮选择性都较低,因为反应温度较低时,反应进行得不完全。当反应温度为50℃时,紫罗兰酮收率和α-紫罗兰酮的选择性达到最大值。继续升高反应温度反应收率和选择性开始下降,因为反应温度过高,反应物或生成物发生了聚合反应,导致副产物生成。因此适宜的反应温度为50℃。
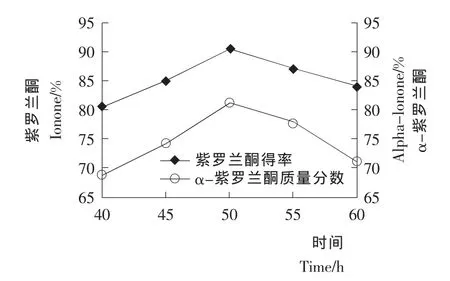
图7 反应温度对环化反应的影响Figure 7 Effects of reaction temperature on Cyclization Reaction
2.2.2 催化剂用量对紫罗兰酮收率和α-紫罗兰酮选择性的影响 按1.3.5的合成方法,考察催化剂用量对紫罗兰酮收率的影响,结果见图8。当催化剂用量n假紫罗兰酮∶n85%磷酸(假紫罗兰酮∶85%磷酸摩尔比)>1∶3时,紫罗兰酮的反应收率和α-紫罗兰酮选择性较低,因为催化剂用量较少时,导致催化环化的反应速率太慢,反应不完全。当催化剂用量n假紫罗兰酮∶n85%磷酸<1∶3时,紫罗兰酮的反应收率和α-紫罗兰酮选择性开始降低,因为催化剂用量太多时,导致副反应发生。因此适宜的催化剂用量为n假紫罗兰酮∶n85%磷酸=1∶3。
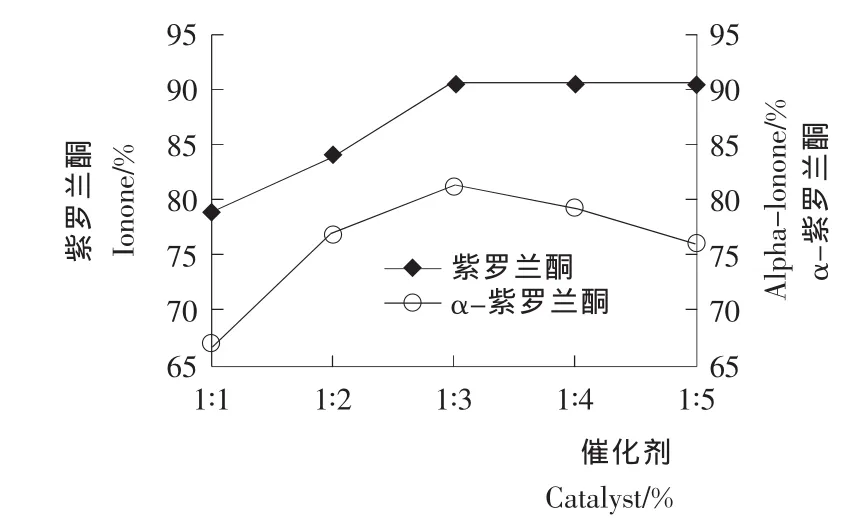
图8 催化剂用量对环化反应的影响Figure 8 Effects of catalyst dosage on Cyclization Reaction
2.2.3 反应时间对紫罗兰酮收率和α-紫罗兰酮选择性的影响 按1.3.5的合成方法,考察反应时间对紫罗兰酮收率的影响,结果见图9。当反应时间少于2 h时,由于反应时间不够,导致反应不充分,虽然反应的选择性较好,但是紫罗兰酮收率太低;当延长反应时间时,由于副产物增多,紫罗兰酮收率和α-紫罗兰酮选择性开始下降。因此适宜的反应时间为2 h。
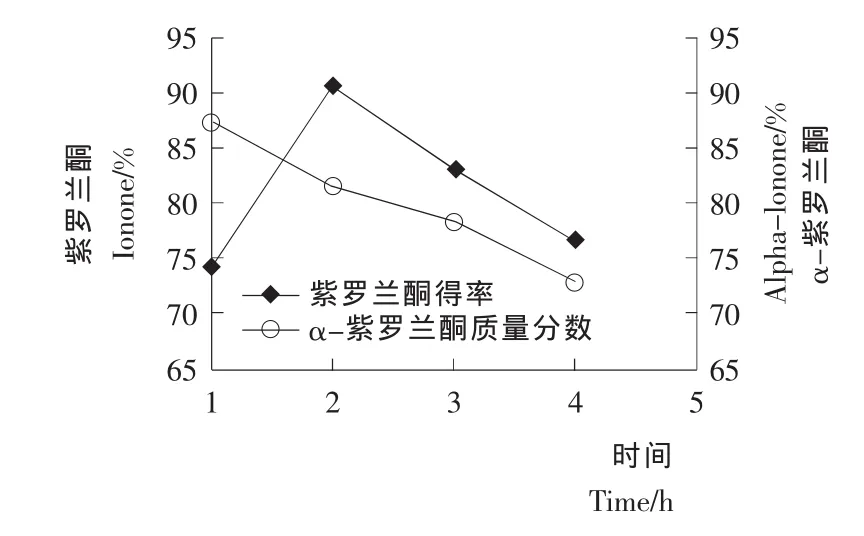
图9 反应时间对环化反应的影响Figure 9 Effects of reaction time on Cyclization Reaction
2.2.4 紫罗兰酮样品结构鉴定 采用核磁共振波谱仪和气-质联用仪对所得的紫罗兰酮样品进行结构鉴定。样品为浅黄 色 液 体:1H NMR (400 MHz,CDCl3)δ:1H NMR(400 MHz,CDCl3)δ:1.27~1.19 (m,1H),1.51~1.42(m,1H),1.57 (s,1 H),1.77 (s,1H),3.13~3.07 (m,1 H),6.68~6.58(m,1H),6.16~6.08(m,1H),6.05(d,J =15.82 Hz,1H),5.50(s,1 H),2.34~2.20 (m,1H),2.11~2.00(m,1H),2.16~2.11 (m,1 H),1.64 (s,1H),7.40~7.35(m,1H),7.33~7.28 (m,1H),7.28~7.23 (m,1H),0.86(s,1H),0.93 (s,1H),1.07 (d,J =1.81 Hz,1H);GC-MS(E1,70 e V,图10、11)m/z):192(M+,8),55(70),69(100),109(54),124(16)。样品经1H-NMR、GC-MS确证该产物即为目标产物紫罗兰酮。
2.2.5 紫罗兰酮组分分析 采用GC-MS法对紫罗兰酮试验样品的组分进行分析,结果见图10、11,紫罗兰酮样品中α-紫罗兰酮质量分数81.4%,β-紫罗兰酮的含量为15.6%。假紫罗兰酮环化合成紫罗兰酮收率89.8%,柠檬醛合成紫罗兰酮两步反应的总收率为81.4%。

图10 紫罗兰酮的GC谱图Figure 10 GC chromatograms of ionone
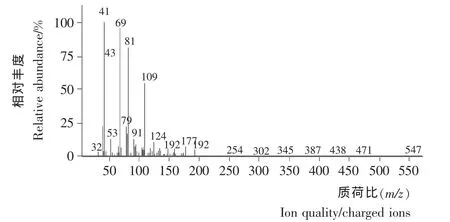
图11 紫罗兰酮的质谱图Figure 11 MS chromatograms of ionone
3 结论
以柠檬醛为原料,经过假紫罗兰酮中间体合成紫罗兰酮。通过反应温度、反应时间,NaOH用量、丙酮与柠檬醛的物料比对假紫罗兰酮收率的影响试验,获得了以柠檬醛为原料,合成假紫罗兰酮中间体的最适工艺条件,假紫罗兰酮的收率为90.6%;通过反应温度、反应时间及催化剂用量对紫罗兰酮收率、α-紫罗兰酮选择性的影响试验,获得了假紫罗兰酮环化合成紫罗兰酮最适工艺条件,紫罗兰酮收率为89.8%,其中α-紫罗兰酮质量分数81.4%,β-紫罗兰酮的含量为15.6%。柠檬醛合成紫罗兰酮两步反应的总收率81.4%。
从工艺优化试验结果来看,柠檬醛合成紫罗兰酮两步反应的总收率比较高,α-紫罗兰酮选择性好,达到工艺简化、产品质优、降低成本的目的,可以为生产过程放大提供工艺数据参考。
1 余红霞,王植.用山苍子油合成α-紫罗兰酮和β-紫罗兰酮的研究[J].湖南理工学院学报,2005,18(2):39~41.
2 陈立军,张心亚,黄洪,等.高纯度β-紫罗兰酮的制备方法[J].香料香精化妆品,2005(3):29~32.
3 黄喜根,刘晓庚.由山苍子油合成甲基紫罗兰酮[J].化学世界,2003,44(8):422~425.
4 唐健.紫罗兰酮的合成及应用[J].化学推进剂与高分子材料,2007,5(1):43~45.
5 许海红,郭岱石,蒋淇忠,等.硫酸根促进的纯硅MCM-41催化假性紫罗兰酮环化合成紫罗兰酮的性能[J].催化学报,2006,27(12):1 084~1 086.
6 周袭非,于群,郭威.假性紫罗兰酮合成条件[J].辽宁科技大学学报,2009,32(3):237~240.
7 赵振华,邹双国.Na HSO4催化假性紫罗兰酮合成紫罗兰酮[J].合成化学,2004,12(6):589~590.
8 吴琴芬,刘燕燕,祝志武,等.紫罗兰酮的合成研究[J].南昌大学学报,2006,28(3):221~226.
9 李春波,马紫峰,沈旻,等.SO/Zr O2-HZSM-5固体超强酸催化环化制β-紫罗兰酮[J].高校化学工程学报,2003,17(4):442~446.
10 唐斯萍,向瑞军.TiO2-Sb2O3/SO催化合成紫罗兰酮[J].湖南科技学院学报,2008,29(8):66~67.
