熔融法制备非诺贝特固体分散体及体外溶出研究
2014-04-30张晶晶王少平
张晶晶,王少平
1南京市鼓楼医院药剂科,南京 210008;2江苏正大天晴药业股份有限公司,南京 210023
熔融法制备非诺贝特固体分散体及体外溶出研究
张晶晶1,王少平2
1南京市鼓楼医院药剂科,南京 210008;2江苏正大天晴药业股份有限公司,南京 210023
目的:制备非诺贝特固体分散体。方法:采用熔融法制备,考察药物和载体的比例、混合温度、冷却温度对溶出率的影响,比较固体分散体和物理混合物的溶出率的区别。结果:药物和载体比例达到1∶2时,载体的量足够使药物分散均匀;混合温度对溶出率影响较大;冷却温度对溶出率影响不大。与物理混合物相比,固体分散体将非诺贝特的溶出率显著提高。结论:非诺贝特固体分散体提高了非诺贝特的体外溶出率。
非诺贝特;共聚维酮(S630);固体分散体;溶出率
非诺贝特(fenofibrate)为氯贝丁酯类降血脂药,能抑制甲基戊二酰辅酶A(HMG-CoA)还原酶,从而减少胆固醇合成;临床常用于治疗高甘油三酯血症、高胆固醇血症和混合型高脂血症,对老年人动脉粥样硬化、心脑血管疾病的防治有着重要意义[1]。非诺贝特为白色或类白色结晶性粉末,熔点为79~82℃,极易溶于氯仿,易溶于丙酮或乙醚,略溶于乙醇,几乎不溶于水,口服吸收差,生物利用度低。普通制剂单次口服给药仅6%剂量被吸收,4~7小时血药浓度达峰值[2]。目前市售产品通过对原料药与十二烷基硫酸钠(SDS)的共微粉化提高了体外溶出效果,但仍难达到体内满意的吸收效果。
固体分散技术可以有效改善难溶性药物的溶出,从而提高生物利用度,是目前药剂学研究的热点之一[3]。为了改善非诺贝特的体外溶出度,本研究通过熔融法制备非诺贝特-共聚维酮(S630)固体分散体,优选处方和工艺参数,并将固体分散体的溶出度同药物和共聚维酮(S630)物理混合物的溶出度进行了对比,证明了该实验确定的处方和工艺参数能够制备得到固体分散体,同时证明了非诺贝特-共聚维酮(S630)固体分散体能够提高药物的溶出度。
1 材料
1.1 仪器
ZRS-8G型智能药物溶出仪(天大天发科技有限公司);HH-2型数显恒温水浴锅(河南省予华仪器有限公司);YXJ-2型高速离心机(金坛市环宇科学仪器厂);FAI0004N型电子天平(上海精密科学仪器有限公司);UV-2401型紫外-可见分光光度计(日本岛津公司);TGA-50型热重分析仪(日本岛津公司);DSC-60型差示扫描量热分析仪(日本岛津公司)。
1.2 试药
非诺贝特(浙江耐司康药业有限公司,纯度99.98%);非诺贝特对照品(市售原料药经反复精制而得,纯度99.74%);共聚维酮(S630)(美国ISP公司);其它试剂均为分析纯。
2 方法与结果
2.1 紫外分析方法的建立
2.1.1 最大吸收波长的确定取非诺贝特对照品适量,用无水乙醇溶解,1%十二烷基硫酸钠(SDS)溶液稀释,在200~400 nm波长范围内扫描,结果显示,非诺贝特在1%SDS溶液中的最大吸收波长为289 nm。
2.1.2 标准曲线的制备取非诺贝特对照品15 mg,精密称定,置于100 mL量瓶中,加无水乙醇溶解并稀释至刻度,摇匀,分别精密量取上述溶液适量,加1%SDS溶液稀释至刻度,制成2、5、7.5、10、12.5、15 μg·mL-1的对照品溶液。照紫外-可见分光光度法(《中国药典》2010年版二部附录ⅣA),在289 nm波长处测定其吸光度。以吸光度(Y)为纵坐标,非诺贝特浓度(X)为横坐标,进行线性回归,得回归方程为Y=0.059X+0.014(r=0.9995)。结果表明,非诺贝特在2~15 μg·mL-1浓度范围内与吸光度线性关系良好。
2.2 非诺贝特-共聚维酮(S630)固体分散体处方和工艺的确定
2.2.1 非诺贝特的熔点测定和热重分析取非诺贝特适量,置于差示扫描量热仪和热重分析仪的铝盘中,以氧化铝为参比物,在氮气流中,升温范围从室温到340℃,以5℃·min-1的速率升温扫描,得DSC和TGA图;由图1可见,药物在78℃附近有一明显的吸热峰,对应于药物的熔点,药物从180℃开始出现失重,故操作温度应低于180℃。
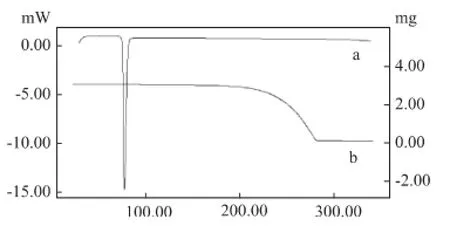
图1 非诺贝特热分析曲线
2.2.2 熔融法制备固体分散体的工艺流程以共聚维酮(S630)为载体,采用熔融法制备非诺贝特固体分散体。在水浴上将1份非诺贝特加热熔融,另将2份共聚维酮加热熔融,在搅拌下将共聚维酮熔融液倒入熔融的非诺贝特中,保温搅拌直至分散均匀,残存固体经粉碎过80目筛,干燥器中贮藏,备用。
2.2.3 溶出度测定方法照溶出度测定法(《中国药典》2010年版二部附录ⅩC第二法)。以水900 mL为溶出介质,转速为50 r·min-1,分别于5、10、15、20、30、45、60 min取溶出液5 mL,同时补加同温度溶出介质5 mL,用0.45 μm的微孔滤膜过滤,取续滤液,照紫外-可见分光光度法(《中国药典》2010年版二部附录ⅣA)在289 nm波长处测定吸光度,根据标准曲线方程计算累积溶出量,并对时间作图得溶出曲线。
2.2.4 混合温度对溶出率的影响混合温度考察范围设定为70、80、90℃;药物与载体的比例为1∶2;冷却温度为0℃。由图2可见,混合温度对溶出率有明显影响,温度过低则不利于固体分散体的形成,而80℃和90℃之间没有明显差异,说明只要药物和载体辅料在熔融状态下充分混合均匀就能形成固体分散体,达到满意的增溶效果。故综合药物稳定性,选用混合温度为80℃。
2.2.5 冷却温度对溶出率的影响冷却温度考察范围设定为0、10、20℃;药物与载体比例为1∶2;混合温度为80℃。由图3可见,不同冷却温度对溶出率的影响较小,但仍能看出,冷却温度较低时溶出率较高,故选用冷却温度为0℃。
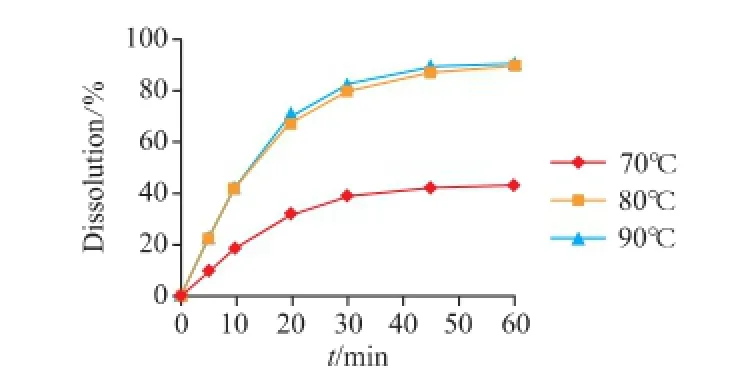
图2 混合温度对溶出率的影响
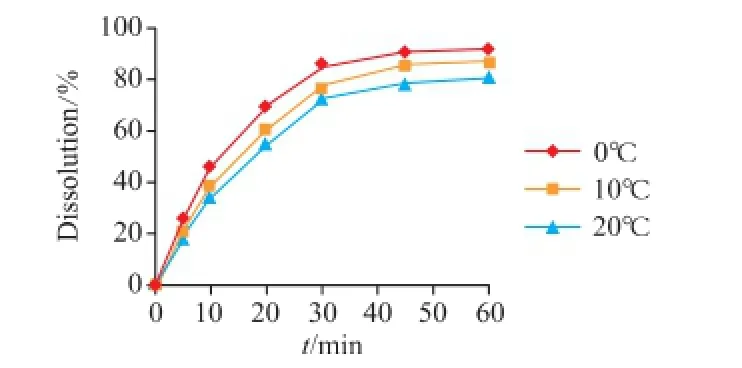
图3 冷却温度对溶出率的影响
2.2.6 药物和载体比例对溶出率的影响设定较宽范围考察药物和共聚维酮比例对溶出率的影响,考察比例为1∶1、1∶2、1∶3、1∶4;药物与共聚维酮的混合温度为80℃;冷却温度为0℃。

图4 药物和载体比例对溶出率的影响
从图4可以看出,在药物和载体比例达到1∶2已能达到较好的溶出效果,说明药物已经充分分散在载体辅料中。
2.3 药物和载体物理混合物与固体分散体溶出率的比较
2.3.1 非诺贝特样品的制备取非诺贝特,过80目筛,充填于1号胶囊,每粒含药100 mg。
2.3.2 物理混合物的制备称取非诺贝特和共聚维酮各20 g,用研钵研磨均匀,过80目筛,充填于1号胶囊,每粒含药100 mg。
2.3.3 固体分散体的制备称取非诺贝特和共聚维酮(S630)各20 g,熔融法制备固体分散体,工艺参数为混合温度80℃、冷却温度0℃、冷却时间30 min。取制得的固体分散体以研钵研细,过80目筛,充填于1号胶囊,每粒含药100 mg。
2.3.4 单药、物理混合物、固体分散体3种胶囊溶出百分率的比较制成固体分散体之后,非诺贝特在各个时间点的溶出百分率显著提高,明显优于机械混合物,证明了制备的产物是固体分散体。单药、物理混合物和固体分散体的溶出曲线见图5。

图5 非诺贝特单药、药物与载体物理混合物及非诺贝特固体分散体的3种胶囊溶出率
2.3.5 非诺贝特-共聚维酮(S630)固体分散体的熔点测定由图6可知,药物熔点峰在固体分散体图中已消失,提示药物以非晶态存在于载体共聚维酮(S630)中。
3 讨论
降低药物的结晶度、提高药物的亲水性,是提高难溶性结晶性化学药物溶出度的技术核心。而固体分散体技术正是将药物高度分散在载体中,处于分子状态,形成固态溶液,加速和增加难溶性药物的溶出,提高其生物利用度或延缓其释放的一种制剂技术;其提高或降低溶出率取决于载体的性质。如果载体是水溶性的,固体分散体就能提高溶出率;反之,如果载体是难溶性的,就能延缓和控制药物的释放。
本研究仅从体外溶出度角度证明了非诺贝特与共聚维酮(S630)形成固体分散体后其溶出百分率显著提高。在动物体内和人体内吸收程度即生物利用度的提高则是下一阶段的研究内容。
[1] 李满,满世伟,金丽丹.非诺贝特降脂特点[J].实用药物与临床,2005,(S1):35-6.
[2] Vogt M,Kunath K,Dressman JB.Dissolution enhancement of fenofibrate by micronization,cogrinding and spray-drying:comparison with commercial preparations [J].Eur J Pharm Biopharm,2008,68(2):283-8.
[3] Van den Mooter G.The use of amorphous solid dispersions:A formulation strategy to overcome poor solubility and dissolution rate[J].Drug Discov Today Technol,2012,9(2):e79-85.
Preparation of Solid Dispersion of Fenofibrate by Melting Method and Its Dissolution Rate
ZHANG Jing-jing1,WANG Shao-ping2
1Department of Pharmacy,Affiliated Nanjing Drum Tower Hospital of Nanjing University Medical College, Nanjing 210008;2Jiangsu Chia Tai Tianqing Pharmceutical Co.Ltd.,Nanjing 210023
Objective:To prepare solid dispersion of fenofibrate.Methods:Melting method was adopted to prepare solid dispersion.The influences of the ratio of the drug to carrier,mixing temperature and cooling temperature on the dissolution of drug were investigated.The differences among the dissolutions of fenofibrate,physical mixture and solid dispersion were explored.Results:When the ratio of the drug to carrier rose to 1∶2,the amount of the carrier was enough to distribute the drug evenly.Cooling temperature had little influence on the dissolution of drugs while mixing temperature had strong influence on the dissolution of drugs.Thein vitrotest showed that dissolution rate of the prepared solid dispersion was faster than that of fenofibrate and physical mixture.As compared with physical mixture,the dissolution rate of fenofibrate was significantly improved by solid dispersion.Conclusion:Solid dispersion with melting improves thein vitrodissolution rate of fenofibrate.
Fenofibrate;PVP-VA(S630);Solid dispersion;Dissolution rate
R943
A
1673-7806(2014)02-109-03
张晶晶,女,硕士,主管药师,研究方向:医院药学 E-mail:1658632781@qq.com
2013-10-22
2014-01-01
