中药艾迪注射液联合化疗药物治疗恶性胸水临床观察
2014-04-26钟安桥范红霞张凤花杜海莲
钟安桥,范红霞,王 磊,张凤花,杜海莲
(1.潍坊市益都中心医院 内科,山东 潍坊 26500;2.青州市中医院,山东 青州 262500)
中药艾迪注射液联合化疗药物治疗恶性胸水临床观察
钟安桥1,范红霞2,王 磊1,张凤花1,杜海莲1
(1.潍坊市益都中心医院 内科,山东 潍坊 26500;2.青州市中医院,山东 青州 262500)
目的:观察胸腔内注入中药艾迪注射液联合化疗药物治疗恶性胸水的临床疗效和安全性。方法:将58例恶性胸水确诊患者分为对照组(n=28)和观察组(n=30),观察组注入艾迪、顺铂及重组人血管内皮抑素,对照组采用艾迪、顺铂联用,每周1次,连用3周后评价近期疗效、安全性及生活质量。结果:治疗后,观察组治疗总有效率为86.7%,明显高于对照组的64.3%,比较差异有统计学意义(P<0.05);观察组生活质量改善率为93.3%,明显高于对照组的64.3%,比较差异有统计学意义(P<0.05);两组患者毒副反应差异无统计学意义(P>0.05)。结论:胸腔内注入中药艾迪注射液联合化疗药物治疗恶性胸水效果显著,无明显不良反应,值得临床推广应用。
中药艾迪注射液; 恶性胸腔积液;临床研究
艾迪注射液主要由斑蝥、人参、黄芪、刺五加等药物组成,具有抑制肿瘤血管新生、抗肿瘤及免疫调节等多靶点治疗功能。实验研究证明,黄芪具有促免疫作用,可加速淋巴细胞转化,增强细胞免疫功能,提高巨噬细胞及NK细胞活性。研究表明,人参、刺五加等可增强人体免疫力、提升白细胞功能。斑蝥素可抑制细胞合成期的DNA合成, 出现合成期与G2-M期阻滞现象, 诱导细胞凋亡。
恶性胸腔积液为晚期恶性肿瘤的常见并发症,严重影响了患者的生存质量,引起呼吸困难,同时患者预后较为困难。该病临床治疗较为困难,为提高患者的生存质量、改善呼吸困难症状,需对胸腔积液进行有效治疗。目前临床上以局部治疗为主,其中主要治疗手段为胸腔内灌注药物抑制恶性胸水生长,可迅速缓解患者症状,有助于提高患者生存质量。重组人血管内皮抑素为新的抗肿瘤药物,具有抑制新生血管的功能,从而抑制胸水的生长,临床以静脉滴注为主,胸腔内注入治疗较少。采用重组人血管内皮抑素联合艾迪、顺铂胸腔内注入治疗恶性胸水,临床效果显著,现具体报告如下。
1 资料与方法
1.1 临床资料
研究对象为肺癌合并大量胸腔积液患者,共58例,均经病理诊断或胸水细胞学检查确诊。其中男32例,女26例,年龄32~79岁,平均年龄55岁;病理类型:腺癌21例,鳞癌18例,小细胞癌15例,未分型4例;Ⅲa期22例,Ⅳ期36例。所有患者均有不同程度的呼吸困难、胸闷、气短、不能平卧等症状。患者无其它重要器官功能障碍,血常规、肝、肾功能及心脏功能基本正常,预计生存期3个月以上。
将所有患者随机分为两组,对照组28例,观察组30例。两组患者性别、年龄、病理类型等比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法
在超声下定位,明确穿刺部位和方向,患者取半卧位,采用单腔静脉导管行胸腔穿刺并置管,导管插入胸腔内6~8cm,导管固定敷帖于胸壁处,导管接引流袋,充分引流胸腔积液直至流尽,每日引流量不超过2 000mL。胸水基本排尽后,胸腔内注入药物治疗。
观察组注入顺铂40mg+恩度注射液30mg+艾迪60mL,对照组注入艾迪60mL+顺铂40mg。注药后嘱患者多次变更体位,保持药液与胸膜充分接触;胸腔内每周注药1次,3次为1疗程。所有患者用药期间均给予对症支持、止吐治疗。治疗前后查血常规,胸部超声,肝、肾功能,心电图。观察指标包括临床疗效、生活质量、不良反应等。
1.3 评价标准
1.3.1 疗效评价 根据世界卫生组织通用疗效评定标准,分为完全缓解、部分缓解、疾病稳定、疾病进展。其中完全缓解(CR):胸腔积液完全消失,持续4周以上;部分缓解(PR):胸腔积液较治疗前减少50%以上(以B 超检查所见积液最大深度为准),持续4周;疾病稳定(SD):胸腔积液较治疗前减少不足50%或增加不超过25%;疾病进展(PD):胸腔积液较治疗前增加超过25%以上。
临床有效率(RR)=(完全缓解+部分缓解)例数/总例数 ×100%
1.3.2 生活质量评定 参照卡氏功能状态评分标准(KPS)评分变化评价。改善:治疗后KPS评分增加10分;稳定:治疗后KPS评分没有增加;下降:治疗后KPS评分减少10分。
1.3.3 不良反应 参照美国国立癌症中心的常见毒性标准(NCI-CTC-AE 3.0 版)进行评价,分为0~4级。
2 结果
2.1 临床疗效比较
经治疗,对照组完全缓解10例、部分缓解8例、无效10例,总有效率64.3%;观察组完全缓解15例、部分缓解11例、无效4例,总有效率86.7%。观察组治疗效果明显高于对照组,比较差异有统计学意义(P<0.05)。
2.2 生活质量比较
对照组KPS评分改善11例,稳定7例,下降10例,改善率为64.3%;观察组KPS评分改善20例,稳定8例,下降2例,改善率为93.3%。观察组生活质量改善率明显高于对照组,比较差异有统计学意义(P<0.05)。
2.3 不良反应比较
患者主要不良反应为不同程度的血细胞减少和发热、胃肠道反应,均为轻度。两组患者均无明显心肌缺血症状,各出现2例轻微ST-T改变,无肝、肾功能损害,比较差异无统计学意义(P>0.05)。
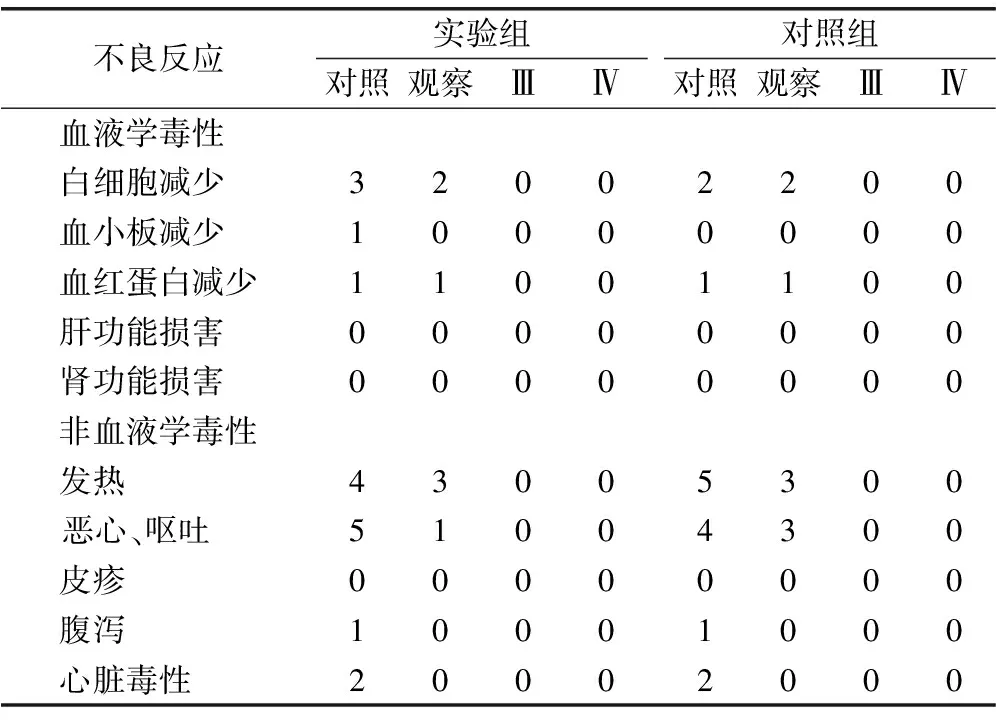
表1 两组患者不良反应比较 (n)
3 讨论
恶性肿瘤会侵犯胸膜引起难以控制的胸腔积液,常见于肺癌、乳腺癌和淋巴瘤,其中肺癌以非小细胞肺癌(NSCLC)最为常见,其次为乳腺癌[1]。恶性胸水的迅速生长常会引起一系列的临床症状,主要包括呼吸困难、咳嗽、腹胀、腹痛、恶心、呕吐、乏力、纳差及恶液质,若不予及时治疗,会导致患者在6个月内死亡。近年来,研究表明恶性胸水形成的主要机制包括:肿瘤直接侵犯浆膜血管致使毛细血管通透性增加;纵隔淋巴结肿大,导致淋巴回流受阻,水和蛋白吸收减少,潴留于胸腔[2];肿瘤引起新生血管形成,导致毛细血管内膜面积增加和血管通透性增高,且与肿瘤细胞产生的多肽(包括血管内皮生长因子(VEGF)和碱性成纤维细胞生长因子(bFGF)等)有关[3]。临床治疗恶性胸水主要采用水盐限制摄入、利尿治疗、化疗药物局部注射等手段,但易引起胃肠道反应、骨髓抑制、发热等毒副反应[4],效果不甚理想,且恶性胸腔积液疾病易复发,严重影响了患者的生活质量。
近年来,研究表明肿瘤细胞浸润或转移至体腔浆膜后,会引起局部VEGF水平升高、肿瘤新生血管生成及血管通透性增加等,这是导致浆膜腔内积液形成的重要机制。VEGF与其受体结合可导致血管内皮细胞分裂增殖、血管通透性增加和血浆蛋白外渗等,为浆膜腔积液形成提供了合适的微环境[5]。抑制VEGF的活性,可减少胸水的生成,因此VEGF成为治疗恶性胸水的作用靶点。血管内皮抑素(Endostatin,ES)为内源性抗血管因子,可特异性地作用于内皮细胞,尤其是微血管内皮细胞,可抑制内皮细胞迁移、增值及分化,诱导其凋亡,具有对抗VEGF、促新生血管形成及增加血管通透性的作用,从而抑制血管生长和肿瘤增生。此外,还可以通过调节肿瘤细胞VEGF的表达及蛋白水解酶活性多靶点抗血管的生成,间接导致肿瘤休眠或退缩[6-7]。体外及动物实验显示,ES具有高效的抑制血管内皮增殖和抗肿瘤作用,且未出现严重不良反应及耐药情况[8]。魏红梅等[9]研究发现,对VEGF的阻滞作用可明显减少恶性浆膜腔积液的形成。提示艾迪注射液具有免疫调节和抗癌的双重功效,可促进骨髓造血干细胞向粒—单核细胞分化,从而增加白细胞数量。
综上所述,采用胸腔内注入重组人血管内皮抑制素、艾迪、顺铂治疗恶性胸水疗效显著,可有效控制胸水生长,改善患者临床症状,提高生活质量,无明显不良反应,为恶性胸水治疗提供新的思路和方法,值得临床推广应用。
[1] 陈群, 石琴, 谢强,等.重组人血管内皮抑制素联合化疗治疗恶性浆膜腔积液的临床观察[J].临床肿瘤学杂志,2008,13(10):938.
[2] 骆益宙,钱建新,秦叔逵,等.恶性心包积液中血管内皮生长因子分泌水平的研究[J].临床肿瘤学杂志,2008,13(7):226.
[3] FOLKMAN J. Antiangiogenesis in cancer therapy endostatin and itsmechanisms ofaction[J].Exp Cell Res,2006,312(5):594-607.
[4] YOSHIDA K,SUGIURA T,TAKIFUJI N,et al.Randomized phaseⅡ trial of three intrapleural therapy regimens for the management of malignant pleural effusion in previously untreated non-small cell lung cancer:JCOG 9515[J].Lung Cancer,2007,58(3):362.
[5] ZHOU WB,BAI M,JIN Y.Diagnostic value of vascular endothelial growth factor and endostatin in malignant pleural effusions[J].Int J Tuberc Lung Dis,2009,13(3):381-386.
[6] 王金万,孙燕,刘永煜,等.重组人血管内皮抑素联合NP方案治疗晚期NSCLC随机、双盲、对照、多中心Ⅲ期临床研究[J].中国肺癌杂志,2005,8(4):283-290.
[7] 吴莹,赵敏,杨莉,等.内皮抑素基因治疗对癌性腹水抑制效应研究[J].四川大学学报:医学版,2004,35(3):316-319.
[8] 高文斌,吕金燕,王若雨.重组人血管内皮抑素的临床疗效及不良反应[J].药物不良反应杂志,2007,9(1):32-35.
[9] 魏红梅,秦叔逵,殷晓进,等.新型重组人血管内皮抑制素对小鼠腹水瘤的作用特点探讨[J].南方医科大学学报,2010,30(7):1509-1513.
[10] 刘晓兰, 陈家旭, 刘燕, 等. 去甲斑蝥素诱导HL60细胞凋亡的研究[J]. 北京中医大学学报,2003,23(4):35- 37.
(责任编辑:李岚春)
Recombinant Human Endostatin Combined Eddy and Cisplatin Intrathoracic InjectionClinical Observation for The Treatment of Malignant Pleural Effusion
Zhong Anqiao,Fan Hongxia,Wang Lei,Zhang Fenghua,Du Hailian
(1. Yidu Central Hospital Of Weifang city,Shangdong 265000,China;2.Traditional Chinese Medicine Hospital of Qingzhou City,Shangdong 265000,China)
Objective:To evaluate the efficacy and safety of Recombinant Human Endostatin combined eddy, cisplatin in the treatment of malignant pleural effusion by chest cavity injection.Methods:58 patients with diagnosis of malignant pleural effusion were divided into 2 groups,the patients in the research groupⅠwas treated only by injection eddy, cisplatin and those in groupⅡwere treated by injection eddy, cisplatin and Recombinant Human Endostatin,The above medicine was given one time every 7 days for 3 weeks, evaluate recent curative effect, safety and quality of life.Results:The total effective rate of two groups in the treatment of malignant pleural effusion control has statistically significant (P<0.05); Ⅱgroup of 20 patients with quality of life improved, stability of 8 cases, decline in 2 cases; Ⅰgroup life quality improvement in 11 cases, stability of 7 cases, decline in 10 cases, the difference of two groups was statistically significant (P<0.05); Two groups has no statistical significance of adverse reaction.Conclusion:Recombinant Human Endostatin combined eddy and cisplatin treatment of malignant pleural effusion curative effect is distinct, not to increase the side effects of chemotherapy, and worthy of clinical popularization and application.
Recombinant Human Endostatin; Malignant Pleural Effusion;Clinical Effects
2014-08-27
潍坊市卫生局中医药科研项目计划(2013-III-040)
钟安桥(1974-),男,山东省潍坊市益都中心医院主治医师,研究方向为COPD、肺癌、肺部介入医学。
R273
A
1673-2197(2014)20-0094-02
