舒眠胶囊辅助治疗抑郁症睡眠障碍的临床研究
2014-04-24焦歆益杨小龙张亚丽杨国周吕红波
焦歆益 杨小龙 张亚丽 杨国周 吕红波
·临床研究·
舒眠胶囊辅助治疗抑郁症睡眠障碍的临床研究
焦歆益 杨小龙 张亚丽 杨国周 吕红波
目的探讨中药制剂舒眠胶囊对抑郁症睡眠障碍者服用新型抗抑郁剂帕罗西汀1周后仍睡眠障碍者的疗效和安全性。方法将112例入选病历随机分为治疗组和对照组,治疗组给予帕罗西汀联合舒眠胶囊,对照组给予帕罗西汀单一治疗。治疗1、2、4周后采用汉密尔顿抑郁量表(HAMD-24)、匹兹堡睡眠质量指数量表(PSQI)评定疗效及不良反应量表(TESS)评价药品不良反应(ADR)。结果治疗4周后,2组HAMD减分均较明显,治疗组减分率为46.9%,对照组为47.3%,2组比较差异无统计学意义(χ2=2.82,P>0.05)。PSQI评分,治疗组有效率(89.47%)高于对照组(67.31%),2组比较差异无统计学意义(χ2=4.29,P<0.05);PSQI减分率:治疗组(4.75±1.81)与对照组(6.27±1.97)比较差异无统计学意义(t=4.92,P=0.000)。治疗组减分率71.82%高于对照减分率53.76%(χ2= 3.97,P<0.05)。结论帕罗西汀联合舒眠胶囊治疗抑郁症睡眠障碍优于单用帕罗西汀,且不增加ADR发生率,依从性好。
舒眠胶囊;帕罗西汀;抑郁症;睡眠障碍
研究发现睡眠障碍是抑郁症最常见的临床症状和生物学特征之一,甚至约62%的抑郁症患者首发症状表现为睡眠障碍[1]。抑郁症睡眠障碍主要表现为入睡困难、夜间多梦、早醒、醒后再入睡困难、睡眠感缺乏、晨起无新鲜感等多种形式,也少数患者有睡眠过多或嗜睡表现,其中早醒和睡眠感缺乏则被认为是抑郁症的特征性症状[2]。大约80%的抑郁症患者都有睡眠障碍的表现[3]。Tylee等研究发现,63%的抑郁症患者伴有夜间睡眠易醒或睡眠时间较正常减少[4]。Ohayon等[5]研究认为,约80%的住院患者、70%的门诊重度抑郁症患者有入睡和睡眠维持困难、早醒等症状。多项临床与流行病学研究提示睡眠障碍不仅是抑郁症的典型症状之一,相反从长期作用看睡眠障碍可能是抑郁症的独立风险因素,睡眠障碍和抑郁存在密切的双向联系[6]。国外一项Meta分析结果显示,睡眠障碍患者罹患抑郁症的发病风险是无失眠患者的2倍,且治疗睡眠障碍可减少人群抑郁症的发病率[7]。M c-Clintock[8]研究证实,患者抑郁症缓解或康复后仍有残留症状,而睡眠紊乱是最常见的残留症状之一。多项长期研究表明存在残留症状提示着抑郁症复发风险增高[9-10]。近年来抑郁症患者的睡眠障碍将成为研究者们关注的热点,对抑郁症患者的治疗不仅要改善抑郁症状,而且要迅速持久地改善失眠症状。因此,在治疗抑郁症的同时常常需要合并镇静催眠药物。目前临床上应用的镇静催眠药以苯二氮艹卓类占主导地位,而此类催眠药容易使患者产生依赖性和耐药性。所以具有宁心安神、镇静催眠作用的新型、不具依赖性的中成药越来越引起临床的关注。为了探讨中成药舒眠胶囊辅助治疗抑郁症睡眠障碍的疗效及安全性,故进行此项研究。
1 资料与方法
1.1 一般资料 选取我院2013年3月至2014年3月门诊或住院抑郁症患者112例,入选标准为:1)符合ICD-10抑郁症诊断标准且单一服用帕罗西汀(20~40 mg/d)1周后仍存在睡眠障碍者:汉密尔顿抑郁量表(HAMD)24项评分≥20分;匹兹堡睡眠指数(PSQI)总分≥8分;2)年龄18~60岁。排除标准:伴严重躯体疾病、脑器质性精神障碍及药物依赖患者;妊娠、哺乳期妇女及有严重自杀企图或行为的患者。在入组前告知患者及家属所用药物并签署知情同意书。112例患者按随机数字表随机分为2组,其中治疗组58例,完成实验57例、脱落1例,其中男性23例、女性34例;平均年龄(36.59±11.71)岁;平均病程(20.79±9.93)月,平均受教育年限(10.68±6.81)年;对照组54例,完成实验52例,脱落2例,其中男性21例、女性31例;平均年龄(35.01±12.28)岁;平均病程(19.79± 10.15)月,平均受教育年限(11.07±6.37)年。2组性别、年龄、病程等比较,差异无统计学意义(P>0.05)。
1.2 治疗方法 对参加研究的人员进行为期1周的培训,培训内容包括:入组标准 (研究对象)、研究方法、评定量表及评定标准、匹兹堡睡眠质量指数 (PSQI)、汉密尔顿抑郁量表(HAMD)、副反应量表(TESS)、国际精神与行为障碍分类(10版)(ICD-10)抑郁症诊断标准等。要求所有研究人员熟练掌握以上培训内容,并进行一致性检验Kapp值≈0.88,然后进行临床研究。2组均已服用1周的帕罗西汀20 mg/d仍存在睡眠障碍,对照组继续口服帕罗西汀 (葛兰素史克有限公司,20 mg/片)每早1片或早晚各1片。治疗组口服帕罗西汀 (葛兰素史克有限公司,20 mg/片)每早1片或早晚各1片,在此基础上加服舒眠胶囊 (贵州大隆药业有限公司,0.4 g/粒),3粒/次,2次/d,晚饭后及临睡前服用。安全性指标采用血常规、尿常规、肝肾功能、心电图等评价。
1.3 疗效判定标准 1)PSQI:PSQI是应用广泛的睡眠障碍评估量表之一,广泛用于精神疾病、躯体疾病伴发的睡眠障碍、原发性失眠及其他非临床研究[11]。PSQI由18个自评条目组成7个成分,分别为睡眠质量、入睡时间、睡眠时间、睡眠效率、睡眠障碍、催眠药物和日间功能障碍,每个成分按0~3等级计分,累计得分为PSQI总分。得分越高表示睡眠质量越差。PSQI由入组患者自我评定,不理解题意者由评定医师逐条念题,确定其听懂后由患者独立作出评定。分别于治疗前、治疗后第1、2、4周各评定1次。疗效依据PSQI的减分率判定,PSQI评分减分率≥80%为痊愈、79%~50%显著有效、49%~25%有效,<25%无效。2)HAMD:采用HAMD-24项版本评估抑郁程度并进行严重程度分级,分为7类因子结构,分级标准:8~19分为无抑郁,20~34分为轻度或中度抑郁,>35分重度抑郁。分别于治疗前、治疗后第1、2、4周各评定1次。3)ADR监测用TESS量表评定药品ADR,于治疗后第1、2、4周各测评1次,记录ADR发生情况。
1.4 统计学方法 采用SPSS 17.0软件进行数据分析,计量资料用 (均数±标准差)表示,组间比较采用χ2检验;组间比较釆用独立样本t检验。P<0.05为差异有统计学意义。
2 结果
2.1 2组治疗前后HAMD-24比较 组间治疗前及治疗1、2、4周后分别比较HAMD评分差异无统计学意义(P>0.05);2组治疗2、4周后分别与治疗前比较HAMD评分均有统计学意义(P<0.05)。见表1。
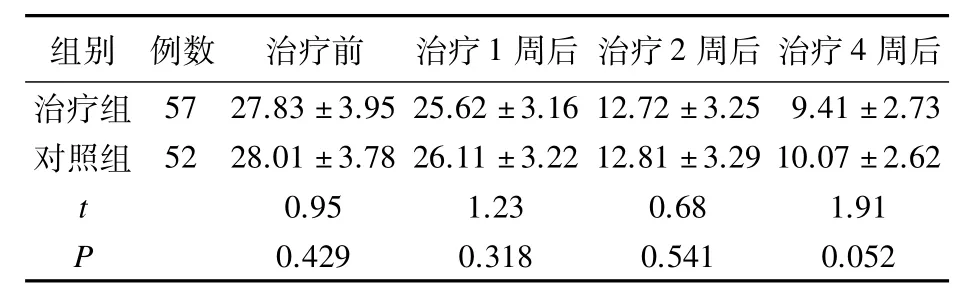
表1 2组患者治疗前后HAMD-24评分比较
2.2 2组治疗前后PSQI评分比较 2组间治疗前及治疗1周后PSQI评分无统计学意义(P>0.05)。治疗2、4周后,治疗组PSQI评分均低于对照组,差异有统计学意义 (P<0.05)。治疗组治疗2、4周后与治疗前比较PSQI评分均有统计学意义(P<0.05),对照组治疗4周后与治疗前比较PSQI评分有统计学意义(P<0.05)。2组治疗后PSQI评分均下降,但治疗组降幅明显优于对照组(P<0.05),见表2。
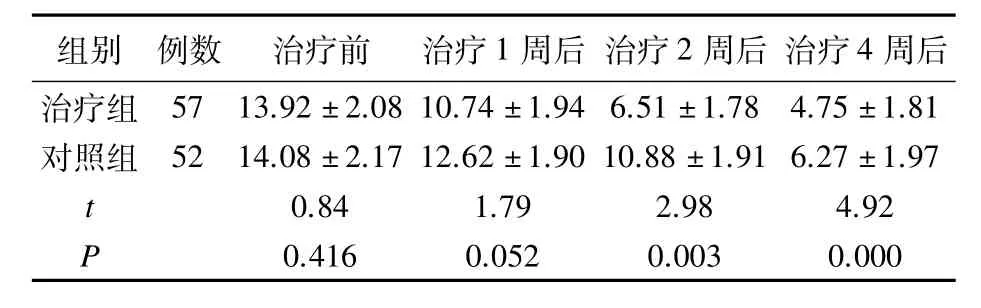
表2 2组治疗前后PSQI评分比较
2.3 2组临床疗效比较 治疗组有效率为89.47%,对照组为67.31%,2组比较差异有统计学意义(χ2=4.29,P<0.05)。治疗组减分率为71.82%,对照组为53.76%,2组比较差异有统计学意义(χ2=3.97,P<0.05),见表3。

表3 2组治疗后疗效比较[例(%)]
2.4 2组安全性比较 治疗组TESS评分为(2.67±1.64)分,对照组为(2.84±1.75)分,2组比较差异无统计学意义(t=0.47,P>0.05);治疗组恶心1例、厌食3例,对照组恶心1例、厌食2例,2组比较差异无统计学意义。治疗组嗜睡、头昏各2例,对照组嗜睡0例、头昏3例,2组比较差异无统计学意义;治疗组视力模糊1例,性功能障碍1例,对照组视力模糊0例,性功能障碍2例,2组比较差异均无统计学意义。
3 讨论
研究认为抑郁症患者中枢神经系统的唤醒作用增强。而使中枢神经系统唤醒作用增强的生物学改变,如去甲肾上腺素 (NE)及促肾上腺皮质激素释放因子活性过度等,可能是抑郁症睡眠障碍的发病机制。抑郁症REMS潜伏期缩短、慢波睡眠明显减少等特异性常可能与5羟色胺 (5-HT)/NE能神经传递减少或胆碱能传递增加有关[12]。不同类型抗抑郁药对睡眠的影响是不一样的,例如某些抗抑郁药物本身会引起药源性睡眠障碍,包括单胺氧化酶抑制剂、5-HT再摄取抑制剂等,这些药物可增加REMS潜伏期、抑制REMS,引起NREMS期的眼球运动,使夜间觉醒及夜间肢体活动增加,降低睡眠效率,缩短总的睡眠时间。
舒眠胶囊由酸枣仁、柴胡、白芍、合欢皮、合欢花、僵蚕、蝉蜕、灯心草组成。酸枣仁、柴胡具宁心安神、疏肝解郁之效;白芍、合欢皮、合欢花可柔肝养血、解郁安神;僵蚕祛风定惊、化痰散结;蝉衣散风除热、疏肝解痞;灯心草清上导下,引诸药归心,全方合奏宁心安神、疏肝解郁之效。舒眠胶囊调节CNS内5-HT化学神经递质含量,因而有效调节慢波睡眠和异常睡眠相的时间比,启动人体的主睡眠机制,使患者得到大脑皮层休息,又得到包括植物性功能在内的全身性休息。因此,舒眠胶囊具有较好的镇静、催眠和抗抑郁作用。本研究探讨舒眠胶囊联合新型抗抑郁药帕罗西汀治疗抑郁症睡眠障碍的临床疗效及不良反应,取得了较满意结果,治疗组在不增加ADR发生率情况下,通过宁心安神、改善睡眠而改善抑郁症状,且显著降低使用帕罗西汀产生的睡眠障碍发生率。因此认为,舒眠胶囊联合帕罗西汀治疗抑郁症睡眠障碍安全有效。提示在目前治疗抑郁症睡眠障碍中,为降低使用5-HT类抗抑郁药物所产生的睡眠障碍、避免合用苯二氮艹卓类所产生的耐药性及依赖性,可考虑与具有宁心安神、镇静催眠作用的中成药联用。
[1]Dennyttenaere K,BrufFaerts K,Posada-Villa,et al. Prevalence,severity and unmetneed for etreatmnt of mental disorders in the WHO World Mental Health surveys[J].JAMA,2004,291(12):2581-2590.
[2] 内山真.睡眠障碍诊疗指南[S].谭新,译.西安:第四军医大学出版社,2005:625-631.
[3]Arm itage R,Hoffmann RF.Sleep EEG,depression and gender[J].Sleep Med Rev,2001,5:237-246.
[4]Tylee A,Gastpar M,Lepine JR DEPRES II(Depression Research in European Society II):a patient survey of the symptoms,disability and current management of depression in the community[J].Intern Clin Psychopharm,1999,14(3):139-151.
[5]Ohayon MM,Shapiro CM.Sleep disturbances and psychiatric disorders associated with posttraumatic stress disorder in the general population[J].Compr Psychiatry,2000,41:469-478.
[6]Ohayon MM,Roth T.Place of chronic insomnia in the course of depressive and anxiety disorders[J].Psychiatric Res,2003,37(1):9-15.
[7]Baglioni C,Battagliese Q,Feige B,etal.Insomnia as a predictor of depression:a meta-analytic evaluation of longitudinal epidemiological studies[J].Affect Disord,2011,135(l-3):10-19.
[8]McClintock SM,Husain MM,W isniewski SR.Residual symptoms in depressed outpatients who respond by 50%but do not rem it to antidepressant medication[J].Clin Psychopharmacol,2011,31(2):180-186.
[9]Karp JF,Buysse DJ,Houck PR,et al.Relationship of variability in residual symptoms with recurrence of major depressive disorder during maintenance treatment[J].Am J Psychiatry,2004,161(10):1877-1884.
[10]Kanai T,Takeuchi H,Furukawa TA.Time to recurrence after recovery from major depressive episodes and its predictors[J].PsycholMed,2003,33(5):839 -845.
[11]肖卫东,刘平,马弘,等.睡眠障碍评定量表的信度和效度分析[J].中国心理卫生杂志,2007,21(1):40.
[12]高之旭.精神疾病的睡眠障碍及治疗[J].实用老年医学,2007,21(1):8-11.
Shumian capsule auxiliary treatment of the dep ression with sleep disorders control clinical study
Jiao Xinyi,Yang Xiaolong,Zhang Yali,Yang Guozhou,Lv Hongbo. The third hospital of Lanzhou Gansu Lanzhou 730050
ObjectiveTo explore the efficacy and safety of Shumian capsule preparation of traditional Chinesemedicine on depression sleep disorder take new antidepressant paroxetine remained after 1 weeks of sleep disorders.Methods112 cases ofmedical records were random ly divided into study group and control group,patients in study group
paroxetine joint Shumian capsule,the controlgroup was given the paroxetine single therapy.For1,2 and 4 weeks after using HAMD-24 and PSQI for efficacy and adverse TESS assessment of ADR.ResultsAfter4 weeks of treatment,two groups of HAMD reduction wasmore obvious,study group reduction rate was 46.9%,control group reduction rate was 47.3%,(χ2=2.82,P>0.05),two comparison results are sim ilar;The PSQIscore comparison of efficiency:the study group(89.47%)was significantly higher than that of the control group(67.31%)(χ2=4.29,P<0.05);Reduction rate comparison:the study group(4.75±1.81)reduction rate(71.82%)was significantly higher than that of the control group(6.27±1.97)reduction rate of 53.76%(χ2=3.97,P<0.05).In the two groups after treatment the incidence of ADR,there was no statistically significant difference(P>0.05).Conclusion Paroxetine combined Shumian capsule treating depression sleep disorders than single with paroxetine,and does not increase the incidence of ADR,and no addiction,good adherence.
Shum ian capsule;Paroxetine;Depression;Sleep disorders
兰州730050,甘肃省兰州市第三人民医院
吕红波,E-mail:hongbolv0308@126.com
