HPLC-MS/MS法测定大鼠血浆中麻黄碱、伪麻黄碱浓度及药动学研究*
2014-04-19欧阳慧子王兴蕊
窦 婷,欧阳慧子,王兴蕊,薄 芳,何 俊
(1.天津中医药大学中医药研究院,天津市现代中药重点实验室,天津 300193;2.天津中医药大学第一附属医院,天津 300193)
·中药研究·
HPLC-MS/MS法测定大鼠血浆中麻黄碱、伪麻黄碱浓度及药动学研究*
窦 婷1,欧阳慧子2,王兴蕊1,薄 芳1,何 俊1
(1.天津中医药大学中医药研究院,天津市现代中药重点实验室,天津 300193;2.天津中医药大学第一附属医院,天津 300193)
[目的]建立同时检测大鼠血浆中麻黄碱、伪麻黄碱的高效液相色谱-质谱联用法(HPLC-MS/MS),并对大鼠口服三拗汤后的麻黄碱、伪麻黄碱进行药代动力学研究。[方法]血浆样品经碱化和乙酸乙酯液-液萃取,以盐酸苯丙醇胺为内标,乙腈-0.1%甲酸水(4∶96)为流动相,经Agilent Zorbax SB-C18柱(4.6 mm×150 mm,5 μm)分离,采用电喷雾离子源(ESI),以多反应监测(MRM)模式进行正离子检测,定量分析的离子反应分别为:m/z 166.2→m/z 148.2(麻黄碱),m/z 166.2→m/z 148.2(伪麻黄碱)和m/z 152.1→m/z 134.1(盐酸苯丙醇胺)。[结果]麻黄碱和伪麻黄碱血药浓度在20~10 000 μg/L范围内线性关系良好,批内、批间精密度RSD均小于5.3%,高、中、低3种浓度平均方法回收率大于64.7%。[结论]该方法专属、快速、灵敏,可用于麻黄碱、伪麻黄碱的药代动力学研究。
麻黄碱;伪麻黄碱;药代动力学;三拗汤;液相色谱-质谱联用
三拗汤出自《太平惠民和剂局方》,由麻黄、杏仁和甘草3味药物组方,临床用于感冒风寒、咳嗽气喘[1-2]、痰多胸闷、头痛鼻塞等证。方中以麻黄为君,具有解表宣肺散寒的作用[3-5]。麻黄的成分主要含多种生物碱和少量挥发油,其中生物碱类以麻黄碱与伪麻黄碱为主。近年来关于麻黄碱与伪麻黄碱的含量测定方法多为毛细管电泳法[6-10]、高效液相色谱法[11-15]、气相色谱法和气-质联用方法[16-18]。毛细管电泳法稳定性和重现性较差[19];高效液相色谱法灵敏度低;气相色谱法和气-质联用方法样品需要衍生化,较复杂。本文建立了同时测定大鼠血浆中麻黄碱、伪麻黄碱血药浓度的高效液相色谱-质谱联用法(HPLC-MS/MS),并将此方法应用于大鼠灌服三拗汤后麻黄碱和伪麻黄碱的药代动力学研究。
1 仪器与材料
1.1 仪器 API 3200型串联三重四级杆质谱仪(美国AB公司),配备电喷雾离子源;Agilent 1200型高效液相色谱仪(美国Agilent公司),Analyst Software数据处理系统(美国AB公司),梅特勒-托利多AX 205分析天平(瑞士Mettler Toledo公司),超纯水系统(Millipore公司)。
1.2 药品与试剂 盐酸麻黄碱、盐酸伪麻黄碱、盐酸苯丙醇胺均购自中国药品生物制品检定所,乙腈(Fisher Scientific)、甲醇(TEDIA)、甲酸(天津市光复化工研究所)均为色谱纯,碳酸钠(天津化学试剂一厂)、乙酸乙酯(天津凯信化学工业有限公司)均为分析纯,水为Millipore超纯水。
1.3 实验动物 SD大鼠,雄性,体质量200~230 g,购自北京维通利华实验动物技术有限公司(合格证编号0163041)。
2 方法与结果
2.1 色谱条件 色谱柱:Agilent Zorbax SB-C18柱(4.6 mm×150 mm,5 μm),保护柱:Agilent Zorbax C18柱(4.6 mm×12.5 mm,5 μm),流动相:乙腈-0.1%甲酸水(4∶96),流速:0.4 mL/min,柱温:25℃。
2.2 质谱条件 离子源为ESI源;帘气Curtain Gas为15 psi;碰撞气Collision Gas为5 psi;源喷射电压Ion Spray Voltage为4 500 V;雾化器GS1为40 psi、加热器GS2为60psi;正离子方式检测,扫描方式为多反应离子监测;定量分析时的离子反应分别为m/z 166.2→m/z 148.2(麻黄碱),m/z 166.2→m/z 148.2(伪麻黄碱)和m/z 152.1→m/z 134.1(盐酸苯丙醇胺)。
2.3 溶液的制备
2.3.1 标准溶液的制备 精密称取麻黄碱、伪麻黄碱各10 mg分别置于25 mL容量瓶,加甲醇定容至刻度,摇匀,即得储备液。量取一定量的麻黄碱、伪麻黄碱储备液混合,用纯水稀释为10 mg/L的工作液,-20℃冰箱储存备用。
2.3.2 内标溶液的制备 精密称取盐酸苯丙醇胺标准品10 mg,置于25 mL容量瓶,加甲醇定容至刻度,摇匀,即得储备液。量取一定量的盐酸苯丙醇胺储备液,用纯水稀释500 ng/mL的工作液,-20℃冰箱储存备用。
2.3.3 供试品溶液的制备 取麻黄9 g,苦杏仁9 g,甘草9g,加水220mL,煎煮60min,滤出药液,再加水160 mL,煎煮60 min,合并药液,于-20℃储存备用。
2.4 血浆样品预处理 精密吸取血浆样品100 μL,加入纯水100 μL,500 μg/L内标溶液100 μL,0.1mol/L碳酸钠溶液100 μL,涡旋30 s,再加入乙酸乙酯800 μL,涡旋2 min,4 000 r/min离心5 min,取上清液650 μL,40℃水浴氮气吹干,100 μL甲醇复溶,超声1 min,13 000 r/min离心5 min,取上清液10 μL进行HPLCMS/MS分析。
2.5 方法学考察
2.5.1 方法专属性 取大鼠的空白血浆100 μL,按“2.4”项下方法操作,获得大鼠空白血浆样品色谱图1A;将一定浓度的混合对照品溶液和内标溶液加入至空白血浆中,依同法操作,得色谱图1B;取大鼠给药后的血浆样品,同法操作,得色谱图1C。其中麻黄碱、伪麻黄碱和内标盐酸苯丙醇胺的保留时间分别为6.04、6.85、3.88 min。结果表明,血浆中内源性成分不干扰麻黄碱、伪麻黄碱和内标的测定,结果见图1。

图1 麻黄碱、伪麻黄碱和盐酸苯丙醇胺HPLC-MS/MS谱图
2.5.2 标准曲线、线性范围及定量限 取大鼠空白血浆100 μL,精密加入不同量的混合工作液,配制麻黄碱、伪麻黄碱终浓度为10 000、5 000、1 000、500、100、50、20 μg/L的血浆样品,按“2.4”项下进行处理与测定,记录待测物峰面积和内标峰面积,利用待测物峰面积和内标峰面积比对样品血药浓度进行线性回归,用加权(1/X2)最小二乘法进行回归运算,得麻黄碱的线性回归方程为Y=0.001 46X+0.113,r=0.993 4,伪麻黄碱的线性回归方程为Y= 0.001 73X+0.048 7,r=0.992 9,麻黄碱和伪麻黄碱的线性范围均为20~10 000 μg/L,以S/N≥10为最低定量限,S/N≥3为最低检测限,测得麻黄碱、伪麻黄碱最低定量限为10 μg/L,最低检测限为1 μg/L。
2.5.3 基质效应 取大鼠空白血浆,按“2.4”项下进行处理得空白基质残渣,精密加入一定浓度的麻黄碱、伪麻黄碱工作液,配制成各待测物终浓度分别为50、1 000、10 000 μg/L的血浆样品,测定各待测物峰面积(A1)。另取上述等量的3个浓度的麻黄碱、伪麻黄碱工作液与水配制成各待测物终浓度为50、1 000、10 000 μg/mL的对照样品,同法操作,测得各待测物峰面积(A0),每个浓度平行操作3份。按基质效应=A1/A0计算,得麻黄碱、伪麻黄碱低、中、高3个浓度的基质效应介于95.6%~102.1%,内标基质效应为98.3%,RSD值为4.2%。表明本方法可有效地避免大鼠血浆中的基质效应。
2.5.4 精密度和回收率实验 取大鼠空白血浆,精密加入一定浓度的麻黄碱、伪麻黄碱工作液,配制麻黄碱、伪麻黄碱的终浓度分别为50、1 000、10 000 μg/L的低、中、高质控样品,按“2.4”项下处理与测定,测得麻黄碱、伪麻黄碱峰面积(Ae)。取上述3个浓度的麻黄碱、伪麻黄碱混合对照品溶液未经提取直接进样测定,测得麻黄碱、伪麻黄碱峰面积(Ac),每个浓度平行操作5份,按Ae/Ac计算回收率,回收率介于64.7%~76.4%;每个浓度平行操作5份,连续测定3 d,计算批内、批间的精密度,得精密度RSD值小于5.3%。结果见表1。
2.5.5 稳定性考察 取空白血浆100 μL,精密加入一定浓度的麻黄碱、伪麻黄碱工作液,配制成各待测物终浓度分别为50、1 000、10 000 ng/mL的血浆样品,分别考察其在室温放置0、12、24 h,-20℃冷冻0、3、7 d和反复冻融3次的稳定性。将测定的峰面积比代入标准曲线,计算质控样品血浆实测值之间的相对差异,在上述条件下麻黄碱稳定性RSD值0.6%~6.4%;伪麻黄碱稳定性RSD值1.3%~5.9%,结果表明,麻黄碱和伪麻黄碱在室温放置、长期冷冻和冻融循环条件下均稳定。
表1 麻黄碱和伪麻黄碱在大鼠血浆中的回收率及精密度(±s,n=5)
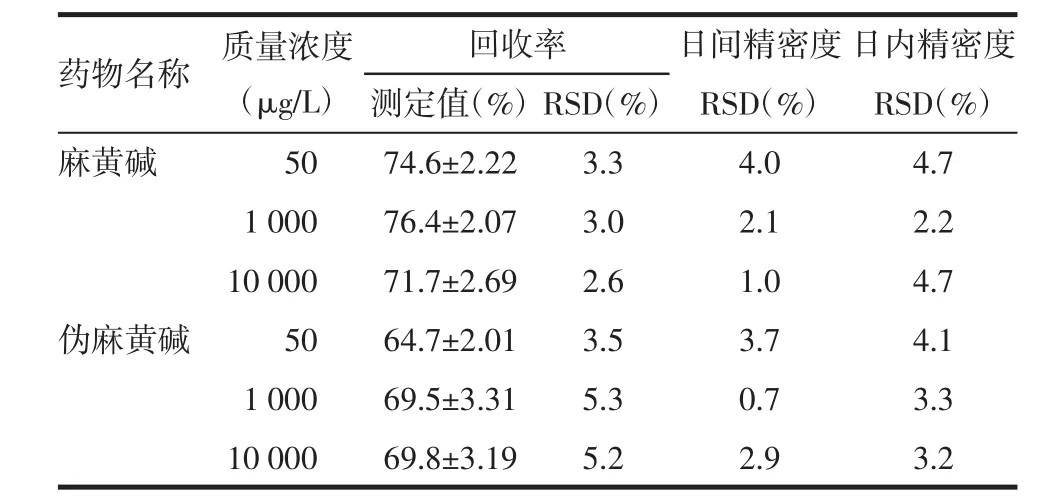
表1 麻黄碱和伪麻黄碱在大鼠血浆中的回收率及精密度(±s,n=5)
回收率测定值(%)RSD(%) RSD(%) RSD(%)麻黄碱 50 74.6±2.22 3.3 4.0 4.7 1 000 76.4±2.07 3.0 2.1 2.2 10 000 71.7±2.69 2.6 1.0 4.7伪麻黄碱 50 64.7±2.01 3.5 3.7 4.1 1 000 69.5±3.31 5.3 0.7 3.3 10 000 69.8±3.19 5.2 2.9 3.2药物名称 质量浓度(μg/L)日间精密度日内精密度
2.6 药动学研究 雄性SD大鼠8只,体质量200~ 230 g,禁食12 h,自由饮水。将供试品溶液按9 mL/kg灌胃给药,分别于给药前及给药后0.25、0.5、0.75、1、1.5、2、3、4、6、8、10、12、24 h经眼球后静脉丛取血0.3 mL,置于经肝素处理的干燥离心管中,4 000 r/min离心10 min,取血浆0.1 mL用于处理、分析,测得麻黄碱、伪麻黄碱平均血药浓度-时间曲线,见图2。采用DAS软件进行房室模型拟合,结果表明各组中麻黄碱、伪麻黄碱在大鼠体内呈一室模型,同时计算大鼠单次口服三拗汤后麻黄碱、伪麻黄碱的主要药动学参数,结果见表2。
3 讨论
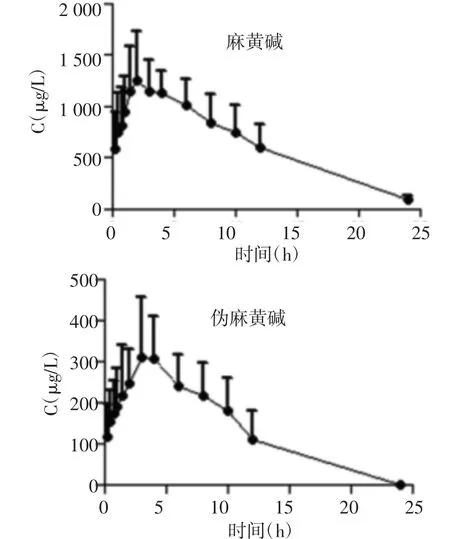
图2 大鼠单次灌服三拗汤后麻黄碱、伪麻黄碱血药浓度-时间曲线图(n=8)
麻黄碱和伪麻黄碱互为旋光异构体,为确保较好的分离效果且不受血浆中内源性物质的干扰,实验以乙腈-甲酸水为流动相,考察了不同比例和pH对质谱响应的影响,最终确定流动相比例为乙腈-0.1%甲酸水(4∶96),在该色谱条件下可同时测定麻黄碱和伪麻黄碱且分离效果良好。实验同时考察了在流动相中加入不同量的甲酸氨对质谱响应的影响,结果表明流动相中的甲酸氨对离子响应影响不大。
表2 大鼠灌服三拗汤后麻黄碱、伪麻黄碱主要药动学参数(±s,n=8)
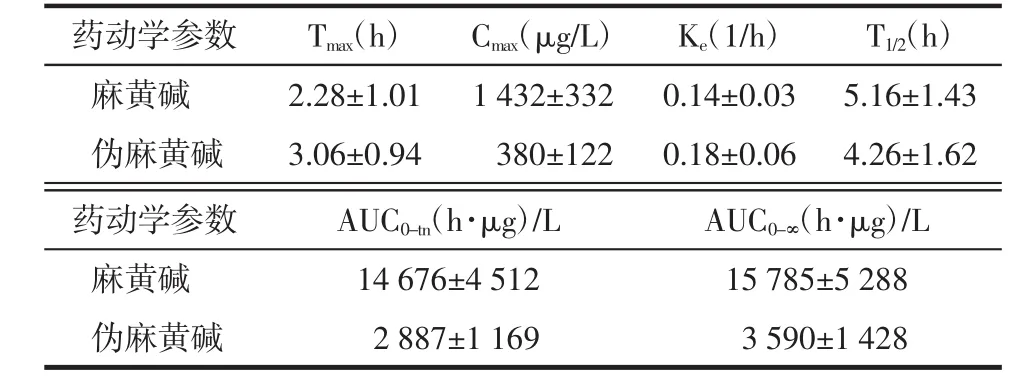
表2 大鼠灌服三拗汤后麻黄碱、伪麻黄碱主要药动学参数(±s,n=8)
药动学参数 Tmax(h) Cmax(μg/L) Ke(1/h) T1/2(h)麻黄碱 2.28±1.01 1 432±332 0.14±0.03 5.16±1.43伪麻黄碱 3.06±0.94 380±122 0.18±0.06 4.26±1.62药动学参数 AUC0-tn(h·μg)/L AUC0-∞(h·μg)/L麻黄碱 14 676±4 512 15 785±5 288伪麻黄碱 2 887±1 169 3 590±1 428
通过对血浆预处理方法的考察,发现固相萃取法(SPE)回收率较低,成本较高,蛋白沉淀法(PPT)会产生严重的基质效应。本实验最终采用液-液萃取法(LEE)对麻黄生物碱的血浆样本进行处理,且对不同的萃取溶剂乙酸乙酯、乙醚、氯仿、正己烷-二氯甲烷-异丙醇等进行考察,结果发现乙酸乙酯萃取后血浆内源性物质对麻黄碱及伪麻黄碱的测定影响最小,且提取回收率较其他溶剂无明显差异。同时还考察了氢氧化钠和碳酸钠溶液碱化血浆样品的影响,结果发现用氢氧化钠作碱化液时提取回收率不稳定,采用最小浓度为0.1 mol/L的碳酸钠溶液作碱化液时提取回收率较稳定。
[1] 徐士伟.感冒后咳嗽临证治验[J].天津中医药,2011,28(2): 133-134.
[2]魏慧利,于文涛.杨牧祥教授治疗支气管哮喘的临床经验[J].天津中医药,2011,28(2):93-94.
[3]阎丽娟,李媛媛,陈爽白.浅谈麻黄的功效[J].天津中医药, 2011,28(4):317-319.
[4] 陈 慧.三拗汤加减治疗小儿寒饮停肺型哮喘临床观察[J].天津中医药,2006,23(1):29-30.
[5]刘恩顺,孙曾涛.麻芩咳喘合剂对支气管哮喘治疗效果及炎性物质的影响[J].天津中医药,2007,24(1):452-455.
[6]马永钧,李琼琳,王伟峰,等.毛细管电泳-电致化学发光法分离测定麻黄中的麻黄碱、伪麻黄碱与甲基麻黄碱[J].分析测试学报,2012,31(2):127-132.
[7]俞励平,王晓可,罗佳波.毛细管电泳法测定麻杏石甘汤中盐酸麻黄碱、盐酸伪麻黄碱和盐酸甲基麻黄碱的含量[J].中药材,2011,34(4):620-623.
[8]徐 静,李 军,胡 强,等.毛细管电泳/发光二极管诱导荧光法测定麻黄中麻黄碱伪麻黄碱含量[J].分析测试学报,2012,31(8):977-981.
[9]孙国祥,孙丽娜.毛细管区带电泳法测定麻黄中麻黄碱和伪麻黄碱的含量[J].中南药学,2009,7(10):773-776.
[10]丁佳佳,李征征,宋粉云.毛细管电泳法测定千柏鼻炎片中盐酸麻黄碱%盐酸伪麻黄碱和盐酸甲基麻黄碱的含量[J].中国实验方剂学杂志,2012,18(10):120-123.
[11]Makino Y.Simple HPLC method for detection of trace ephedrine and pseudoephedrine in high-purity methamphetamine[J].Biomed Chromatogr,2012,26(3):327-330.
[12]张志鹏,朱胜山,李苑山,等.大鼠血浆中麻黄碱伪麻黄碱含量的高效液相色谱测定[J].时珍国医国药,2012,23 (8):1878-1880.
[13]张建军,欧丽娜,李 伟,等.小青龙颗粒中麻黄碱及伪麻黄碱在大鼠体内的药代动力学研究[J].中华中医药杂志,2012,25(12):1991-1995.
[14]葛 斌,罗燕梅,徐爱霞,等.HPLC测定麻黄药材中麻黄碱与伪麻黄碱的含量[J].中华中医药杂志,2008,43(3): 173-175.
[15]张 俐,王 玉.高效液相色谱法测定鼻炎康片中麻黄碱和伪麻黄碱的含量[J].中南药学,2013,10(11):761-764.
[16]贺 丰,罗佳波,陈飞龙,等.GC-MS法研究麻黄汤中麻黄碱伪麻黄碱的人体内过程[J].中药新药与临床药理,2004, 15(5):336-347.
[17]李吉来,陈飞龙,刘传明,等.麻黄汤中麻黄碱与伪麻黄碱的GC-MS法测定及配伍因素对汤剂中该成分含量的影响[J].中草药,2002,33(4):21-23.
[18]赵 婕,邵 兵,孟 娟,等.气相色谱-质谱测定保健食品中的麻黄碱和伪麻黄碱[J].色谱,2004,22(2):188.
[19]吕 霞,郭 青,钟文英.色谱法在麻黄生物碱手性分析中的研究进展[J].现代药物与临床,2011,26(3):181-187.
Simultaneous determination of ephedrine and pseudoephedrine in rat’plasma and their pharmacokinetics determined by LC-MS/MS
DOU Ting1,OUYANG Hui-zi2,WANG Xing-Rui1,BO Fang1,HE Jun1
(1.Tianjin State Key Laboratory of Modern Chinese Medicine,Institute of Traditional Chinese Medicine,Tianjin University of Traditional Chinese Medicine,Tianjin 300193,China;2.The First Affiliated Hospital of Tianjin University of Traditional Chinese Medicine,Tianjin 300193,China)
[Objective]To develop a LC-MS/MS method for the determination of ephedrine and pseudoephedrine in rat’s plasma simultaneously and to study the pharmacokinetics of ephedrine and pseudoephedrine of rat’s plasma after oral administration of SD(Sanao Decoction).[Methods]The blood plasma samples were extracted through alkali and ethyl acetate liquid-liquid.Phenylalanine hydrochloride was used as the internal standard.Separation was performed using an Agilent Zorbax SB-C18(4.6 mm×150 mm,5 μm).The analytical column was acetonitrile-0.1%formic acid in water solution(4:96).Electrospray ionization(ESI)source was applied and operated in the positive ion mode.Multiple reaction monitoring(MRM)mode with the transitions of m/z 166.2→m/z 148.2,m/z 166.2→m/z 148.2 and m/z 152.1→m/z 134.1 were used to quantify ephedrine,pseudoephedrine and phenylalanine hydrochloride,respectively.[Results]The linearity ranged from 20 to 10 000 μg/L.RSD for inter-match and intra-match were not more than 5.3%and the average extracted recovery for all the high,middle and low concentration was more than 64.7%.[Conclusion]The analytical method is proved to be special,sensitive,rapid and suitable for the pharmacokinetic study of ephedrine and pseudoephedrine.
ephedrine;pseudoephedrine;pharmacokinetic;Sanao decoction;LC-MS/MS
R285.5
:A
:1673-9043(2014)06-0355-04
2014-08-14)
10.11656/j.issn.1673-9043.2014.06.10
高等学校博士学科点专项科研基金项目(20131210 120015);天津市高等学校科技发展基金计划项目(20110212)。
窦 婷(1989-),女,硕士研究生,主要研究方向为药物分析。
何 俊,E-mail:hejun673@163.com。
