应用A型肉毒毒素治疗特发性偏侧面肌痉挛现状研究
2014-04-01王琳胡兴越董红娟王文昭黄月靳令经骆裕民张为西连亚军梁战华商慧芳冯亚波吴逸雯陈俊罗蔚锋万新华
王琳 胡兴越 董红娟 王文昭 黄月 靳令经 骆裕民 张为西 连亚军梁战华 商慧芳 冯亚波 吴逸雯 陈俊 罗蔚锋 万新华
特发性偏侧面肌痉挛是以一侧面部肌肉阵发性不自主抽动为特点的面神经病变。在大多数此病患者,眼轮匝肌是最初受累部位,随后病变逐渐播散至同侧面部的其他肌肉。特发性偏侧面肌痉挛一般不会危及生命,但可能影响面部肌肉功能,而且鲜有自发缓解,对患者的工作、生活和社会交往造成一定的影响,绝大多数患者有治疗的需要。国际上主要的治疗方法有口服药、A型肉毒毒素(botulinum toxin type A,BTX-A)局部注射和手术治疗,而在国内,大多数患者更倾向于采取非手术治疗,除了口服药和BTX-A,还包括针灸以及应用酒精进行神经阻滞的方法。 目前我国应用的BTX-A有两种,即兰州生物制品研究所生产的衡力(CBTX-A)和美国爱力根公司生产的保妥适(BOTOX)。本文作者对全国15个运动障碍病中心门诊就诊的特发性偏侧面肌痉挛患者进行较为全面的调查,目的在于全面了解我国应用BTX-A治疗特发性偏侧面肌痉挛的治疗现状,分析不同BTX-A的疗效和不良反应,期望对推动临床治疗该病的规范化有所帮助。
1 对象和方法
1.1观察对象收集2012-03-01-2012-08-31期间,全国15个运动障碍病中心门诊就诊的特发性偏侧面肌痉挛患者1033例患者,包括北京协和医院228例、浙江大学邵逸夫医院192例、湖北省人民医院120例、上海长征医院41例、河南省人民医院56例、上海同济医院40例、西安市中心医院40例、中山大学附属第一医院40例、郑州大学附属第一医院40例、大连医科大学附属第一医院40例、四川大学华西医院40例、山东省立医院40例、上海瑞金医院39例、南京脑科医院37例及苏州大学附属第二医院40例,其中资料完整的有效病例1003例。入选标准:临床诊断为特发性偏侧面肌痉挛[1],患者自愿参与调查并签署知情同意书。
排除标准:(1)继发性偏侧面肌痉挛:脑桥小脑脚肿瘤或手术、面神经炎、面神经损伤等;(2)其他原因的面部不自主运动:各种原因的面瘫后联合运动、抽动症、面部纤维搐颤及癫痫局限性运动发作;(3)因认知障碍、精神疾病无法配合完成本调查。
1.2方法所有观察对象均完成面肌痉挛临床特点及治疗选择调查问卷的填写。调查问卷的内容包括患者基本资料、起病部位、病程、曾经接受的治疗方法、不同治疗方法的疗效及不良反应等内容。由神经科医生评定患者的病变部位和病情严重程度。BTX-A的治疗情况来自于每个运动障碍病中心既往的医疗记录和调查问卷。这项研究得到北京协和医院和各家参与医院的伦理委员会批准,每位患者在接受调查前均签署书面的知情同意书。
患者病情严重程度采用Cohen评分方法[2]进行评定。1级:外部刺激引起瞬目增多或面肌轻度颤动;2级:眼睑、面肌自发轻微颤动,无功能障碍;3级:痉挛明显,有轻微功能障碍;4级:严重痉挛和功能障碍。
1.3统计学处理数据分析应用SPSS V20.0软件。计量资料符合正态分布者用均数±标准差表示,不符合正态分布者用中位数(上、下四分位数)表示。计数资料用百分比表示(%)。衡力和保妥适剂量、起效时间、疗效持续时间比较采用u检验,不良反应持续时间比较采用Mann-WhitneyU检验。最佳疗效和不良反应的发生率比较采用χ2检验或Fisher确切检验。以P<0.05为差异有统计学意义。对30例数据不完整的临床资料未予统计。
2 结果
2.1临床特点在1003例有效病例中,男360例、女643例,男∶女之比1∶1.8。起病年龄15~92岁,平均(46.6±11.5)岁。起病高峰在41~50岁,病程0~49年,中位病程6.0(3.0,10.0)年。按照病情严重度分级,1级23例(2.3%),2级145例(14.5%),3级558例(55.6%),4级277例(27.6%)。
2.2治疗患者的治疗目的主要为痉挛消失934例(93.1%),功能改善492例(49.1%),美观281例(28.0%)。多数患者接受过多种治疗,其中BTX-A注射的比例最高,共有665例,占全部患者的66.3%,其次为针灸治疗628例(62.6%)、口服药治疗513例(51.1%),曾接受过酒精阻滞治疗患者仅有21例(2.1%)。有24例(2.4%)接受过手术治疗,因无效(15例)或复发(9例)转而寻求非手术治疗。
在非手术治疗方法中,BTX-A重复治疗的比例最高,达68.7%。在停用BTX-A的患者中,最常见的停用原因是复发,占停用原因的98.6%。重复治疗比例最低的是针灸,98.4%的患者放弃治疗。停用针灸治疗的主要原因是疗效差,占97.6%。长期口服药治疗的患者只占全部患者的3.1%,其中最常用的药物是卡马西平,占口服药治疗人数的45.8%,其次是B族维生素,占36.8%,其他药物还包括巴氯芬、硫必利、苯海索、氯硝西泮和多种中成药等,所占比例均在3.5%以下。停用卡马西平的主要原因是疗效差,占停药患者的85.0%,其次是不良反应,占13.2%。停用其他药物的原因均为疗效差。
2.3BTX-A治疗BTX-A的治疗疗效见表1,不良反应见表2。
在曾经接受BTX-A治疗的665例患者中,最近1次应用保妥适治疗的患者123例,应用衡力治疗的患者542例。应用BTX-A总剂量10~100 u,起效时间1~30 d,中位数4(2,7) d,平均5.0 d,疗效持续时间2~128周,中位数16(12,24)周,平均19.5周。总有效率98.9%,有95.9%患者偏侧面肌痉挛的严重度和功能中度以上改善,58.2%患者显著改善。其中保妥适的平均应用剂量多于衡力(分别为45.2 u与41.6 u,P=0.01),保妥适的起效时间较衡力长(分别为6.2 d与5.1 d,P=0.023),保妥适的疗效持续时间长于衡力(分别为23.5周与18.6周,P<0.001),二者在总有效率、中度以上改善率和显著改善率方面的差异无统计学意义。
在不良反应中,最常见的是口角歪斜146例(22.0%),其次为闭眼无力101例(15.2%)、流泪48(7.2%)。其他常见的不良反应如上睑下垂、局部水肿等相对少见。其中应用保妥适的患者出现口角歪斜和流泪的比例低于衡力(10.6%与24.5%,P=0.001;2.4%与8.3%,P=0.023),其他不良反应的发生率和所有不良反应的持续时间差异无统计学意义(表2)。所有不良反应均未经处理即自行缓解。
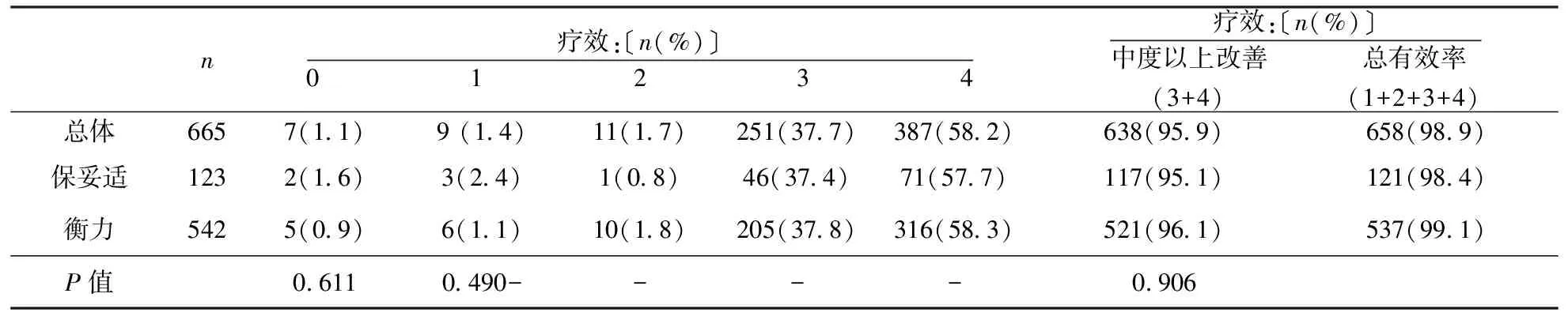
表 1 BTX-A治疗疗效评价
注:0:无效;1:严重度轻度改善;2:严重度中度改善,无功能改善;3:严重度及功能中度改善;4:严重度及功能显著改善;表中P值为保妥适与衡力的相应指标比较所得;“-”未比较
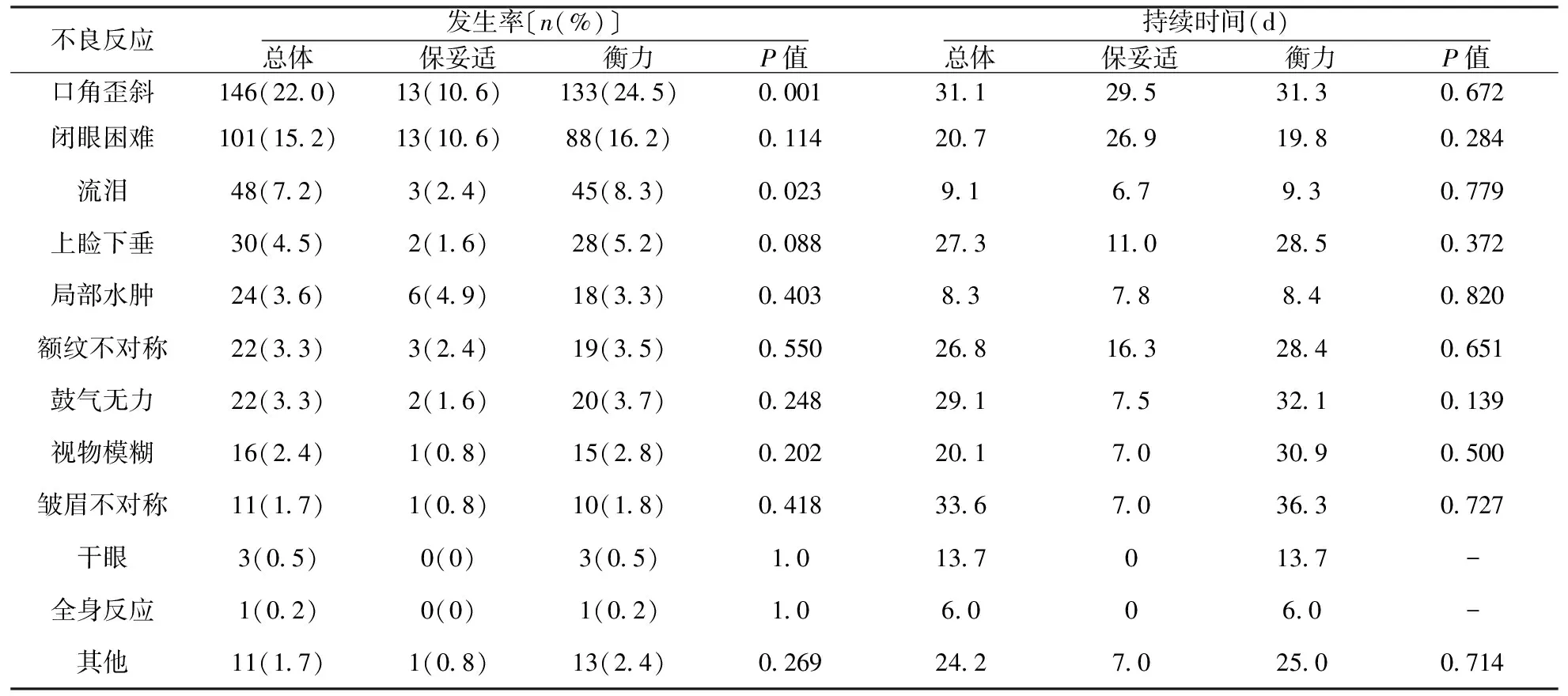
表 2 BTX-A治疗的常见不良反应情况
注:表中P值为保妥适与衡力的相应指标比较所得;患者总例数665,其中保妥适123例,衡力542例;“-”未比较
3 讨论
1947年Campbell最早提出面神经在出脑干的部位受异常血管压迫可能是特发性面肌痉挛的病因,在此基础上发展起来的微血管减压术已成为一种有效的治疗特发性偏侧面肌痉挛的方法,小脑前下动脉、小脑后下动脉、椎动脉是最常见的责任血管[3]。随着对疾病认识的深入和手术方式的改进,目前微血管减压术对特发性偏侧面肌痉挛的治愈率可以达到82%~92%[4-5],手术并发症主要包括复发、脑神经和血管损伤等,部分患者手术治疗无效。
在我国,基于对手术及其并发症的担心,多数特发性偏侧面肌痉挛患者倾向于选择非手术治疗,主要包括口服药、针灸、BTX-A注射、应用酒精进行神经阻滞等。本项研究显示前3种治疗方法的应用更为广泛,与其操作简便、安全性高、患者易于接受有关。其中卡马西平是应用最多的口服药,对部分轻症患者疗效尚可,少数患者长期应用,但是不良反应较大,一部分患者因此停药。针灸是我国特有的治疗方法,但对特发性偏侧面肌痉挛的疗效欠佳,研究显示绝大多数患者因疗效差放弃继续治疗。患者常因疾病复发停用原治疗方法,本研究中BTX-A重复治疗的比例最高(68.7%),提示BTX-A疗效确切,得到了多数患者认可。肉毒毒素注射在我国已成为一项成熟稳定的治疗手段,其平均起效时间、疗效持续时间和中度以上疗效改善的情况与文献报道相当[6]。
BTX-A治疗的不良反应总体上可以分为4类:(1)药物直接作用导致注射肌肉无力,如闭目无力、双侧的额纹、眉间纹、鼻唇沟不对称等,在BTX-A治疗中难以完全避免;(2)药物的弥散作用,如上睑下垂、复视等,药物由眼轮匝肌弥散至提上睑肌或眼外肌导致;(3)注射的局部症状,如瘀斑、水肿等;(4)全身症状及过敏。本项研究中最常见的不良反应是口角歪斜和闭眼困难,都是治疗相关的面肌无力表现,在后续注射中通过调整剂量和注射部位可以减轻。流泪也是患者提及较多的不良反应,主要是由于药物弥散导致泪囊部眼轮匝肌无力而影响泪小管的引流所致。此外,注射后眼睑位置改变如睑外翻,可能直接影响眼睑对泪液的存留,并通过改变泪小点的位置影响泪液的引流[7]。干眼是另一种常见的眼部不良反应,主要是由于注射后眨眼减少,闭眼无力导致[7]。也有学者推测由于眼球外侧的泪腺主要由副交感神经支配,外眦周围的BTX-A注射可以通过弥散作用影响副交感神经突触前膜的乙酰胆碱释放,从而减少泪腺的分泌,加重干眼症状[8]。上睑下垂曾是BTX-A治疗中最常见的不良反应[9],但随着经验积累,其发生率已大大降低。衡力应用明胶作为毒素结合蛋白,易出现皮疹,但本项研究中并无相关病例报告。
本项研究设计基于临床工作常态,并未对BTX-A的使用剂量进行限制,研究者可以根据患者不同部位和严重程度进行个体化治疗。研究显示保妥适和衡力在最佳疗效方面无统计学差异,应用保妥适治疗的患者疗效持续时间较长,可能与保妥适的使用剂量较大有关。衡力在起效时间上较短,但保妥适在口角歪斜和流泪方面的发生率略低,在其他不良反应的发生率方面二者相似。保妥适不良反应持续时间似乎较短,但二者的差异并无统计学意义。两种BTX-A在起效时间和不良反应方面的细微差异,可能与二者不同的弥散性有关。弥散性高的药物往往吸收速度快,起效时间短,但更容易弥散至靶肌肉以外的其他肌肉,出现治疗之外的不良反应。有学者认为BTX-A的弥散性与毒素蛋白复合物的相对分子质量(Mr)相关,Mr越大越不易弥散,还有学者认为药物的弥散性与剂量、浓度、体积和注射方法等因素有关[10]。目前国际上关于BTX-A弥散性的研究尚缺乏公认的研究方法,试验结果也不尽相同[11-12]。此外,BTX-A的临床疗效和不良反应受到多种因素的影响,除药物外,还包括患者的病程长短、病情严重程度以及不同研究中心的注射技术等,需要综合考虑。此外,选择衡力的患者要明显多于选择保妥适的患者(分别为542例与123例),除了衡力具有安全有效的特点之外,相对低廉的价格使其在药物经济学上占有明显的优势。
这项关于BTX-A治疗特发性偏侧面肌痉挛的多中心研究规模较大,参与调查的病例总数超过了以往国际国内的同类研究,涉及我国内地全部7个行政区域。参与调查的15个中心都是区域内著名的运动障碍病中心,具有比较丰富的特发性偏侧面肌痉挛的诊断和治疗经验。因此,这项研究的结果可以较为真实反映我国应用BTX-A治疗特发性偏侧面肌痉挛的现状,具有一定代表性。
致谢:感谢清华大学于歆杰博士在数据统计方面提供的帮助。
[1]Batla A, Goyal C, Shukla G, et al. Hemifacial spasm: clinical characteristics of 321 Indian patients[J]. J Neurol, 2012, 259:1561-1565.
[2]Wabbels B, Roggenkämper P.Botulinum toxin in hemifacial spasm: the challenge to assess the effect of treatment[J].J Neural Transm, 2012, 119:963-980.
[3]Campos-Benitez M, Kaufmann AM. Neurovascular compression findings in hemifacialspasm[J].J Neurosurg, 2008, 109: 416-420.
[4]Sindou MP. Microvascular decompression for primary hemi- facial spasm.Importance of intraoperative neurophysiological monitoring[J].Acta Neurochir (Wien), 2005, 147:1019-1026.
[5]Zhong J, Zhu J, Li ST, et al. An analysis of failed microvascular decompression in patients with hemifacial spasm: focused on the early reoperativefindings[J]. Acta Neurochir (Wien), 2010, 152: 2119-2123.
[6]Moriyama L, ChienHF.Botulinum toxin type A in the treatment of hemifacial spasm: an 11-year experience[J].Arq Neuropsiquiatr, 2010, 68:502-505.
[7]Ozgur OK, Murariu D, Parsa AA, et al. Dry eye syndrome due to botulinum toxin type-A injection: guideline for prevention[J]. Hawaii J Med Public Health,2012, 71:120-123.
[8]Arat YO, Yen MT. Effect of botulinum toxin type A on tear production after treatment of lateral canthalrhytids[J].Ophthal Plast Reconstr Surg, 2007, 23:22-24.
[9]Rieder CR, Schestatsky P, Socal MP, et al. Double-blind, randomized, crossover study of prosigne versus botox in patients with blepharospasm and hemifacial spasm [J].Clin Neuropharmacol, 2007, 30: 39-42.
[10]Wohlfarth K, Schwandt I, Wegner F, et al. Biological activity of two botulinum toxin type A complexes (Dysport and Botox) in volunteers: a double-blind, randomized, dose-ranging study[J].J Neurol, 2008,255:1932-1939.
[11]Trindade de Almeida AR, Marques E, de Almeida J, et al. Pilot study comparing the diffusion of two formulations of botulinum toxin type A in patients with forehead hyperhidrosis[J].Dermatol Surg, 2007, 33: S37-43.
[12]Wohlfarth K, Muller C, Sassin I, et al. Neurophysiological double-blind trial of a botulinum neurotoxin type A free of complexing proteins [J].Clin Neuropharmacol, 2007, 30:86-94.
