基质辅助激光解析/电离飞行时间质谱法和表面等离子谐振法在HPV分型检测中的应用比较
2014-03-28赵金银曲守方
万 敏 赵金银 曲守方 黄 杰,*
1.华北石油管理局总医院检验科(任丘,062550);2.中国科学院北京基因组研究所;3.中国食品药品检定研究院
人乳头瘤病毒(HPV)是一种非均质、双股环形DNA病毒。现在报道的HPV型别已经超过了140种,其致病范围从机体表皮、泌尿生殖系已扩展到头颈部癌组织。其中约有40种与肛门生殖道感染有关,30余种可从受感染的生殖道中分离出来,有20余种已证实与宫颈肿瘤有关[1]。目前HPV分型检测的主要技术是分子生物学方法,采用的方法有液相芯片法[2]、多聚酶链反应(PCR)产物杂交分析法[3]、基因芯片法、PCR 表面等离子谐振法[4]、杂交捕获化学发光法(HC2)[5]等。基质辅助激光解析/电离飞行时间质谱法(MALDI-TOF-MS)和表面等离子谐振法(SPR)是新近发展的两种新的检测技术。本研究采用中国食品药品检定研究院体外诊断试剂一室建立的HPV L1基因分型国家参考品[6]和临床样本对MALDI-TOF-MS法和SPR法进行评价,对其性能质量进行初步评估。
1 材料与方法
1.1 试 剂
HPV L1基因分型国家参考品含有14种高危型 HPV(16,18,31,33,35,39,45,51,52,56,58,59,68,73),3种中等危险型(26,53,66)和13种低危型HPV(6,11,40,42,43,44,54,61,70,72,81,83,CP8304),由中国食品药品检定研究院提供,用于以L1基因为靶序列HPV基因分型试剂盒的质控。参考品包含的30种型的质粒DNA浓度均约为105~106拷贝/ml。HPV基因分型检测试剂盒(SPR法,批号:20120601)购自北京金菩嘉公司,能检测的HPV型别包括24种(16,18,31,33,35,39,45,51,52,53,56,58,59,66,68,6,11,40,42,43,44,54,70,81),其中高危型有13种(16,18,31,33,35,39,45,51,52,56,58,59,68)、2种中等危险型(53和66)。MALDI-TOF-MS法检测HPV基因分型技术由深圳华大基因研究院建立,能检测的HPV型别包括14种型别(16,18,31,33,35,39,45,51,52,56,58,59,66,68)。
1.2 样 本
从华北石油管理局总医院收集129份经液基薄层细胞检测的样本,其中细胞学检查诊断结果为鳞状细胞异常病变(包括不能明确意义的非典型鳞状上皮细胞及以上级别)样本89例(包括一例鳞状细胞癌);另外40例未见上皮内病变细胞或恶性细胞。
1.3 方 法
将HPV基因分型质控品盘30种HPV质粒(原始浓度为105~106拷贝/ml),分别以10倍梯度稀释,稀释至质粒浓度为104~105拷贝/ml。稀释液含正常人类全基因组,浓度为2μg/ml。按照各个试剂盒说明书进行提取、扩增、检测。对129份经液基薄层细胞检测的样本进行了测序。扩增引物采用MY11/MY09引物[7],由生工生物工程(上海)股份有限公司进行序列测定。
2 结果
2.1 HPV L1基因分型国家参考品检测一致性
采用HPV基因分型检测试剂盒(SPR法)和MALDI-TOF-MS法对 HPV L1基因分型国家参考品进行检测,结果表明两种方法对检测范围内的参考品具有100%的准确性,不在检测范围内的型别未发现交叉,结果见表1。
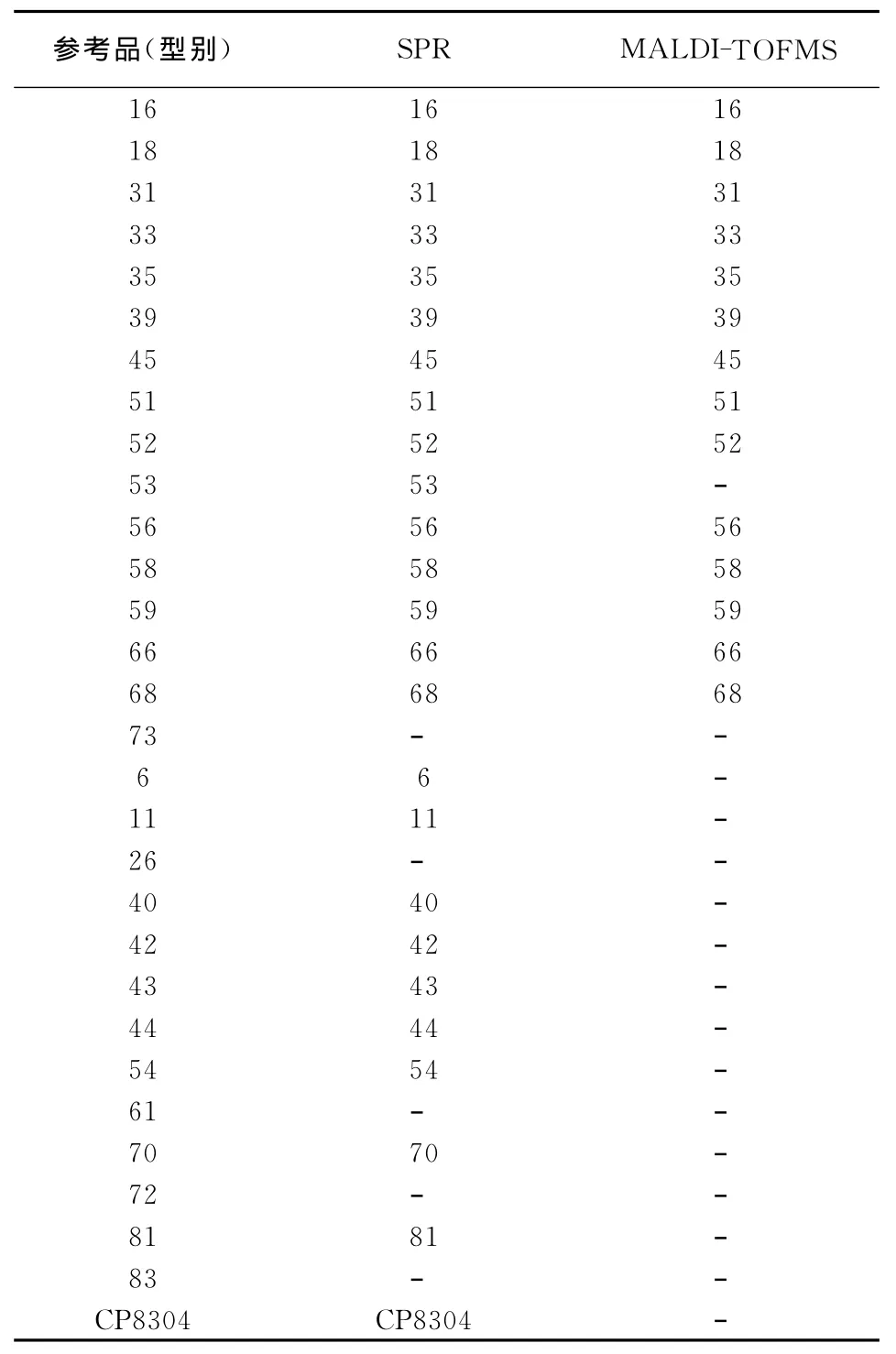
表1 HPV L1基因分型国家参考品检测结果*
2.2 临床样本检测一致性
测序分析结果129份样本中有93份为HPV阳性,36份为 HPV阴性。MALDI-TOF-MS法检测结果为阳性(与测序结果一致)样本82份,阴性(与测序结果一致)样本32份,HPV分型灵敏性为88.2%(82/93)、特异性为88.9%(32/36);而SPR法的 分 型 灵 敏 性 为 98.9% (92/93)、特 异 性 为97.2%(35/36)。结果表明这两种方法检测临床样本具有较好的灵敏性、特异性和一致性(表2)。129份样本中高危型样本有77份,高危型样本的分型准确率 MALDI-TOF-MS法为100%(77/77),SPR法为94.8%(73/77)。

表2 两种方法的临床灵敏性和特异性(份)
2.3 两种检测方法的灵敏性和特异性分析
经统计分析,129份样本中有104份样本两种方法分型检测结果一致,25份分型结果不一致,包括MALDI-TOF-MS法检测的12份HPV阴性样本和13份HPV阳性样本。12份HPV阴性的样本,其中11份经SPR和测序确定是低危型HPV样本,不在MALDI-TOF-MS检测范围内,另1份是阴性。13份HPV阳性样本中,有5份样本经SPR法和测序法确定为低危型 HPV (HPV 11,40,54,6,43),MALDI-TOF-MS法出现分型错误(SPR分型结果与测序法一致),4份经SPR法和测序法确定为阴性,表明该试剂盒存在着一定的交叉反应;另外4份样本结果表明SPR法出现分型错误(MALDI-TOF-MS分型结果与测序法一致),表明该试剂盒也存在着交叉反应(表3),两者的交叉反应结果没有差异(P>0.05)。
3 讨论
国内外有多位研究人员进行了PCR产物MALDI-TOF-MS法检测HPV型别的研究。国内深圳华大基因研究院的研究人员建立的PCR产物基质辅助激光解析/电离飞行时间质谱法可以检测14种HPV型别。SPR法是利用在金属膜/液面界面,由光的全反射引起的物理光学现象来分析分子间相互作用的技术。北京金菩嘉公司利用SPR法检测24种HPV基因型,其原理是使PCR产物流过表面包被有24种HPV基因型特异性探针的SPR生物传感芯片,与芯片表面HPV基因型特异探针反应,通过检测芯片上的杂交信号从而同时对HPV的24种基因型进行检测。

表3 阳性临床样本中两种方法检测的分型结果不一致的案例分析(份)
包含30种不同型别的HPV L1基因分型国家参考品均包含有不同型别L1基因全长(除了HPV CP8304是MY09/11引物扩增产物),几乎涵盖了临床所有最常见型别,能评价绝大多数HPV基因分型试剂盒。但是由于各型别HPV均有一定的变异度,且国内尚未见不同型别HPV分离株以及同一型别不同分离株序列分析的系统资料,故试剂盒的研发以及临床选择应在通过参考品的考核下加大临床样本的验证。
通过检测129份HPV临床样本,初步评价了两种HPV基因分型检测方法:MALDI-TOF-MS法和SPR法。选用测序法作为参考方法评价这两种方法检测结果不一致的样本。两种方法对129份样本中高危型HPV分型的准确率分别为100%(77/77,MALDI-TOF-MS)和94.8%(73/77,SPR),表明这两种方法在高危型HPV临床检测中具有很好的准确性。MALDI-TOF-MS法HPV分型检测的灵敏性为88.2%(82/93)、特异性为88.9%(32/36);而SPR法HPV分型检测的灵敏性为98.9%(92/93),特异性为97.2%(35/36),结果表明这两种方法检测临床样本具有较好的灵敏性和特异性。
HPV基因具有一定的同源性,当根据不同基因型的核酸序列设计特异性的引物和探针时,引物和探针与不同HPV基因型的序列有一定程度匹配,引物探针能够识别不同基因型从而导致交叉反应现象。研究报道特定型别的HPV基因具有高度同源性,单基因位点检测可能导致假阳性[8]。在本研究的检测中也发现了存在一定程度的交叉。因此在进行我国常见HPV基因型临床样本的筛查时,可以考虑不同原理的检测方法互相补充进行检测,以便获得更准确的结果。
1 Muñoz N,Bosch FX,de SanjoséS,et al.Epidemiologic classification of human papillomavirus types associated with cervicad cancer[J].N Engl J Med,2003,348(6):518-527.
2 Jiang HL,Zhu HH,Zhou LF,et al.Genotyping of human papillomavirus in cervical lesions by Ll consensus PCR and the Luminex xMAP system[J].Jonrnal of Medical Microbiolog,2006,55(pt6):715-720.
3 van den Brule AJ,Pol René,Fransen-Daalmeijer N,et al.GP5+/6+ PCR followed by reverse line blot analysis enables rapid and high-throughput identification of human papillomavirus genotypes[J].Journal of Clinical Microbiology,2002,40(3):779-787.
4 Wang R,Minunni M,Tombelli S,et al.A new approach for the detection of DNA sequences in amplified nucleic acids by a surface plasmon resonance biosensor[J].Biosensors and Bioelectronics,2004,20(3):598-605.
5 Halfon P,Trepo E,Antoniotti G,et al.Prospective evaluation of the hybrid capture 2and amplicor human papillomavirus(HPV)tests for detection of 13high-risk HPV genotypes in atypical squamous cells of uncertain significance[J].Journal of Clinical Microbiology,2007,45(2):313-316.
6 黄杰,曲守方,徐任,等.HPV基因分型质控品的建立[J].中华检验医学杂志,2010,33(6):559-562.
7 Castle PE,Schiffman M,Gravitt PE,et al.Comparisons of HPV DNA detection by MY09/11PCR methods[J].J Med Virol,2002,68:417-423.
8 Matthews CP,Shera KA,McDougall JK.Genomic changes and HPV type in cervical carcinoma[J].Proc Soc Exp Biol Med,2000,223:316-321.
