酸化水与方解石石膏反应的模拟计算研究
2014-03-20陈振吉龙江徐显义王学民
陈振,吉龙江,徐显义,王学民
(山东省物化探勘查院,山东 济南 250013)
运用水文地球化学模拟软件PHREEQIC可对水中组分的存在形式和化合物的饱和指数进行模拟计算,几乎能解决水、气、岩土相互作用系统中所有平衡热力学和化学动力学问题。它是进行地球化学模拟,定量研究地球化学作用的一个重要手段[1,2]。
1 模拟计算的目的及意义
该次模拟计算中,以HCl与蒸馏水的混合溶液做为溶浸液,HCl酸化蒸馏水的pH梯度为3,4,5,6,7;根据样品矿物成分分析数据,运用PHREEQIC程序,对酸化液与可溶矿物的反应进行模拟计算。
通过对溶浸液与含矿层可溶矿物相互作用的模拟计算,可以了解不同酸度条件下的溶浸液对可溶矿物的溶蚀效果,对试验效果进行理论预测研究,从而提出适合室内试验的溶浸液配方。
2 模拟计算的模型建立
为了计算的简便,将蒸馏水看作纯水,pH值为7。模拟的过程中主要是对方解石和石膏2种矿物的反应过程进行模拟,黄铁矿会有一定的溶解,但不作为此次模拟的对象。模拟过程中假设反应过程中矿物是足量的,反应温度为25℃,反应平衡条件是:SI石膏=0,SI方解石=0,在此条件的基础上建立“盐酸+蒸馏水+方解石”、“盐酸+蒸馏水+石膏”、“盐酸+蒸馏水+方解石+石膏”3种模型来进行模拟计算。
3 模拟计算结果
3.1 盐酸+蒸馏水+方解石
模型为“盐酸+蒸馏水+方解石”平衡完全反应,反应至SI方解石=0停止。为了计算的简便,将蒸馏水看作纯水,pH值为7,并要求初始方解石的量满足足够完全反应需要。反应初始条件可见表1。酸化蒸馏水(1L)与足量方解石在SI方解石=0的平衡条件下完全反应后的结果可见表2。

表1 酸化蒸馏水与方解石反应的初始条件

表2 酸化蒸馏水与方解石平衡反应结果
注:溶蚀量(方解石)即指达到平衡状态所需要溶蚀的方解石量。
由于酸化溶液对方解石的溶蚀过程中,可以看作是弱碱的水解过程,所以溶液对方解石的溶蚀能力与溶液中的pH值密切相关,其过程是:
(1)
而在反应后pH值范围为7.96~9.92,所以重碳酸根会进一步发生水解:
(2)

图1 酸化蒸馏水初始pH值与方解石平衡反应后溶液pH值关系
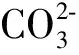
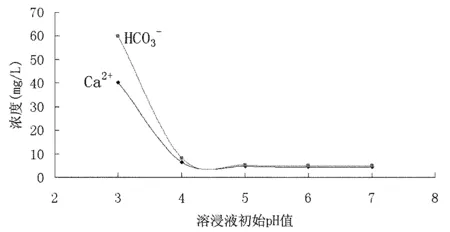
图2 酸化蒸馏水初始pH值与方解石平衡反应后溶液离子成分

图3 酸化蒸馏水初始pH值与方解石溶蚀量关系图
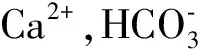
总的来说,当酸化溶液pH<4时,酸化蒸馏水对方解石具有较好的溶蚀能力。从溶蚀方解石并进而增大渗透性的角度来讲,在室内柱浸试验使用蒸馏水的过程中,应使酸化蒸馏水的pH值不大于4,以pH=3或更低为宜。
3.2 盐酸+蒸馏水+石膏
反应初始条件见表3。假设石膏量为足量,使得酸化蒸馏水与石膏完全反应,反应平衡条件为SI石膏=0。平衡反应的结果见表4。

表3 酸化蒸馏水与石膏反应的初始条件
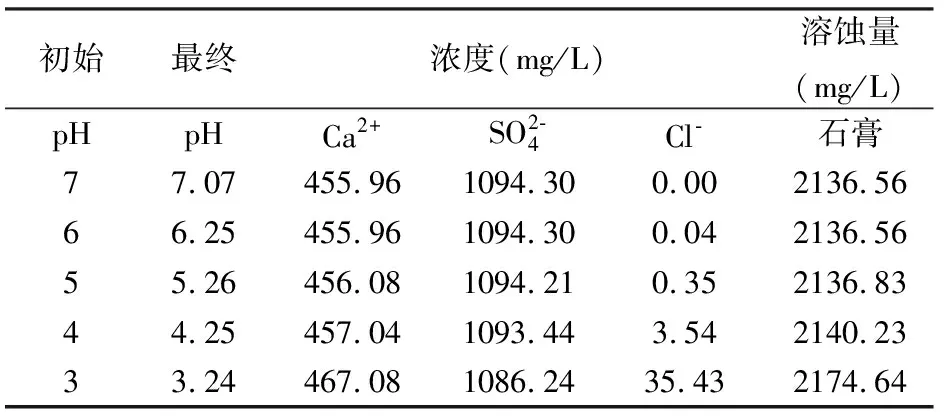
表4 酸化蒸馏水与石膏平衡反应结果
石膏与溶液的化学反应方程式为:
(3)


图4 酸化蒸馏水初始pH值与石膏平衡反应后溶液pH值关系
从图5,图6中可以看出,酸化蒸馏水在初始溶液中无钙离子、硫酸根离子存在的条件下,对石膏具有极强的溶蚀能力,其溶蚀能力可达2174.64~2136.56mg/L,且蒸馏水的酸化程度(酸性和中性)对石膏溶蚀能力的影响不大,例如在pH=3的条件下,酸化蒸馏水对石膏的溶蚀能力为2174.64mg/L,在pH=7的条件下仅为2136.56mg/L。表明在加盐酸与不加盐酸条件下,溶液对石膏的溶解能力相差不大。所以单纯从对石膏的溶蚀能力来讲,在室内柱浸试验的过程中可以直接利用蒸馏水进行石膏矿物的浸出,而无需利用盐酸酸化。
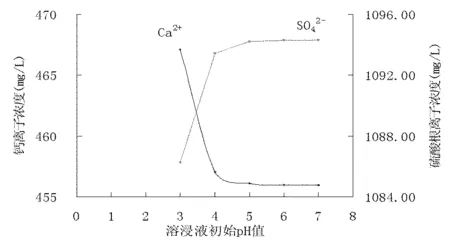
图5 酸化蒸馏水初始pH与石膏平衡反应后溶液离子成分
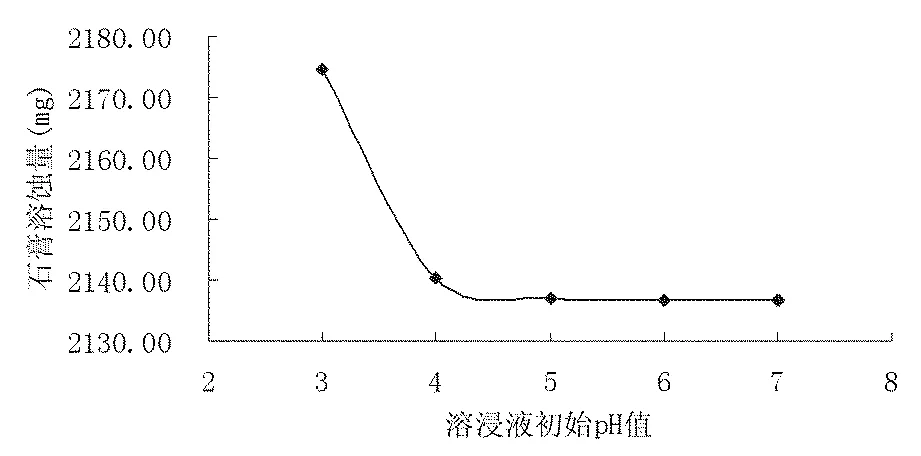
图6 酸化蒸馏水初始pH与石膏溶蚀量关系图
3.3 盐酸+蒸馏水+石膏+方解石
模型“盐酸+蒸馏水+矿物”,其中矿物为方解石和石膏同时存在的情况,酸化蒸馏水的初始条件见表5,反应过程中假设矿物的质量是足够酸化蒸馏水反应的,平衡反应条件是SI石膏=0,SI方解石=0,反应结果见表5。
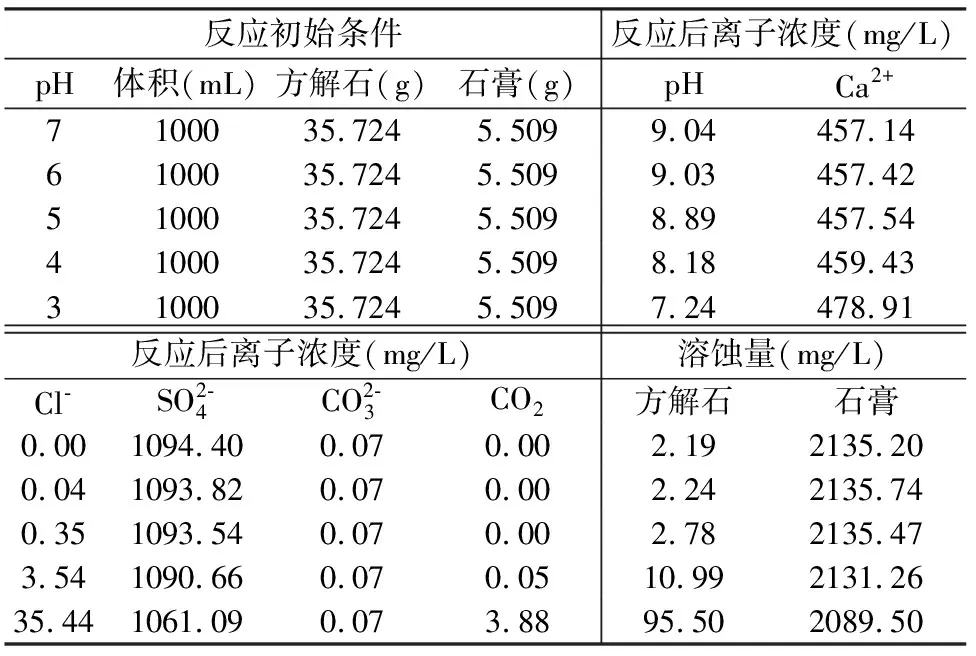
表5 酸化蒸馏水与石膏、方解石反应
从图7可以看出,溶液与方解石和石膏矿物反应完成后的pH值呈现出一定的规律性,即反应后溶液的pH值总是要高于溶浸液的pH值,这是由于可溶解矿物不断溶解消耗溶液中的H+,使得浸出液中H+减少,从而反映为pH值不断升高[4]。

从图9可以看出,在酸化蒸馏水pH=4.00~7.00的初始条件下,方解石和石膏的溶蚀量变化不大。而当pH值降低至3的时候,方解石的溶蚀量有增加的趋势,而溶液对石膏的溶蚀却下降。

图7 酸化蒸馏水初始pH值与反应后溶液pH值的关系
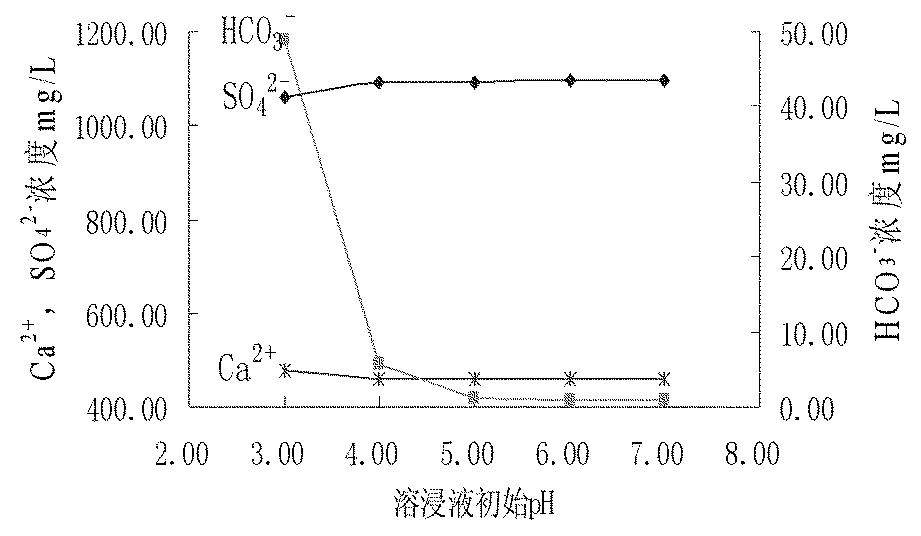
图8 酸化蒸馏水初始pH与方解石、石膏平衡反应后溶液离子成分

图9 方解石、石膏平衡条件下的溶浸液溶蚀能力
从图10中可以看出,在酸化蒸馏水pH=4~7的初始条件下,溶液对矿物的溶蚀能力没有显著的变化,当酸化蒸馏水pH值酸化到3时,溶液对矿物的溶蚀能力有增加的现象(总溶蚀量为方解石和石膏的溶蚀量总和)。

图10 酸化蒸馏水的总溶蚀能力
4 结语
从表5中可以看出,利用蒸馏水(将其看作纯水)与盐酸混合后,在设定完全反应后方解石和石膏皆要达到平衡状态的条件下,溶蚀的矿物成分以石膏为主,方解石的溶蚀量很小,特别是在酸化程度较弱的溶液中,在pH值从7到4的范围内,方解石在1L酸化溶液中的溶蚀量仅从2.19mg增加到10.99mg,而石膏的溶蚀量自2135.20mg降低至2131.26mg,变化值基本可以忽略不计,只有在pH值降低至3的条件下方解石的溶蚀量才明显增高至95.50mg/L,而石膏的溶蚀量仍保持为2089.50mg/L。根据这些认识,在实际不断的渗流条件下,石膏应该是早于方解石溶蚀完毕,后期的工作主要以溶蚀方解石为主。在实际的工作中,考虑到试验周期以及试验成本的问题,酸化溶液的pH值不宜太低,但当溶浸液pH值从4变化到7时,溶浸液对矿物的溶蚀能力没有明显变化,所以在室内试验中,溶浸液的pH值选择范围是4~7或只在该范围内选取一个梯度即可。
参考文献:
[1] 周文斌,史维浚.地球化学模式程序的原理、分类与功能[J].铀矿地质,1990,(4):217-222.
[2] Parkhurst D L,Thorstenson D C,Plummer,L N.PHREEQE-A computer program for geochemical calculations[R].u.S.Geological Survey Water Resources Investigations Report 80-96,1980(Revised and reprinted August,1990)
[3] Taylor J R.The influence of calcite dissolution on reservoir porosity in Miocene sandstones,Picaron field,offshore Texas Gulf Coast[J].Journal of Sedimentary Petrology,1989,60:322-334.
[4] 殷蓬勃.改善砂岩型铀矿含矿层渗透性的溶液-矿物相互作用模拟研究[D].江西:东华理工大学,2008,13-14
[5] 闫志为.硫酸根离子对方解石和白云石溶解度的影响[J].中国岩溶,2008,(1):24-31.
