银、L-半胱氨酸修饰电极同时测定多巴胺和抗坏血酸
2014-03-11汤优霞孙登明
汤优霞,孙登明
(淮北师范大学化学与材料科学学院,安徽淮北235000)
0 引言
多巴胺(DA)是下丘脑和脑垂体中的一种关键神经递质,其浓度又受精神因素的影响,脑内DA 失调是引起帕金森氏症和精神分裂症的重要原因[1~2]。此外,DA 还具有兴奋心脏、增加肾血流量的功能,可用于治疗先血性、心源性及感染性休克。抗坏血酸(AA)是广泛存在于新鲜水果蔬菜及许多生物中的一种重要的维生素,作为一种高活性物质,它参与许多新陈代谢过程。在生物体内,抗坏血酸是一种抗氧化剂,保护身体免于自由基的威胁。因此,对DA和AA进行测定有着非常重要意义。近年来用修饰电极测定DA 和AA已有许多的报道[3~5]。金属掺杂聚氨基酸修饰电极也曾用于DA和AA的同时测定[6],但在测定过程中,修饰在电极表面的金属会在实验过程中因电位超过氧化电位而出现氧化脱落的现象,影响电极寿命和测定的重现性。为了更好的提高电极性能,在实验中采用层层自组装的方法,将银和L-半胱氨酸聚合在玻碳电极表面,制备了银、L-半胱氨酸修饰电极(PLC/Ag/GCE)。并且用该修饰电极研究了DA和AA的电化学行为,实现了对DA和AA同时测定。
1 实验部分
1.1 仪器与试剂
LK2006A 电化学工作站(中国,天津市兰力科化学电子高技术有限公司);pHS-3C 精密酸度计(中国,上海康仪仪器有限公司);KQ-250B型超声波清洗器(中国,昆山超声波仪器有限公司)。三电极系统:修饰电极或裸的玻碳电极为工作电极,铂电极为对电极,Ag/AgCl为参比电极。
DA 储备液:5.00×10-3mol/L;AA 储备液:5.00×10-2mol/L,避光冷存,使用时再稀释至实验所需要的浓度;L-半胱氨酸溶液:5.0×10-3mol/L;硝酸银(AgNO3)溶液:1.0×10-2mol/L,避光冷存;硝酸 (HNO3):1.5 mol/L;pH2.0~pH11.0的磷酸盐缓冲溶液(PBS),实验用水均为亚沸蒸馏水。
1.2 修饰电极的制备
按文献[7]对玻碳电极进行预处理,把处理后的电极放入10 mL 含有一定体积的1.0×10-2mol/L AgNO3和1.5 mol/L HNO3的溶液中,静置10 s,在-0.2~-0.7 V 的电位范围内,扫速160 mV/s 下循环扫描10 圈。把修饰好的电极(Ag/GCE)取出,清洗干净后,放入10 mL 含有一定体积的5.0×10-3mol/L L-半胱氨酸的PBS (pH=3.0)聚合溶液中,静置12s,在-0.4~2.4V 电位范围内,以140 mV/s 扫描速率循环扫描9 圈,取出用二次亚沸水对电极表面进行淋洗,晾干,即可制得PLC/Ag/GCE 修饰电极。
1.3 实验方法
准确加入一定量的DA和AA标准溶液于pH=3.0 的PBS溶液,充分摇匀,并转移到电解池中,用三电极系统:PLC/Ag/GCE (工作电极),铂电极(辅助电极)和Ag/AgCl(参比电极),静置10 s,在-0.3 ~0.8 V 的电位范围内,利用循环伏安法进行扫描,记录图中峰电位和峰电流。若需进行下次实验,修饰电极要在空白底液中,扫至无峰,再用二次亚沸水冲洗,滤纸吸干后,才可进行测定。
2 结果与讨论
2.1 修饰电极的聚合条件
实验结果表明,Ag 修饰电极的最佳修饰条件:3.0 mL 1.0×10-2mol/L AgNO3、3.5 mL 1.5 mol/L HNO3、3.5 mL 亚沸水,扫描电位范围为-0.7 ~-0.2 V,扫描速率为160 mV/s,扫描周次为10 圈,静置时间为10 s。L-半胱氨酸聚合条件:5.0 mL 5.0×10-3mol/L 的L-半胱氨酸和5.0 mL pH=3.0的PBS 缓冲溶液,扫描电位范围为-0.4 ~2.4 V,扫描速率为140 mV/s,扫描周次为9 圈,静置时间为12 s。
2.2 DA和AA在修饰电极上的循环伏安特性
图1分别为5.00×10-5mol/L DA(A);5.00×10-4mol/L AA (B);5.00×10-5mol/L DA 和5.00×10-4mol/L AA 共存(C)时,在GCE(a)、Ag/GCE(b)、PLC/GCE(c)、PLC/Ag/GCE(d)上的循环伏安图。由图可知,DA 在四个电极上的氧化峰和还原峰的电位基本不变;而AA 由于存在氧化过电位,使得AA 在GCE 上的氧化峰电位高于其他三个修饰电极。DA和AA在Ag/GCE,PLC/GCE、PLC/Ag/GCE 电极上,DA和AA都存在一个明显的氧化峰,且峰电流逐渐增大。当DA和AA共存时,在GCE 上,DA和AA的氧化峰重叠在一起,不能进行同时测定,在其他三个修饰电极上DA 和AA都有较好的分离,在PLC/Ag/GCE 电极上,峰电流最大。这说明经银、L-半胱氨酸分层修饰的电极对两种物质的电化学催化作用明显增强,测定的选择性和灵敏度有较大提高,且DA和AA共存时,两者的氧化峰电位差达到了0.209 V,不需分离就可进行同时测定。
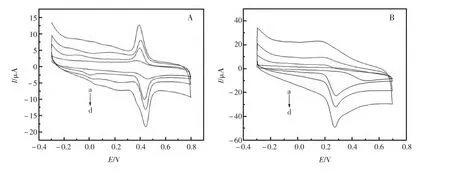
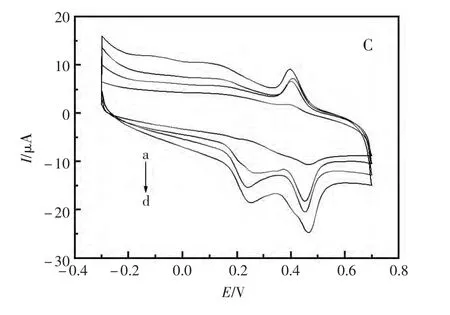
图1 DA(A)、AA(B)和DA 与AA 共存(C)时在GCE(a)、Ag/GCE(b)、PLC/GCE(c)、PLC/Ag/GCE(d)上的CV 曲线Fig.1 Cyclic voltammetric curves of DA(A)、AA(B)and the mixed solution of DA and AA(C)at GCE(a)Ag/GCE(b),PLC/GCE(c),PLC/Ag/GCE(d).Scan Rate:(A)100 mV/s,(B)120 mV/s,(C)120 mV/s.
2.3 DA和AA在修饰电极上的电化学行为
2.3.1 底液酸度的影响
在pH为2.0~11.0 范围内,仅改变底液的酸度,分别单独测定DA 和AA。实验结果表明,随着pH值的增加,DA和AA的峰电位均向负电位移动。DA 的氧化峰电位与pH 在2.0~11.0 之间呈良好的线性关系,线性方程为:Epa(V)=0.622 5-0.056 7 pH,r=0.998 2,斜率为56.7 mV/pH;AA 的氧化峰电位与pH 在2.0 ~8.0 之间呈良好的线性关系,线性方程为:Epa(V)=0.323 0-0.030 0 pH,r=0.990 8,斜率为30 mV/pH。说明DA 在该修饰电极上发生的为等电子等质子的反应过程,且AA 的反应过程也有质子参与。在pH=3.0时,DA 响应电流达最大;而对AA 而言,当pH=2.0时,AA 的响应电流达到最大值,考虑到灵敏度和选择性,pH=3.0 被选作是同时测定DA和AA的最佳酸度。
由于DA和AA发生电化学作用的峰电流与得失电子数有关,因此根据文献[8~9]与实验结果,DA和AA在修饰电极上可能的电化学反应分别为:
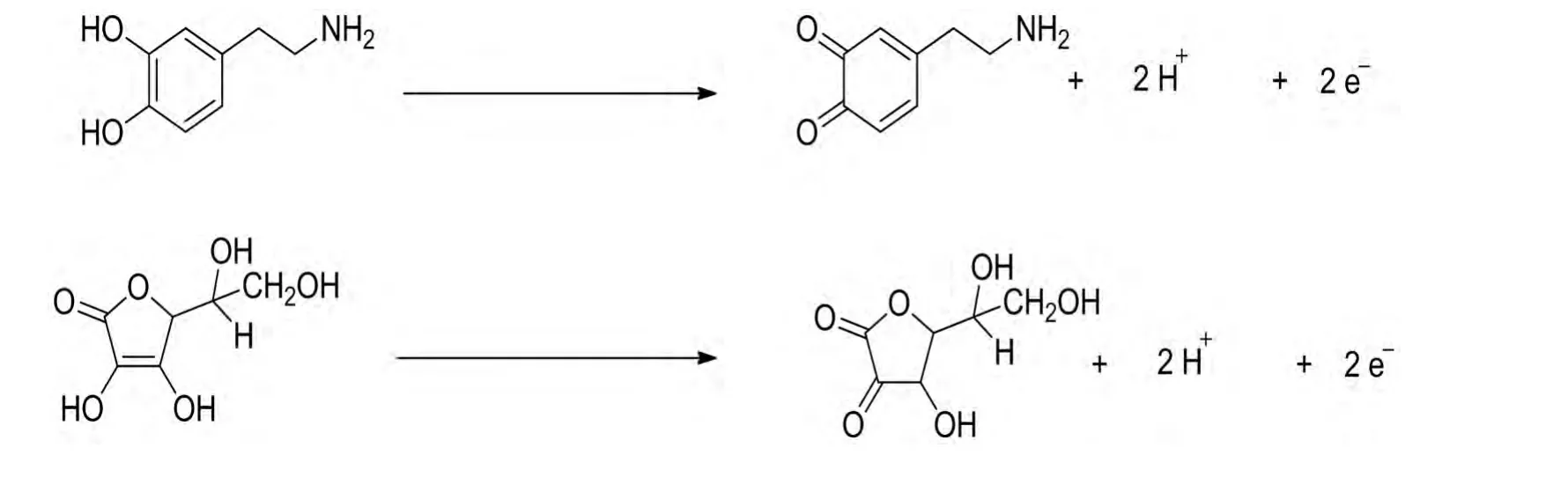
2.3.2 扫速影响
改变扫描速率,分别对含5.00×10-5mol/L DA 和5.00×10-4mol/L AA 的溶液进行实验测定。实验结果表明,在60~600 mV/s 范围内,随着扫速的不断增加,DA和AA的氧化峰电流不断增大,峰电位正移,当扫描速率过高时,充电电流较大且峰型变宽,影响测定的精密度和准确性。在同时测定时DA 和AA时,扫速选择为120 mV/s。
DA和AA的峰电流的对数和扫速的对数成线性关系,DA 的斜率接近于1.0,它在电极表面的氧化还原过程主要受吸附控制,DA 在修饰电极表面的吸附量可根据文献[10]计算。在底液p H=3.0,扫速100 mV/s时,DA 在修饰电极的吸附量为Γ=2.20×10-10mol/cm2。而AA 的斜率接近0.5,它在电极表面的氧化过程主要受扩散控制。AA 在电极上的扩散性质可以用计时电流法研究,图2(A)为5.00×10-4mol/L AA 在pH=2.0 的PBS 中,分别在四种不同类型的电极上的计时电流曲线,图2(B)为不同电流强度I 相对于t-1/2的关系图。
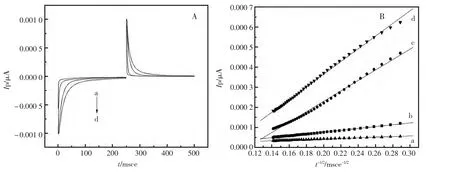
图2 AA 在不同电极上的计时电流曲线(A)及电流I 与t-1/2 的关系图(B)Fig.2 Chronoamperometry of AA at GCE(a)、Ag/GCE(b)、PLC/GCE(c)and PLC/Ag/GCE(d)(A)and the relationship curve between I and t-1/2(B)
根据Cottrell 方程,计算不同电极的扩散系数见表1。由计算结果可见在PLC/Ag/GCE 上,AA 的扩散系数大于在其他三个电极上的扩散系数,这说明AA 在PLC/Ag/GCE 上的电化学响应高于其它三种电极,这与AA 在修饰电极上的循环伏安法测定的结果一致。

表1 AA 在不同修饰电极上的扩散系数Tab.1 The diffusion coefficient of AA on different modified glassy carbon electrode
2.4 工作曲线
在最佳测定条件下,用循环伏安法对DA和AA进行分别和同时测定,其线性范围、线性回归方程和检出限结果见表2。
2.5 精密度和稳定性
对5.00×10-5mol/L DA 和5.00×10-4mol/L AA 分别进行5次平行实验,RSD 分别为3.2%和4.1%,表明该电极测定具有良好的重现性。PLC/Ag/GCE 在室温下放置1 周,相同条件下再次测定时,峰电位和峰电流仍较为稳定,表明PLC/Ag/GCE 具有良好的稳定性。
2.6 干扰离子
对含有5.00×10-5mol/L DA 和 5.00×10-4mol/L AA 的10 mL 混合溶液进行测定,测定允许误差介于-5%~+5%之间时,测定结果表明,共存物质的允许量(mg)为:Cl-、SO42-、NO3-、K+、Na+、Ca2+、Al3+、Mg2+、Ba2+、L-缬氨酸、L-苏氨酸、L-酪氨酸、L-天冬氨酸、L-赖氨酸、L-组氨酸(≥1.0 mg,未做最高限),Cu2+、I-(0.2 mg),Fe2+(0.3 mg),Pb2+、Cr3+(0.7 mg)。
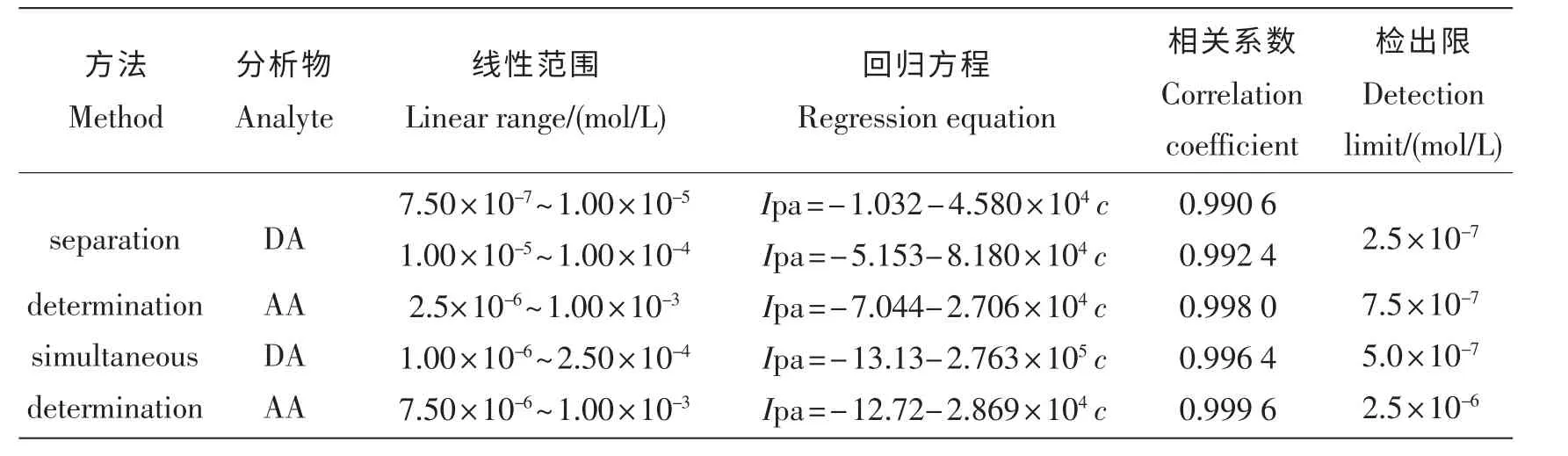
表2 在PLC/Ag/GCE 上测定DA和AA的分析结果Tab.2 Analytical parameters for determination of DA and AA at PLC/Ag/GCE
2.7 样品分析
取多巴胺针剂(10 mg/mL,2 mL/支),稀释到一定的浓度,取一定的量按照实验方法进行实验;取维生素C 片研细后,称取一定量的样品,溶解,配制成一定浓度的AA溶液,取一定样品按实验方法进行测定,结果如下表3所示:
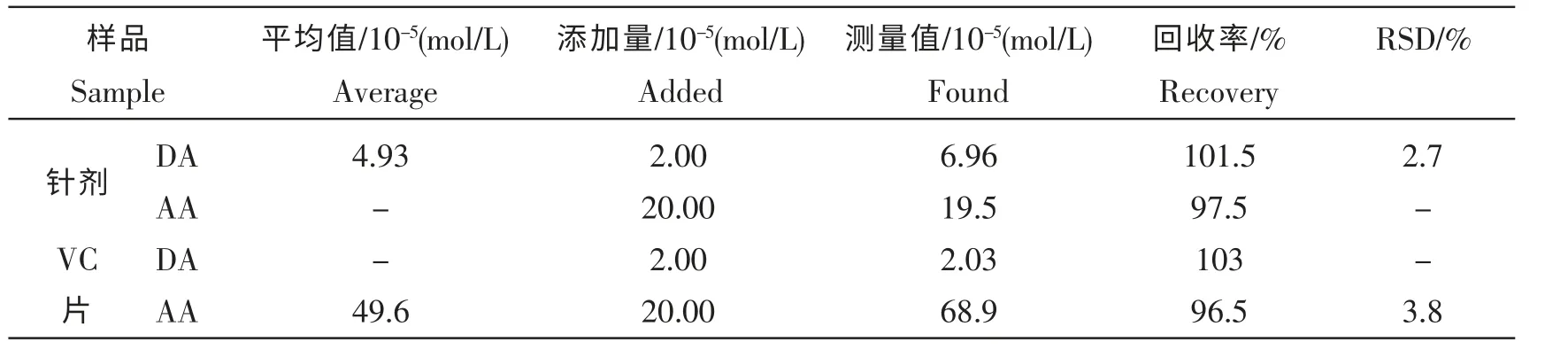
表3 测定针剂和VC 药片中的AA 和DATab.3 Determination of DA and AA acid in injection and VC tablet(n=5)
3 结论
制备了银、L-半胱氨酸分层修饰电极,并对DA和AA的电化学行为进行研究,证明了该修饰电极会使测定的灵敏度与精密度提高,发展前景较好。
[1]李素娟,邓德华,王贵芳,等.纳米金/石墨烯修饰电极的制备及其对多巴胺的测定[J].分析试验室,2012,31(3):14~17.
[2]胡玉斐,章竹君.以马铃薯组织为酶供体化学发光新方法测定血清中游离多巴胺[J].化学学报,2008,66(7):783~787.
[3]Chih Y K,Yang M C.Simultaneous detection of dopamine and ascorbic acid using silver/silver sulfide modified carbon nanotube electrodes[J].Journal of the Taiwan Institute of Chemical Engineers,2014,45:833~839.
[4]Wang C Q,Du J,Wang H W,et al.A facile electrochemical sensor based on reduced graphene oxide andAu nanoplates modified glassy carbon electrode for simultaneousdetection of ascorbic acid,dopamine and uric acid[J].Sensors and Actuators B,2014,204:302~309.
[5]Habibi B,Pournaghi-Azar M H.Simultaneous determination of ascorbic acid,dopamine and uric acid by use of a MWCNT modified carbon-ceramic electrode and differential pulse voltammetry [J].Electrochimica Acta,2010,55:5 492~5 498.
[6]马伟,田相星,孙登明.铜掺杂聚L-酪氨酸修饰电极同时测定尿酸、多巴胺和抗坏血酸[J].分析试验室,2011,30(12):45~50.
[7]孙登明,由文颖.聚L-谷氨酸修饰电极的制备及对多巴胺的测定[J].分析科学学报,2005,21 (5):530 ~532.
[8]刘传银,陆光汉.巯基乙酸自组装电极对多巴胺的电催化及其分析应用[J].理化检验-化学分册,2005,41(9):644~647.
[9]金晓艳,张宏,孙林.抗坏血酸在纳米Ag2O 修饰电极上电化学行为研究[J].阜阳师范学院学报,2003,20(2):7~10.
[10]陆宝仪,赖艳艳,李红.功能化碳纳米管的电化学性质及在6-巯基嘌呤分析检测中的应用[J].电化学,2009,15(1):67~72.
