正交设计试验优选去甲斑蝥素在大鼠肝细胞中代谢的影响因素Δ
2014-03-09王晓辉李光远陶遵威李毅敏天津市医药科学研究所天津300020
王晓辉,高 萍,李光远,王 瑛,陶遵威,李毅敏(天津市医药科学研究所,天津 300020)
去甲斑蝥素(Norcantharidin,NCTD)是斑蝥素的衍生物。与斑蝥素相比,其对泌尿系统的刺激性显著降低,并具有独特的升高白细胞总数的作用,也是我国首先合成的新型抗肿瘤药物[1]。其衍生物众多而且很多衍生物都表现出抗肿瘤活性[2],其新型制剂研发工作也取得一些进展[3]。但由于NCTD 自身化学性质活泼、代谢快速以及代谢产物的复杂性,导致其代谢机制和代谢物的深入研究非常困难,限制了NCTD开发应用。
利用细胞株对药物进行代谢的研究方法可以排除体内因素的干扰,为整体药物研发提供可靠的试验数据。对体内代谢率低、毒性大以及缺少灵敏检测方法的药物来说,细胞代谢法更是首选的研究方法。由于细胞对药物的代谢受到细胞接种密度、给药浓度等多种因素影响,所以本文设计正交设计试验研究NCTD 在大鼠肝细胞(Buffalo rat liver,BRL)中代谢的相关影响因素,以提高代谢效率、获得最佳培养方案,为后续及相关研究提供科学依据。
1 材料
1.1 仪器
GC-17A 气相色谱仪[中国(上海)岛津有限公司];Infinite M200酶标仪[帝肯(上海)贸易有限公司];Legend Micro17R高速离心机(美国Therme Electron Corportion公司,离心半径:78 mm);TMS-PH-3倒置显微镜[尼康仪器(上海)有限公司]。
1.2 药品与试剂
NCTD 对照品(中国食品药品检定研究院,批号:100414-200501,纯度:100%);NCTD原料药(南京景竹生物科技有限公司,批号:JZ130421A,纯度:99%);达尔伯克改良伊格尔(DMEM)培养基(美国Gibco公司,批号:12800-027)。
1.3 细胞
大鼠BRL细胞(国家科学院典型培养保藏委员会细胞库)。
2 方法与结果
2.1 检测NCTD对BRL细胞的半数抑制浓度(IC50)
参考相关资料[4],将BRL 细胞按照25 000、50 000、75 000个/ml 3 种密度进行接种,用培养液将NCTD 配成10.0、7.14、5.10、3.64、2.60、1.86、1.33、0.949、0.678、0.484 μg/ml 10 个质量浓度,培养48 h,用MTT法检测细胞抑制率,重复3次。结果3种细胞接种密度下的IC50分别为(6.04±0.22)、(5.82±0.31)、(6.07±0.18)μg/ml,其平均值5.98 μg/ml即为NCTD对BRL细胞的IC50。
2.2 检测NCTD相对含量的方法
2.2.1 色谱条件。色谱柱:DM-1 毛细管色谱柱(30 m×0.25 mm,0.25 μm);流动相:氮气,流速:1 ml/min;检测器:氢离子火焰检测器(FID);柱温:200 ℃;进样口温度:250 ℃;检测器温度:280 ℃;无分流;进样量:1 μl。
2.2.2 样品的处理。收集各组培养液,加入10%三氯乙酸[10%三氯乙酸:培养液(0.6 ∶1)]除蛋白,以10 000 r/min离心5 min,取上清液浓缩干燥,将固体干燥物用200 μl水定容,静置30 min充分溶解,取上清液滤过作为待测样品。
2.2.3 方法专属性考察。分别将NCTD对照品、空白培养液、培养液+NCTD对照品,经“2.2.2”项下处理后,按“2.2.1”项下色谱条件检测,记录色谱。结果空白培养液对NCTD 色谱峰几乎无干扰,色谱图见图1。
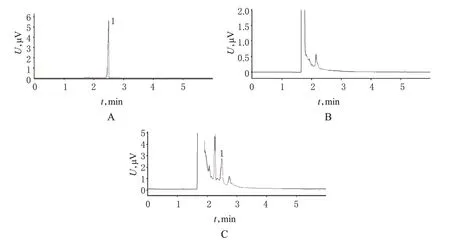
图1 气相色谱图A.对照品;B.空白培养液;C.培养液+NCTD对照品;1.NCTDFig 1 GC chromatogramsA.substance control;B.blank culture medium;C.culture medium sample+NCTD control;1.NCTD
2.2.4 精密度试验。配制质量浓度分别为0.200 0、0.800 0、3.200 μg/ml 的NCTD 培养液样品,按“2.2.2”项下方法处理后进样。同日内测定5次,得日内RSD为(2.58±0.37)%;每日测定1次,连续测定5 d,得日间RSD为(5.10±0.55)%。
2.2.5 检测限考察。以信噪比为3 时,NCTD 的检测限为10 ng/ml。
2.3 正交设计试验优选最优培养条件
根据“2.1”项下方法与结果,参考相关文献[5-6],选取细胞接种密度(A)、给药浓度(B)、培养时间(C)为考察因素。因素A、C 的考察水平参考文献选取3 个水平;因素B 考察水平以NCTD 对BRL 细胞的IC50为参考,选取3 个水平,具体数值见表1。
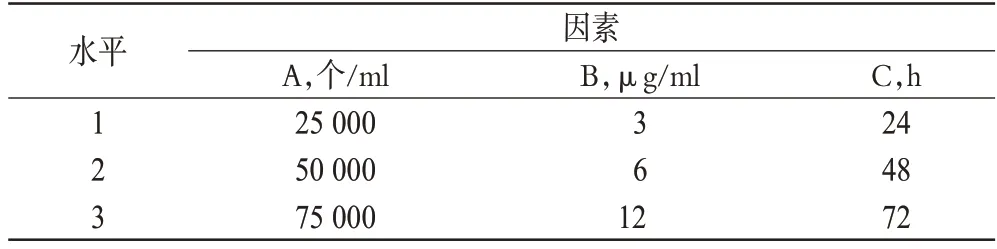
表1 正交设计试验因素与水平Tab 1 Factors and levels of orthogonal test
按照4因素3水平L9(34)正交试验表进行试验,培养体系置于37 ℃、5%二氧化碳及饱和湿度条件下培养相应时间,以培养体系中NCTD的相对含量的峰面积为评价指标。正交设计试验结果及极差分析见表2,方差分析结果见表3。
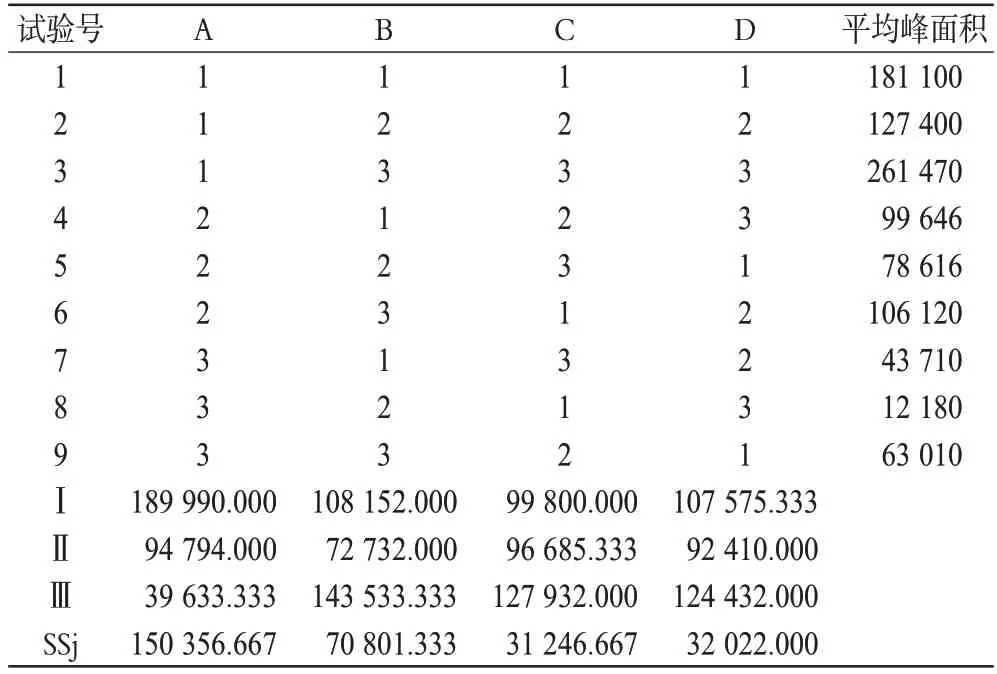
表2 正交设计试验结果与极差分析(n=3)Tab 2 Results of orthogonal test and analysis of range(n=3)
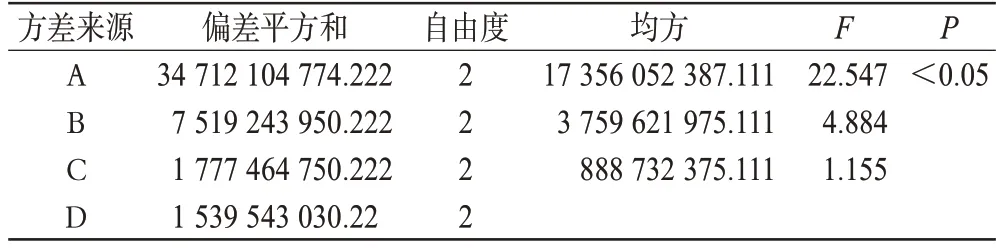
表3 正交设计试验的方差分析Tab 3 Results of orthogonal test and analysis of variance
由表2、表3可知,各因素对培养体系中NCTD相对含量的影响顺序为A>B>C。其中,因素A 有显著性影响(P<0.05),选择水平3;而因素B、因素C 各水平间差异不大,从培养效率方面考虑,均选择水平2。故最优培养条件为A3B2C2,即接种密度为75 000个/ml,给药浓度为6 g/ml,培养时间为48 h。根据最优条件培养,试验重复3次,检测其体系中NCTD的相对含量的峰面积为10 567±664。
3 讨论
有资料报道NCTD 对人肝癌细胞Bel-7402、HL-7702 的IC50分别为18.84、22.66 μg/ml[7],对海拉癌细胞Hela 的IC50为261 μg/ml[8],对人胃癌细胞BGC-823的IC50为7.85 μg/ml[9]。本研 究 中NCTD 对BRL 细 胞 的IC50为5.98 μ g/ml,由 此 表 明NCTD对不同细胞株的抑制率是不一样的,所以在对不同细胞株试验研究时,应该对其抑制率进行研究。通过预试验,笔者将NCTD对BRL细胞IC50的0.5、1、2倍作为正交设计试验的给药浓度,即3、6、12 μg/ml。
由于NCTD分子结构中不含共轭结构,无强生色团,导致NCTD 无紫外特征吸收峰,所以使用紫外检测法进行体内药动学研究和体外代谢产物研究时会受较多干扰,达不到检测要求。本试验建立气相色谱法测定培养基中NCTD 药物浓度,并对该方法进行方法学考察研究。结果表明,该方法符合生物样品的分析要求,可为NCTD的体内外药动学研究、临床给药监测以及开发高效低毒的NCTD衍生物和新剂型等提供简单快捷的检测方法。体外代谢是利用各种体外代谢模型对候选化合物进行高通量筛选,可以对代谢过快或生成毒性代谢物的候选化合物进行结构改良,也可以通过模拟或合成活性代谢物的结构得到新的候选化合物。与体内代谢研究相比,体外代谢研究可在新药研发早期利用候选化合物的体外代谢参数合理预测候选化合物的体内药动学行为,指导后期药效学、药动学以及安全性评价的模型选择,缩小体内研究的筛选范围,具有广阔的应用前景[10]。
通过正交设计试验研究发现,接种密度对以代谢快慢具有显著的影响且影响最大;而给药浓度和培养时间没有显著性,通过直观分析看到给药浓度的影响次之,培养时间影响最小。当接种密度为75 000个/ml、给药浓度为6 g/ml、培养时间为48 h时,在培养液中剩余NCTD含量是最低的,说明在此条件下,NCTD 在BRL 细胞中代谢效率最高。NCTD 在BRL 细胞中代谢最优培养条件的研究结果可为NCTD体外代谢产物的相关研究提供可靠的科学数据和必要的前提条件。
[1]余涛,刘曼曼,侯风刚,等.去甲斑蝥素抗肿瘤分子机制研究进展[J].辽宁中医药大学学报,2012,14(4):73.
[2]李贺敏,彭国平,陈农,等.新型斑蝥素羧酸衍生物的合成及其抗癌活性[J].合成化学,2013,21(5):518.
[3]牛砚涛,武冬雪,董文娜,等.去甲斑蝥素新型制剂研究进展[J].中国药学杂志,2013,48(9):663.
[4]魏伟,吴希美,李元建.药理实验方法学[M].4版.北京:人民卫生出版社,2010:1 568-1 569.
[5]杨慈清,李小英.Hepal-6细胞的最佳培养条件研究[J].安徽农业科学,2010,38(28):15 507.
[6]王爽,梁伟伶,刘斯斯,等.正交试验法优选HepG2 细胞最佳培养条件[J].中国现代医学杂志,2007,17(13):1 603.
[7]胡玮,章良,王钦,等.去甲斑蝥素N-乳糖酰壳聚糖纳米粒的肝靶向抗肿瘤药效学评价[J].中国新药杂志,2010,19(19):1 814.
[8]刘洪月,杨红,吴秀凤,等.叶酸修饰去甲斑蝥素隐形泡囊的制备、表征及体外药效学评价[J].中国新药杂志,2013,22(18):2 174.
[9]王晨宇,李猛,王天阳,等.DHA 联合去甲斑蝥素对人胃癌细胞BGC-823增殖及凋亡的影响[J].世界华人消化杂志,2013,21(11):1 008.
[10]吴慧,彭英,孙建国,等.体外代谢在新药早期评价中的应用与发展[J].药学学报,2013,48(7):1 071.
