蘘荷红色素分离纯化及喷雾干燥工艺优化
2014-03-08卜晓英卜小庆
卜晓英,卜小庆,杨 勇
(1.吉首大学 林产化工工程湖南省重点实验室,湖南 张家界 427000;2.张家界市敦谊小学,湖南 张家界 427000;3.张家界市民族中学,湖南 张家界 427000)
蘘荷红色素分离纯化及喷雾干燥工艺优化
卜晓英1,卜小庆2,杨 勇3
(1.吉首大学 林产化工工程湖南省重点实验室,湖南 张家界 427000;2.张家界市敦谊小学,湖南 张家界 427000;3.张家界市民族中学,湖南 张家界 427000)
研究分离纯化及喷雾干燥化蘘荷红色素的工艺条件。比较10 种大孔吸附树脂对红色素的静态、动态吸附与解吸效果,红色素纯化液经真空浓缩后用喷雾干燥法制备红色素的粉末。结果表明:LSA-21大孔吸附树脂分离纯化蘘荷红色素效果好,其工艺条件为上柱液pH 5.0、上样液质量浓度3.85 mg/mL、吸附流速 2 BV/h,以酸性蒸馏水为解吸剂,解吸流速3 BV/h;喷雾干燥工艺条件为加入待喷液质量 分数2%的可溶性淀粉,调整可溶性固形物质量分数 达到 12%~14%、进料速率3.0~4.0 kg/h、进口风温度 174~177 ℃、出口风温度 65~71 ℃、排风速率 0.34~0.38 m3/min、雾化压强100 kPa。红色素粉末经薄层层析色谱与高效液相色谱检测均由3 种单体构成。
喷雾干燥;大孔吸附树脂;红色素;薄层层析色谱;高效液相色谱
蘘荷(Zingiber mioga Rosc.),俗称野姜,为姜科姜属多年生食药同源蔬菜[1],而食用天然色素大多为花青素类、黄酮类、类胡萝卜素类化合物,对人体健康没有不良影响,安全性高,而且许多还具有营养、保健及药效作用[2-4]。而合成色素对人体有一定的危害性,有的甚至有致癌作用,因此,不少合成色素在各国允许使用的程度被大大限制,尤其是在食品、医药和化妆品行业中,越来越多的国家开始禁止使用合成色素[5-7]。到目前为止,我国允许使用的食用合成色素有:日落黄、柠檬黄、苋菜红、胭脂红、赤藓红、诱惑红、新红、亮蓝、靛蓝和它们各自的色淀以及酸性红、β-胡萝卜素、氧化铁黒(红)、叶绿素铜钠和二氧化钛等,并对其使用范围和最大使用量作了严格的限制[8-10]。利用食用植物提取天然色素符合消费者对天然健康食品趋势的要求,受到消费市场青睐,因此用食物提取天然色素来取代合成色素已成必然趋势[11-13]。
在前期微波烫漂辅助提取蘘荷中红色素[14]的基础上,研究蘘荷红色素提取液经旋转真空浓缩后LSA-21大孔吸附树脂分离纯化红色素的效果[15-17],以及分离纯化后红色素溶液喷雾干燥法制备红色素粉末的优化条件。尚未见对蘘荷红色素大孔吸附树脂分离纯化和喷雾干燥制备红色素粉末的报道,因此本实验以武陵山区蘘荷红色素为研究对象,利用LSA-21大孔吸附树脂对红色素进行分离纯化并研究用小型GB-22喷雾干燥器制备红色素粉末的工艺条件,为武陵山区蘘荷红色素开发利用提供节能、环保性工业化生产工艺提供理论依据。
1 材料与方法
1.1 材料与试剂
蘘荷采集于湖南省张家界山区沙提蘘荷种植基地,洗去泥沙,取苞片,沥干水分,置于-4 ℃冰箱中保存备用;大孔吸附树脂 LX-5、D101、AB-8、LSA-10、LSA-21、LSA-40、XDA-1、LX-17、LSA-7、XDA-7 安徽三星树脂科技有限公司;硅胶G 青岛海洋化工有限公司;羧甲基纤维素钠(carboxymethylcellulose sodium,CMCNa) 上海德津实业有限公司。
丙酮、甲醇、无水乙醇、95%乙醇、乙酸乙酯、石油醚、乙酸、甲酸、36% HCl溶液、2% NaOH溶液、NaCl均为分析纯;酸性乙醇用无水乙醇与质量分数36% HCl溶液配制,且现用现配,酸性蒸馏水用36% HCl溶液调pH值至4.5~5.5;CMC-Na(质量分数1%)溶液现用现配。
1.2 仪器与设备
AEG-220电子分析天平、RE540-AW旋转蒸发仪、LC-20AT型高效液相色谱仪 日本岛津公司;D8023CTL-K4微波炉 格兰仕集团;UV3900紫外-可见分光光度计 日本日立公司;LGJ-1真空冷冻干燥仪 西安中诺尔仪器有限公司;HH-6恒温水浴锅 富华仪器公司;MHA恒温电热套 北京科永兴仪器有限公司;SHE-D(Ⅲ)循环水式真空泵 予华仪器有限责任公司;FD-230红外水分仪 日本KETT公司;MDF-292AT超低温冰箱 日本三洋公司;DF42恒温干燥箱、DN-63烘箱、GB-22小型喷雾干燥器 日本雅马拓公司;HM-20S便携pH计 日本TOA公司。
1.3 方法
1.3.1 蘘荷红色素的提取
取蘘荷新鲜材料100 kg按文献[14]所选提取条件,分20 批次经微波烫漂处理后,用体积分数60%的酸性乙醇按料液比1∶60(g/mL)、温度 55 ℃ 、时间40 min进行红色素提取。每份提取液用旋转蒸发仪在50 ℃、40 r/min的真空条件下浓缩,得20 份500 mL浓缩液待用。
1.3.2 大孔吸附树脂的选择
1.3.2.1 大孔吸附树脂预处理
称取10 种大孔吸附树脂各10.00 g,先以蒸馏水浸泡12 h,再用质量分数40% 的NaCl 溶液浸泡12 h,然后用质量分数2% NaOH溶液搅拌浸泡5 h,水洗至中性,再用质量分数5% HCl溶液搅拌浸泡5 h,水洗至中性,最后用体积分数70%乙醇浸泡12 h,水洗至无絮状物,去离子水浸泡备用。
1.3.2.2 大孔吸附树脂静态吸附
将10 种湿树脂自然风干,红外水分仪测各自水分含量,按比例称相当干质量3.00 g大孔吸附树脂于100 mL锥形瓶中,分别加入20 mL已浓缩的蘘荷红色素溶解液,搅匀后静置,室温条件下静态交换6 h过滤,测定吸附前、后红色素溶液535 nm波长处的吸光度,以红色素浓缩原液质量分数为1计算出各树脂对红色素的吸附量与吸附率。
1.3.2.3 大孔吸附树脂静态解吸
将1.3.2.2节吸附了蘘荷红色素的大孔吸附树脂分别置于20 mL体积分数为70%的酸性乙醇中,室温条件下静置解吸6 h,滤液用紫外分光光度计测其535 nm波长处的吸光度,计算出各树脂对红色素的解吸率。
1.3.3 解吸剂的选择
称取处理好的LSA-21树脂3.00 g(相当干质量)共6 份,分别加入20 mL红色素浓缩液,6 h后过滤,用50 mL醇体积分数60%的乙醇、酸性乙醇、甲醇、丙酮、蒸馏水和酸性蒸馏水各解吸一组已吸附的树脂,测各解吸液535 nm波长处的吸光度。
1.3.4 不同质量浓度色素液对LSA-21树脂吸附的影响
称取5 份处理好的LSA-21树脂3.00 g(相当干质量),分别加入20 mL上述解吸液经旋转真空浓缩、冷冻干燥成粉末的红色素所配成质量浓度为7.85、3.85、2.56、1.18、0.876 mg/mL的红色素溶液,置50 ℃恒温水浴锅中,每隔1 h取样检测溶液中红色素质量浓度,按下式计算LSA-21树脂吸附红色素的量。

式中:q为树脂吸附量/(mg/g);C0为溶液初始质量浓度/(mg/mL);Ct为t时刻时质量浓度/(mg/mL);V为溶液体积/mL;m为树脂质量/g;n为树脂含水量/%。
1.3.5 上柱液pH值对LSA-21树脂吸附的影响
称取6 份已处理好的LSA-21树脂各3.00 g(相当干质量),加入质量浓度为3.85 mg/mL的溶液,pH值分别为3、4、5、6、7、8的红色素粉末液20 mL,于50 ℃恒温水浴锅中静置6 h,测滤液535 nm波长处的吸光度并计算树脂吸附量。
1.3.6 LSA-21树脂的动态吸附与解吸实验
取20.0 g LSA-21树脂(3 份)按湿法装柱,分别用2、3、4 BV/h的流速对红色素溶液进样,按每管5 mL收集流出液,稀释至10 mL测流出液535 nm波长处的吸光度,至流出液质量浓度与进样质量浓度一致来检测LSA-21树脂动态吸附量;然后用酸性蒸馏水分别以2、3、4 BV/h的流速对其进行解吸,按每管5 mL收集解吸液,稀释至10 mL,测定各管解吸液535 nm波长处的吸光度,以红色素的吸光度代替其含量进行比较分析。
1.3.7 蘘荷红色素解吸液喷雾干燥条件的优化[18-20]
为探索喷雾干燥最佳工艺参数,在雾化压强确定为100 kPa的情况下,本研究选用A进口风温度、B出口风温度、C进料速率、D排风速率、E可溶性淀粉添加量、F待喷雾溶液质量分数 6 个影响因素,按文献[20]设计正交试验方案进行喷雾干燥条件优化,每个处理重复3 次,每次500 mL。因素水平安排见表1,试验设计及结果见表2。

表1 喷雾干燥正交试验因素水平Table 1 Factors and levels used in orthogonal array design for spray drying
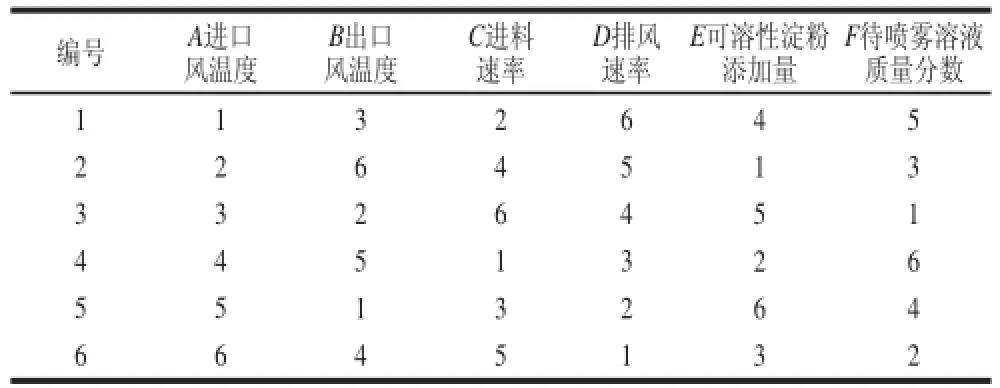
表2 红色素溶液喷雾干燥正交试验设计Table 2 Orthogonal array design scheme for spray drying
按选择的喷雾干燥条件对10.0 kg蘘荷样品提取液经真空浓缩与大孔吸附树脂吸附分离纯化后的溶液进行喷雾干燥,在控制室内相对湿度低于65%时,将色素粉末过200 目筛后密封于干燥器中保存待测。
1.3.8 薄层层析色谱(thin layer chromatography,TLC)分析
1.3.8.1 硅胶薄板的制备
将1 份硅胶G和3 份CMC-Na溶液在研钵中研磨混匀,去除表面气泡,然后将其均匀涂布(厚度为0.25 mm)于玻璃平板上,置水平台上室温晾干,110 ℃活化30 min,置密封干燥剂中保存备用。
1.3.8.2 蘘荷红色素的层析检测
称取蘘荷红色素粉末3.85 g,用酸性乙醇溶解并定溶于1 000 mL容量瓶中,得3.85 mg/mL红色素溶液,用该溶液点样50 μL于硅胶G薄层板上,在展层剂正丁醇-乙酸-水(4∶1∶2,V/V)中展开。
1.3.9 高效液相色谱(high performance liquid chromatography,HPLC)分析
色谱条件:SpheriSorb ODS C18(250 mm×4.6 mm,5 μm)色谱柱,柱温为室温,流速为1.00 mL/min,进样量20 μL,质量浓度3.85 mg/mL,流动相为甲醇-水-甲酸(39.5∶60∶0.5,V/V),检测器为紫外吸收检测器。
2 结果与分析
2.1 大孔吸附树脂的选择
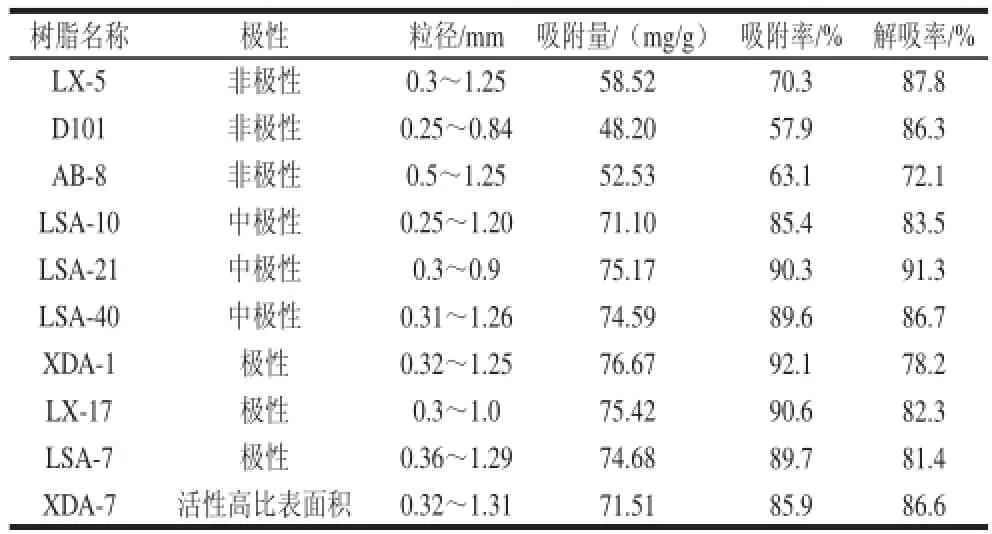
表3 树脂的选型Table 3 Adsorption and desorption performance of ten kinds of macroporous reessiinn
由表3可知,LSA-21、LSA-40两种中极性树脂及XDA-1、LX-17、LSA-7三种极性树脂对蘘荷红色素的吸附能力较强;LSA-21型中极性树脂及LX-5型非极性树脂对蘘荷红色素的解吸能力较强;从吸附与解吸效果来看,LSA-21的吸附率与解吸率均较大,综合考虑,选择LSA-21为蘘荷红色素的大孔吸附树脂。
2.2 解吸剂的选择
用体积分数60%的乙醇、酸性乙醇、甲醇、丙酮、蒸馏水和酸性蒸馏水解吸已吸附蘘荷红色素的LSA-21树脂,解吸液的535 nm波长处吸光度见表4,乙醇及酸性乙醇的解吸效果较好,但考虑到工业生产的成本以及喷雾干燥时乙醇易爆炸的特性,同时酸性蒸馏水与乙醇的解吸效果相差不大,因此本研究选择酸性蒸馏水作为解吸剂。

表4 不同洗脱液中红色素的测定结果Table 4 Effect of different solvents on the desorption efficiency of red pigment
2.3 不同色素质量浓度对LSA-21树脂吸附红色素的影响
LSA-21树脂对质量浓度分别为7.85、3.85、2.56、1.18、0.876 mg/mL红色素的吸附效果见图1,显示LSA-21树脂对红色素吸附起始阶段呈线性加速,随后逐渐趋于平缓,最后达到吸附平衡。吸附速率与溶液质量浓度密切相关,溶液质量浓度为7.85 mg/mL时树脂吸附平衡所需时间约1 h到质量浓度0.876 mg/mL平衡所需时间约6 h不等,因此初始质量浓度选择为3.85 mg/mL。

图1 不同质量浓度红色素溶液的吸附量动态变化图Fig.1 Dynamic adsorption curves of red pigment with different concentrations
2.4 上柱液pH值对树脂吸附的影响

图2 上柱液不同pH值对吸附量的影响Fig.2 Effect of sample pH on adsorption quantity
由图2可见,当上柱液pH值为4~5时红色 素的吸附效果最好,上柱液的pH 5.0时达到高点,而随着上柱液pH值的继续升高,吸附率明显下降,但树脂上仍有一定的吸附量,因此选择上柱液pH值为5.0。
2.5 吸附流速对树脂动态吸附效果的影响

图3 不同流速条件下色素在树脂上的动态吸附曲线Fig.3 Effect of sample loading flow rate on adsorption efficiency
当用质量浓度为3.85 mg/mL的红色素溶液分别以 2、3、4 BV/h流速进样时,各进样液前20 管流出液中红色素质量浓度基本一致(图3),而收集时间差异明显。收集21~40 管流出液时,红色素质量浓度在流出液中增大。至流出液质量浓度与进样质量浓度一致时各进样流速平均需收集120、103、92 管,耗时平均分别为3.2、3.0、2.5 h,综合考虑选择进样流速为2 BV/h。
2.6 解吸流速对解吸效果的影响
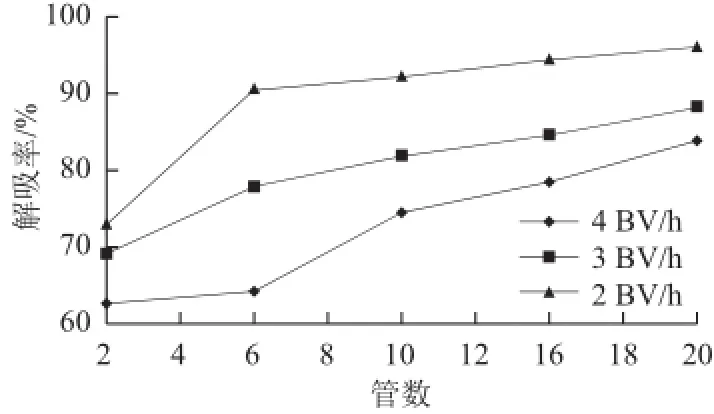
图4 解吸流速对树脂上红色素解吸的影响Fig.4 Effect of desorbent flow rate on desorption efficiency
分别采用不同流速对已吸附色素的树脂进行解吸,结果如图4所示。解吸流速为2、3、4 BV/h时,开始洗脱时洗脱效果相差较大,即当洗脱液流速为4 BV/h时,开始阶段解吸效果明显较弱,而2 BV/h流速的解吸效果较好(图4),虽然解吸流速越慢效果越好,但太慢又会使工作周期延长,综合考虑,选择解吸液流速为3 BV/h。
2.7 喷雾干燥优化结果
蘘荷红色素溶液喷雾干燥正交试验结果以喷雾干燥制品的含水量、溶解时间、红色素在水溶液中的溶解性和粉末的吸湿性为检验指标,各指标按文献[21]的方法测定,对各因素进行综合考察,选出蘘荷红色素溶液喷雾干燥的优化试验条件,3 次平行结果见表5。

表5 红色素溶液喷雾干燥正交试验结果Table 5 Results of the orthogonal array design for spray drying
运用文献[20]对正交试验分析,对表5的试验结果结合实验仪器性能进行综合评选,得出蘘荷红色素溶液喷雾干燥的优化实验条件如下:加入待喷液质量分数2%的可溶性淀粉,用以调整其可溶性固形物质量分数达到12%~14%;进料速率3.0~4.0 kg/h;进口风温度174~177 ℃;出口风温度65~71 ℃;排风速率0.34~0.38 m3/min;雾化压强100 kPa。
2.8 薄层层析及高效液相色谱分析
蘘荷红色素在展层剂中分离结果见图5,经LSA-21树脂分离纯化后的蘘荷红色素经薄层层析出现3 个分离点,检测与计算三点的比移值(Rf)分别为0.285、0.335、0.449,据此可知该红色素由3 个组分构成。

图5 薄层层析图谱Fig.5 TLC profile

图6 高效液相色谱图谱Fig.6 HPLC chromatogram
按上述HPLC色谱条件进行紫外检测器的检测其结果见图6,经LSA-21纯化后的蘘荷红色素的HPLC检测时出现3 个波峰,可见该红色素溶液由3 个组分构成。由薄层层析与高效液相色谱检测结果可知LSA-21树脂对蘘荷红色素的分离纯化较好。
3 结 论
本研究通过对10 种大孔吸附树脂对蘘荷红色素的静态吸附与解吸、动态吸附与解吸实验,研究各大孔吸附树脂对红色素的分离纯化效果。结果LSA-21树脂对蘘荷红色素分离纯化效果最佳,分离纯化时上柱液pH 5.0、上样液质量浓度3.85 mg/mL、吸附流速2 BV/h,以酸性蒸馏水为解吸剂,解吸液流速3 BV/h。
将可溶性淀粉按质量分数2%加入到红色素浓缩液中,充分搅匀,去除杂质沉淀,使可溶性固形物含量达到12%~14%。通过正交试验研究了喷雾干燥的最佳工艺条件:进料速率3.0~4.0 kg/h、进口风温度174~177 ℃、出口风温度65~71 ℃、排风速率0.34~0.38 m3/min、雾化压强100 kPa;按以上条件对10.0 kg蘘荷样品提取液经真空浓缩与大孔吸附树脂吸附分离纯化后的溶液进行喷雾干燥,喷雾干燥所得红色素粉末经检测各项指标都达到或超过了文献[15]中的各项指标,通过薄层层析与HPLC法检验了LSA-21分离纯化后喷雾干燥成粉末的蘘荷红色素,显示该红色素均由3个组分构成。因此LSA-21树脂完全适合蘘荷红色素的分离纯化,经检测喷雾干燥所得红色素粉末含水量约4.25%、在水中溶解时间约148s、溶解性0.719、色价13.17、吸湿性0.069 3,其微生物的含量远低于国家标准(细菌总数(个/g)<100、大肠杆菌(个/g)<20、致病菌未检出),说明此喷雾干燥法完全适宜于工业化生产。
[1] 吴德邻. 中国植物志[M]. 北京: 科学出版社, 1981: 140.
[2] 魏丽, 童军茂. 大孔树脂纯化向日葵籽壳红色素的研究[J]. 食品工业科技, 2010, 31(6): 263-266.
[3] 刘伟, 黄立新, 张彩虹. 天然栀子黄色素的低温真空干燥研究[J].林产化学与工业, 2011, 31(1): 57-62.
[4] ARAPITSAS P, SJOBERG P J, TURNER C. Characterisation ofanthocyanins in red cabbage using resolution liquid chromaigraphy coupled with photodiode array detection and electrospray ionization-linear ion trap mass spectromery[J]. Food Chemistry, 2008, 109(1): 219-226.
[5] MEKKAWY H A, ALI M O, El-ZAWAHRY A M. OP3A18—Toxic effect of synthetic and natural food dyes on renal and hepatic functions in rats[J]. Toxicology Letters, 1998, 95(S1): 155.
[6] PAZMIÑO-DURÁN E A, GIUSTI M M, WROLSTAD E, et al. Anthocyanins from Oxalis triangularis as potential food colorants[J]. Food Chemistry, 2001, 75(2): 211-216.
[7] 杨青珍, 王锋, 孙元琳. 甜樱桃果实红色素的提取和稳定性研究[J].食品科学, 2010, 31(4): 120-122.
[8] 刘成梅, 游海. 天然产物有效成分分离与应用[M]. 北京: 化学工业出版社, 2003: 442.
[9] 胡金奎, 戴军, 张九勋, 等. 树脂法分离纯化桑葚花色苷[J]. 食品与发酵工业, 2012, 38(8): 190-196.
[10] 丁成翔, 代汉慧, 陈冬东. 六种着色剂毒性研究进展[J]. 检验检疫学刊, 2009, 19(2): 70-73.
[11] 钱疆, 杨方, 陈弛, 等. 超高效液相色谱飞行时间质谱测定食品中36 种合成色素[J]. 食品科学, 2013, 34(6): 215-218.
[12] 董爱文, 唐纯翼, 向中, 等. HPD-600树脂吸附和分离爬山虎色素及色素的理化性质研究[J]. 食品科学, 2004, 25(4): 74-80.
[13] 许立松, 马银海. 大孔树脂吸附法提取玫瑰茄红色素[J]. 食品科学, 2009, 30(12): 120-122.
[14] 卜晓英, 唐克华, 陈晓华, 等. 微波烫漂蘘荷苞片后红色素提取工艺条件的研究[J]. 食品工业科技, 2012, 33(21): 227-230.
[15] 赵慧芳, 李维林, 王小敏, 等. 黑莓果实色素纯化及干燥工艺研究[J].食品科学, 2009, 30(12): 35-39.
[16] 刘晶晶, 刘进前, 王雪锋, 等. 树脂法纯化鸭血糯色素的研究[J]. 食品科学, 2011, 32(12): 156-159.
[17] 刘广文. 喷雾干燥[M]. 北京: 化学工业出版社, 2005: 58-69.
[18] SEDA E, YURDAGEL U M I. Croencapsulation of anthocyan in pigments of black carrot (Daucus carota L.) by spray drier[J]. Journal of Food Engineering, 2007, 80: 805-812.
[19] RODRÍGUEZ-HERNÁNDEZ G R, GONZÁLEZ-GARCÍA R, GRAJALES-LAGUNES A, et al. Spray drying of cactus pear juice (Opuntia streptacantha): effect on the physicochemical properties of powder and reconstituted product[J]. Drying Technology, 2005, 23(4): 955-973.
[20] 方开泰. 均匀设计[J]. 战术导弹技术, 1994, 3(1): 55-56.
[21] 董爱文, 卜晓英, 李悦丰. 喷雾干燥法制备爬山虎色素粉末工艺条件研究[J]. 食品科学, 2010, 31(2): 6-9.
Separation and Purification by Macroporous Resin, and Spray Drying of Red Pigment from Zingiber mioga Rosc.
BU Xiao-ying1, BU Xiao-qing2, YANG Yong3
(1. Forest Products Chemical Engineering Key Laboratory of Hunan Province, Jishou University, Zhangjiajie 427000, China; 2. Zhangjiajie Dun Yi Primary School, Zhangjiajie 427000, China; 3. Zhangjiajie Min Zu Middle School, Zhangjiajie 427000, China)
Objective: To investigate the separa tion and purification of red pigment from the bracts of Zingiber mioga Rosc. and the preparation of red pigment powder by spray drying. Methods: Comparison of ten kinds of macroporous resin was carried out for the static and dynamic adsorption and desorption of red pigment. The purified red pigment was vacuumconcentrated before spray drying. Results: LSA-21 macroporous resin was found to be the best sorbent for the purification of red pigment. The best results were obtained when the sample (3.85 mg/mL, pH 5.0) was loaded at a flow rate of 2 BV/h and the adsorbed red pigment was eluted with acidified distilled water at a flow rate of 3 BV/h. The purified pigment solution was added with 2% soluble starch a nd adjusted to a soluble solid content of 12%-14% prior to spray drying at a feeding rate of 3.0-4.0 kg/h, an air inlet temperature of 174-177 ℃, an air outlet temperature of 65-71 ℃, an exhaust velocity of 0.34–0.38 m3/min, and an atomization pressure of 100 kPa. The resulting powder consisted of three monomers as detected by high performance liquid chromatography (HPLC) and thin layer chromatograph (TLC). Conclusion: LSA-21 macroporous adsorption resin is applicable for separation and purification of red pigment from Zingiber mioga Rosc. and the optimized spray drying conditions are suitable for industrial production of red pigment powder from Zingiber mioga Rosc.
spray drying; macroporous resin; red pigment; TLC; HPLC
TS202.3
A
1002-6630(2014)22-0104-05
10.7506/spkx1002-6630-201422019
2014-03-24
张家界市科技局科技计划项目(2013YB26;2014ZK02);湖南省重点实验室——“林产化工重点实验室”开放基金资助课题(JDZ201404);湖南省科技厅科技计划项目(2013NK3078);生态旅游湖南省重点实验室开放基金资助课题(JDSTLY1403)
卜晓英(1971—),女,高级实验师,硕士,研究方向为药用植物及功能食品。E-mail:xyingbu@163.com
