非贵金属催化碱性硫离子-空气燃料电池
2014-03-04黄永茂张志艳程艳坤李永真张贺
黄永茂,张志艳,程艳坤,李永真,张贺
(河北化工医药职业技术学院化学与环境工程系,河北 石家庄 050026)
燃料电池由于能够将物质的化学能高效率地转化为电能,因而成为当前研究的热点之一。国内外学者相关研究工作主要集中在燃料的选取与催化剂的研究上[1-4]。理想的燃料电池应具有以下特性:①燃料来源广泛,价格低廉;②电化学活性高,使用的催化剂成本低;③产物对环境友好。氢-氧燃料电池因其高比能量密度成为理想的研究对象[1,5-6],然而,由于贵金属催化剂的高成本以及氢的存储运输问题,使得它在实用化过程中遇到了困难[7-8];以甲醇为代表的液体有机物燃料电池以其比能量高、便于运输等特点受到了青睐[9-10],但是贵金属催化剂的高成本以及甲醇渗透成为不可忽略的问题[11-12];硼氢化钠燃料电池继承了甲醇燃料的优点,并且在使用廉价催化剂的情况下表现出较高的电化学活性[13-15],因而也成为新兴的研究方向,但是由于燃料中的氢容易析出,导致了该项研究受到一定的阻碍[16-17]。在此基础上,对于不含氢的无机物盐燃料的探索成为当前研究的一个方向。
Bolmer[18]于 1966年以专利的形式提出在碱性条件下构建硫离子燃料电池的概念;Zito等[19]于1975年提出以硫化钠溶液作为燃料构建硫离子-重铬酸盐(或过氧化氢等)燃料电池,1996年Zito[20]又在研究空气电极的专利中建立起硫化钠-空气燃料电池模型。然而此后,硫化钠燃料电池就一直停滞在概念阶段,极少有文献报道相关的研究进展[21]。2012年樊玉欠等[22]进行了非贵金属催化的碱性硫离子燃料电池放电特性研究。以碱性硫化钠溶液作为燃料构建碱性硫离子-空气燃料电池具有以下优点:硫化钠来源广泛,成本廉价,并且便于运输;容易实现催化氧化过程,催化剂成本低;产物可回收利用并且具有商业价值,不会对环境产生污染;应用前景广泛,可用于天然气净化、污水处理等其他领域。基于以上优点,对硫化钠燃料电池进行基础性研究并且获得基础性数据是完全有必要的。
1 实验部分
1.1 仪器与试剂
CHI660A型电化学工作站(上海辰华仪器公司),Arbin电池测试仪(美国 Arbin公司),SCE参比电极(上海精密科学仪器有限公司);本文所用试剂均为分析纯;实验室用水为去离子水。
1.2 电极制备
粉末活性炭涂膏的制备:按比例(活性炭∶乙炔黑∶石墨=50∶15∶10)准确称量活性炭 0.5g,乙炔黑0.15g,石墨0.1g放入100m L小烧杯中,加入无水乙醇10m L,然后称量0.25g PTFE乳液(60%,质量分数)搅拌混合均匀,超声分散5m in,得到的膏状活性物质密封保存。其中,活性炭为电极活性物质,乙炔黑、石墨起导电作用,PTFE为黏结剂。涂膏电极的制备:用移液枪准确吸取膏状物30μL,均匀涂敷在已打磨抛光的石墨基体表面(膏状物质量为2mg),然后将电极置于60℃真空干燥箱中烘干,取出后浸到配置好的电解液中浸泡2h,待用。
1.3 电化学性能测试
三电极体系的建立:将制备的电极作为研究电极,多孔石墨电极作为对电极,饱和甘汞电极作为参比电极,参比电极与碱性硫化钠(Na2S)溶液通过饱和氯化钾盐桥连通构成三电极。实验所用电解液中KOH浓度均为1mol/L,硫化钠浓度根据实验需要进行配制。由于硫离子在电极表面上放电容易受扩散影响,如无特别说明,在实验中采用磁力搅拌器对溶液进行搅拌。
电池模型的建立及测试:将制备的膏状物涂覆到多孔导电基体上作为阳极,将含 La0.6Ca0.4CoO310%(质量分数)的催化层、镍网、气体扩散层用热压的方法制备成空气电极,以阳离子交换膜作隔膜所组装的单电池模型见图1[23]。阳极以1mol/L 的Na2S 和 1mol/L的KOH作为燃料,阴极为3mol/L的KOH电解液,流速为10m L/min。为了便于研究,实验采用搅拌代替流场以减小扩散的影响。单体电池的测试在Arbin电池测试仪上进行,在室温25℃,通过连续改变电池的外电阻(1000~10Ω)来获得电池的电压和相应的电流数据。
2 结果与讨论
2.1 碱性硫离子的电化学性能
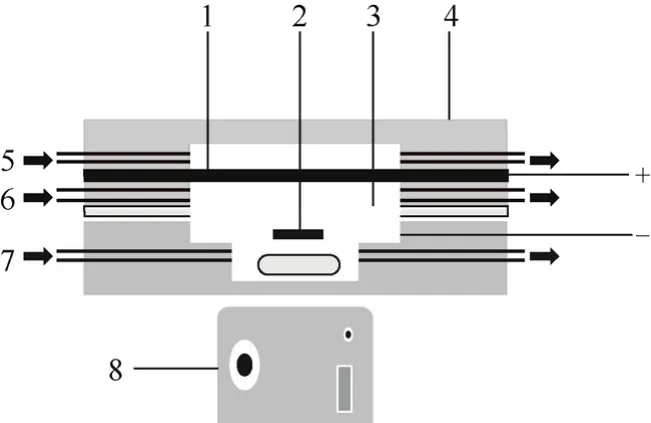
图1 碱性硫离子-空气燃料电池示意图
图2为电极在不同浓度碱性硫化钠溶液中开路电位随温度的变化曲线。当温度由 20℃升高至 50℃时,电极在硫化钠浓度 1.0mol/L、1.5mol/L、2.0mol/L的溶液中的电位分别由-0.717V、-0.757V、-0.764V向负方向变化至-0.781V、-0.801V、-0.808V,由此可见,不同硫化钠浓度下的电极开路电位随着温度的提高而向负方向变化的趋势是一致的。电极电位与温度的变化近似正比关系,由此计算出不同硫化钠浓度下电极电位随温度的变化速率分别为2.13mV/℃、1.47mV/℃、1.53mV/℃,这一结果说明电极电位在低硫化钠浓度下受温度的影响更为明显,当硫化钠浓度提高时,受硫离子活度及溶液黏度的影响,电极开路电位趋于一致。其次,温度一定时,随着硫化钠浓度的提高,电极电位向负方向变化率趋向减小,这主要是由于硫离子活度以及溶液黏度导致的。
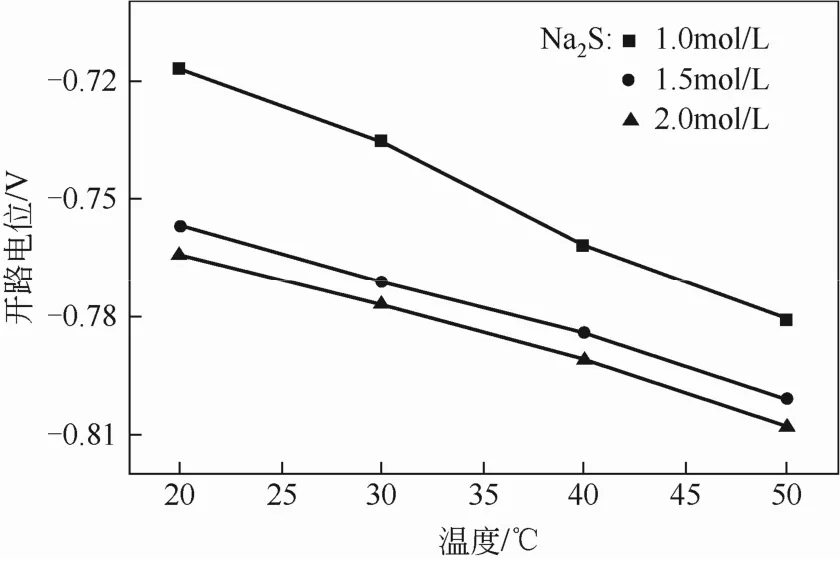
图2 电极在不同浓度的碱性硫化钠溶液中开路电位随温度变化的曲线
由此可以得出:①电极在碱性硫化钠溶液中有较负的开路电位,理论上可以以空气电极作为阴极构建燃料电池;②溶液中硫化钠的浓度以及体系温度对电极开路电位有较为明显的影响,根据实验需要适当地改变条件可以改善体系性能。
电极在不同硫离子浓度溶液中的极化曲线如图3所示,可以看出该体系具有稳定的放电平台,随着硫化钠浓度的提高,电位平台向负电位方向移动。相关文献[21]指出,在较低电位时,硫离子的放电反应为:
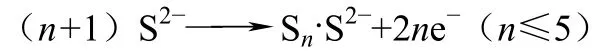
多硫离子的生成使得电极表面不会造成硫单质的积累而导致放电终止,因而对构建燃料电池是有利的。
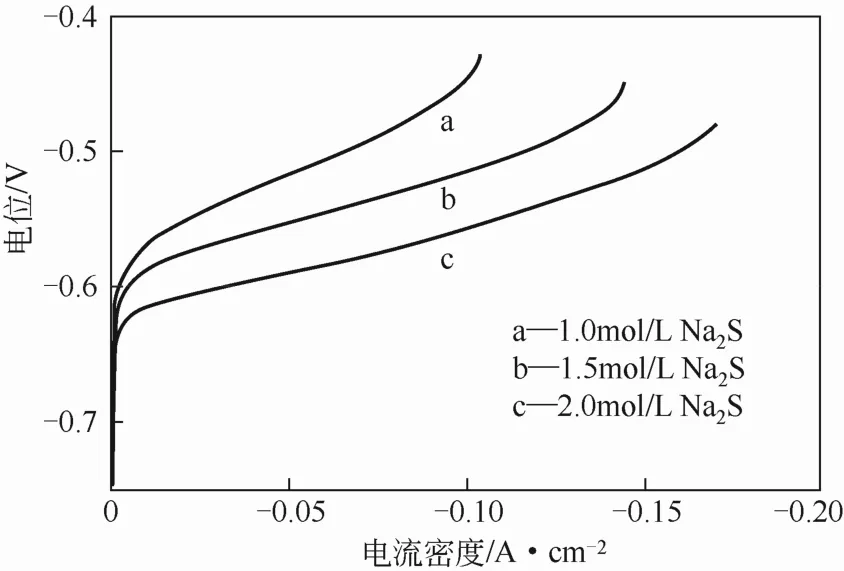
图3 活性炭电极在硫化钠溶液中的极化曲线
图4所示为电极在不同体系温度时的极化曲线,由曲线可以看出随着体系温度的升高,电极在溶液中的放电平台向负电位方向移动,并且具有稳定的放电平台,以上结果与前文中的测量结果是一致的。由此得出:①电极在碱性硫化钠溶液中具有较负(-0.6~-0.5V)的、稳定的放电平台,并且以活性炭作为催化材料表现出大电流放电特性;②溶液中硫化钠的浓度及体系温度对电极的放电平台有较为明显的影响,通过适当地改变条件,电极放电性能可以获得一定的改善。
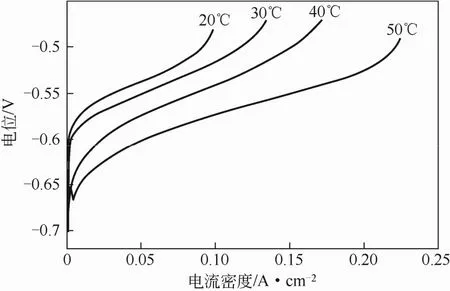
图4 活性炭电极在不同温度硫化钠溶液中的极化曲线
2.2 碱性硫离子-空气燃料电池的放电性能
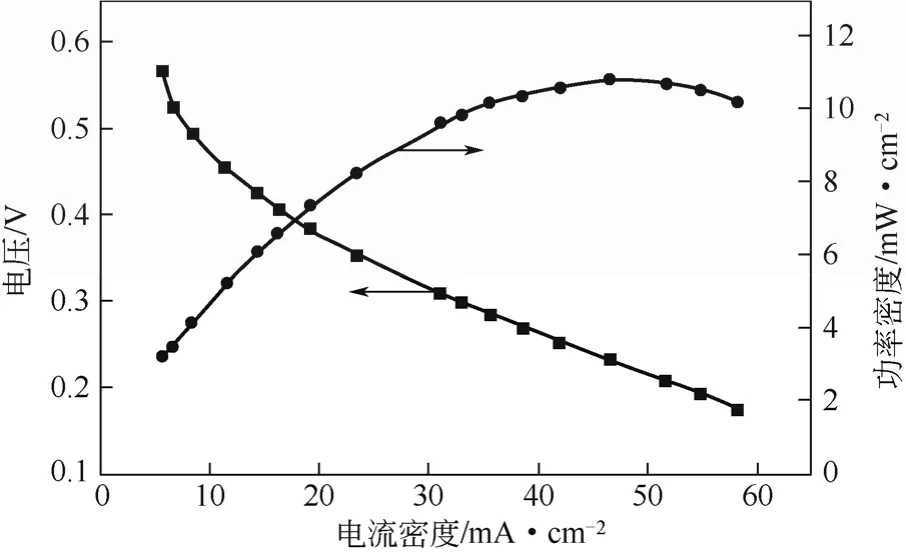
图5 碱性硫离子-空气燃料电池电压-功率密度-电流密度曲线
为了进一步测量电极在碱性硫化钠中的放电性能,将制备的阳极与空气电极组装成燃料电池进行测试,通过不断改变外路电阻得到的电压-功率密度-电流密度曲线如图5所示。燃料电池单体的开路电压为 0.68V,低于理论计算电压值,导致开路电压降低的原因可能在于氧的还原是高度不可逆的电极反应,其开路电位远比其平衡电位负。电池具有较为平稳的放电平台,在 0.24V电压下获得了11mW/cm2的最大功率密度,此时电池的电流密度为 46mA/cm2。这一结果充分证明了以碱性硫离子溶液作燃料构建燃料电池是可行的,并且以廉价的活性炭作电极材料获得了较高的功率密度和电流密度,与其他同类液体燃料电池相比,成本大大降低。在阳极不使用贵金属催化剂的情况下,放电性能同比表现更优,亦即更容易实现氧化过程。需要指出的是,实验中电池的电压降很大部分是由于空气电极极化所致,如果设法改善阴极性能,减小阴极极化,将获得更大的功率密度。
2.3 碱性硫离子放电过程的动力学
为了进一步深入探讨电极表面在硫化钠溶液中的动力学过程,采用循环伏安法在静止溶液中对三电极模型进行研究,在-1.0~0V(vs.SCE)的电位下测得的不同扫速下的循环伏安曲线如图6所示。从曲线中可以看出:①电位正扫和负扫分别出现了明显的氧化峰和还原峰;②氧化峰与还原峰电位差随着扫速的增大而迅速增大;③通过计算得到I阳极/ I阴极>1,由以上结果判断电极上发生的是准可逆的氧化还原反应。Zito等[19-20]在研究中发现硫离子与多硫离子之间的可逆转换可以应用于二次电池中。由以上推测碱性硫离子电极表面以及电池总反应为:
阳极 2(n+1)S2-—→ 2Sn·S2-+4n e-(n≤5)
阴极n O2+2n H2O +4n e-—→ 4n OH-
电池反应2(n+1)S2-+n O2+2n H2O—→2Sn·S2-+4n OH-
电池放电产物是多硫离子和碱液,分离后可回收单质硫。此外,峰值电流Ip对扫描速率的平方根v1/2作图得到的曲线为直线,由此判断出电极反应受到扩散的控制,因此如何在电池放电过程中通过流场或搅拌减小扩散的影响是应当注意的问题。
3 结 论
以粉末活性炭为电极材料,以碱性硫离子溶液为阳极燃料,以空气电极为阴极,构建了碱性硫离子-空气燃料电池。通过三电极模型以及电池的研究测试,能够得出以下结论。
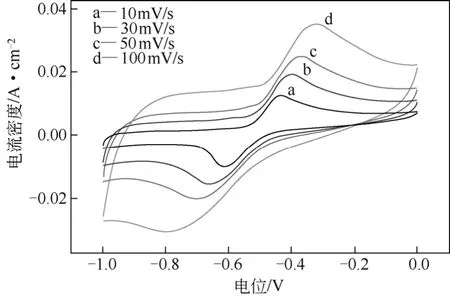
图6 活性炭电极在硫化钠溶液中的循环伏安曲线
(1)电极在碱性硫化钠溶液中有较负的开路电位,理论上可以以空气电极作为阴极构建燃料电池,电极在碱性硫化钠溶液中具有较负的(-0.6~-0.5V)、稳定的电位平台,并且以活性炭作为催化材料表现出大电流放电特性;溶液中硫化钠的浓度及体系温度对电极开路电位以及放电平台有较明显的影响,根据实验需要适当改变条件可以改善体系性能。
(2)通过单体电池测试获得了 11mW/cm2的最大功率密度,此时电池的电流密度为46mA/cm2,证明碱性硫离子燃料电池在不使用昂贵催化剂的情况下表现出良好的放电性能。这一结果充分证明了以碱性硫离子溶液作燃料构建燃料电池是可行的,并且以廉价的活性炭作电极催化材料获得了较高的功率密度和电流密度。在不使用贵金属催化剂的情况下,其放电性能同比其他液体燃料电池表现为更优。
(3)通过循环伏安研究判断电极上发生的是准可逆的氧化还原反应,并且推测了电极/电池的反应方程式,为下一步研究工作奠定了基础。另外,通过循环伏安的分析,还得出了电极过程容易受扩散控制的结论,因此,通过流场设计或增加搅拌条件以减小扩散影响则是研究中应当注意的问题。
[1] Steele Brain C H,Heinzel Angelika.Materials for fuel-cell technologies[J].Nature,2001,414:345-352.
[2] 安筱莎,樊友军.低温燃料电池阳极催化剂的研究进展[J].材料导报,2010,24(1):64-67.
[3] 郑聪聪,郭庆杰,王许云,等.MFC聚苯胺碳纳米管阳极电化学法制备及其性能[J].化工学报,2012,63(5):1599-1606.
[4] 马紫峰,张慧娟,原鲜霞,等.低温燃料电池用非贵金属氧化还原催化剂研究进展[J].化工进展,2011,30(1):150-154.
[5] Jain I P.Hydrogen the fuel for 21st century[J].Int.J.Hydrog.Energy,2009,349(17):7368-7378.
[6] Thomas C E,James Brian D,Lomax Jr Frank D,et al.Fuel options for the fuel cell vehicle:Hydrogen,methanol or gasoline?[J].Int.J.Hydrog.Energy,2000,25(6):551-567.
[7] Litster S,M cLean G.PEM fuel cell electrodes[J].J.Power Sources,2004,130:61-76.
[8] Zhang S S,Yuan X Z,Hin J N C,et al.A review of platinum-based catalyst layer degradation in proton exchange membrane fuel cells[J].J.Power Sources,2009,194:588-600.
[9] Demirci U B.Direct liquid-feed cells:Thermodynamic and environmental concerns[J].J.Power Sources,2007,169:239-246.
[10] 易清风.甲酸在钛基纳米多孔网状铂电极上的电化学氧化[J].化工学报,2007,58(2):446-451.
[11] Liu H S,Song C J,Zhang L,et al.A review of anode catalysis in the direct methanol fuel cell[J].J.Power Sources,2006,155:95-110.
[12] Wasmus S,Küver A.Methanol oxidation and direct methanol fuel cells:A selective review[J].J.Electroanal.Chem.,1999,461:14-31.
[13] Amendola S C,Onnerud P,Kelly M T,et al.A novel high powerdensity borohydride-air cell[J].J.Power Sources,1999,84:130-133.
[14] Liu B H,Li Z P,Suda S.Anodic oxidation of alkali borohydrides catalyzde by nickel[J].J.Electrochem.Soc.,2003,150(3):A398-A402.
[15] 王贵领,兰剑,曹殿学,等.直接NaBH4/H2O2燃料电池的研究进展[J].化工学报,2008,59(4):805-813.
[16] Leon C P de,Walsh F C,Pletcher D,et al.Direct borohydride fuel cells[J].J.Power Sources,2006,155:172-181.
[17] Raman R K,Choudhury N A,Shukla A K.A high output voltage direct borohydride fuel cell[J].Electrochem.Solid-State Lett.,2004,7(12):A488-A491.
[18] Bolmer P W.Electrochem ical oxidation of hydrogen sulfide:US,3249522[P].1966-05-03.
[19] Zito Jr R,Kunz Jr L J.Method of operating a fuel cell using sulfide fuel:US,3920474[P].1975-11-18.
[20] Zito R.Electrochem ical apparatus for power delivery utilizing an air electrode:US,5545492[P].1996-08-13.
[21] 易清风.石墨电极上硫化钠的阳极氧化机理探索[J].物理化学学报,2000,16(3):263-268.
[22] 樊玉欠,邵海波,王建明,等.非贵金属催化的碱性硫离子燃料电池放电特性[J].物理化学学报,2012,28(1):90-94.
[23] Bursell M,Pirjamali M,Kiros Y.La0.6Ca0.4CoO3,La0.1Ca0.9MnO3and LaNiO3as bifunctional oxygen electrodes[J].Electrochim.Acta,2002,47(10):1651-1660.
