复方乳酸依沙吖啶散中乳酸依沙吖啶含量测定方法研究
2014-02-27王庆芬郑绍忠
王庆芬,郑绍忠
复方乳酸依沙吖啶散中乳酸依沙吖啶含量测定方法研究
王庆芬,郑绍忠
目的探讨复方乳酸依沙吖啶散中乳酸依沙吖啶含量的测定方法。方法 排除影响乳酸依沙吖啶吸光度值的因素,筛选出供试液制备的最佳方法:减少取样量,采用微孔滤膜于80℃以下条件下加压过滤。采用紫外分光光度法在362 nm处测定吸光度(A),计算乳酸依沙吖啶含量。结果 乳酸依沙吖啶在5~22.5 mg/L(r=0.9997)范围内线性关系良好,高、中、低含量样品(n=5)平均测定率分别为93.132%、93.074%和93.261%。结论 该方法简单、快速,测定结果符合要求,可作为复方乳酸依沙吖啶散中乳酸依沙吖啶含量的测定方法。
质量控制;乳酸依沙吖啶;复方乳酸依沙吖啶散;分光光度法,紫外线
复方乳酸依沙吖啶散是《中国人民解放军医疗机构制剂规范》(简称《军规》)2002年版收载的标准制剂,是一种消炎收敛药,主要用于新生儿脐带的干燥。该制剂处方组成为乳酸依沙吖啶5 g、氧化锌300 g、硼酸30 g、滑石粉665 g,制成1000 g 制剂[1]。《军规》中该制剂含量测定项下提供的乳酸依沙吖啶的测定方法,经多次实验,得率仅为标示量的56%上下。查阅有关报道,认为与处方中的共存成分滑石粉对乳酸依沙吖啶的吸附有关[2-3];方法中并未对其过滤过程中所采取的滤材作具体规定,因此不同滤材对其含量测定也有影响[4];供试液制备中取样量过大也会影响含量测定。为此,本研究在减少了样品取用量、改善供试液制备方法后进行直接紫外含量测定,取得了较满意的效果,现报告如下。
1 仪器与试剂
紫外分光光度计(日本岛津UV-2550),电子分析天平(Sartorius BT224S),LD5-2A型低速离心机(北京医用离心机厂),KH-100B型超声波清洗器(昆山禾创超声仪器有限公司),数显恒温水浴锅(江苏省金坛市江南仪器厂)。乳酸依沙吖啶对照品(中国药品生物制品检定所,批号:100290、199901);乳酸依沙吖啶原料(辽源市银鹰制药有限责任公司,批号:0705001);滑石粉、氧化锌、硼酸均为药用规格;高、中、低含量供试品,混合物A、B、C(笔者所在医院制剂科实验室配制),复方乳酸依沙吖啶散剂(笔者所在医院制剂科制剂室配制,批号:080322、081229、090115)。
2 方法与结果
2.1 供试品制备
2.1.1 高、中、低含量与空白对照供试品制备:取105℃干燥3 h的乳酸依沙吖啶原料精制品,参照《军规》制备主药含量为标示量120%、100%、80%和0的各供试品100 g,含乳酸依沙吖啶分别为6.0370、5.0330、3.69120 mg/g[5]。
2.1.2 混合物制备:按处方量,参照《军规》制备混合物A(含乳酸依沙吖啶、硼酸、氧化锌)、混合物B(含乳酸依沙吖啶、氧化锌)及混合物C(含乳酸依沙吖啶、滑石粉),其中含乳酸依沙吖啶分别为15.1253、17.0251、7.5486 mg/g。
2.2 供试液制备方法
2.2.1 制备法Ⅰ:取中含量供试品(相当于含乳酸依沙吖啶1.2 mg),精密称定,置100ml硅化离心管中,加80℃以上热水20 ml,搅匀,超声波水浴加热提取10 min,倾取上清液至100 ml容量瓶中。照此制取100 ml,放至室温,定容。针头注射器(内装0.45μm滤膜,下同)加压过滤(压滤),弃去前30 ml,备用。
2.2.2 制备法Ⅱ:将“超声波水浴加热提取10 min”改为“水浴加热10 min”,离心(4000 r/min)10 min,余照“2.2.1”项下方法制备。
2.2.3 制备法Ⅲ:取中含量供试品适量(相当于含乳酸依沙吖啶1.2 mg),精密称定,分置50 ml烧杯中,加80℃以上热水20 ml,搅拌下水浴加热10 min,针头注射器压滤至100 ml容量瓶中,续以热水,每次10 ml同法压滤至100 ml,冷至室温,定容。
2.2.4 制备法Ⅳ:将所用溶媒改为热硫酸溶液(0.05 mol/L)外,余照“2.2.3”项下方法制备。
2.3 排除影响乳酸依沙吖啶吸收值因素
2.3.1 不同过滤材料的吸附作用:精密量取乳酸依沙吖啶对照品储备液(0.125 mg/ml)10.0 ml 9份,分置100 m l量瓶中,加水至刻度,摇匀,其中3份用普通定性滤纸过滤,3份用0.45μm滤膜过滤,3份不过滤,测定吸光度值,结果3次测定均值分别为0.511、0.578和0.584。与不过滤比较,普通定性滤纸过滤吸收值降低12.5%,0.45μm滤膜过滤吸收值降低1.03%。表明普通定性滤纸过滤对乳酸依沙吖啶有明显的吸附作用。
2.3.2 共存成分对乳酸依沙吖啶吸收值的影响:分别取混合物 A、B、C 0.1、0.1、0.2 g各 3 份,精密称定,照“2.2.3”项下方法制备供试液,测定。结果混合物 A、B、C测得率分别为 98.26%、98.69%和46.33%(n=3),表明共存成分滑石粉对乳酸依沙吖啶有明显的吸附作用,影响测得率。
2.3.3 供试液制备方法对乳酸依沙吖啶吸收值的影响:取各制备法制备的供试液,分别测定乳酸依沙吖啶含量,结果制备法Ⅰ~Ⅳ制备的供试液的乳酸依沙吖啶测得率依次为89.58%、87.65%、92.47%和90.61%(n=3)。虽然高、低测得率之间行t检验差异无统计学意义(P>0.05),但照制备法Ⅲ制备的供试液测得率最高。
2.4 紫外吸收光谱与标准曲线
2.4.1 乳酸依沙吖啶储备液制备[6-7]:取经105℃干燥至恒重的乳酸依沙吖啶对照品25 mg,精密称定,加适量80℃以上热水使溶解,至200 ml量瓶中,放置室温,加水定容,摇匀,即得乳酸依沙吖啶储备液(0.125 mg/ml,下称储备液)。
2.4.2 乳酸依沙吖啶紫外吸收光谱:精密量取储备液5.0 ml,至50 ml量瓶,加水定容,摇匀,在300~400 nm波长处测定吸收光谱,可见在362 nm有一最大吸收峰[8-9],而空白对照溶液在此范围内未见吸收,对测定无干扰,故确定测定波长为362 nm。
2.4.3 标准曲线制备:精密量取储备液2.0、3.5、5.0、7.0、9.0 ml,分置50 ml量瓶中,加水至刻度,摇匀,以水为参比溶液,在362 nm波长处测定吸光度(A),以A(Y)对浓度(X)作线性回归,得回归方程:Y=0.04157X+0.05930(r=0.9997),表明乳酸依沙吖啶在5~22.5 mg/L范围内与吸光度呈良好线性关系。
2.5 测定方法与验证
2.5.1 测定方法:按制备法Ⅲ制备供试液,以水为参比溶液,在362 nm处测定吸光度(A)。
2.5.2 方法学验证
2.5.2.1 测定范围与精密度试验:取高、中、低含量供试品适量(相当于含乳酸依沙吖啶1.2 mg),各5份,精密称定,至50 ml烧杯中,照制备法Ⅲ制备各供试液,以水作空白,测得量为根据样品称重量与测定成分含量计算而得。在362 nm处测定吸光度(A),求出相对标准偏差(RSD)。结果见表1。
2.5.2.2 加样回收率测定:取低含量样品、乳酸依沙吖啶原料精制品适量,精密称定,充分碾匀,测得供试品含量5.7491 mg/L。称取该供试品5份(每份约含乳酸依沙吖啶1.2 mg),精密称定,照制备法Ⅲ制备各供试液,以水作空白对照,在362 nm处测定吸光度(A),求出RSD。结果见表2。
2.5.2.3 专属性试验:分别取混合物 A、B、C各0.1、0.1、0.2 g,各3 份,精密称定,照制备法Ⅲ制备供试液,以水为空白对照液,在200~400 nm波长处扫描,所用供试液仅在362 nm处有单一峰出现,而空白对照液则无吸收,表明其他成分对乳酸依沙吖啶的紫外吸收测定方法无干扰。
2.5.2.4 稳定性试验:取“2.5.2.1”项下主法测得的供试液,分别于 0、1.5、3、4.5、6 h 在 362 nm 处测定吸收值,结果分别为 0.536、0.539、0.532、0.538、0.537,RSD=0.5037%,表明供试液在6 h 内稳定。
2.6 样品测定 按拟定的方法取3批样品进行测定,结果见表3。
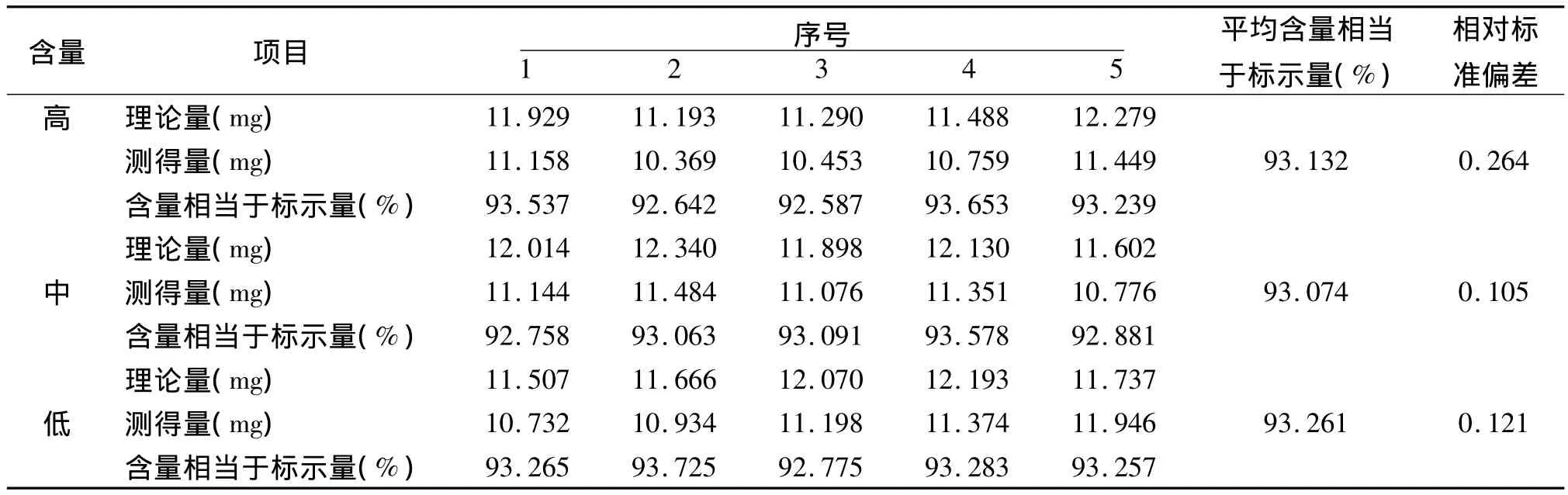
表1 高、中、低含量供试品中乳酸依沙吖啶精密度测定结果

表2 低含量对照样品中乳酸依沙吖啶加样回收率测定结果
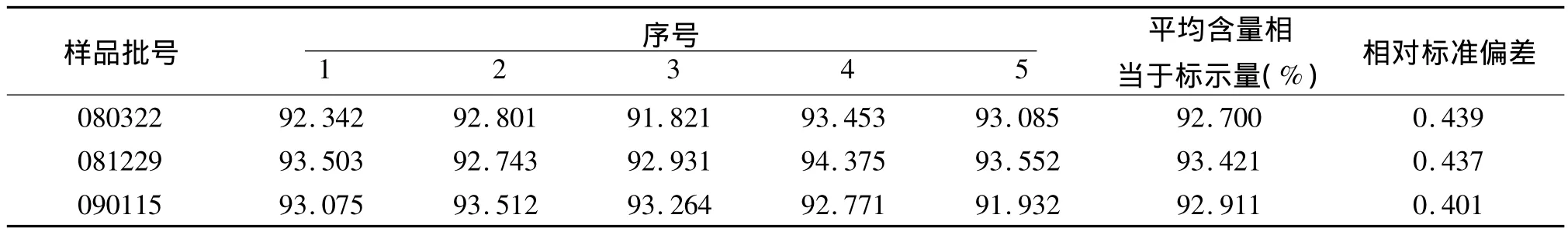
表3 3批复方乳酸依沙吖啶散样品中乳酸依沙吖啶含量测定结果
3 讨论
针对《军规》中乳酸依沙吖啶测定方法测得率低的情况,本实验研究表明,滤材选用方面,普通定性滤纸较混合纤维滤膜对乳酸依沙吖啶的吸附明显增加,前者吸收值降低 12.5%,而后者仅降低1.03%。将滤材改为孔径0.45μm的混合纤维微孔滤膜,可减少滤材[10]对乳酸依沙吖啶的吸附。微孔滤膜的孔径为椎体状,光滑的一面孔径小为正面;粗糙的一面孔径大为反面,安装时应将正面朝下,反面朝上,否则易被杂质阻塞孔径,影响滤速[11-13]。
共存成分中,处方比例的滑石粉可使乳酸依沙吖啶测得量降低46.33%,氧化锌和硼酸则对测定结果无影响;供试液制备方法方面,本研究设计了制备法Ⅰ~Ⅳ,虽然各制备法测得率经t检验差异无统学意义,但制备法Ⅲ制备的供试液测得率最高。
在以上试验的基础上提出的改进的供试液制备法与原法比较,具有以下特点[4]:一是供试液制备从取样10 g、制成 50 ml,改为取样 0.25 g、制备成100 ml,滤层冲洗液量增加约160倍,明显提高了冲洗效果;二是由原来的自然过滤改为压滤,提高了过滤速度,改善了过滤效果;三是供试液制备过程减少了再稀释操作和加试剂的反应过程,简化了操作环节,减少了误差。
组方中的成分对乳酸依沙吖啶有吸附作用,但由于各组分都有其独特的作用,特别是滑石粉还能起到稀释作用[2],因此,不建议改变组方的组成及比例。虽然测得的主药回收率偏低,但系滑石粉对被测成分的吸附所致,并不影响其临床应用效果。
乳酸依沙吖啶在热水中易溶,在水中略溶[5],因此供试品在过滤时应保持滤液的温度,防止由于药液温度过低影响药液浓度,导致测定结果偏低。乳酸依沙吖啶见光易分解,实验过程中应注意避光操作,以免影响测定结果[14-16]。此外,过滤过程中的操作压力、操作速度也会对供试液的制备有一定的影响[17-19],可进一步探讨。
[1] 中国人民解放军总后勤部卫生部.中国人民解放军医疗机构制剂规范(2002年)[M].北京:人民军医出版社,2002:212-213.
[2] 王芊,丁鑫芳.脐带散中依沙吖啶的含量变化[J].中国药师,2001,4(6):430-431.
[3] 李爱英,尹艳莲.复方乳酸依沙吖啶混悬液的制备与临床应用[J].医药导报,2006,25(4):338-339.
[4] 许亚夫,邹大江,熊俊.滤膜材料及微滤技术的应用[J].中国组织工程研究与临床康复,2011,15(16):2949-2952.
[5] 国家药典委员会.中华人民共和国药典[K].北京:化学工业出版社,2010:194-195,481.
[6] 张一帆,林辉,汤秋华.不同处方乳酸依沙吖啶溶液稳定性试验[J].海峡药学,2011,23(11):20-21.
[7] 刘瑞丽,杜习智,李金伟.乳酸依沙吖啶栓的制备及质量控制[J].中国现代医生,2009,47(2):37-38.
[8] 沈德荣.乳酸依沙吖啶软膏的制备及含量测定[J].中国医药导报,2008,5(30):33-34.
[9] 黎玉红,范小阳,彭德芳.乳酸依沙吖啶软膏的制备及质量控制[J].中国药房,2007,18(25):1964-1965.
[10]张彦文,石澍,段蓉,等.滤材对制剂中盐酸二甲双胍含量测定的影响[J].中国现代应用药学杂志,2008,25(8):714-716.
[11]齐钦华.微孔滤材的性能与应用[J].安徽医药,2005,9(4):301-302.
[12]徐国兴.微孔滤膜的选择和应用[J].现代应用药学,1988(4):24,32.
[13]张亚明.微孔滤膜使用应注意的问题[J].黑龙江中医药,2000(6):55-56.
[14]刘玉春,李艳娜.HPLC法测定乳酸依沙吖啶注射液的含量[J].安徽医药,2008,12(3):225-226.
[15]李坚,谭瑞威.分光光度法测定依沙吖啶溶液中乳酸依沙吖啶的含量[J].华西药学杂志,2001,16(2):133-134.
[16]曹嫣嫣,胡蓉梅,龚睿林,等.乳酸依沙吖啶溶液的制备及质量标准研究[J].中国药房,2010(21):1987-1988.
[17]王芸芸,杨玲.超滤膜纯化甘草渣中总黄酮的工艺研究[J].化学与生物工程,2013,30(4):47-48.
[18]颜继忠,廖倩,李行诺.超滤法纯化茯苓多糖的工艺优化[J].浙江工业大学学报,2013,41(2):122-125.
[19]彭菲,叶正良,李德坤,等.不同材质及不同截留分子量超滤膜对人参皂苷类成分的影响[J].中成药,2013,35(5):937-940.
Discussion on Content Determ ination of Ethacridine Lactate in Compound Ethacridine Lactate Powder
WANG Qing-fen,ZHENG Shao-zhong(Departmentof Pharmacy,175 Hospital of PLA the Affiliated SoutheastHospital of Xiamen University,Fujian 363000)
ObjectiveTo discuss the content determination of Ethacridine Lactate in Compound Ethacridine Lactate Powder.MethodsThe best preparationmethod of reducing the amountof sample and pressuring filterwithmicropore film below 80℃ was screened by excluding the interference factors.The absorbance(A)and contentwere detected at362 nm with UV spectrophotometry.ResultsThe Ethacridine Lactate had good linear relationship during 5-22.5 mg/L(r=0.9997)of linear range.The average detection rates of samples with high,middle and low contents(n=5)were 93.132%,93.074%and 93.261%respectively.ConclusionThemethod is simple,quick and feasible,and can be used to detect the content of Ethacridine lactate in Compound Ethacridine Lactate Powder.
Quality control;Ethacridine Lactate;Compound ethacridine lactate powder;Spectrophotometry,ultraviolet
R927.2
A
2095-140X(2014)05-0082-04
10.3969/j.issn.2095-140X.2014.05.023
363000福建漳州,解放军175医院,厦门大学附属东南医院制剂科
郑绍忠,电话:13860894774
2013-12-26 修回时间:2014-01-23)
检验与病理
·论著·
