聚乙烯吡咯烷酮包覆硫/碳复合材料的制备及其电化学性能
2014-02-06崔晓兰单忠强田建华
崔晓兰,单忠强,田建华
(天津大学化工学院,天津 300072)
电动车和移动电子设备的飞速发展迫切需要开发更高能量密度的电池,在众多电池体系中,单质硫具有1672 mAh/g的高理论比容量,以锂为负极、硫为正极的锂硫电池具有2567 Wh/kg的高理论能量密度,是商业锂离子电池的3~5倍,并且硫廉价易得,对环境友好,使其有望成为高储能体系的正极材料,因此受到越来越多的关注[1-4]。
Li-S电池的研究始于20世纪60年代,在硫/碳复合材料的制备方面,液相化学沉积法近期得到了很多研究者的关注。液相化学沉积法操作简单、能耗小,它是先将碳均匀分散于水溶液中,再利用化学反应在碳材料表面均匀沉积硫单质。目前有研究者采用Na2S2O3作为硫源来制备石墨烯-硫复合材料[5]和碳-硫复合材料[6]。其中,王等[7]合成了含硫70%的PEG改性石墨烯-硫复合材料,0.2 C充放电100次后比容量保留600 mAh/g。还有报道采用Na2S和S作为硫源。Nazar课题组[8]采用此方法制备了含硫87%的石墨烯载硫复合材料,0.2 C充放电时首次放电达705 mAh/g,50次保留500 mAh/g。Rao等采用Na2S和S合成了纳米碳/硫复合材料[9]和碳纳米纤维/硫复合材料[10],0.05 C循环时首次放电比容量分别为1200 mAh/g和1313 mAh/g,纳米碳/硫复合材料50次循环后保留668 mAh/g,碳纳米纤维/硫复合材料60次循环后保留586 mAh/g。循环稳定性是Li-S电池一个很重要的指标,但是采用Na2S和S作为硫源制备硫/碳复合材料的相关文献中并未给出更长的循环寿命。
聚乙烯吡咯烷酮(PVP)是一种非离子型水溶性高分子,既溶于水、又溶于大部分有机溶剂,具有优良的化学稳定性以及胶体保护作用,常用作分散剂、黏合剂[11]。PVP用作分散剂来制备纳米材料时,有助于控制粒子在纳米尺度内。硫/碳复合材料中的硫粒若尺寸较大会导致硫与碳之间结合不够紧密;在充放电过程中,硫核不能充分反应,降低了活性物质的利用率,从而降低比容量和循环性能。
本研究以聚乙烯吡咯烷酮(PVP)作分散剂,采用液相化学沉积法来制备硫/碳复合材料,通过有效控制硫粒尺寸,得到分散均匀且结合紧密的硫/碳复合材料,并研究其电化学性能。
1 实验
1.1 制备S/C复合材料
w(S)∶w(Na2S·9H2O)以 1∶2的比例溶于质量分数为10%NaOH中形成橙黄色溶液,加入一定量质量分数为1%PVP于所制得的Na2Sx溶液中,将一定量基体碳(Cabot Black Pearl 2000)分散于以上溶液并超声1 h。随后滴加质量分数为5%HCl到以上制备得到的悬浮液中至酸性,再搅拌2.5 h至反应完全;所得的硫/碳复合材料经水洗、离心后,于50℃真空干燥,记作 S/C-PVP。不加碳源,重复以上过程制备得到单质硫样品。
不添加PVP重复以上步骤,所制得的硫/碳复合材料记作S/C。不加碳源,重复以上过程制备得到单质硫样品。
1.2 封装扣式电池
以 w(S/C复合材料)∶w(Super P)∶w[聚四氟乙烯(PTFE)]=70∶20∶10 的比例,乙醇作分散剂来制备浆料,并将浆料涂覆在泡沫镍上作为正极,50℃真空干燥12 h。以金属锂作负极,多孔聚丙烯膜Celgard 2000作隔膜。采用添加0.1 mol/L LiNO3的 1 mol/L LiTFSI/[DOL∶DME(体积比)=1∶1]为电解液,在手套箱中组装2032扣式电池。
1.3 硫/碳复合材料物理及电化学性能表征
以10℃/min的流速,在N2保护下由室温升至600℃进行热重测试(Q500,TA Instrument),采用 X射线衍射分析(Bruker AXS),在1.5~3.0 V之间以0.35 C(585 mA/g)、0.5 C(836 mA/g)、1 C(1672 mA/g)、2 C(3344 mA/g)进行恒流充放电(LANDCT2001A);以 0.1 mV/s进行循环伏安测试(LK3200电化学工作站)。
2 结果与讨论
如图1所示,PVP表现出2个失质量阶段,第1阶段在100℃之前为水的损失,PVP在第2阶段350~475℃会发生分解。对硫/碳复合材料来说,硫在115℃开始熔融,随着温度升高而不断升华。S/C复合材料中硫含量为59%;S/C-PVP复合材料的质量损失为62%,实际硫含量经计算为52.2%,PVP含量为11.5%。
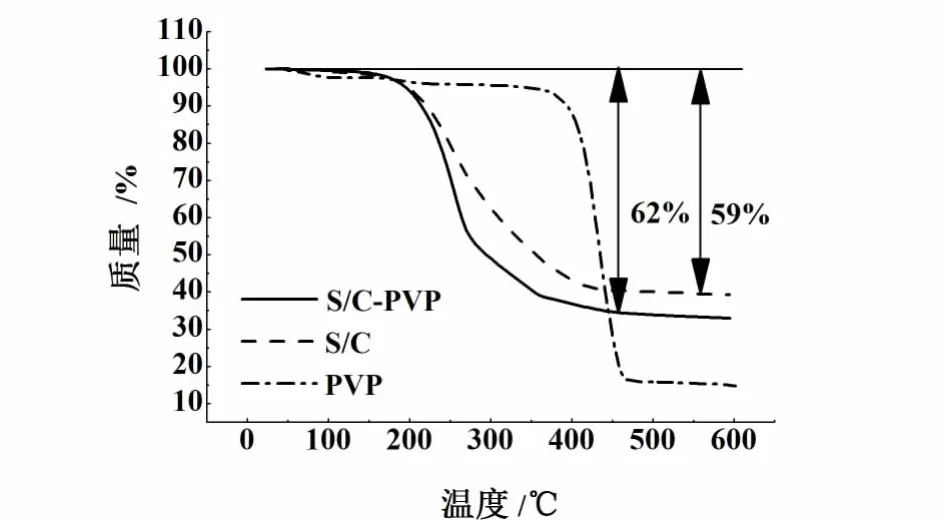
图1 S/C-PVP复合材料与S/C复合材料的热重分析Fig.1 Thermogravimetric analysis of S/C-PVP composite and S/C composite
图2所示为基体碳、未添加 PVP制备的单质硫、添加PVP制备的单质硫、S/C复合材料和 S/CPVP复合材料的SEM图。

图2 SEM的形貌Fig.2 SEM images
从图2a)可看出,碳的粒径主要分布在 30~40nm之间。通过液相化学反应,未添加PVP生成的单质硫经过非均相成核形成粒径分布不规则的块状,从1μm到5μm变化[图 2b)];采用 PVP制备的硫颗粒[图2c)]大幅度减小,粒径得到有效控制。S/C-PVP复合材料[图2e)]与 S/C复合材料[图2d)]相比,粒径更小一些,几乎保留基体碳的原始形貌,这说明了大部分单质硫填充到了碳孔中,部分硫吸附在碳表面。
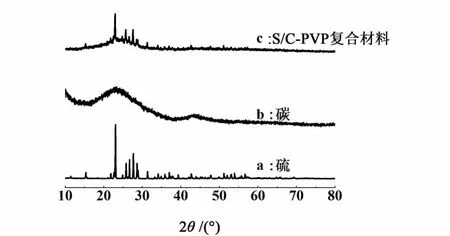
图3 硫、碳和S/C-PVP复合材料的XRD谱图Fig.3 Wide-Angle X-ray diffraction patterns of elemental sulfur,carbon and S/C-PVP composite material
图3所示为单质硫、基体碳和S/C-PVP复合材料的 XRD谱图。谱线 a中,2θ=23°~29°多个强度不等的特征衍射峰证明单质硫为Fddd斜方晶型,谱线b中24°和45°左右的宽峰说明了基体碳的非晶态结构。谱线c中有相对谱线a强度较弱的硫峰,证明基体碳中结晶态硫的存在。
S/C-PVP复合材料与S/C复合材料以0.35 C、0.50 C充放电的循环性能如图4所示。
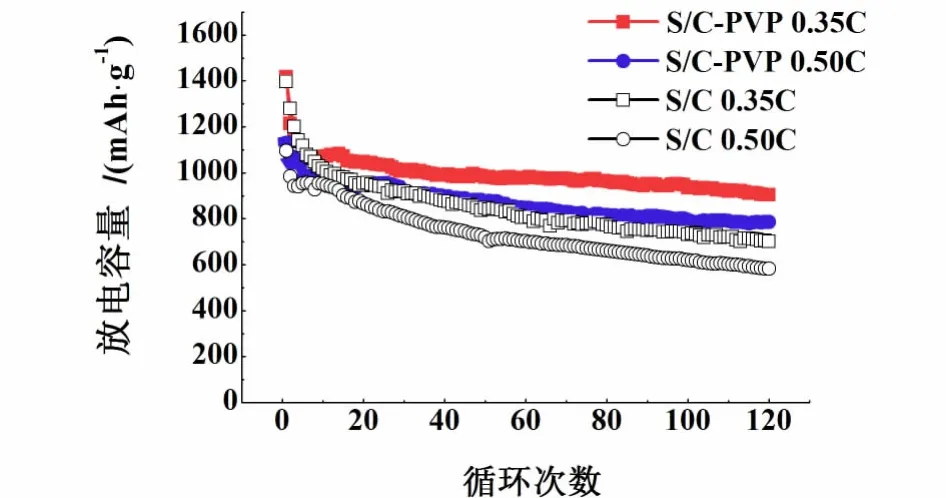
图4 S/C-PVP复合材料与S/C复合材料在0.35 C、0.50 C的循环性能Fig.4 Cycling performance of S/C-PVP composite material and S/C composite material at 0.35 C and 0.50 C
由图4可见,S/C-PVP复合材料 0.35 C和0.50 C的循环性能明显优于S/C复合材料。S/C复合材料在0.35和0.50 C时的首次放电比容量分别为1396.9和1096.4 mAh/g,120次后比容量保留699.8 mAh/g(容量保持率为50.1%)、583.1 mAh/g;S/C-PVP复合材料在0.35 C、0.50 C时的首次放电比容量分别为1415.3和1129 0 mAh/g,120次后比容量保留903.3 mAh/g(容量保持率为63.8%)、785.3 mAh/g。这说明了PVP包覆S/C复合材料能够有效抑制活性物质流失,提高硫/碳复合材料的循环稳定性。
如图5反映了S/C-PVP与S/C复合材料以0.35和0.50 C充放电时第1次和第120次充放电曲线。
2.3和2.0 V的2个高低放电平台分别对应单质硫或可溶的高聚硫化物(比如,Li2S8)向可溶的低聚硫化物(Li2Sx,8>x≥4)以及低聚硫化物向不溶的 Li2S2/Li2S的转变[12]。S/C-PVP复合材料的首次放电平台略低于S/C复合材料,这可能是由于PVP的存在引起的。循环120次后 S/C复合材料的放电平台降低,而S/C-PVP复合材料的放电平台基本维持不变,说明了S/C复合材料在循环过程中的极化现象比S/C-PVP复合材料严重,比容量下降较快。而S/C-PVP复合材料一直维持比较稳定的电化学过程。
引入PVP可以有效提高硫/碳复合材料的电化学性能有2个方面的原因:首先,单质硫减小的粒径及硫/碳复合材料提高的载硫均匀性是比容量提高的一个原因。PVP作为水溶性的非离子表面活性剂,可以有效控制单质硫的粒径。PVP通过其聚合链吸附在纳米硫胶体粒子的表面,使得形成的纳米硫溶胶具有很好的分散性,得到粒径更小、分布更均匀的单质硫。不添加PVP时,在制备单质硫的过程中可观察到溶液中的硫颗粒团聚在一起,没有形成均匀相的悬浮液;添加PVP作分散剂时,随着HCl的滴加,生成分散均匀、纳米级的硫溶胶,最后形成均匀的、呈乳白色且边缘泛蓝光的微乳液;同样,在制备S/C-PVP纳米复合材料时,最后得到呈黑色、分散均匀的悬浮液。大部分硫在碳的微孔和介孔中均匀沉积,硫与碳之间结合更紧密,碳的多孔结构可以抑制硫颗粒进一步增大[13]。其次,PVP在一定程度上起到黏合剂的作用,与PTFE起到了协同作用。多硫化物在电解液中可以与PVP形成凝胶状混合物,增加了液体电解液的黏度,这可以有效减小多硫化物的迁移[14],从而抑制了“穿梭效应”的发生,减少了Li2S2/Li2S在复合材料及锂负极表面沉积,进而保证正极结构的稳定性,提高了电池的循环性能,这也可以从图6循环120次后 S/CPVP与S/C正极结构的不同得到印证。S/C-PVP复合材料保持了原来的球形形貌,正极结构相对完整;而S/C形貌发生较大变化,碳颗粒黏连在一起,不能观察到独立的碳颗粒。PVP可以在一定程度上抑制S/C-PVP正极中多硫化物的迁移,从而降低正极中有效反应界面的流失,使得S/C-PVP复合材料的电化学性能大幅度提高。
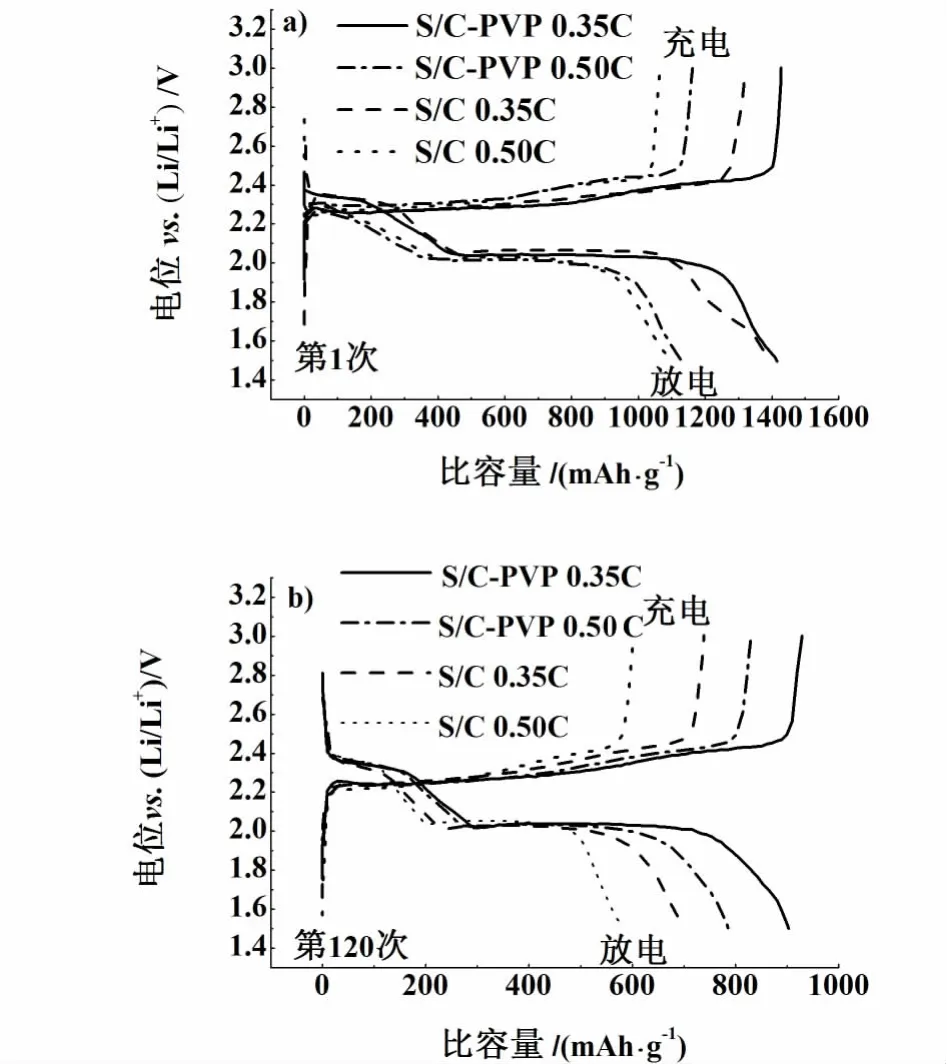
图5 S/C-PVP与S/C复合材料以0.35 C、0.50 C充放电时第1次和第120次充放电曲线Fig.5 Typical voltage vs.capacity profiles of the first cycle and 120th cycle of S/C-PVP composite material and S/C composite material at 0.35 C and 0.50 C

图6 循环120次后S/C-PVP正极 a)和S/C正极 b)的 SEM图Fig.6 SEM images of the cycled electrodes after 120 cycles a)S/C-PVP,b)S/C
图7所示为S/C-PVP复合材料第1次、第2次和第5次的CV曲线。2.3和2.0 V的2个还原峰与图5中充放电曲线的高低2个平台相对应。在2.45 V处重叠的氧化峰对应Li2S2/Li2S向低聚硫化物,之后向高聚硫化物的转变。在连续5次的扫描过程中,还原峰保持稳定,氧化峰随着扫描过程的继续,峰电流有一定程度降低,并且氧化峰向低电位移动,这意味着活性物质硫在1个离子/电子易迁移的环境中,说明S/C-PVP复合材料具有良好的电化学可逆性。
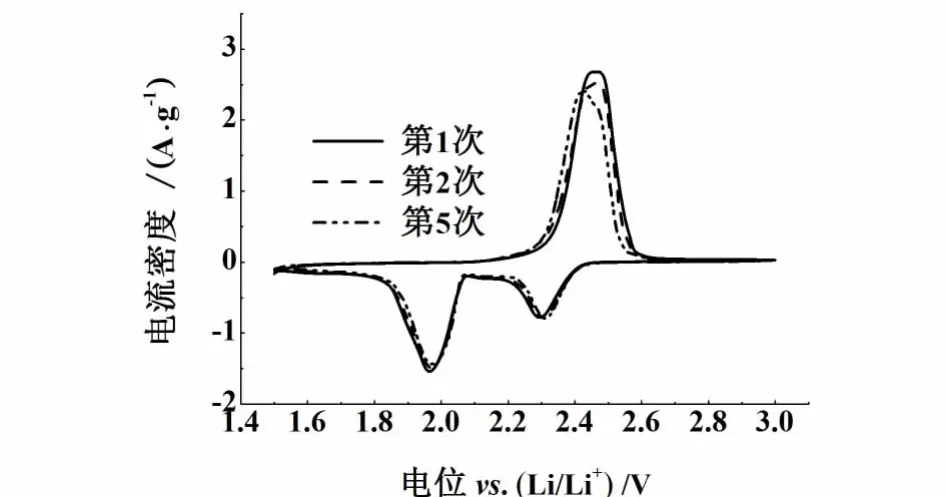
图7 S/C-PVP复合材料的循环伏安曲线Fig.7 Cyclic voltammogram curves of S/C-PVP composite
为进一步验证S/C-PVP复合材料优异的循环性能,S/C-PVP复合材料在高倍率1 C和2 C时的循环曲线如图8所示。
1和2 C时的首次放电比容量分别为1102.9和904.0 mAh/g,之后得到 961.6和 753.3 mAh/g的可逆比容量,200次后比容量仍能保留557.3和486.8 mAh/g,容量保持率分别为50.5%和53.8%。
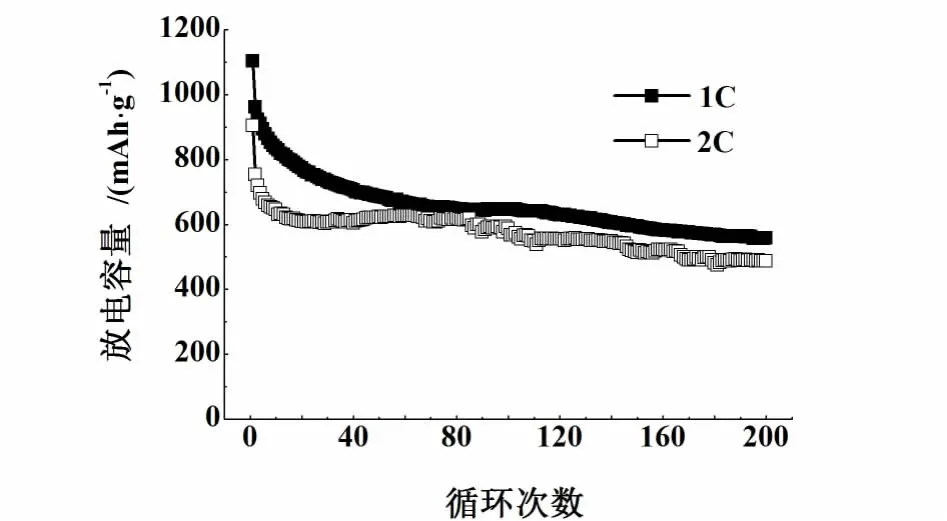
图8 S/C-PVP复合材料1和2 C充放电时的循环性能Fig.8 Discharging-Charging behavior of S/C-PVP composite at 1 and 2 C
3 结论
采用液相化学沉积法制备硫/碳复合材料,引入聚乙烯吡咯烷酮(PVP)作分散剂,获得电化学性能优异的S/C-PVP复合材料。通过电化学测试表明,0.35 C充放电时,该材料首次放电比容量达到1415.3 mAh/g,120次后比容量保留903.3 mAh/g,容量保持率为63.8%。尤其在2 C充放电时,首次放电也可达到904.0 mAh/g,200次后比容量仍能保留486.8 mAh/g。PVP作为一种水溶性的表面活性剂,在制备过程中能够控制单质硫的纳米尺寸,并且对硫/碳复合材料形成包覆层,有效提高了锂硫电池的电化学性能,为今后硫/碳复合材料的研究提供一条可行性的思路。
[1]Bruce P G,Freunberger S A,Hardwick L J,et al.LiO2and Li-S batteries with high energy storage[J].Nature Materials,2011,11:19-29
[2]Ji X L,Lee K T,Nazar L F.A highly ordered nanostructured carbon-sulphur cathode for lithium-sulphur batteries[J].Nature Materials,2009,8:500-506
[3]董全峰,王翀,郑明森.锂硫电池关键材料研究进展与展望[J].化学进展,2011,23(2/3):533-539 Dong Quanfeng,Wang Chong,Zheng Mingsen.Research progress and prospects of lithium sulfur batteries[J].Progress in Chemistry,2011,23(2/3):533-539(in Chinese)
[4]Ji X,Nazar L F.Advances in Li-S batteries[J].Journal of Materials Chemistry,2010,20:9821-9826
[5]Park M S,Yu JS,Kim K J,et al.One-Step synthesis of a sulfur-impregnated graphene cathode for lithium-sulfur batteries[J].Physical Chem istry Chemical Physics,2012,14:6796-6804
[6]Su Y,Manthiram A.A facile in situ sulfur deposition route to obtain carbon-wrapped sulfur composite cathodes for lithium-sulfur batteries[J].Electrochimica Acta,2012,77:272-277
[7]Wang H,Yang Y,Liang Y,et al.Graphene-Wrapped sulfur particles as a rechargeable lithiumsulfur battery cathode material with high capacity and cycling stability[J].Nano Letter,2011,11:2644-2647
[8]Evers S,Nazar L F.Graphene-Enveloped sulfur in a one pot reaction:A cathode with good coulombic efficiency and high practical sulfur content[J].Chemical Communications,2012,48:1233-1235
[9]Rao M,Song X,Cairns E J.Nano-Carbon/sulfur composite cathode materials with carbon nanofiber as electrical conductor for advanced secondary lithium/sulfur cells[J].Journal of Power Sources,2012,205:474-478
[10]Rao M,Song X,Liao H,et al.Carbon nanofiber-sulfur composite cathode materials with different binders for secondary Li/S cells[J].Electrochimica Acta,2012,65:228-233
[11]汪立德.聚乙烯吡咯烷酮及其应用的进展[J].现代化工,1995,9:21-25 Wang Lide.Recent advance in polyvinylpyrrolidone and its applications[J].Modern Chemical Engineering,1995,9:21-25(in Chinese)
[12]Xiong S,Xie K,Diao Y,et al.Oxidation process of polysulfides in charge process for lithium-sulfur batteries[J].Ionics,2012,18(9):867-872
[13]Liu Y,Zhan H,Zhou Y.Investigation of S/C composite synthesized by solvent exchange method[J].Electro chimica Acta,2012,70:241-247
[14]Fu Y,Su Y,Manthiram A.Sulfur-Carbon nanocomposite cathodes improved by an amphiphilic block copolymer for high-rate lithium-sulfur batteries[J].Applied Material Interfaces,2012,4:6046-6052
