注射用间苯三酚与6种常用输液的配伍稳定性考察
2013-12-03刘光斌赵丽萍姜芳宁谢六生张玉叶张莉莉甘肃嘉峪关市酒钢医院药学部甘肃嘉峪关735100
刘光斌,赵丽萍,姜芳宁,谢六生,张玉叶,张莉莉(甘肃嘉峪关市酒钢医院药学部,甘肃嘉峪关 735100)
间苯三酚直接作用于胃肠道和泌尿生殖道的平滑肌,是亲肌性非阿托品非罂粟碱类纯平滑肌解痉药[1-2]。注射用间苯三酚说明书中要求使用5%或10%葡萄糖注射液作为静脉滴注的溶媒,但在临床有些患者不适合用葡萄糖作输液。关于间苯三酚与常用输液的配伍稳定性也尚未见报道。本研究从临床实际需要出发,采用高效液相色谱法对注射用间苯三酚与5%葡萄糖注射液、10%葡萄糖注射液、0.9%氯化钠注射液、5%葡萄糖氯化钠注射液、乳酸林格氏注射液和转化糖电解质注射液等6种常用输液配伍后的稳定性进行考察,以便为临床用药提供参考依据。
1 材料
1.1 仪器
LC-2010 AHT型高效液相色谱仪,岛津LC solution工作站(日本岛津公司);AUY220电子分析天平(日本岛津公司);756紫外可见分光光度计(上海奥谱勒仪器有限公司);PHS-3 C型实验室酸度计(上海伟业仪器厂)。
1.2 药品与试剂
间苯三酚对照品(上海紫一试剂厂,纯度:99.0%);注射用间苯三酚(湖北午时药业股份有限公司,批号:120101、120303、120314,规格:40 mg);5%葡萄糖注射液(批号:1205275 B,规格:250ml)、10%葡萄糖注射液(批号:1204124 B,规格:500 ml)、0.9%氯化钠注射液(批号:1205148 B,规格:250 ml)、5%葡萄糖氯化钠注射液(批号:120508 YT,规格:500 ml)均来自于安徽双鹤药业有限责任公司;乳酸林格氏注射液(山东辰欣药业有限责任公司,批号:1112295105,规格:500 ml);转化糖电解质注射液(扬子江药业集团上海海尼药业有限公司,批号:1207048,规格:500 ml);乙腈为色谱纯,水为超纯水。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液:准确称取间苯三酚对照品5 mg,置于100 ml量瓶中,加水稀释制成50 μg/ml间苯三酚对照品贮备溶液。
2.1.2 供试品溶液:取注射用间苯三酚1支(40 mg),置于100 ml量瓶中,加水稀释至刻度;精密量取该溶液适量,用水稀释制成每1 ml约含间苯三酚10 μg的溶液。
2.1.3 配伍溶液:取上述6种输液200 ml,按照临床常用量分别加入80 mg注射用间苯三酚,摇匀;精密量取上述配伍液适量,用水稀释制成每1 ml约含间苯三酚10 μg的溶液。
2.1.4 阴性样品溶液:参考文献[3],按照其处方量除不加间苯三酚外,其他辅料正常加入,按其工艺制备阴性制剂。按“2.1.2”项下方法制备阴性对照液。
2.2 检测波长的确定
取间苯三酚对照品,分别制成20 μg/ml和2 μg/ml溶液,置于紫外-可见分光光度计中,以水为空白对照,在200~400 nm波长范围内进行光谱扫描,记录紫外吸收光谱图(见图1)。由图1可见,20 μg/ml的间苯三酚溶液在265 nm波长处有特征吸收峰,约240 nm以下吸收较强,所以在240 nm以下无法甄别特征吸收峰;2 μg/ml的间苯三酚溶液在205 nm波长有特征吸收峰,而在240 nm以上吸收较弱,无特征吸收峰出现。考虑到在低波长处,有机溶剂有紫外吸收,会对间苯三酚的检测产生干扰,故确定中间苯三酚的测定波长为210 nm。

图1 间苯三酚紫外吸收光谱图Ⅰ.20 μg/mL 间苯三酚溶液;Ⅱ.2 μg/ml间苯三酚溶液Fig 1 UV absorption spectrum of phloroglucinolⅠ.20 μg/ml phloroglucinol;Ⅱ.2 μg/ml phloroglucinol
2.3 色谱条件
色谱柱:Kromasil C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈-水(9∶91);流速:1.0 ml/min ;柱温:30℃;检测波长:210 nm;进样量:20 μL。间苯三酚对照品、阴性对照液、6种配伍剂溶液和6种配伍液的色谱图见图2。结果可见,阴性对照液中的辅料和6种配伍剂溶液对配伍液中间苯三酚的测定不产生干扰。
2.4 线性关系考察
分别精密量取50μg/ml间苯三酚对照品贮备溶液0.5、1.0、1.5、2.0、2.5、3.0 ml于10 ml量瓶中,加水至刻度,摇匀,配制成质量浓度分别为2.5、5.0、7.5、10.0、12.5、15.0μg/ml的溶液。按“2.3”项下色谱条件测定峰面积。以峰面积(A)对质量浓度(c)进行线性回归,得回归方程:A=1501670 c+12573.8(r=0.9999,n=6)。结果表明,间苯三酚检测浓度在2.5~15.0 μg/ml范围内线性关系良好。
2.5 精密度试验
取“2.4”项下浓度10.0 μg/ml的溶液,按照“2.3”项下色谱条件进样6次,记录峰面积,测得RSD=0.88%。结果表明,该方法精密度良好。
2.6 回收率试验
取已知含量的同批样品(批号:120314)3份,分别取40 mg,再分别准确加入间苯三酚对照品32mg(80%)、40mg(100%)、48mg(120%),按“2.1.2”项下方法制备溶液。按“2.3”项下色谱条件进样测定,记录色谱图,用回归方程计算,然后计算加样回收率。结果表明,该方法回收率良好,详见表1。
2.7 含量测定
分别取批号为120101、120303、120314的注射用间苯三酚各5支(40 mg),按“2.1.2”项下方法制备样品溶液,按“2.3”项下色谱条件进样测定,记录色谱图,按外标法以峰面积计算。样品含量测定结果详见表2。
2.8 配伍稳定性考察
2.8.1 pH值的变化情况:在室温[(25±1)℃]条件下,测定6种输液的pH值后,模拟临床用药,将注射用间苯三酚80mg与5%葡萄糖注射液、10%葡萄糖注射液、0.9%氯化钠注射液,5%葡萄糖氯化钠注射液、乳酸林格氏注射液和转化糖电解质注射液各200 ml配伍后,在0、1、2、3、4、5、6 h时分别测定配伍液放置不同时间的pH值。结果6种配伍液的pH值均未发生明显变化,详见表3。

图2 高效液相色谱图A.阴性对照液;B.间苯三酚对照品溶液;C.0.9%氯化钠注射液;D.0.9%氯化钠注射液配伍液;E.乳酸林格氏注射液;F.乳酸林格氏注射液配伍液;G.转化糖电解质注射液;H.转化糖电解质注射液配伍液;I.5%葡萄糖氯化钠注射液;J.5%葡萄糖氯化钠注射液配伍液;K.5%葡萄糖注射液;L.5%葡萄糖注射液配伍液;M.10%葡萄糖注射液;N.10%葡萄糖注射液配伍液;1.间苯三酚Fig 2 HPLC chromatogramsA.negative control;B.phloroglucinol control;C.0.9%Sodium chloride injection;D.mixture of 0.9%Sodium chloride injection;E.Lactated Ringer’s injection;F.mixture of Lactated Ringer’s injection;G.Invert sugar and electrolytes injection;H.mixture of Invert sugar and electrolytes injection;I.5%Glucose and sodium chloride injection;J.mixture of 5%Glucose and sodium chloride injection;K.5%Glucose injection;L.mixture of 5%Glucose injection;M.10%Glucose injection;N.mixture of 10%Glucose injection;1.phloroglucinol
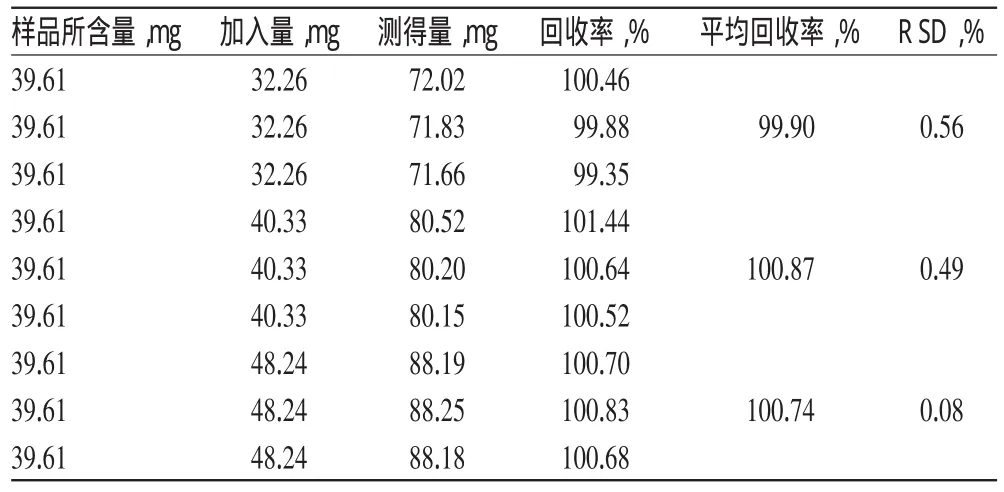
表1 回收率试验结果(n=9)Tab 1Results of recovery tests(n=9)
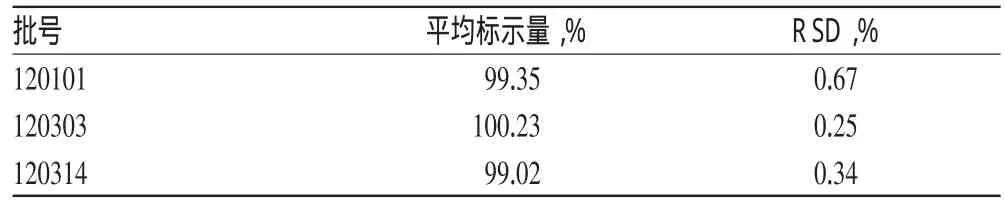
表2 样品含量测定结果(n=5)Tab 2 Results of contents determination of samples(n=5)

表3 6种配伍液的pH值变化结果Tab 3 pH value of 6 kinds of mixtures at different time points
2.8.2 间苯三酚含量的变化情况:在室温条件下,模拟临床用药,将注射用间苯三酚80 mg与6种输液各200 ml配伍后,在0、1、2、3、4、5、6 h时分别按照“2.1.3”项下方法制备配伍溶液,测定配伍液放置不同时间的主药含量。结果6种配伍液的主药含量均无显著变化,基本保持稳定,详见表4。

表4 6种配伍液中间苯三酚的相对含量随时间变化结果(%%)Tab 4 Relative contents of phloroglucinol in 6kinds of mixtures at different time points(%%)
2.8.3 5-羟甲基糠醛(5-hydroxymethyl furfural,5-HMF)的变化情况:按照2010年版《中国药典》方法,在0、1、2、3、4、5、6 h时分别精密量取注射用间苯三酚与含糖溶液中的配伍液适量,置于100 ml量瓶中,用水稀释至刻度,在284 nm波长处测定吸光度。结果4种含糖配伍液的5-HMF吸光度均在限度控制范围内,且在不同时间无显著变化,详见表5。
2.8.4 溶液颜色变化和可见异物观察:在0、1、2、3、4、5、6 h时分别用灯检法检查6种配伍液的颜色和可见异物。结果,配伍液在灯检装置下无明显可见异物和微细可见异物检出;在6 h内配伍液的颜色均无变化,检查结果符合规定;对各时间点高效液相色谱图进行观察,未见有新物质峰出现。

表5 4种含糖配伍液的5-HMF吸光度随时间变化结果Tab 5 Absovption of 5-HMF in 4 kinds of sugar mixtures at different time points
3 讨论[3-4]
文献报道间苯三酚的高效液相法测定以十八烷基硅烷键合硅胶为填充剂,以乙腈-水(50∶50,V/V)为流动相,检测波长为248nm[4];或以乙腈-水(9∶91,V/V)为流动相,检测波长为265 nm[3]。本研究选择210 nm作为检测波长,信号相应更强、分离度更好,对照溶液所需要的浓度较小,可以节约对照品。
5-HMF是葡萄糖等单糖化合物在高温或弱酸等条件下脱水产生的一个醛类化合物,该化合物对人体横纹肌和内脏有损害[5]。药品与葡萄糖注射液配伍后在放置过程中可能会分解产生5-HMF。因此,在药物与含糖输液配伍稳定性研究中不可忽视,必须检测5-HMF的含量。5-HMF的最大吸收波长为284nm,该波长处5%葡萄糖注射液、10%葡萄糖注射液、5%葡萄糖氯化钠注射液及转化糖电解质注射液的干扰较少,故可用紫外分光光度法检测其吸光度。
试验结果表明,间苯三酚与6种输液的配伍液的pH值、主药含量在前6 h变化不显著;与4种含糖溶液配伍液的5-HMF的吸光度6 h内均在限度控制范围内,且颜色无显著变化,也无明显可见异物;与2种不含糖输液配伍液的颜色无显著变化,也无明显可见异物。6种配伍液不同时间点的高效液相色谱图也未见有新物质色谱峰。说明常温下,间苯三酚与临床6种常用输液配伍,在6 h内相对稳定。药品使用溶媒应遵照药品说明书,本试验可为临床特殊情况下使用该药提供参考。
[1]Louvel D,Delvaux M,Staumout G,et al.Intracolonic injection of glycerol:a model for abdominal pain in irritable bowel syndrome[J].Gastroenterology,1996,110(2):351.
[2]Chassany O,Bonaz B,Bruleydes VS.Acute exacerbation of pain in irritable bowel syndrome:efficacy of phloroglucinol/trimethylphloroglucinol-a randomized,double-blind,placebo-controlled study[J].Aliment Pharmacol Ther,2007,25(9):1115.
[3]李健和,胡弘霞,黎银波,等.注射用间苯三酚的制备、质量控制及稳定性考察[J].中国药房,2007,18(4):286.
[4]陈咏昕,林冬煌.高效液相色谱法测定间苯三酚口服冻干片的溶出度[J].广东药学院学报,2005,21(6):679.
[5]何伍,凌霄.含葡萄糖注射液中5-羟甲基糠醛限度的检测方法[J].中国医药工业杂志,2008,39(1):47.
