无糖型藏药安儿宁颗粒工艺研究
2013-11-29李宝文马文俊东知多杰
李宝文 马文俊 贾 明 东知多杰
(青海阿如拉藏医药研究开发有限公司,青海 西宁 810003)
安儿宁颗粒为藏药复方制剂,由天竺黄、红花、人工牛黄、岩白菜、甘草、高山辣根菜、短管兔耳草、白檀香、唐古特乌头九味中药组成,具有清热祛风,化痰止咳的功效。用于小儿风热感冒,咳嗽有痰发热咽痛,上呼吸道感染等。目前,已上市的安儿宁制剂为安儿宁颗粒,是以蔗糖为辅料,以传统的湿法制粒工艺制备而成,其蔗糖含量近90%。由于蔗糖不宜于糖尿病等禁糖患者,且易导致龋齿及引发肥胖等。鉴于安儿宁颗粒含蔗糖量大,每次服用量大。本研究以传统藏医药理论为指导,在不改变提取工艺的基础上,以甜菊素为辅料制备无蔗糖型安儿宁颗粒—安儿宁颗粒(无蔗糖),其工艺是集混合、制粒、干燥等一体的制备颗粒技术,是一种低能耗、低污染、绿色的颗粒成型方法。
1 材料和方法
1.1 材料:处方中组成的各中药材(购自青海九州中药饮片厂);辅料:甜菊素(河南明瑞食品添加剂有限公司)可溶性淀粉(河南明瑞食品添加剂有限公司);水溶性淀粉(河南明瑞食品添加剂有限公司);糊精 (河南明瑞食品添加剂有限公司),以上辅料均为药用级。
1.2 方法
1.2.1 浸膏制备[1-2]:除人工牛黄外,红花、白檀香提取挥发油后的药渣与其余药材混合,加水提取两次,第一次3h,第二次2h,合并煎液,滤过,滤液浓缩至相对密度为1.26(50℃)的清膏,加入两倍量的95%乙醇,搅拌均匀后静置24h,取上清夜,浓缩至相对密度为 1.30 ~1.35(50℃)的清膏。备用。
1.2.2 颗粒成型率的测定:取样品颗粒称重,分别过1号筛与4号筛,收集能通过1号筛而不能通过4号筛的颗粒称重,按下式计算成型率:
成型率(%)=通过1号筛而不能通过4号筛颗重 /样品颗粒重 ×100%
1.2.3 吸湿百分率的测定:称取样品颗粒约1g,置称量瓶干燥至恒重后精密称取重量,置于相对湿度为75% 的密闭干燥器中,室温放置,定时取出精密称量,按下式计算吸湿百分率。吸湿百分率(%)=(吸湿后重量 -吸湿前重量)/吸湿前重量 ×100%
2 颗粒辅料的筛选
2.1 辅料的筛选[3-4]:实验设计见表 1。

表1 辅料的筛选
取3份稠膏,每份50 g,按表 1方案进行实验。按上表设计,加入所列相应的辅料各200 g,混匀,用95% 乙醇制软材,过14目筛制粒,55℃烘干,依次过1号筛及4号筛,收集通过1号筛而不能通过4号筛的颗粒,称重,计算成型率。取上述各样品颗粒约1 g,60℃恒重后,精密称定,置于相对湿度为75% 的密闭干燥器中,室温放置,隔24 h测定其吸湿性,至颗粒轻摇不散完全吸湿结块。将不同辅料制成的样品颗粒的成型率与吸湿百分率进行综合评分,确定最佳辅料。结果见表2。

表2 单一辅料筛选综合评分
3号样品的成型率及吸湿率均较差,从综合评分可知,用糊精作为辅料效果较好,颗粒成型率高 ,吸湿性小 ,符合颗粒剂辅料的质量要求。
2.2 根据糊精、甜菊素的用量设计试验
2.2.1 取6份提取浓缩好的清膏(为一个处方量的1/10);
2.2.2 根据已确定的糊精、甜菊素总用量(263.3g、425g),以及甜菊素代替蔗糖矫味的用量(3、4、5g)进行试验,达到确定糊精、甜菊素用量的目的。设计试验
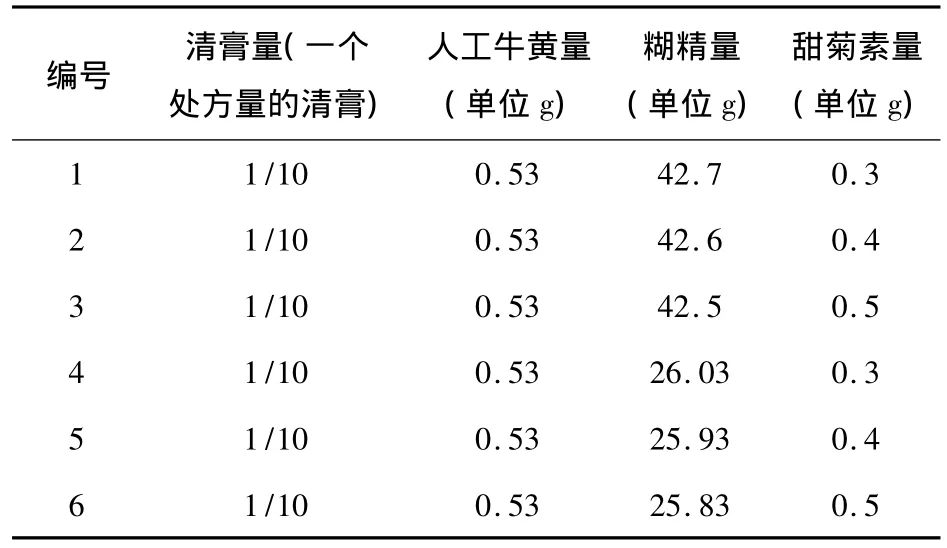
表3 糊精、甜菊素的用量设计试验
根据以上原辅料配比进行试验,1、2、3号配比有利于后续工艺研究的进行,便于烘干、粉碎;而4、5、6号配比不利于后续操作。因此确定处方中辅料总量为430g,即制剂量为500g。
在确定制剂量的基础上,针对1、2、3号试验,进行了后续操作(烘干、粉碎),得到的细粉进行甜菊素用量的确定性试验。
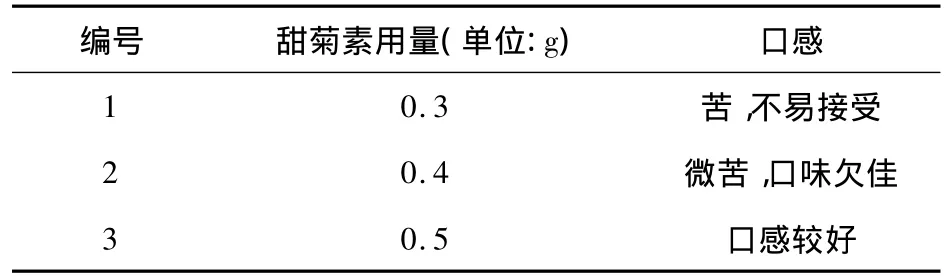
表4 甜菊素用量的确定性试验
试验结果表明:甜菊素作为矫味剂,1/10处方量的清膏用量0.5g为宜。即一个处方甜菊素用量为5g。
3 成型工艺的选择[5]
取剩余的清膏,加0.4倍处方量的人工牛黄和糊精170g、甜菊素2g混匀,烘干,粉碎成细粉与试验3所得的细粉混合。备用。
3.1 粘合剂乙醇浓度的选择
分别以65%、75%、85%不同浓度的乙醇为粘合剂制粒,选择颗粒的合格率、机械强度、溶解性作为考察指标,确定适宜的制粒酒精浓度。
试验方法:取上述粉碎的细粉,均匀的分成3份,分别以 65%、75%、85% 不同浓度的乙醇为粘合剂制粒[6-7],制粒采用手工挤压法,合格率经制得的颗粒烘干后整粒考察。其试验结果如下:

表5 粘合剂乙醇浓度的选择
试验结果表明:75%的乙醇制得的颗粒,合格率高、不易碎、溶解性合格。因此选用75%乙醇进行颗粒的制备。
3.2 挥发油的处理[8]
挥发油用少量的乙醇溶解,在合格的颗粒上喷洒均匀,密闭放置一段时间,即可。
3.3 颗粒流动性的考察
置的坐标纸上1cm的高度处,将75%乙醇制得的颗粒沿漏斗倒入直到形成的粉末圆锥休尖端接触到最下的漏斗口为止。由坐标纸测出圆锥底部的直径,计算出休止角(tgα=H/R/2)。结果见表6。
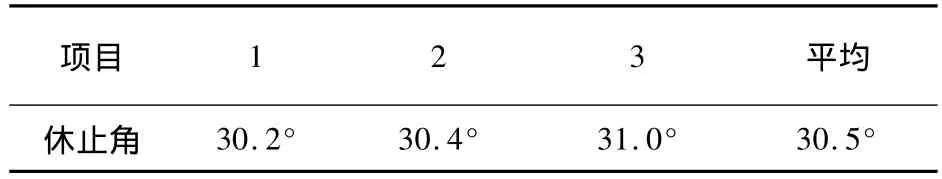
表6 休止角测定
结果表明:颗粒休止角小于45°,说明75%乙醇制得的颗粒流动性较好。
3.4 颗粒临界相对湿度的测定
3.4.1 试验方法:将75%乙醇制得的颗粒放入恒重的称量瓶内[9-10],准确称量,分别置于盛有不同浓度硫酸和不同盐的饱和溶液的玻璃干燥器内,于25℃恒温放置72h,取称重,计算吸湿百分率。以吸湿率为纵坐标,相对湿度为横坐标,绘制临界相对湿度曲线。
3.4.2 试验结果:见表7。
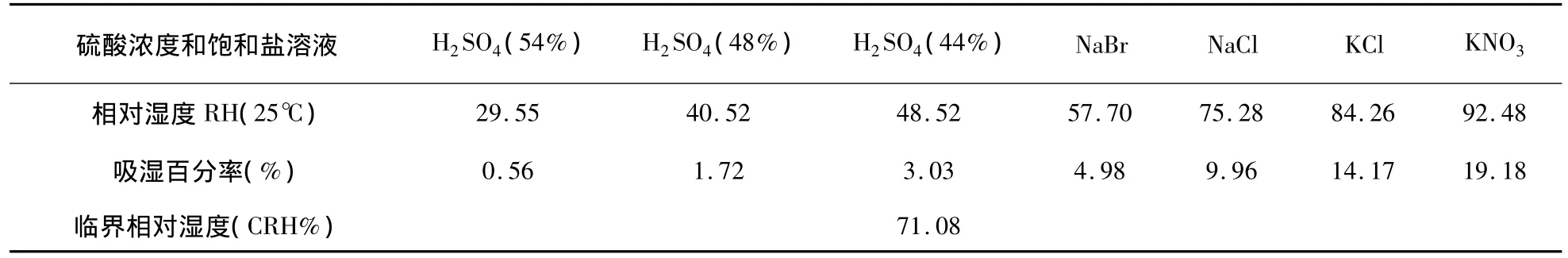
表7 临界相对湿度考察结果
表7 结果表明,颗粒的临界相对湿度为71.08%,即制粒、填充时的车间环境湿度应控制在71.08%以下。
4 制备工艺的小试生产考察
根据确定的制法,进行三批小试生产,按1倍处方量进行投料,以考察工艺的稳定性,重现性,试验结果如表8。

表8 小试生产考察结果
小试结果表明:确定的工艺具有较好的重现性,稳定性,可以进行中试生产。
5 中试生产考察
根据确定的制法,以及小试生产的技术参数,按处方10倍量投料,进行中试生产,以达到进一步考察工艺的稳定性,重现性的目的,试验结果如表9。
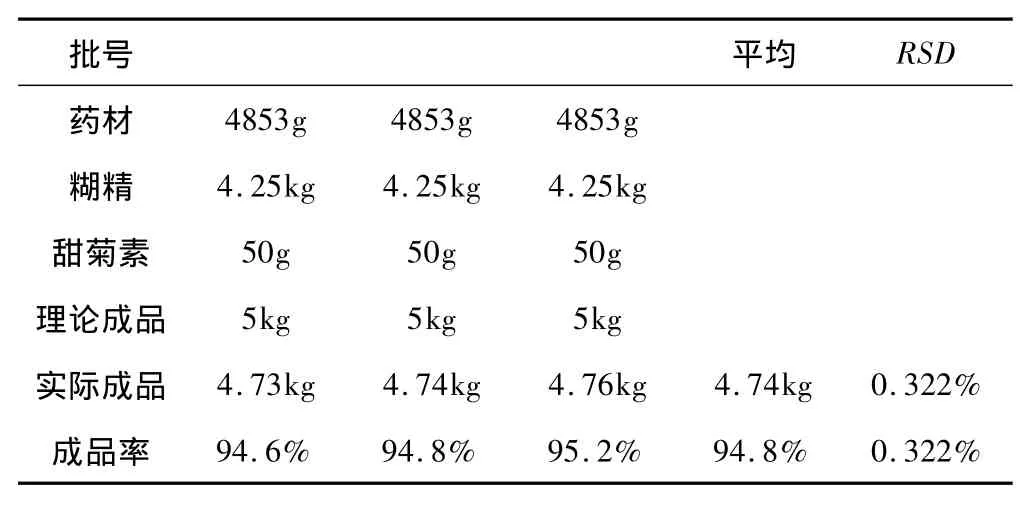
表9 中试生产考察结果
中试结果表明:确定的工艺简便,具有较好的重现性,稳定性,工艺容易控制,产品成品率高。
6 中试生产颗粒的包装
此次试验确定的处方制剂量是原处方制剂量的一半,为保证有效成分理论上保持一致,经检验合格的中试生产的颗粒,按原规格的1/2进行包装,全检合格后入库。
7 结论
现生产的安儿宁颗粒所用辅料为蔗糖,使得一些糖尿病患者不能服用;大量蔗糖的应用,其服用量大。经过此次研究,欲将蔗糖辅料更换,使其治疗人群范围扩大;服用量减小。我们根据处方中药物的性质,结合制剂的稳定性、生产的可行性,对颗粒剂的更换辅料制备工艺进行了研究,并确定了相关工艺参数。安儿宁颗粒制成无糖型颗粒后,增加了适用范围,扩大了患者群,减少了辅料用量,为其扩大临床应用提供了依据。
[1]谢秀琼.中药新制剂开发与应用[M].人民卫生出版社,1994.
[2]杨基森,等.中药制剂设计学[M].贵州科技出版社,1992.
[3]罗明生,等.药剂辅料大全[M].四川科技出版社,1995.
[4]刘振丽,等.中成药,1996,18(2):4.
[5]刘祥兰,等.中成药,2002,22(6):402.
[6]沈红梅,等.中草药,1995,26(2):105.
[7]沈阳药学院.药剂学,人民卫生出版社,1984.
[8]中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准[S].藏药第一册.1995.140.
[9]中华人民共和国国家药典委员会.中国药典(一部)[S].北京:化学工业出版社,2005.
[10]郑俊华.生药学[M].第3版.北京:人民卫生出版社,1999.279.
