皮炎康颗粒对小鼠慢性变应性接触性皮炎的实验研究
2013-11-21关小红王小辉李钰瑶
刘 彬 关小红 王小辉 李钰瑶
(1辽宁中医药大学附属医院皮肤科,沈阳,110032;2美国加利福尼亚州安大略基督教高中加州安大略市西菲力刀飞亚街931号ca91762,加利福尼亚,91762)
皮炎康颗粒由炙黄芪、黄芩、黄柏、白芍、白术、当归、大黄、青蒿、生地黄、甘草等中药组成,具有清热利湿解毒、凉血疏风解痒、益气养血固表之功效,是我科临床协定方,长期应用于湿热及血虚证的急、慢性变应性接触性皮炎和急、亚急性、慢性湿疹的治疗并取得了比较满意的临床疗效。本实验通过观察皮炎康颗粒对小鼠慢性变应性接触性皮炎耳肿胀度、胸腺指数、脾指数的影响,为进一步临床应用提供了实验依据。
1 资料及方法
1.1 药物 皮炎康颗粒(含药材2.55 g生药/kg),由辽宁中医药大学附属医院实验中心提供,批号:20110501。氯雷他定片,国药准字H10970410,由上海先灵葆雅制药公司生产,批号09JRXF1043,规格10 mg/片,1 次/d,1 片/次。
1.2 动物 SPF级雄性昆明种小鼠,体重18~22 g,购自中国医科大学实验动物部,生产许可证号:SCXK(辽)2008-0005。于辽宁中医药大学附属医院实验中心饲养,许可证号:SYXK(辽)2007-0010。实验室温度20℃ ~23℃,湿度50% ~60%。
1.3 试剂及仪器 2,4-二硝基氯苯(分析纯),天津市津科精细化工研究所,批号:20070622;丙酮(分析纯),沈阳化学试剂厂;批号:0303011:大豆油,嘉里粮油有限公司生产,批号:20090522;娃哈哈纯净水,杭州娃哈哈集团有限公司生产。YLS-Q4耳肿打耳器,山东省医学科学院;电子数显卡尺,桂林广陆数字测控股份有限公司生产;FA2004分析天平,由上海舜宇恒平科学仪器有限公司生产;TD10001电子天平,浙江余姚金诺天平仪器有限公司。
2 方法
2.1 药品的配制方法 取皮炎康颗粒,用蒸馏水配制成所需的浓度,给药体积为小鼠40 mL/kg。
2.2 剂量选择和分组 根据受试药临床使用的剂量和预试验的结果设定空白组、模型组、皮炎康颗粒高(4倍等效量)、中(2倍等效量)、低(等效量)3个剂量组和氯雷他定片高剂量(4倍量)组。
2.3 小鼠慢性ACD模型的建立[1]及给药方法[2]取体重18~22 g的小鼠60只,随机分为6组,空白组、模型组、氯雷他定片组、皮炎康颗粒4倍量(58.73 g生药/kg)组、2倍量(29.47 g生药/kg)组、1倍量(14.73 g生药/kg)组。每组10只,实验前1 d,在小鼠背部去毛,面积约4 cm2,实验当日各组(除空白组)于去毛区涂以7%DNCB液(丙酮/大豆油 =4∶1)100 μL致敏1次。5 d后涂1%DNCB丙酮液5 μL于小鼠右耳内侧激发,每隔3 d激发1次,左耳涂抹等量基质,空白组左右耳均涂抹等量的基质。分别于第4次激发后72 h处死小鼠。致敏前1 d各组按规定的剂量灌胃给药,空白组和模型组给予同体积蒸馏水,1次/d,再于末次激发后6 h灌药。
2.4 取材方法 激发后72 h,将动物颈椎离断处死,用游标卡尺测量小鼠耳中部厚度后立即剪下双侧耳廓备检。使用0.8 cm半径的金属耳肿打孔器在左右耳中部打孔,取相同大小的耳组织,用电子天平称重,计算左右耳重量差。完整摘取小鼠胸腺及脾,用电子天平测定其重量,分别以每10 g小鼠的脾重(mg)和胸腺重(mg)作为脾指数和胸腺指数。
3 结果
3.1 皮炎康颗粒对慢性ACD小鼠耳厚度差、重量差的影响 模型组与空白组相比耳重量差、耳厚度差均明显增加,与空白组相比,有统计学意义(P<0.01)。皮炎康颗粒各剂量组和氯雷他定片组均能减轻小鼠耳重量差、耳厚度差,与模型组相比,有统计学意义(P<0.01或P<0.05)。
3.2 皮炎康颗粒对慢性ACD小鼠胸腺指数、脾指数的影响 由表2可以看出,模型组与空白组相比胸腺指数、脾指数均明显增加,与空白组相比,有统计学意义(P<0.01)。皮炎康各剂量组和氯雷他定片组均能降低小鼠胸腺指数、脾指数,与模型组相比,有统计学意义(P<0.01或P<0.05)。
表1 皮炎康颗粒对慢性ACD模型小鼠耳肿胀的影响(±s)
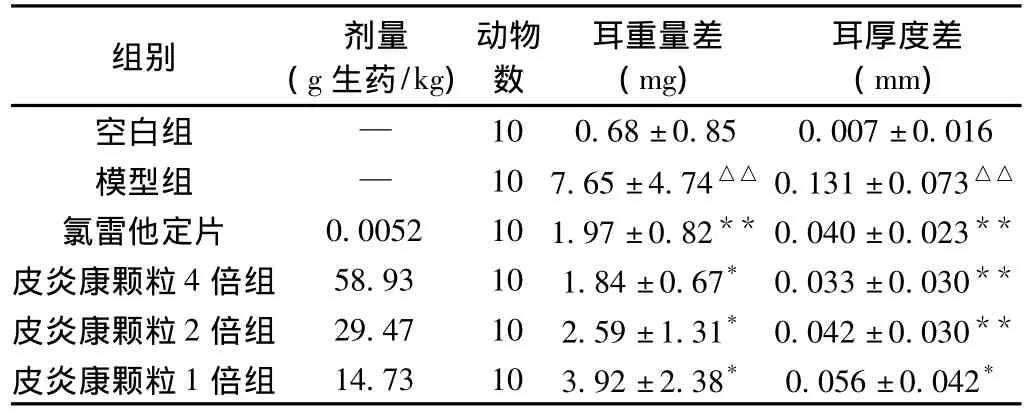
表1 皮炎康颗粒对慢性ACD模型小鼠耳肿胀的影响(±s)
注:与模型组相比有统计学意义(*P<0.05,**P<0.01);与空白组比较有统计学意义(△△P<0.01)。
?
表2 皮炎康颗粒对慢性ACD模型小鼠脏器指数的影响(±s)
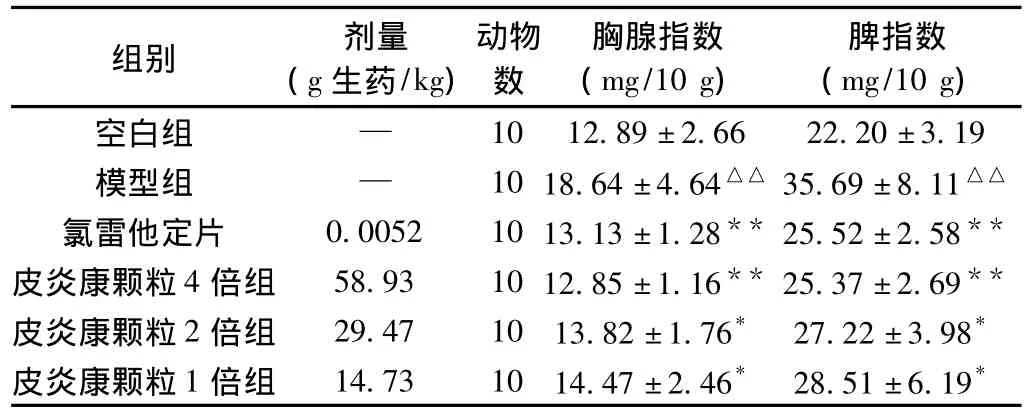
表2 皮炎康颗粒对慢性ACD模型小鼠脏器指数的影响(±s)
注:与模型组相比,*P<0.05,**P<0.01;与空白组相比,△△P<0.01。
?
4 讨论
ACD是机体经皮肤接受抗原刺激后当再次接触相同抗原时发生以皮肤损害为主要特征的Ⅳ型变态反应[3-4],导致以单核细胞浸润为主,变性坏死为特征的炎性反应[5]。ACD发生的机理是针对皮肤接触性变应原发生的迟发型超敏反应,多数由Th1型CD4+T细胞激发活化效应细胞和分泌细胞因子,介导的炎症反应[6]。ACD接触部位甚至以外的部位表现为红斑、水肿、水疱甚至大疱[7]。胸腺及脾是重要的免疫器官,机体发生超敏反应的同时脾脏、胸腺肿大,重量增加。脾指数、胸腺指数可衡量药物对免疫器官的抑制作用[8]。而动物实验一般又常以鼠左右耳厚度和质量差值作为衡量炎性反应轻重程度指标。随着科学技术的提高,工业化的发展,出现了许多新的过敏原,接触性皮炎和湿疹发病率都呈逐渐上升的趋势。目前抗组胺药广泛应用于过敏性疾病的治疗,但由于其作用机制主要对Ⅰ型超敏反应有着良好拮抗作用,治疗Ⅳ型变态反应效果不理想。虽有文献报道新一代抗组胺药物在体外呈现良好抗炎,抑制细胞的趋化以及对细胞介质的抑制作用,但是往往其浓度达到目前所应用的体内药物浓度数百倍以上[9]。传统医学对慢性变应性接触性皮炎和慢性湿疹的治疗有着大量临床实践和经验积累[10-11],特别对中药的有效成分的研究显示,其可作用于过敏反应不同环节[12-16]。皮炎康颗粒作为科内临床协定方长期用于上述疾病的治疗并取得了比较满意的临床疗效。此方由黄芪、黄芩、黄柏、白芍、白术、当归、大黄、青蒿、生地黄、甘草等组成。方中黄芩、黄柏、大黄、青蒿、生地黄、牡丹皮、白鲜皮清热利湿,凉血疏风;而黄芪、白芍、白术、当归健脾利湿,养血益气,固表御邪;甘草调和诸药。目前慢性变应性接触性皮炎、慢性湿疹的现代医学治疗是以抗炎、抗组胺为主要方法,同时可配以免疫调节治疗。本方的治疗原则与现代医学治疗方法有相通之处,既清热利湿、凉血疏风,亦养血益气、固表御邪。本动物实验研究结果表明,皮炎康颗粒可改善DNCB引起的慢性变应性接触性皮炎模型小鼠的耳部肿胀,具有一定的抗炎作用,同时可降低小鼠胸腺、脾指数。
[1]李敏.疏风饮对变应性接触性皮炎小鼠脾指数、胸腺指数及IFN-γ与 IL-4分泌的影响[J].实用中医内科杂志,2011,25(1):24-25.
[2]郝光荣.实验动物学[M].2版,上海,第二军医大学出版社,2002:276.
[3]Bradley J,McCluskey J.Clinical Immunology[M].Chapter 16.Oxford:Oxford University Press,1997:330-348.
[4]Abbas AK.Cellular and molecular immunology[M].3rd ed.Chaper 14 Philadelphia:W.B.Saunders company,1997:301-308.
[5]陈妍,郭在培.变应性接触性皮炎的原位免疫学研究[J].华西医学,2006,21(1):217-218.
[6]SehimiuT,AbeR,NishihiarJ,et al.Impaired contact hypesensitivity in macrophage migration inhibitory factor- deficient mice.EurJ Immunol,2003,33:1478-1487.
[7]赵辨.中国临床皮肤病学[M].南京:江苏科学出版社,2009:717-718.
[8]梁秀宇.消风散对变应性接触性皮炎抑制作用及其免疫学机制实验研究[D].沈阳:辽宁中医药大学,2007.
[9]Walsh GM,Annunziato L,Frossard N,etal.New insigts into the second generation antihisatanmines[J].Durgs,2001,61:207-236.
[10]杨宝华,陈德宇,肖顺汉.消风胶囊对小鼠迟发型超敏反应的影响及其作用机理研究[J].中国中西医结合皮肤性病学杂志,2003,2(1):13-15.
[11]杨宝华,陈德宇,肖顺汉.消风胶囊对小鼠迟发型超敏反应的影响及其作用机理研究[J].中国中西医结合皮肤性病学杂志,2003,2(1):13-15.
[12]黄礴,吴铁,樊翌明,6种中药抑制二硝基氟苯所致小鼠接触性皮炎的实验研究[J].现代中西医结合杂志,2007,16(13):1756-1757.
[13]韩春雷,陈学荣,马俊江.氧化苦参碱对大鼠变应性接触性皮炎药效学作用[J].北京医科大学学报,1996,28(1):59-61.
[14]郝飞.甘草酸国外研究进展[J].中国药房,2001,12(8):500-502.
[15]郑咏秋,魏伟,戴敏,等.木瓜总甙抑制小鼠接触性超敏反应及对胸腺T淋巴细胞亚型的调节作用[J].中国药理学通报,2004,20(9):1016-1020.
[16]陈子珺,李庆生,淤泽愽,等.防风与刺蒺藜抗过敏作用的试验研究[J].云南中医中药杂志,2003,24(4):30-32.
