GC-EI/MS同时测定水中9种N-亚硝胺
2013-11-15鲜啟鸣
李 婷,鲜啟鸣
(污染控制与资源化研究国家重点实验室,南京大学环境学院,江苏 南京 210023)
0 引 言
饮用水中的N-亚硝胺不仅与人类膀胱癌的发生有关[1-2],还可能诱导食管和肝脏等器官产生肿瘤[3-4]。目前水中发现的N-亚硝胺包括:N-亚硝基二甲胺(NDMA)、N-亚硝基甲基乙基胺(NMEA)、N-亚硝基二乙基胺(NDEA)、N-亚硝基二丙基胺(NDPA)、N-亚硝基二丁基胺(NDBA)、N-亚硝基吡咯烷(NPyr)、N-亚硝基吗啉(NMor)、N-亚硝基哌啶(NPip)和N-亚硝基二苯胺(NDPhA)。美国加利福尼亚州规定饮用水中NDMA、NDEA和NDPA的浓度限制均为10 ng/L[5],远低于US EPA中对常规消毒副产物THM4和HAA5的浓度限值:80μg/L和60μg/L。因此,检测水中痕量的N-亚硝胺,对于评价饮用水质,进一步研究去除水中的N-亚硝胺以提高饮用水的安全性具有重要意义。
目前,水中N-亚硝胺的提取方法主要有固相萃取(SPE)和固相微萃取(SPME)。测定仪器主要有GC-NCD[6]、GC-NPD[7]、GC/MS[8]、GC/HRMS[9]、GC/MS/MS、LC/MS/MS[10]、LC/MS/HRMS[11]和 UPLC/MS/MS[12],一般选用CI源为离子源。对于不同的前处理,固相微萃取影响因素多、灵敏度低,仅适用废水中N-亚硝胺的检测[13]。对于不同的进样方式,采用LC进样时,检测低分子量的N-亚硝胺易受杂质的影响[10],采用GC进样效果较好。对于不同的检测器,MS检测的效果优于 NCD和NPD[6,14],与 HRMS和 MS/MS相比也可以满足分析要求[8-9,15]。因此本实验采用固相萃取、GC/MS测定9种N-亚硝胺,确定了水样前处理和采用EI作为离子源、GC/MS检测N-亚硝胺的条件,并应用于测定自来水厂水样中9种N-亚硝胺的含量。
1 材料与方法
1.1 仪器、材料与试剂
仪器材料:TRACE GC ULTRa型气相色谱与FINNIGAN Polaris Q型质谱联用仪(美国Thermo ELECTRON CORPORATION公司);PTA-5型色谱柱(美国 Supelco公司):30m×0.25mm×0.5μm;12管防交叉污染固相萃取装置(美国Supelco公司);RV10 basic型旋转蒸发仪(德国IKA集团);SE812型氮吹仪(北京帅恩科技有限责任公司);SPE小柱(2g椰壳活性炭/6mL,美国Restek公司);高纯氮气(南京天泽气体有限责任公司);MILLI-Q A10超纯水机(美国Millipore公司)。
试剂:2 000 mg/L 9种N-亚硝胺的混合标准溶液(美国Supelco公司);NDMA-d6和 NDPA-d14(98%,美国 Cambridge Isotope Laboratories公司);二氯甲烷(HPLC级,美国ROE Scientific公司);甲醇(HPLC级,美国Tedia公司);无水硫酸钠(分析纯,南京化学试剂有限公司);硫代硫酸钠(分析纯,南京化学试剂有限公司);超纯水(经紫外灯照射后使用);蒸馏水。
1.2 标准溶液
以二氯甲烷为溶剂,配置9种N-亚硝胺及NDMA-d6的混合标准溶液,浓度依次为:2,5,10,20,50,100,200,500,1000μg/L,每一浓度的标准溶液中定量内标NDPA-d14的浓度均为250μg/L。
1.3 样品制备
向棕色采样瓶中预先加入浓度为100mg/L的硫代硫酸钠,以脱去水样中的氯。采样时,水样充满采样瓶。采样后水样在4℃下避光保存,在14d内完成分析。水样分析前NDMA-d6加标浓度为20ng/L。
2 结果与讨论
2.1 气质联用仪分析条件的优化
采用GC/MS分析9种N-亚硝胺,EI为电离源,高纯氦气为载气,不分流进样1μL。
实验就不同的进样口温度(140,200,250℃)、传输线温度(170,280℃)、离子源温度(150,170,210℃)和不同的载气流速(1.0,1.5,2.0 mL/min)对 N-亚硝胺分离及响应的影响分别进行了比较。结果发现:进样口温度、传输线温度和离子源温度对N-亚硝胺的分离及响应的影响不大。从防止污染的角度考虑,最终选择进样口温度为250℃,传输线温度为280℃,离子源温度为210℃。较低的载气流速有利于N-亚硝胺的分离,但会降低响应,因此选择了较高的载气流速2.0mL/min。同时,通过分析柱温对9种N-亚硝胺分离的影响,确定了N-亚硝胺的GC/MS程序升温条件:初始柱温设为35℃,保持4min,以8℃/min的速度升至220℃,再以40℃/min的速度升至280℃,保持2min。采用保留时间和特征碎片离子定性,选择离子检测法(SIM)定量,N-亚硝胺的峰形见图1,具体参数见表1。

图1 2mg/L 9种N-亚硝胺、NDMA-d6及250μg/L NDPA-d14标准溶液的色谱图
2.2 样品前处理条件的选择
2.2.1 固相萃取材料的选择与活化
N-亚硝胺固相萃取常用的材料有椰壳活性炭、Ambersorb572及Ambersorb 572与LiChrolut EN的组合材料。不同的填充材料对不同N-亚硝胺的萃取效果不同。椰壳活性炭对NDMA的萃取回收率远高于Ambersorb 572和Ambersorb 572+LiChrolut EN,分别为 88%[9],43%[9]和 60%[16],而 NDMA 是毒性较大、研究较为广泛的N-亚硝胺之一,因此选用椰壳活性炭作为固相萃取材料。采用椰壳活性炭萃取前,依次用6mL二氯甲烷、12mL甲醇和15mL超纯水活化。
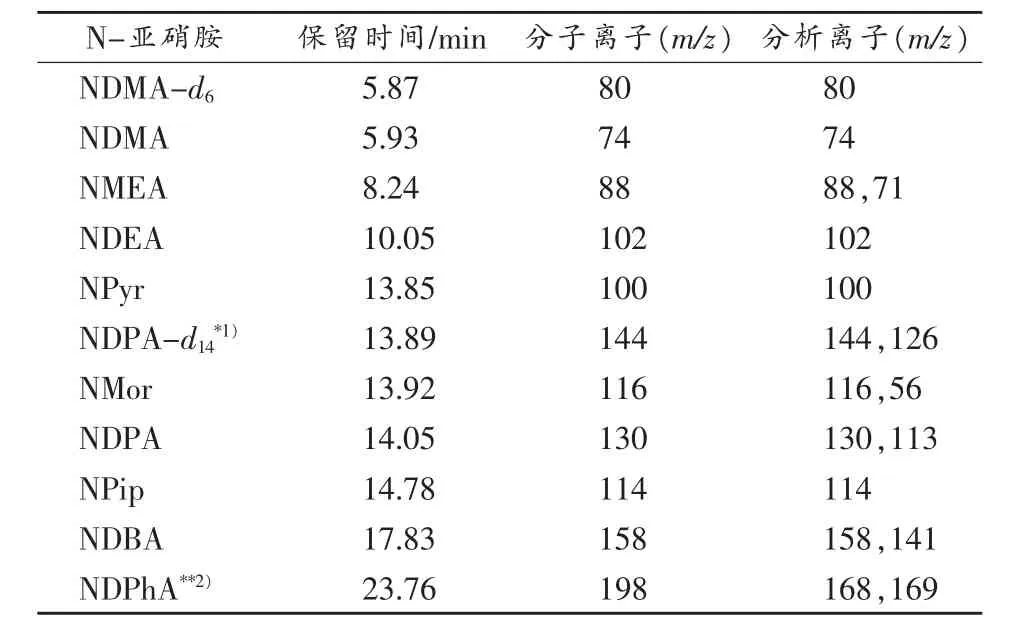
表1 N-亚硝胺的GC/MS分析条件
2.2.2 水样体积及浓缩倍数的选择
根据已有的研究,水样的体积一般选取0.25,0.5,1 L,由于自来水样中N-亚硝胺的浓度低至ng/L级别,而GC/MS分析时选用的是EI源,响应较CI源低,因此,水样体积选为1L,以提高方法的检出性能。
不同N-亚硝胺在GC-EI/MS上检出的最低浓度为2~20μg/L,因此要将水样浓缩。已有研究一般将水样浓缩500倍、1000倍和2500倍,即当提取液浓缩后的浓度为20μg/L时,对应水样中N-亚硝胺的浓度分别为40,20,8 ng/L,而目前N-亚硝胺的浓度限值一般为10ng/L,因此应尽量降低N-亚硝胺的检出限。据此,水样的浓缩倍数选为5000倍,即1L水样应浓缩至0.2mL。
2.2.3 水样的萃取、洗脱与干燥
试验分别比较了5,10 mL/min的水样萃取流速,结果N-亚硝胺的回收率无显著差异。为缩短样品处理时间,以10mL/min为最终萃取流速。水样萃取后,用15mL二氯甲烷洗脱,洗脱液经6 g无水硫酸钠(预先用二氯甲烷清洗湿润)干燥,再用6mL二氯甲烷淋洗无水硫酸钠,收集流出液。
2.2.4 提取液浓缩条件的优化
由于N-亚硝胺为挥发性物质,为减少在提取液浓缩时N-亚硝胺的损失,在浓缩前向提取液中加入500 μL 甲醇,同时加入 50 ng NDPA-d14混匀,采用旋转蒸发在室温下浓缩至1mL,再加入2mL二氯甲烷冲洗内壁,在25℃水浴下缓慢氮吹至0.2mL。由于甲醇的沸点略高于二氯甲烷,加入甲醇可以尽量减少N-亚硝胺在氮吹时随二氯甲烷挥发而造成的损失。旋转蒸发可以极大缩短液体浓缩的时间,21mL洗脱液浓缩至1mL只需6~8min,而3mL预浓缩液氮吹至0.2mL需要1h。实验表明:21mL洗脱液旋蒸发预浓缩再氮吹至0.2 mL与直接氮吹浓缩至0.2 mL相比,N-亚硝胺的回收率可以增大4%~12%。
2.3 方法的线性、检出限、回收率和精密度
采用内标法绘制2~1 000 μg/L不同N-亚硝胺的标准曲线,r2范围为 0.9976~0.9996,见表 2。

表2 N-亚硝胺的标准曲线
在选定的仪器条件下,分别用标准偏差(SD)法和信噪比(S/N)法测定N-亚硝胺的检出限(LOD)。SD法是配制7份加标浓度为10ng/L的水样,测定N-亚硝胺的浓度,计算标准偏差,根据标准偏差计算检出限。S/N法是取仪器响应信噪比为3时对应水样中N-亚硝胺的浓度。SD法和S/N法的检出限分别为 0.8~4.3ng/L 和 0.2~5.0ng/L,详见表 3。
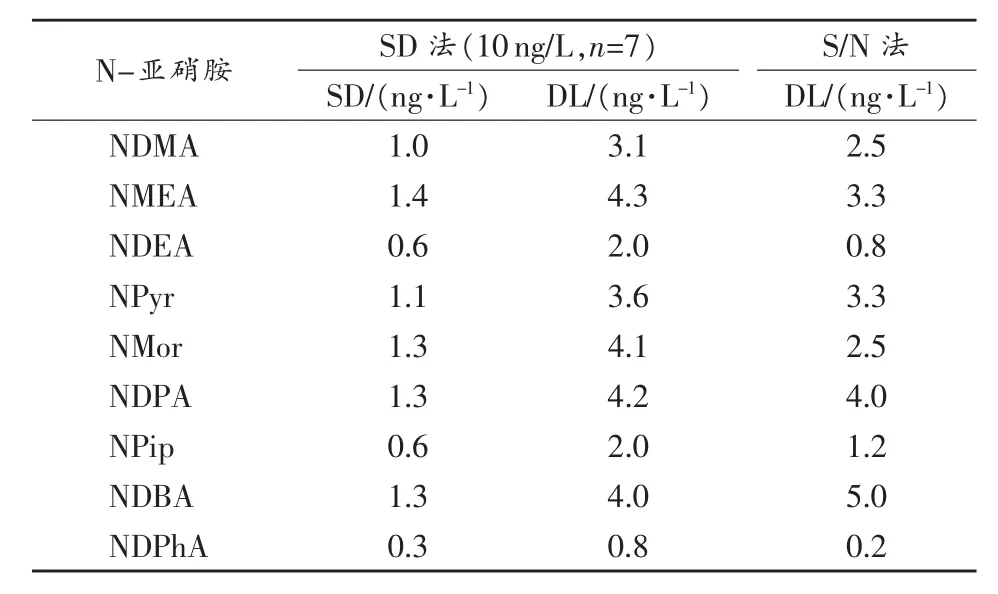
表3 N-亚硝胺的检出限
实验分别测定了蒸馏水加标10,50,200 ng/L N-亚硝胺的回收率,分别平行测定7次,计算相对标准偏差(RSD)。结果加标10ng/L N-亚硝胺的回收率为75%~103%,加标50ng/L N-亚硝胺的回收率为62%~101%,加标200 ng/L N-亚硝胺的回收率为48%~97%,详见表4。除加标50ng/L和200ng/L NDPhA的回收率低于70%外,其余回收率结果均在70%~130%范围内,满足EPA 521的要求。

表4 N-亚硝胺蒸馏水加标回收率
2.4 实际样品的测定
选取以江水、河水、湖水为水源的3家水厂I、II、III的进水、出水和管网水分别进行测试,结果见表5。水样NDMA-d6加标的回收率均在70%以上。其中水厂III的进水、出水和管网水中检测的NDEA的色谱图见图2。
不同水厂检出N-亚硝胺的种类和浓度不同,表明N-亚硝胺与源水水质以及水厂的处理工艺有关。水厂进水中检出的N-亚硝胺种类多、浓度较高,而管网水检出的N-亚硝胺种类少且浓度低,表明饮用水厂的处理工艺可有效去除部分N-亚硝胺。
NDMA在水厂Ⅲ的进水、出水和管网水中的浓度逐渐升高,可能是源水中含有的NDMA前驱物,在水处理过程中难以去除,在管网中与消毒剂继续反应生成。NDMA在水厂III的管网水中浓度达45.3ng/L,低于上海报道的管网水浓度78.93ng/L[17]。
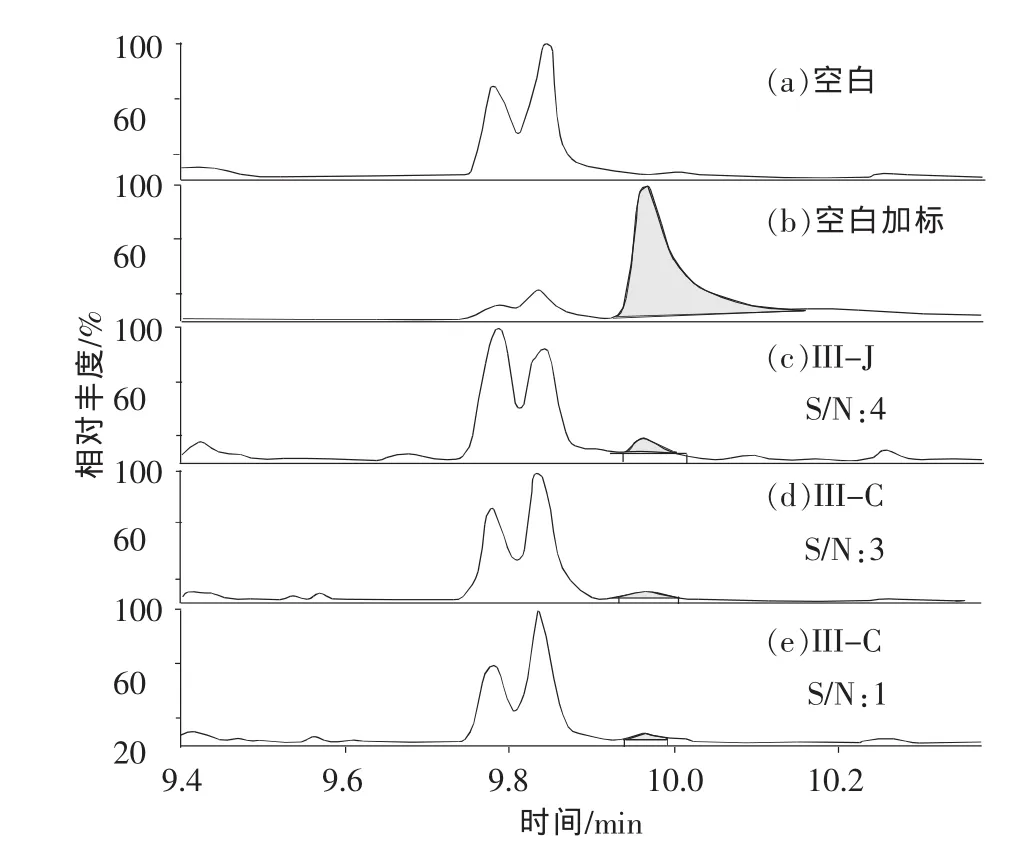
图2 水厂Ⅲ检出的NDEA色谱图
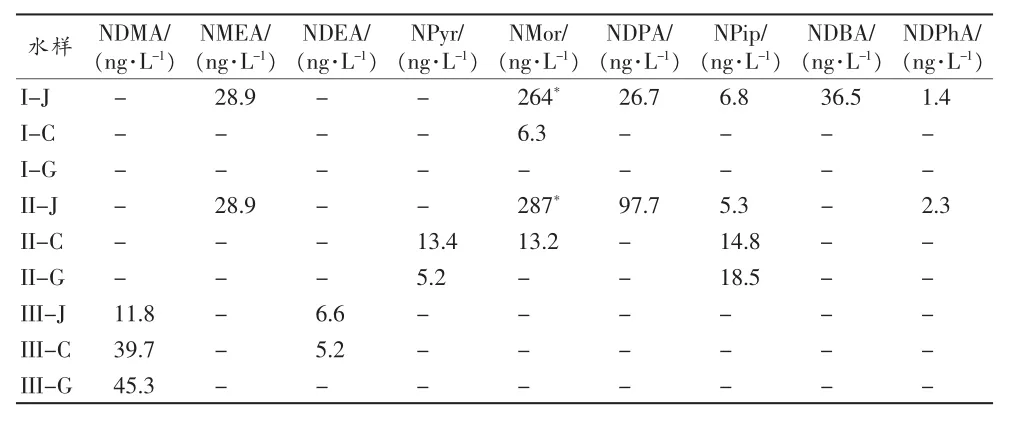
表5 不同水厂不同水样中N-亚硝胺的浓度1)
3 结束语
本方法采用椰壳活性炭固相萃取、建立了GC-EI/MS测定水中9种N-亚硝胺的定性定量方法,该方法灵敏度高、回收率好。能适用于自来水厂中N-亚硝胺的痕量分析。
[1]RadomskiJ L,Greenwald D,Hearn W L,et al.Nitrosamine formation in bladder infections and its role in the etiology of bladder cancer[J].Journal of Urology,1978,120(1):48-50.
[2]Mostafa M H,Sheweita S A,O’Connor P J.Relationship between Schistosomiasis and bladder cancer[J].Clinical Microbiology Reviews,1999,12(1):97.
[3]World Health Organization International Agency for Research on Cancer,IARC Monographs on the Evaluation of Carcinogenic Risks to Humans,volume 17:Some NNitroso Compounds,1978[EB/OL].[2013-3-7].http://monographs.iarc.fr/ENG/Monographs/allmonos47.php.
[4]Brown J L.N-Nitrosamines[J].Occupational Medicine-State of the Art Reviews,1999,14(4):839-848.
[5]California Departmentof Public Health.NDMA and other nitrosamines-Drinking water issues [EB/OL].[2012-3-7].http://www.cdph.ca.gov/certlic/drinkingwater/pages/NDMA.Aspx,2008.
[6]Grebel J E,Young C C,Suffet I H M.Solid-phase microextraction of N-nitrosamines[J].Journal of Chromatography A,2006(1):11-18.
[7]Jurado S B,Ballesteros E,Gallego M.Screening of N-nitrosamines in tap and swimming pool waters using fast gas chromatography[J].Journal of Separation Science,2010,33(4-5):610-616.
[8]Pozzi R,Bocchini P,Pinelli F,et al.Determ-ination of nitrosamines in water by gas chromatography/chemical ionization/selective ion trapping mass spectrometry[J].Journal of Chromatography A,2011(14):1808-1814.
[9]Planas C,Palacios O,Ventura F,et al.Analysis of nitrosamines in water by automated SPE and isotope dilution GC/HRMS-Occurrence in the different steps of a drinking water treatment plant,and in chlorinated samples from a reservoir and a sewage treatment plant effluent[J].Talanta,2008,76(4):906-913.
[10]Zhao Y Y,Boyd J M,Woodbeck M,et al.Formation of N-nitrosamines from eleven disinfection treatments of seven different surface waters[J].Environmental Science&Technology,2008,42(13):4857-4862.
[11]Krauss M,Hollender J.Analysis of nitrosamines in wastewater:exploring the trace level quanti-fication capabilities of a hybrid linear ion trap/orbitrap mass spectrometer[J].AnalyticalChemistry,2008,80(3):834-842.
[12]罗茜,王东红,王炳一,等.超高效液相色谱串联质谱快速测定饮用水中9种N-亚硝胺的新方法[J].中国科学:化学,2011,41(1):82-90.
[13]Hung H W,Lin T F,Chiu C H,et al.Trace analysis of n-nitrosamines in water using solid-phase microextraction coupled with gas chromatograph-tandem mass spectrometry[J].Water Air and Soil Pollution,2010,213(1-4):459-469.
[14]Grebel J E,Suffet I H M.Nitrogen-phosphorus detection and nitrogen chemiluminescence detection of volatile nitrosamines in water matrices:Optimization and performance comparison[J].Journal of Chromatography A,2007(1):141-144.
[15]Charrois J W A,Arend M W,Froese K L,et al.Detecting N-nitrosamines in drinking water at nanogram per liter levels using ammonia positive chemical ionization[J].Environmental Science &Technology,2004,38(18):4835-4841.
[16]Zhao Y Y,Boyd J,Hrudey S E,et al.Characterization of new nitrosamines in drinking water using liquid chromatography tandem mass spectrometry[J].Environmental Science&Technology,2006,40(24):7636-7641.
[17]梁闯,徐斌,夏圣骥,等.SPE/LC/MS/MS检测水中痕量二甲基亚硝胺[J].中国给水排水,2009,25(14):82-85,92.
