细胞连接在慢性鼻窦炎中的表达及意义
2013-10-25范尔钟伯铭羽王向东
李 颖 范尔钟 伯铭羽 王向东 张 罗*
(1.首都医科大学附属北京同仁医院耳鼻咽喉头颈外科,北京100005;2.北京市耳鼻咽喉科研究所,耳鼻咽喉头颈科学教育部重点实验室,鼻病研究北京市重点实验室,北京100005)
呼吸道的黏膜上皮细胞构成了机体与外界环境的第一道屏障,上皮黏膜细胞与细胞之间通过各种细胞连接紧密联系在一起,包括紧密连接(tight junctions,TJs)、黏附连接(adherens junctions,AJs)、缝隙连接(gap junctions)以及桥粒(desmosomes)[1]。当在感染、炎性反应等条件下,细胞连接被扰乱,上皮屏障功能被破坏。本研究通过免疫组织化学方法检测紧密连接蛋白(zonular occludens-1,ZO-1)、黏附连接蛋白(E-cadherin)和桥粒连接蛋白(desmoglein-1,dsg-1)在不同类型慢性鼻窦炎中的表达,旨在探究细胞连接蛋白表达的改变与上皮屏障功能的破坏及上皮组织重塑的关系,和其在慢性鼻窦炎发病机制中的作用。
1 材料与方法
1.1 研究对象
选取2010年12月至2012年8月在首都医科大学附属北京同仁医院行鼻内镜手术的患者标本60例。不伴鼻息肉的慢性鼻窦炎(chronic rhinosinusitis without nasal polyps,CRSsNP)患者(CRSsNP 组)15例,伴鼻息肉的慢性鼻窦炎(chronic rhinosinusitis with nasal polyps,CRSwNP)患者(CRSwNP 组)30 例,对照鼻中隔偏曲患者(control组)15例。所有患者术前2周均未应用糖皮质类固醇激素及抗生素,并排除有变应性真菌性鼻-鼻窦炎、原发性不动纤毛综合征、囊性纤维化疾患的患者。CT提示CRSsNP组患者无鼻息肉性疾病,对照组患者无鼻窦炎性疾病。术中取CRSsNP组患者钩突或鼻窦黏膜组织、CRSwNP组患者息肉组织和对照组患者中鼻甲黏膜组织。所有患者术前均签署知情同意书,本研究经过首都医科大学附属北京同仁医院伦理委员会批准。
1.2 苏木精-伊红(HE)染色
所有标本均用10%中性甲醛固定,石蜡包埋,切片厚4 μm对石蜡切片常规脱蜡、水化后,苏木精染色10 min,分化、返蓝,伊红染色3 min,脱水、透明、封片。HE染色切片用于组织形态学观察和对组织的总炎性细胞、嗜酸性粒细胞进行计数。每张切片随机选取10个高倍视野计数并计算嗜酸性粒细胞占总炎性细胞的百分比,根据文献[2]将本研究中对照组嗜酸性粒细胞的平均百分比与两倍标准差之和(2.58%+2×1.55%=5.68%,约为6%)作为区分嗜酸性粒细胞性鼻息肉(Eos CRSwNP)和非嗜酸性粒细胞性鼻息肉(non-Eos CRSwNP)两个亚型的标准,>6%为嗜酸性粒细胞性鼻息肉,否则为非嗜酸性粒细胞性鼻息肉,两组各15例。
1.3 免疫组织化学染色
切片常规脱蜡至水,高压抗原热修复,3%H2O2阻断内源性过氧化物酶,5%脱脂奶粉封闭非特异性染色,兔抗多克隆抗体 ZO-1(1∶500,购自美国 Invitrogen公司)、鼠抗单克隆抗体E-cadherin(工作液,购自北京中杉金桥生物技术有限公司)、兔抗多克隆抗体 dsg-1(1 ∶500,购自美国 Santa Cruz Blotechnology公司)4℃过夜。通用型二抗PV-6000(工作液,购自北京中杉金桥生物技术有限公司)室温40 min,DAB显色,苏木精复染,脱水、透明、封片。以PBS代替一抗作为阴性对照。阳性染色细胞为胞膜或胞质内清晰的棕黄色颗粒。
1.4 结果判定
将染色结果在OlympusBX51显微镜下进行半定量分析。采用免疫组织化学评分(immunohistochemical score,IHS)方法[3],结合阳性细胞百分比和阳性细胞染色强度2个方面评分:a为阳性细胞百分比(无阳性细胞为0分,阳性细胞占1% ~10%为1分,11% ~50%为2分,51% ~80%为3分,81% ~100%为4分);b为阳性细胞染色强度(阴性为0分,弱阳性为1分,中度阳性为2分,强阳性为3分),a和b两项乘积即为该例组织的IHS。3种连接蛋白表达情况以IHS表示,每张切片高倍镜下选取上皮组织中5个不重复视野,取这5个视野的均数,并做统计分析。
1.5 统计学方法
应用SPSS 18.0进行统计分析。实验结果以均数±标准差(ˉ±s)表示,组间比较采用单因素方差分析和LSD法。以P<0.05为差异有统计学意义。
2 结果
2.1 样本特征
60例样本中,CRSsNP组鼻黏膜标本15例,其中男12例,女3例,患者年龄17~70岁,平均年龄(43.5±16.6)岁;CRSwNP组鼻息肉标本30例,其中男23例,女7例,患者年龄14~67岁,平均年龄(45.6±15.8)岁;对照组15例,其中男7例,女8例,患者年龄14~53岁,平均年龄(37.0±11.2)岁。
2.2 细胞连接的表达
3种细胞连接在不同组别鼻黏膜上皮中均可见阳性表达,表现为胞膜或胞质内有棕黄色颗粒沉积,且在上皮的上、中、下层均有表达。但各组的表达强弱和多少存在不同程度的差异。
在ZO-1的表达中,只有Eos CRSwNP组与对照组相比有明显下降(P<0.05);non-Eos CRSwNP组和CRSsNP组与对照组两两相比虽有下降,但差异无统计学意义(P>0.05);两个CRSwNP亚型之间,CRSw-NP亚型与CRSsNP组之间两两相比,差异均无统计学意义(P>0.05,表 1,图1)。

表1 不同组别鼻黏膜上皮中细胞连接的表达结果Tab.1 The expression of cell junction proteins from nasal epithelial cells under different conditions

图1 紧密连接蛋白在不同组别鼻黏膜上皮中的表达情况(二步法免疫组织化学染色)Fig.1 The expression of ZO-1 from nasal epithelial cells(two-step immunohistochemical staining results)(400×)
在E-cadherin的表达中,两个CRSwNP亚型以及CRSsNP组与对照组两两相比呈明显上调表达(P<0.05),两个 CRSwNP亚型之间,CRSwNP亚型与CRSsNP组之间两两相比,差异无统计学意义(表1,图2)。
在 dsg-1的表达中,两个 CRSwNP亚型以及CRSsNP组与对照组两两相比明显下调(P<0.05),并且两个CRSwNP亚型与CRSsNP组两两相比也有明显下调(P<0.05),但两个CRSwNP亚型之间差异无统计学意义(表1,图3)。
3 讨论
上皮屏障是通过邻近的细胞间由紧密连接(TJs)、黏附连接(AJs)、桥粒和缝隙连接组成的连接复合体紧密地联系在一起来维持的[4]。TJs位于上皮细胞间连接的最顶部,是维持黏膜通透性的重要组成部分[5]。TJs由多种蛋白组成[6],ZO-1(zonular occludens-1)是 1986 年发现的与 TJ 相关的蛋白[7]。其与维持和调节上皮篱笆和屏障功能有关,还参与调节细胞物质转运、维持上皮极性、细胞增生分化、肿瘤细胞转移等重要过程。ZO-1是最具特征的胞质紧密连接蛋白[8]。以膜结合蛋白丢失为特点的TJs的破坏,导致贯通上皮电阻的显著减少和贯通上皮渗透性的明显增加[9]。贯通上皮电位差的存在,表明鼻息肉患者屏障功能的改变[10]。
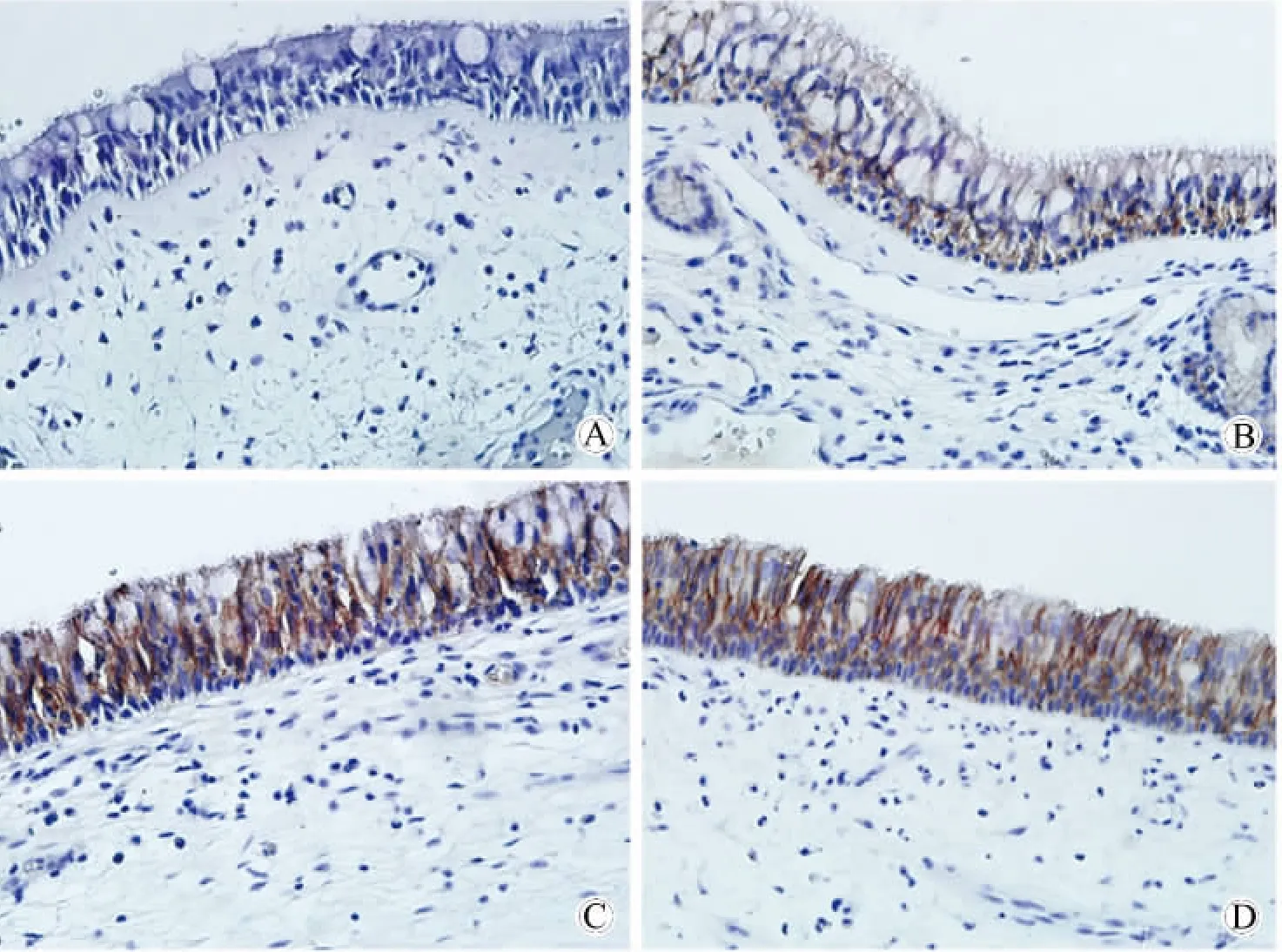
图2 黏附链接蛋白在不同组别鼻黏膜上皮中的表达情况(二步法免疫组织化学染色)Fig.2 The expression of E-cadherin from nasal epithelial cells(two-step immunohistochemical staining results)(400×)
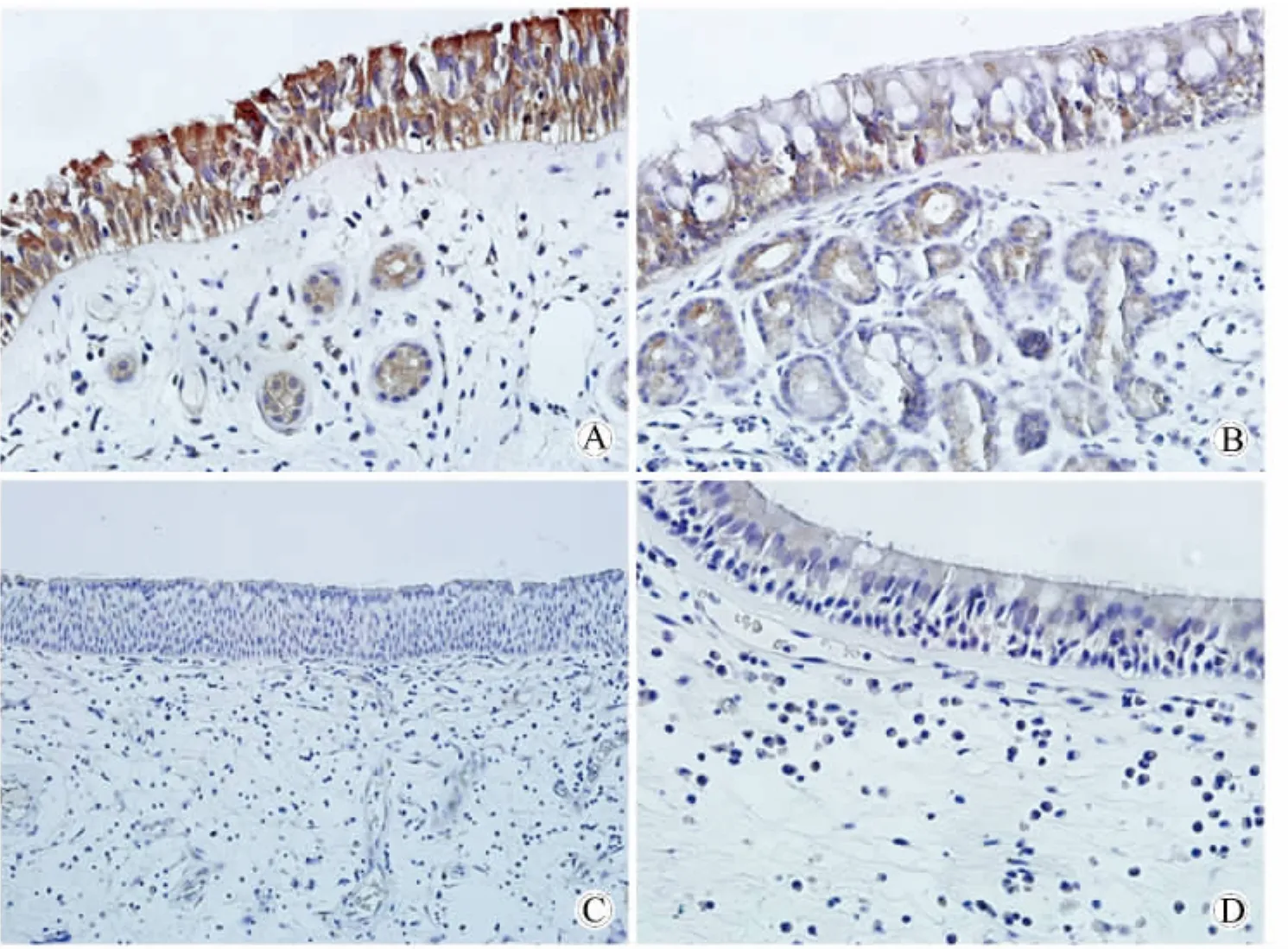
图3 桥粒连接蛋白在不同组别鼻黏膜上皮中的表达情况(二步法免疫组织化学染色)Fig.3 The expression of dsg-1 from nasal epithelial cells(two-step immunohistochemical staining results)(400×)
AJs在上皮细胞间起着加强细胞间连接的功能。其中上皮钙黏素(E-cadherin)是一类钙依赖性跨膜糖蛋白,是AJ的主要成分。它与形态分化和细胞增生的控制、特定位置基因表达、形态发生、免疫功能、细胞运动、伤口愈合和炎性反应有密切关系[11]。
桥粒存在于所有的上皮细胞以及某些特化的组织。其主要由两类蛋白组成:一类是跨膜蛋白,主要由桥粒芯糖蛋白(desmoglein,dsg)和桥粒胶蛋白(desmocollin,dsc)构成;另一类为细胞质内的蛋白,主要成分为桥粒斑蛋白(desmoplakin)和桥粒斑珠蛋白(plakoglobin)。其也起加强连接的作用。Dsg是桥粒的主要跨膜蛋白,是构成细胞间桥粒的主要糖蛋白,分为 dsg-1、dsg-2 和 dsg-3。dsg-1 为 160 000 糖蛋白。一般认为,dsg-1主要分布于正常表皮细胞的上部,被认为系落叶性天疱疮的主要靶抗原。Dsg-1的表达下调可能在角质形成细胞的分化及肿瘤的发生中有一定的作用[12]。Spindler等[13]认为,在正常表皮细胞的中、下部也可有dsg-1的明显表达。
本研究探讨了3种细胞连接在不同类型的慢性鼻窦炎上皮组织中的表达情况,发现TJs蛋白ZO-1和桥粒连接蛋白dsg-1与对照组相比呈下调表达,而AJs蛋白E-cadherin呈上调表达。Jang等[14]的研究显示,在鼻息肉组织中,ZO-1随上皮细胞增生和鳞状化生程度的增加呈下调表达,而E-cadherin随上皮细胞增生和鳞状化生程度的增加呈上调表达。在本研究中,ZO-1的表达只有Eos CRSwNP组与对照组相比下降的程度差异有统计学意义,其中non-Eos CRSwNP组与对照组相比,差异也较明显。因此,笔者将两个CRSwNP亚型之和的总鼻息肉组与对照组进行了比较,结果差异亦有统计学意义。说明在CRSsNP中,还不足以引起ZO-1表达的显著变化。只有在鼻息肉组织中,才使ZO-1的表达产生明显变化,Eos CRSw-NP的ZO-1表达比non-Eos CRSwNP更低一些,提示嗜酸性粒细胞可能在其中发挥一定作用,但由于每组例数较少(只有15例),且2个CRSwNP亚型间差异无统计学意义,还不足以说明问题,有待在今后的研究中探讨详尽机制。鼻息肉上皮中E-cadherin相对于正常黏膜的表达上调可以被认为是一种补偿现象,是为维持在炎性反应条件下的正常细胞结构[15]。本研究结果也证实了这一现象,除了鼻息肉组的E-cadherin表达上调,CRSsNP组的E-cadherin表达也明显上调,说明E-cadherin的表达与鼻黏膜的炎性反应程度和组织重塑程度呈正相关性。与对照组相比,dsg-1在鼻息肉组和 CRSsNP组的表达均明显下调,且CRSwNP组也与CRSsNP组相比有明显下降趋势,但两个CRSwNP亚型之间差异无统计学意义,说明随黏膜炎性反应程度的加剧,对dsg-1蛋白的破坏也逐渐增强,但嗜酸性粒细胞的浸润并没有对其产生明显影响。
在 Zuckerman 等[16]的研究中显示,dsg-2、dsg-3 蛋白在人鼻息肉中的表达明显低于正常鼻黏膜,而ZO-1和E-cadherin在这两组中的表达却没有明显区别。这可能与其病例的筛选和分组不同有关。在Zuckerman的研究中,将产生上皮鳞状化生的鼻息肉组织排除在外,鼻息肉组包括有Samter’s三联征患者,囊性纤维变性患者和变应性真菌性鼻窦炎患者,其中有5人有已知过敏和2人接受了通常的免疫治疗,且所有患者在手术前都接受了5天的类固醇激素治疗。在另一研究[17]中,哮喘和过敏性疾病中可有桥粒表达的减弱,提示变态反应对桥粒的表达是有影响的。但是也有研究[18]显示,过敏性鼻炎的鼻黏膜中,紧密连接的蛋白表达、结构和功能被很好地维持。
有研究证明在炎性肠疾病[19],过敏性炎性反应[20-22]和病毒感染中[23],TJs和 AJs 的破坏在其发病机制中发挥重要作用。由于每个研究者的研究角度、分类方法和所采用的检测指标及手段不同,研究结果也有一定差异。但对于上述原因可导致上皮屏障功能的破坏与改变,还是得到大多数研究的支持。关于上气道炎性反应疾病尤其是慢性鼻窦炎中细胞连接的作用报道较少,且多数研究者仅对鼻息肉与正常鼻黏膜进行了比较。笔者在此项研究中,按组织的炎性反应程度进行了更为细致的分组,且将3种主要细胞连接中最具代表性的连接蛋白进行了检测。通过对其表达改变情况的观察和相互关系的分析,对鼻黏膜不同炎性反应状态下,细胞连接的改变有了更进一步的了解,以期对慢性鼻窦炎发病机制的研究提供新的认识。
[1]Chang E H,Pezzulo A A,Zabner J.Do cell junction pro-tein mutations cause an airway phenotype in mice or humans?[J].Am J Respir Cell Mol Biol,2011,45(2):202-220.
[2]Cao P P,Li H B,Wang B F,et al.Distinct immunopathologic characteristics of various types of chronic rhinosinusitis in adult Chinese[J].J Allergy Clin Immunol,2009,124(3):478-484.
[3]Soslow R A,Dannenberg A J,Rush D,et al.COX-2 is expressed in human pulmonary, colonic, and mammary tumors[J].Cancer,2000,89(12):2637-2645.
[4]Liu Y,Nusrat A,Schnell F J,et al.Human junction adhesion molecule regulates tight junction resealing in epithelia[J].J Cell Sci,2000,113(Pt13):2363-2374.
[5]Pizzuti D,Bortolami M,Mazzon E,et al.Transcriptional downregulation of tight junction protein ZO-1 in active coeliac disease is reversed after a gluten-free diet[J].Dig Liver Dis,2004,36(5):337-341.
[6]Köhler K,Zahraoui A.Tight junction:a co-ordinator of cell signalling and membrane trafficking[J].Biol Cell,2005,97(8):659-665.
[7]Stevenson B R,Siliciano J D,Mooseker M S,et al.Identification of ZO-1:a high molecular weight polypeptide associated with the tight junction(zonula occludens)in a variety of epithelia[J].J Cell Biol,1986,103(3):755-766.
[8]Jesaitis L A,Goodenough D A.Molecular characterization and tissue distribution of ZO-2,a tight junction protein homologous to ZO-1 and the Drosophila discs-large tumor suppressor protein[J].J Cell Biol,1994,124(6):949-961.
[9]Klingler C,Kniesel U,Bamforth S D,et al.Disruption of epithelial tight junctions is prevented by cyclic nucleotidedependent protein kinase inhibitors[J].Histochem Cell Biol,2000,113(5):349-361.
[10]Bernstein J M,Gorfien J,Noble B,et al.Nasal polyposis:immunohistochemistry and bioelectrical findings(a hypothesis for the development of nasal polyps)[J].J Allergy Clin Immunol,1997,99(2):165-175.
[11]Harrington K J,Syrigos K N.The role of E-cadherin-catenin complex:more than an intercellular glue?[J].Ann Surg Oncol,2000,7(10):783-788.
[12]Harada H,Iwatsuki K,Ohtsuka M,et al.Abnormal desmoglein expression by squamous cell carcinoma cells[J].Acta Derm Venereol,1996,76(6):417-420.
[13]Spindler V,Drenckhahn D,Zillikens D,et al.Pemphigus IgG causes skin splitting in the presence of both desmoglein 1 and desmoglein 3[J].Am J Pathol,2007,171(3):906-916.
[14]Jang Y J,Kim H G,Koo T W,et al.Localization of ZO-1 and E-cadherin in the nasal polyp epithelium[J].Eur Arch Otorhinolaryngol,2002,259(9):465-469.
[15]Demetter P,De Vos M,Van Damme N,et al.Focal upregulation of E-cadherin-catenin complex in inflamed bowel mucosa but reduced expression in ulcer-associated cell lineage[J].Am J Clin Pathol,2000,114(3):364-370.
[16]Zuckerman J D,Lee W Y,DelGaudio J M,et al.Pathophysiology of nasal polyposis:the role of desmosomal junctions[J].Am J Rhinol,2008,22(6):589-597.
[17]Shahana S,Jaunmuktane Z,Asplund M S,et al.Ultrastructural investigation of epithelial damage in asthmatic and non-asthmatic nasal polyps[J].Respir Med,2006,100(11):2018-2028.
[18]Takano K,Kojima T,Go M,et al.HLA-DR-and CD11cpositive dendritic cells penetrate beyond well-developed epithelial tight junctions in human nasal mucosa of allergic rhinitis[J].J Histochem Cytochem,2005,53(5):611-619.
[19]Fries W,Mazzon E,Squarzoni S,et al.Experimental colitis increases small intestine permeability in the rat[J].Lab Invest,1999,79(1):49-57.
[20]Kobayashi N,Terada N,Hamano N,et al.Transepithelial migration of activated eosinophils induces a decrease of E-cadherin expression in cultured human nasal epithelial cells[J].Clin Exp Allergy,2000,30(6):807-817.
[21]Takeuchi K,Kishioka C,Ishinaga H,et al.Histamine alters gene expression in cultured human nasal epithelial cells[J].J Allergy Clin Immunol,2001,107(2):310-314.
[22]Wan H,Winton H L,Soeller C,et al.Quantitative structural and biochemical analyses of tight junction dynamics following exposure of epithelial cellsto house dust mite allergen Der p 1[J].Clin Exp Allergy,2000,30(5):685-698.
[23]Dickman K G,Hempson S J,Anderson J,et al.Rotavirus alters paracellular permeability and energy metabolism in Caco-2 cells[J].Am J Physiol Gastrointest Liver Physiol,2000,279(4):G757-G766.
