铜电极表面铜锡合金电结晶机理
2013-10-18史纪鹏杨防祖田中群周绍民
史纪鹏 杨防祖 田中群 周绍民
(厦门大学化学化工学院,固体表面物理化学国家重点实验室,福建厦门 361005)
1 引言
铜锡合金镀层具有较高耐蚀性.锡质量含量(ωSn)在8%-15%的低锡铜锡合金呈(金)黄色外观,可做为装饰性镀层;ωSn高于45%时则呈银白色,硬度介于镍与铬之间,是理想的代镍镀层.铜和锡的标准电极电位分别为E(Cu|Cu2+)=0.340 V、E(Sn|Sn2+)=-0.138 V,二者电位相差0.478 V.因此,在无络合剂的简单金属盐水溶液中,难以电沉积获得Cu-Sn合金镀层.目前,电沉积铜锡合金的溶液基本为剧毒的氰化物-锡酸盐体系.1近年来,针对柠檬酸盐和焦磷酸盐为络合剂的无氰体系已有许多文献报道,2-6但大多侧重于工艺配方与参数优化、镀液性能和镀层表征方面的研究;而对铜锡合金电沉积机制与初期的成核和生长过程机理少有论述.
电结晶过程是电沉积的最初阶段,主要包括成核与生长过程.金属离子在电极表面的活性位点上被还原成原子,大量原子堆积在一起并超过一定的尺寸后,就可以形成晶核并稳定的存在;然后,随着其它被还原的金属原子不断并入晶核的晶格中,晶核不断生长,生长速率正比于原子并入晶核的速率.关于电沉积的成核与生长机制已经有很多的理论研究.在早期的Scharifker-Hills(SH)理论模型7中,考虑了瞬时成核与连续成核的两种极限情况,被广泛用作定性地判断成核过程.8-12Scharifker和Mostany(SM)理论模型13对SH理论模型改进后,可以比较准确地计算出A(成核速率常数)的值;随后,Sluyters-Rehbach等14(SR理论)又对SM模型中应用的扩散层厚度的假设提出不同见解,认为在垂直于电极表面的方向上,各个晶核的浓度梯度是一致的,即扩散层厚度是一致的,都等于Nernst扩散层厚度(πDt).1/2Heerman-Tarallo(HT)理论模型15,16是在SM、SR等理论的基础之上,认为扩散层的变化是时间t和形核速率常数的两个量的函数,而不是SM、SR等理论模型中认为的只是t的函数,并提出新的计算暂态电流j(t)的公式,许多研究者用HT理论模型对计时安培曲线拟合17-20来计算金属成核过程中的相关参数.
在金属电结晶机理的研究过程中,人们多采用很低金属离子浓度、简单溶液组成和单金属的研究体系.基于实际应用溶液来研究金属成核过程已有文献报道,如Emekli和West等21研究了酸性镀铜溶液中添加剂和电沉积方法对铜在Ru表面成核的影响,指出在溅射了30 nm Ru的晶圆表面上,用脉冲电镀方法可以获得更细小致密的铜晶核;Zhang和Hua22研究了酸性硫酸盐镀锌溶液中添加剂[BMIM]HSO4对锌在铝电极上电结晶过程的影响,指出,添加剂可使锌晶核的数量增多、尺寸变小.但是,针对铜锡合金实际应用溶液及合金电极电结晶机理未见报道.研究金属电沉积初期的成核与生长机理,对获得致密且结合力良好的优良金属镀层有重要意义.本文用实际体系的铜锡合金电解液,铜电极作为工作电极(铜锡合金多镀覆在铜镀层表面),应用线性伏安扫描、循环伏安和计时安培实验方法考察铜锡合金在铜电极上的电沉积过程和成核机理,运用SH、HT理论模型对实验数据拟合分析,计算电结晶过程的动力学参数.
2 实验条件
基础电解液组成为 CuSO4·5H2O,0.050 mol·L-1;SnSO4,0.11 mol·L-1;柠檬酸三铵((NH4)3C6H5O7),0.42 mol·L-1;(NH4)2SO4,0.38 mol·L-1;NH4H2PO4,0.14 mol·L-1;丁二酰亚胺(C4H5NO2),0.20 mol·L-1;pH为5.5(氨水调节),电解液的温度为30°C,所用试剂皆为国药集团化学试剂有限公司生产的分析纯试剂,用去离子水配制电解液.
电化学实验使用的仪器为Autolab PGSTAT30恒电位仪(荷兰Eco Chemie BV公司).实验采用三电极体系,铂片为对电极,饱和甘汞电极(SCE)为参比电极,铜圆盘电极(直径为5 mm)为工作电极,文中电位都相对于SCE.实验前,工作电极分别用粒径为1 μm、300 nm和50 nm的Al2O3抛光粉依次抛磨至电极表面镜亮,再分别于无水乙醇中超声波清洗(4 min)和去离子水中超声波清洗(2 min),最后用去离子水冲洗电极表面后使用.实验前电解液通高纯氩气15 min以除去溶液中的溶解氧.
不同沉积电位下铜锡合金镀层组成的测定方法:以镍片为阴极,在铜锡合金电解液中,恒定不同电位电沉积2 min后,用能量色散谱(EDS)分析镀层的组成.EDS为日本日立公司生产的扫描电子显微镜Hitachi S-4800随机附带仪器.
3 结果与讨论
3.1 线性伏安扫描曲线分析
图1是含不同金属离子电解液的线性扫描伏安(LSV)曲线,测试时从开路电位往负向扫描.在不含金属盐的电解液中(曲线a)无明显的阴极电流峰,至-0.80 V后阴极电流逐渐增大,归因于电极表面氢气的析出;在仅含有Cu2+的电解液中(曲线b),电位负于-0.42 V,阴极电流逐渐增大,归因于铜络合离子的还原;在只含有Sn2+的电解液中(曲线c),在-0.75 V附近阴极电流迅速增大并在-0.80 V附近出现阴极还原峰,归因于锡络合离子的还原;在同时含有Cu2+和Sn2+的电解液中(曲线d),在-0.45 V附近,阴极电流开始明显大于只含Cu2+(曲线b)和Sn2+(曲线c)的阴极还原电流,说明在该电位下,溶液中不仅有铜的沉积,也有锡的沉积;能量色散谱(EDS)测试结果证明,在-0.45 V下沉积的镀层中含有锡质量含量(ωSn)10%,即在此电位下,铜和锡可共沉积.显然,Cu2+和Sn2+共存时,有利于锡络合离子的阴极还原.在曲线d中,当电位负于-0.75 V后,出现类似于曲线b且阴极电流明显大于曲线b的还原峰,说明该电位区间下铜和锡也共同析出.EDS测试结果显示-0.80至-0.85 V电位下,镀层中ωSn分别为56%-76%.LSV结果显示:在本研究体系中可以实现铜和锡的共沉积;铜络合离子促进锡络合离子阴极还原;控制不同的沉积电位,可以得到不同锡含量的铜锡合金.

图1 铜电极上不同主盐组成镀液的LSV曲线Fig.1 Linear sweep voltammograms of copper electrode in the electrolytes containing different metal ions
3.2 循环伏安曲线分析
铜电极在Cu-Sn电解液中不同扫描速率下的循环伏安曲线(CV)示于图2.CV曲线皆从开路电位(-0.17 V)负向扫描,在大量析氢发生之前回扫至-0.20 V得到第一圈曲线.由图2可知,阴极过程中,铜锡合金的沉积峰型与图1中曲线d相似.Pewnim和Roy23在甲基磺酸盐体系铜锡合金电解液中得到的循环伏安曲线分别在-0.40和0.10 V附近存在阳极溶出峰,分别归因于合金中锡和铜的溶出.因此,本文在-0.60 V附近的阳极峰归因于沉积物中Sn的溶出.图2中插图(100 mV·s-1扫描速率)显示,在-0.78 V附近有一个“电流环”出现,说明合金在铜电极上的电沉积经历了成核过程,24成核过电位约为0.02 V.随着扫描速率增大,阴极峰电位逐渐向负电位方向移动,峰电流也逐渐变大.对于不可逆电极过程,阴极峰电流jp与扫描速率ν1/2的线性关系25如下:

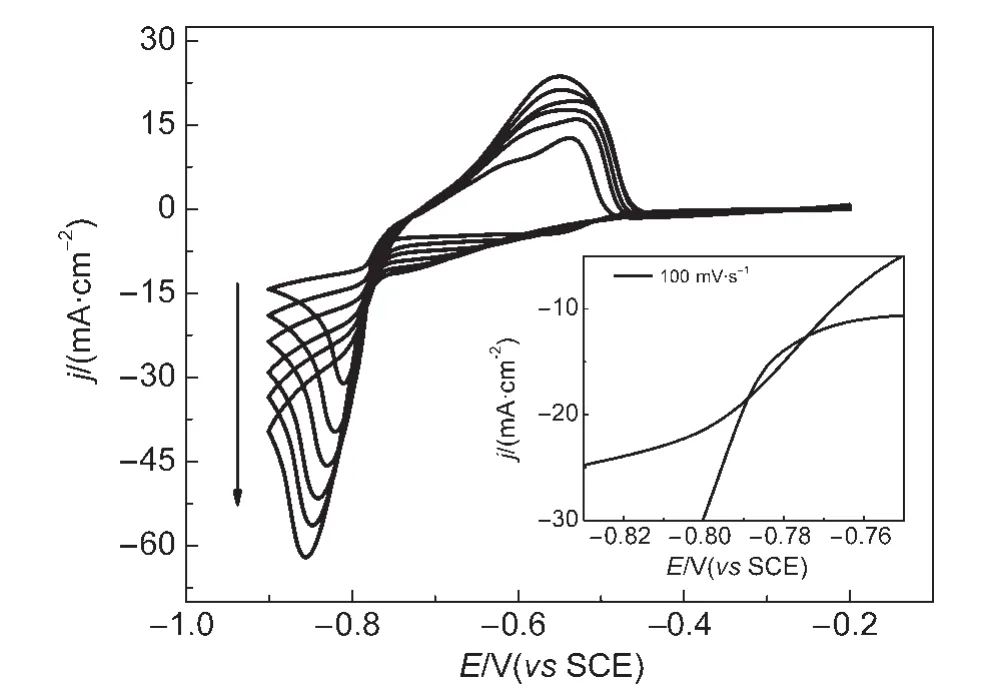
图2 铜电极在Cu-Sn电解液中20-120 mV·s-1扫描速率下的循环伏安曲线Fig.2 Cyclic voltammograms of copper electrode in the Cu-Sn electrolyte between 20 and 120 mV·s-1 scan rates
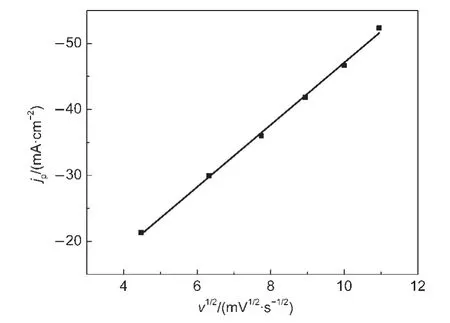
图3 阴极峰电流密度(j p)与扫描速率的平方根(ν1/2)关系Fig.3 Variations in the current density of cathodic peaks(j p)with square root of scan rate(ν1/2)
式中,jp为峰电流密度(A·cm-2);D为扩散系数(cm2·s-1);n为转移电子数;ν为扫描速率(mV·s-1);F为法拉第常数,96500 C·mol-1;α为传递系数;c0为溶液本体摩尔浓度,mol·cm-3;R=8.314 J·mol-1·K-1;T为反应的绝对温度(K).以图2中不同扫描速率下的峰电流jp对ν1/2作图(如图3所示),线性拟合得到一条拟合优度(R2)为0.998的直线,说明阴极还原过程为扩散控制的不可逆过程.
3.3 计时安培曲线分析
为了进一步研究Cu-Sn合金电结晶的动力学过程,应用计时安培法(分别在铜电极上施加-0.80、-0.81、-0.82、-0.83、-0.84和-0.85 V的阶跃电位),得到不同阶跃电位下的计时安培曲线,如图4所示.电位阶跃后,电极表面经过短暂的双电层充电过程,随后阴极电流开始增大,在时间tm(成核的诱导时间)时达到最大电流Im(由成核过程引起电流).超过tm后电流密度开始下降并趋于恒定.随时间延长,电流密度不是指数型地下降至零,说明合金的电结晶呈现典型的三维成核生长特征.阶跃电位越负,成核诱导时间越短,最大成核电流值越大.由SH经典理论模型7推导出计时安培实验中暂态电流的无因次理论关系式:
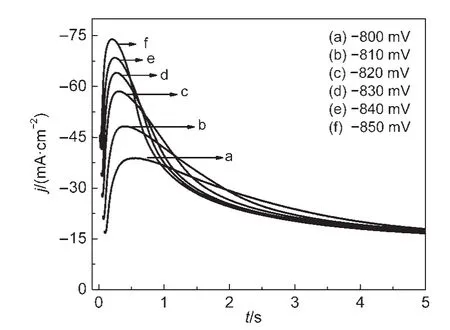
图4 铜电极上不同阶跃电位下的计时电流曲线Fig.4 Chronoamperometric curves on copper electrode at different potentials
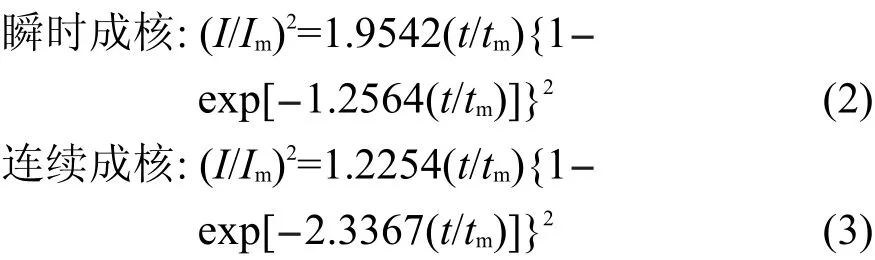
将实验得到的计时安培曲线处理成无因次的(I/Im)2-(t/tm)形式(图5中点划线),并与SH理论模型的瞬时成核与连续成核理论曲线(图5中实线)比较.如图5所示,在实验电位区间内,铜锡合金共沉积的成核机理符合扩散控制下的三维瞬时成核,与Correia等2报道的在焦磷酸盐体系中铜锡合金的成核过程类似.当t/tm<1,实验结果与瞬时成核理论曲线较吻合;而当t/tm>1后,实验曲线逐渐与瞬时成核理论曲线发生偏离,说明合金的电结晶过程要比理论假设的更加复杂.所以,当电极表面发生其它副反应(如析氢等)时,理论分析中需要考虑更多的影响因素.
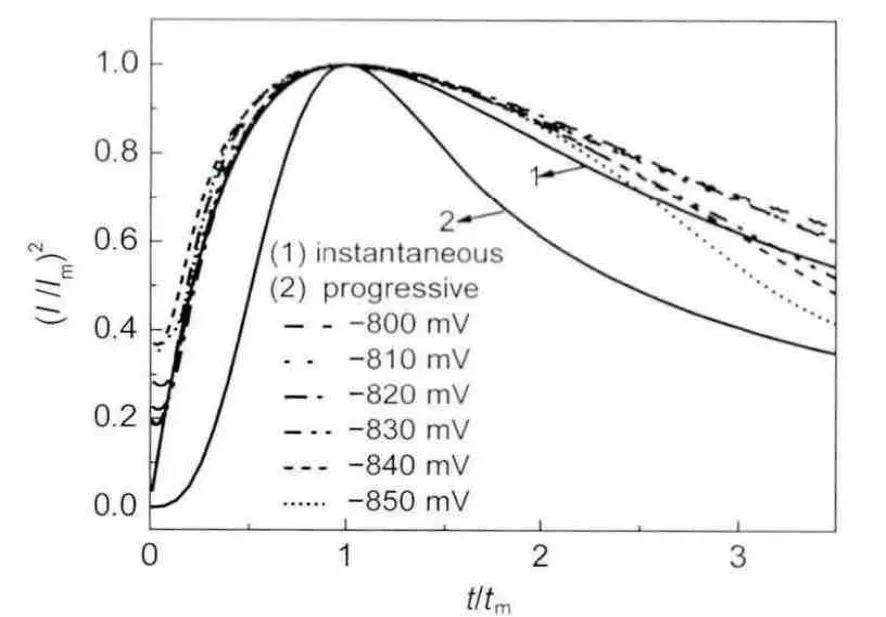
图5 无因次计时电流曲线(I/I m)2-t/t m对比图Fig.5 Comparisons of theoretical non-dimensional(I/I m)2-t/t mcurves to the experimental current transient curves
Heerman和Tarallo在SM和SR理论模型中关于晶核周围扩散层厚度与时间的关系基础上,提出扩散层厚度应当是时间(t)和成核速率常数(A)的函数,得到电流密度与时间、成核速率常数和成核密度数(N0)方程如下:
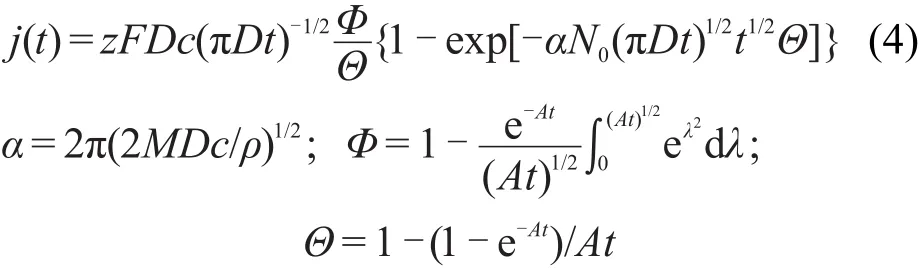
式中j(t)为电流密度;z为电子转数,z=2;F为法拉第常数,96500 C·mol-1;c为摩尔浓度;ρ为合金平均密度(g·cm-3);A为成核速率常数(对于连续成核A<1,瞬时成核A>1),s-1;M为平均摩尔质量(g·mol-1);N0为电极表面成核活性位点密度数(cm-2);λ为虚拟量,无实际意义.函数Φ反映了形核过程中电流密度的变化,Θ是反映成核过程中电极表面被沉积物覆盖程度的函数.
函数Φ直接与道森积分有关,可以通过式(5)进行近似计算:

为了进一步计算成核过程中的动力学参数,基于Levenberg-Marquardt运算法则的非线性最小二乘法原理,以A、N0、D为拟合参数,由公式(4)用origin 8.5进行非线性拟合(如图6所示),得到参数值如表1所示.拟合时用到的参数值:z=2,F=96500 C·mol-1,c=1.6×10-4mol·cm-3,由EDS分析得到不同阶跃电位(-800--850 mV)下合金中锡的平均质量含量为ωSn=68%,折算出平均密度ρ=7.76 g·cm-3,平均摩尔质量M=92.90 g·mol-1.
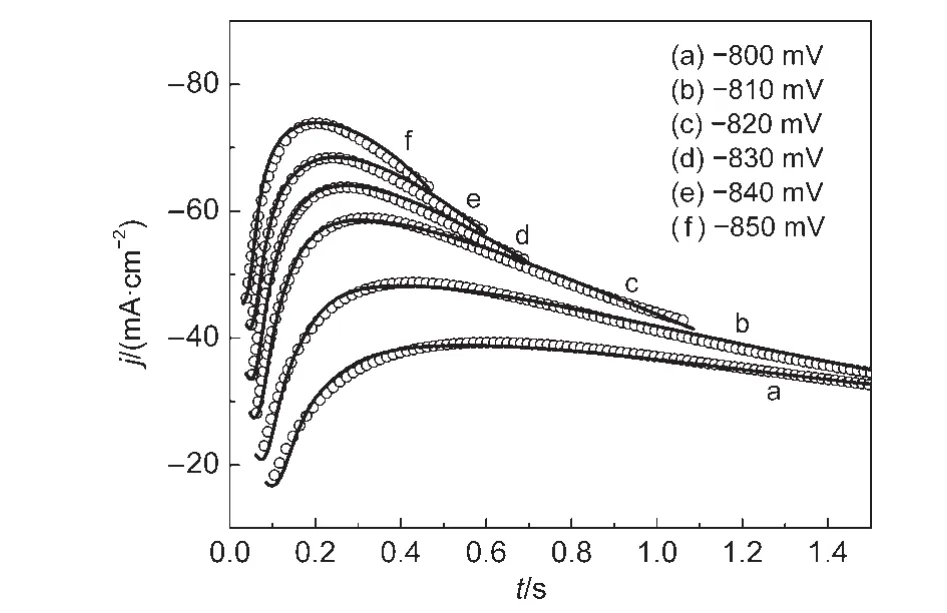
图6 计时电流曲线(实线)与HT(点线)模型拟合曲线对比图Fig.6 Comparisons between experimental current transients(solid line)and the corresponding theoretical current transients(dot line)generated by non-linear fitting of HT model
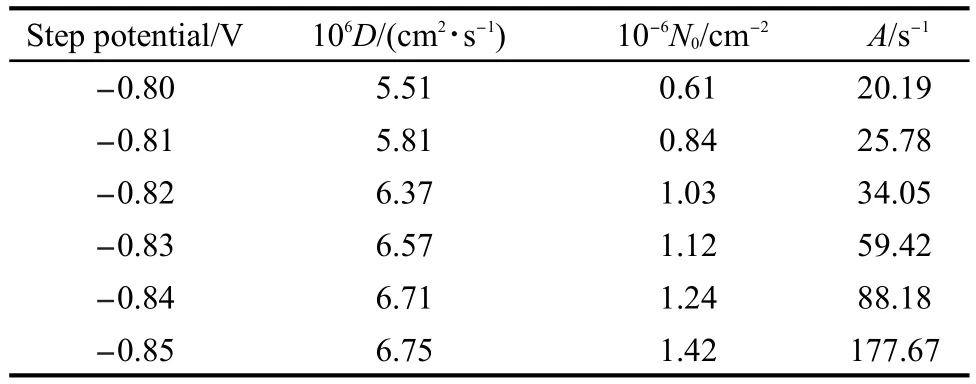
表1 根据HT模型拟合得到在不同阶跃电位下的成核参数值Table 1 Kinetic parameters extracted from the current transients according to HT model
由表1可知,表观扩散系数D的数值为(6.13±0.62)×10-6cm2·s-1,这一数值介于柠檬酸-铜络离子26(2.1×10-6cm2·s-1)和纯锡离子27((8.0±0.4)×10-6cm2·s-1)的扩散系数之间,与胡炜等28报道的柠檬酸盐体系电沉积SnCu合金的扩散系数(6.435×10-6cm2·s-1)结果相近.扩散系数D与溶液中金属离子浓度和溶液温度均有关,本文拟合得到的扩散系数值在低过电位下介于铜和锡离子之间,在高过电位下对应于镀层锡含量的提高而更接近于锡的扩散系数.随着阶跃电位逐渐负移,N0的值逐渐增大,说明电位愈负,单位面积内成核的活性位点数目越多,越有利于得到更多的晶核,使镀层晶粒细小、致密.然而,值得注意的是,电位很负时往往伴有析氢反应的发生而影响合金的沉积.在实验电位区间内,N0值在(1.01±0.41)×106cm-2范围内(远小于金属表面的原子密度数(1015cm-2)29),Heerman和Tarallo16指出,N0的范围在104-1010cm-2之间,对于不同的实验条件(如温度、金属离子浓度等),N0会有很大变化,追求真实的N0值实际意义不大.因此,根据N0值变化规律可以从理论上半定量地分析实验结果.实验中随着电位变负,成核速率常数A值从20.19增长到177.67,说明电位越负,诱导成核所需要的时间也越短;这与计时电流曲线中tm随电位变负而变小的规律相一致.在析氢反应影响较小的前提下,沉积电位越负,成核时间越短,成核活性位点越多,越有利于沉积出晶粒细小、致密且与基底结合牢固的金属镀层.
4 结论
以浓度相对较高和组成更加复杂的铜锡合金电解液为研究体系,研究结果更接近于实际情况.揭示铜锡合金的电沉积过程与电结晶机理及成核过程的动力学参数,为电沉积获得不同锡含量的铜锡合金提供科学依据,并为铜锡合金的电沉积提供理论指导.铜锡合金在铜电极上的沉积表现为扩散控制下的不可逆过程,遵循三维瞬时成核机理.随阶跃电位从-0.80 V负移至-0.85 V,扩散系数为(6.13±0.62)×10-6cm2·s-1,成核速率常数从20.94提高至188.46 s-1,成核活性位点密度数从6.11×105cm-2提高至1.36×106cm-2.
(1)Hoffacker,G.;Kaiser,H.;Reissmueller,K.;Wirth,G.Cyanidic-Alkaline Baths for the Galvanic Deposition of Copper-tin Alloy Coatings,Uses Thereof,and Metallic Bases Coated with Said Copper-tin Alloy Coating.US Patent:US 5534129,1996-07-09.
(2)Correia,A.N.;Façanha,M.X.;de Lima-Neto,P.Surf.Coat.Technol.2007,201(16),7216.
(3)Hovestad,A.;Tacken,R.A.Physica Status Solidi(c)2008,5(11),3506.doi:10.1002/pssc.v5:11
(4)Sürme,Y.;Gürten,A.A.;Bayol,E.;Ersoy,E.J.Alloy.Compd.2009,485(1),98.
(5)Finazzi,G.A.;De Oliveira,E.M.;Carlos,I.A.Surf.Coat.Technol.2004,187(2),377.
(6)Low,C.T.J.;Walsh,F.C.Surf.Coat.Technol.2008,202(8),1339.doi:10.1016/j.surfcoat.2007.06.032
(7)Scharifker,B.;Hills,G.Electrochim.Acta 1983,28(7),879.doi:10.1016/0013-4686(83)85163-9
(8)Palomar-Pardavé,M.;Scharifker,B.R.;Arce,E.M.;Romero-Romo,M.Electrochim.Acta 2005,50(24),4736.doi:10.1016/j.electacta.2005.03.004
(9)Ballesteros,J.C.;Chainet,E.;Ozil,P.;Meas,Y.;Trejo,G.Int.J.Electrochem.Sci.2011,6,2632.
(10)Gu,M.;Zhong,Q.J.Appl.Electrochem.2011,41(7),765.doi:10.1007/s10800-011-0293-0
(11)Rudnik,E.;Wojnicki,M.;Wιoch,G.Surf.Coat.Technol.2012,207,375.doi:10.1016/j.surfcoat.2012.07.027
(12)Garfias-García,E.;Romero-Romo,M.;Ramírez-Silva,M.T.;Palomar-Pardavé,M.Int.J.Electrochem.Sci.2012,7,3102.
(13)Scharifker,B.R.;Mostany,J.J.Electroanal.Chem.1984,177,13.doi:10.1016/0022-0728(84)80207-7
(14)Sluyters-Rehbach,M.;Wijenberg,J.H.O.J.;Bosco,E.;Sluyters,J.H.J.Electroanal.Chem.1987,236(1),1.
(15)Heerman,L.;Tarallo,A.J.Electroanal.Chem.1998,451(1),101.
(16)Heerman,L.;Tarallo,A.J.Electroanal.Chem.1999,470(1),70.doi:10.1016/S0022-0728(99)00221-1
(17)Yue,J.P.;Yang,F.Z.;Tian,Z.Q.;Zhou,S.M.Acta Phys.-Chim.Sin.2011,27(6),1446.[岳俊培,杨防祖,田中群,周绍民.物理化学学报,2011,27(6),1446.]doi:10.3866/PKU.WHXB20110620
(18)Zhou,L.;Dai,Y.;Zhang,H.;Jia,Y.;Zhang,J.;Li,C.Bull.Korean Chem.Soc.2012,33(5),1541.doi:10.5012/bkcs.2012.33.5.1541
(19)Lomax,D.J.;Kinloch,I.A.;Dryfe,R.A.W.Au Electrodeposition on Carbon Materials.In Nanotechnology(IEEE-NANO),201212th IEEE Conference on Nanotechnology,Birmingham,United Kingdom,Aug 20-23,2012;IEEE;2012;pp 1-4.
(20)Granados-Ner,M.;Huizar,L.H.M.;Rios-Reyes,C.H.Química Nova 2011,34(3),439.
(21)Emekli,U.;West,A.C.Electrochim.Acta 2009,54(4),1177.doi:10.1016/j.electacta.2008.08.065
(22)Zhang,Q.B.;Hua,Y.X.J.Appl.Electrochem.2011,41(6),705.doi:10.1007/s10800-011-0283-2
(23)Pewnim,N.;Roy,S.Electrochim.Acta 2013,90,498.doi:10.1016/j.electacta.2012.12.053
(24)Fletcher,S.Electrochim.Acta 1983,28(7),917.doi:10.1016/0013-4686(83)85167-6
(25)Bard,A.J.;Faulkner,L.R.Electrochemical Methods:Fundamental and Applications,2nd ed.;John Wiley:New York,2001;pp 234-236.
(26)Ying,R.Y.J.Electrochem.Soc.1988,135(12),2957.doi:10.1149/1.2095469
(27)Barry,F.J.;Cunnane,V.J.J.Electroanal.Chem.2002,537(1),151.
(28)Hu,W.;Tan,C.Y.;Cui,H.;Zheng,Z.Q.The Chinese Journal of Nonferrous Metals 2010,20(5),1006.[胡 炜,谭澄宇,崔 航,郑子樵.中国有色金属学报,2010,20(5),1006.]
(29)Michailova,E.;Milchev,A.J.Appl.Electrochem.1991,21(2),170.doi:10.1007/BF01464299
