长牡蛎中国群体与日本群体杂交子一代的生长和存活比较
2013-10-13孔令锋滕爽爽
孔令锋, 滕爽爽, 李 琪
(中国海洋大学 海水养殖教育部重点实验室, 山东 青岛 266003)
长牡蛎(Crassostrea gigas), 俗称太平洋牡蛎,是世界性的水产养殖种类[1]。长牡蛎的产量在世界所有渔业和养殖的贝类种类中位居首位, 2010年全球产量达 66万吨, 产值约 12.6亿美元[2]。在我国, 长牡蛎大规模的人工育苗与养殖始于20世纪70年代末和80年代初, 目前辽宁、山东、江苏、浙江、福建、广东、广西等沿海地区已成为长牡蛎的主要养殖产区, 2010年全国牡蛎的总产量超过364万吨, 占我国贝类养殖总产量的32.9%[3], 取得了显著的经济效益和社会效益。近年来, 随着养殖规模的扩大, 长牡蛎的产量大幅度提高, 但品质却在下降, 种质也出现退化, 表现出出肉率低下、形态不规则、肉质不好等缺点[4-5], 因此, 市场价格偏低, 达不到牡蛎活体出口标准, 严重影响了牡蛎养殖业的健康、稳定和持续发展。虽然通过改善生态环境和养殖结构能够使上述问题得到一定程度的解决, 但从长远上, 还需要深入研究牡蛎的种质资源, 培育出产量高、品质好的长牡蛎优良品种。
杂交育种是遗传育种的主要手段之一, 是改良遗传性状、培育优良品种的可靠途径。杂交育种的主要目的是获得杂种优势, 由于杂种优势和杂种活力的存在, 杂交能迅速和显著地提高杂种的产量和生活力[6-7]。因此杂交育种广泛应用在动植物的种质改良中[8-11], 并且在水产动物的品种改良和生产中发挥了重要作用[12]。
近年来, 许多研究报道了贝类群体间杂交的结果。不同群体杂交的子代在生长、存活和生产性能等方面的表现都优于其亲本的自繁群体。Cruz等[13]对扇贝(Argopecten circularis)的两个群体进行了杂交实验, 他们发现在幼虫初期壳长生长存在明显的母体效应, 在第15天后存在一定的杂种优势。刘小林等[14]进行了栉孔扇贝中国群体和俄罗斯群体的杂交实验, 对杂交后代和亲本群体后代进行了比较, 发现杂交后代在壳高、壳长、壳宽和活体质量 4个生长发育指标上均表现不同程度的杂种优势。Zhang等[15]开展了海湾扇贝加拿大群体和墨西哥湾群体的杂交实验工作, 对杂种一代及对照群体的生长和存活进行了比较, 在第 10天后, 两个杂交组的壳长显著大于两个对照群体, 体现出明显的杂种优势。但有关牡蛎不同群体或亚种间的杂交还少有报道。Newkirk等[16]和Newkirk[17]报道了美洲牡蛎C. virginica4个种群杂交后代在存活率和生长方面优于亲本。Stiles[18]利用C. virginica不同地理种群以及与C. gigas进行了杂交, 结果表明不同地理种群间杂交后代幼体的存活率和生长速度都比种间杂种要高。
为了探索利用杂交培育长牡蛎优良养殖新品种的可行性, 本研究利用长牡蛎中国群体和日本群体进行杂交实验, 比较不同杂交组与对照组幼虫、稚贝及养成期的生长、存活, 研究杂交组是否存在杂种优势, 进而为长牡蛎的杂交育种提供理论依据, 为长牡蛎杂交的生产实践提供基础资料。
1 材料和方法
1.1 材料
长牡蛎中国群体为2007年群体选育F1子代, 日本群体为2007年群体选育F1子代。实验于2008年5月在山东省文登市水产综合育苗试验基地进行。
1.2 实验设计
利用长牡蛎中国群体与日本群体进行 4个组合的杂交与自交试验, 杂交实验组: 长牡蛎中国群体♀ × 长牡蛎日本群体♂(C♀ × J♂, CJ), 长牡蛎日本群体♀ × 长牡蛎中国群体♂(J♀ × C♂, JC),自交实验组: 长牡蛎中国群体♀ × 长牡蛎中国群体♂(C♀ × C♂, CC), 长牡蛎日本群体♀ × 长牡蛎日本群体♂(J♀ × J♂, JJ)。实验设2个重复。
1.3 人工授精, 孵化及幼虫培育
从每个群体中选择雌雄各10个性腺发育完全成熟的个体。采用解剖法收集卵子, 在盛有10 L, 24℃海水的小桶中促熟, 将长牡蛎中国群体10个雌性个体的卵子充分混合; 同样操作获得混合的长牡蛎中国群体精子, 长牡蛎日本群体卵子和长牡蛎日本群体精子。再把两个群体的卵子等份分开, 每一群体的卵子分别与群体内或群体间的精子授精。得到四个交配组合 C♀ × C♂, C♀ × J♂, J♀ × C♂, J♀ × J♂。
孵化时持续微充气, 并每隔 1~2 h 搅拌一次,以防止受精卵的堆积。受精后24 h, 受精卵发育到D形幼虫。将每个交配组合的幼虫分别选幼至 100 L聚乙烯桶中培育, 设 3组重复, 初始 D形幼虫密度10个/mL, 水温控制在 23~24℃, 持续充气, 每天换水一次, 换水量1/3。随着幼虫长大, 增大换水量, 到面盘幼虫后期, 日换水量 1/2, 所用海水经过砂滤处理。饵料以等边金藻(Isochrysis galbana)为主, 后期辅助投喂扁藻(Platymonassp.), 牟氏角毛藻(Chaetoceros muslleri), 投饵量根据幼虫的摄食情况和水中残饵情况确定。各实验组投饵、换水、充气等操作一致。所用试验器具都在淡水中浸泡 5 min,以杀死残留在网上的幼虫, 以防混杂污染, 各试验组之间严格避免相互混杂。
1.4 稚贝中间培育及养成
大约 22 d后, 幼虫开始陆续出现眼点, 当30%左右的幼虫出现眼点时, 开始投放附着基。在室内继续培养 15 d后, 挂到室外在沉淀池暂养, 确认自然海区无野生牡蛎浮游幼虫污染后, 转至文登市东港海上笼式浮筏悬挂养殖。各实验组的放养密度、水层深度等环境条件均保持一致。养成期间, 每隔2月将笼取回, 剔出笼上附着生物, 观察生长情况, 并逐渐疏散密度。
1.5 分析的性状、取样及测量
分析的性状包括: (1)受精率; (2)孵化率; (3)幼虫期, 壳高、壳长和存活率; (4)稚贝和养成期, 壳高、壳长和存活率。
受精率(%)= 出现第一极体的卵子/所有卵子 ×100;
孵化率(%)= 孵化出的D形幼虫/受精卵 × 100;
幼虫期存活率(%)= 测量日存活的幼虫/第1天的幼虫 × 100;
稚贝养成期存活率(%)= 测量日存活的稚贝/第60天的稚贝 × 100;
幼虫期, 在第1, 5, 10, 15, 20, 25天取样, 每组每次取样30个体, 用卢戈氏液杀死固定, 在100 ×的显微镜下, 用目微尺测量测量其壳高、壳长; 稚贝和养成期, 在第60, 100, 150, 210, 280天, 各实验组取样30个, 用游标卡尺(精度0.02 mm)测量壳高、壳长。
1.6 数据分析
计算杂交子代各性状的杂种优势率(H, Heterosis), 公式为:
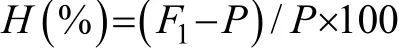
式中,F1为杂交子代性状的平均值,P为两自交组子代性状的平均值[19]。
用EXCEL软件统计4个实验组间在不同阶段各性状指标的平均数和标准差, 并采用SPSS13.0统计分析软件对 4个实验组间数据进行单因素方差分析及Tukey’s多重比较分析。
2 结果
2.1 受精率、孵化率的比较
4个实验组的受精率变化范围为 76.76%~91.33%,其中JC组的受精率最低, 为76.76%, CJ组的受精率最高, 为 91.33%, 自交组 CC和 JJ的受精率介于杂交组CJ和JC之间, 经方差分析表明, 杂交组与自交组之间无显著差异。4个实验组的孵化率变化范围为71.25%~96.00%, 其中 CJ组的孵化率最低, 为71.25%, JJ组的孵化率最高, 为96.00%, 相同卵子来源的组合在孵化率上无差异, 即CC组与CJ组之间,JC组与JJ组之间无显著差异(表1)。
2.2 幼虫期生长、存活以及杂种优势率的比较分析
2.2.1 幼虫期壳高、壳长的比较分析
本杂交实验中, 幼虫期自 1 d起, 到投附着基,自交组JJ和杂交组JC的壳高始终大于自交组CC和杂交组CJ, 经方差分析表明, JJ组和JC组之间, CC组和 CJ组之间无显著差异(P>0.05), 即相同卵子来源的组合在壳高上无差异; 而 JJ、JC与 CC、CJ各组之间差异显著(P<0.05)。到了25 d, JJ组壳高最大,为 266.2 μm; 其次是 JC 组, 为 258.1 μm; CJ组为238.2 μm; CC 组壳高最小, 为 222.5 μm。幼虫期间, 4个实验组的壳长生长趋势与壳高相同, 即自交组 JJ和杂交组JC的壳长始终大于自交组CC和杂交组CJ。在25 d, JJ组生长最快, 壳长为241.9 μm; JC组壳长略微小于 JJ组, 为 237.7 μm; CJ组壳长 215.4 μm; CC组壳长最小, 仅为 195.7 μm(表 2)。

表1 各实验组的受精率、孵化率比较Tab. 1 Comparison of fertilized rate and hatching rate of the four groups (%)
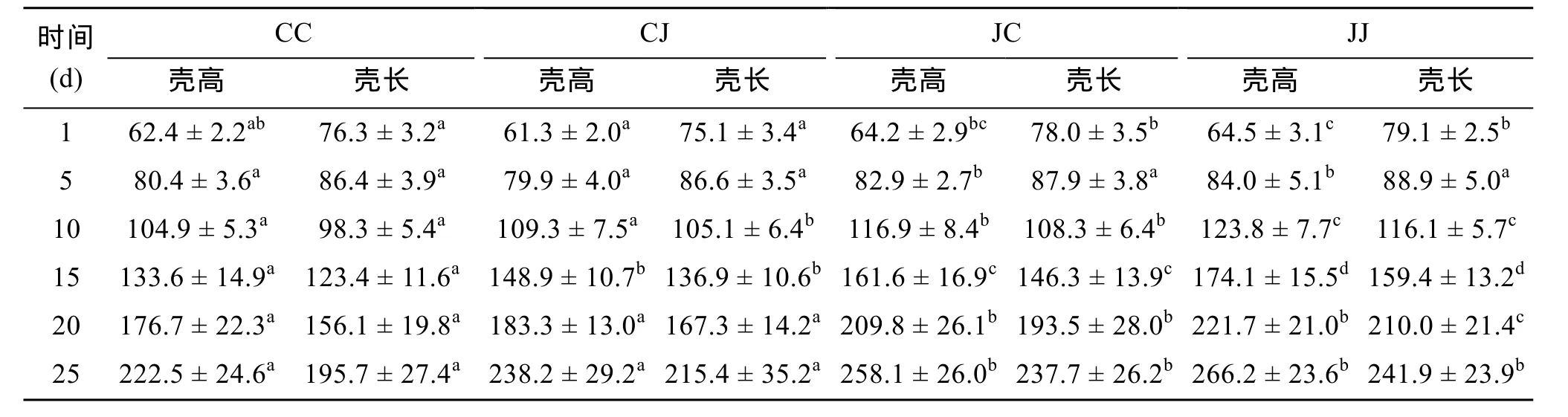
表2 幼虫期各实验组幼虫的壳高和壳长Tab. 2 Shell height and shell length of the four groups at larvae stage (μm)
2.2.2 幼虫期存活率的比较分析
两个自交组和杂交组幼虫阶段的存活率如表 3所示。在5~15 d, JC组和CC组的存活率明显大于JJ组和CJ组; JC、CC和JJ、CJ各组之间差异显著。15 d后, CC组和CJ组的存活率出现明显下降, CC组的存活率由15 d的74.8%下降到20 d的25.6%, CJ组由53.5%下降到4.9%; 而JC组和JJ组存活率无明显下降。到了25 d, 4个实验组的存活率均出现明显下降现象, 方差分析表明, CC组和CJ组之间, JC组和JJ组之间无显著差异。
2.2.3 幼虫期杂种优势率的比较分析
幼虫阶段, 杂交组生长和存活的杂种优势率见表 4。同自交组相比, 杂交组 JC在壳高、壳长和存活率上均具有明显的杂种优势, 并且在幼虫生长阶段, 杂交组JC的壳高、壳长和存活率的杂种优势率随着生长逐渐增加。1~25 d, JC组壳高的杂种优势率为 0.85%~5.63%, 壳长的杂种优势率为 0.29%~8.64%,存活率的杂种优势率为12.31%~96.45%, 而CJ组则无杂种优势率。
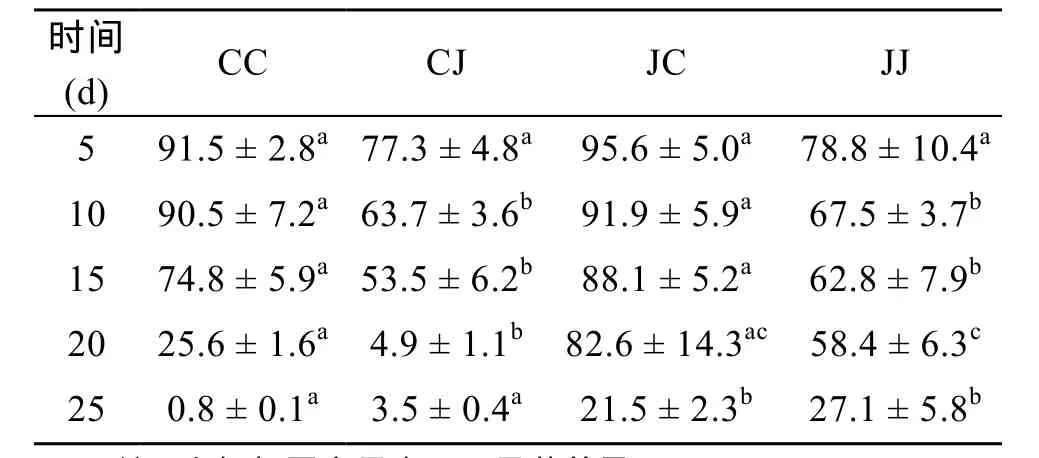
表3 幼虫期各实验组幼虫的存活率Tab. 3 Percent survival means of the four groups at larvae stage (%)
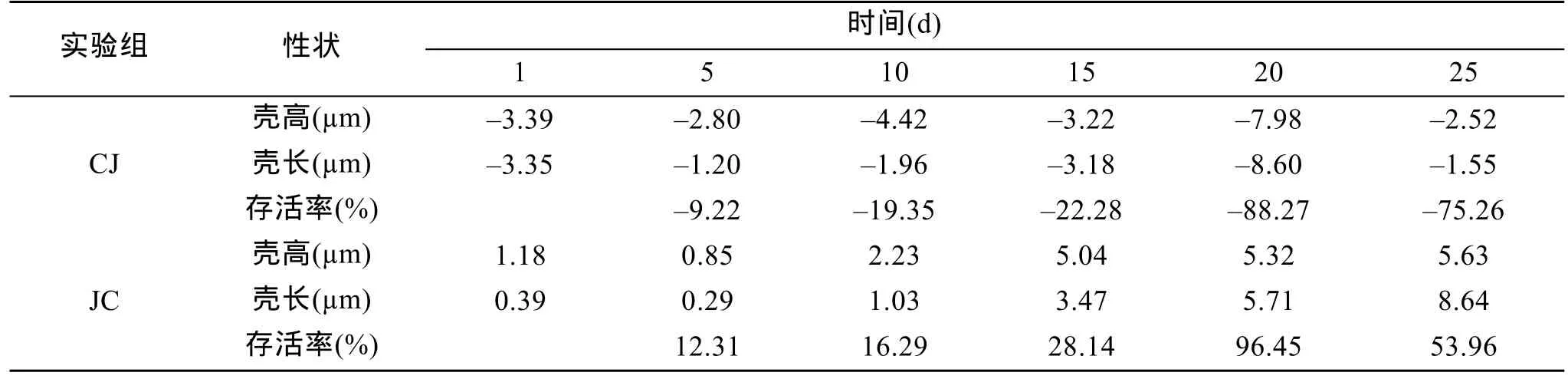
表4 幼虫期各杂交组生长和存活的杂种优势率Tab. 4 Heterosis for growth and survival of the four groups at larvae age
2.3 稚贝、养成期生长、存活以及杂种优势率的比较分析
2.3.1 稚贝、养成期壳高、壳长的比较分析
各实验组稚贝在60, 100, 150, 210和280日龄的壳高和壳长的生长变化见表5。CC, CJ, JC, JJ 4个实验组的壳高和壳长随着日龄的增加均呈上升趋势,280日龄时壳高分别为23.1, 29.6, 33.3, 37.4 mm, 壳长分别为17.6, 22.2, 26.8, 28.2 mm。在整个稚贝, 养成期, 杂交组CJ和JC的平均壳高、壳长均介于自交组CC和JJ之间, 到了280 d, 杂交组CJ、JC和自交组 CC、JJ在壳高和壳长上显著差异(P<0.05), 杂交组CJ和JC之间无显著差异(P>0.05)。
2.3.2 稚贝, 养成阶段存活率的比较分析
各实验组稚贝在100, 150, 210和280日龄的存活率变化见表6。CC, CJ, JC, JJ 4个实验组的存活率日龄的增加均呈下降趋势, 280日龄时各实验组存活率分别为34.4, 12.2, 1.1, 1.1%。在整个稚贝, 养成期,CC组存活率最高, 其次是CJ组和JJ组, JC组存活率最低。JC组和 JJ组之间无显著差异(P>0.05), 但与CC组, CJ组之间差异显著(P<0.05)。
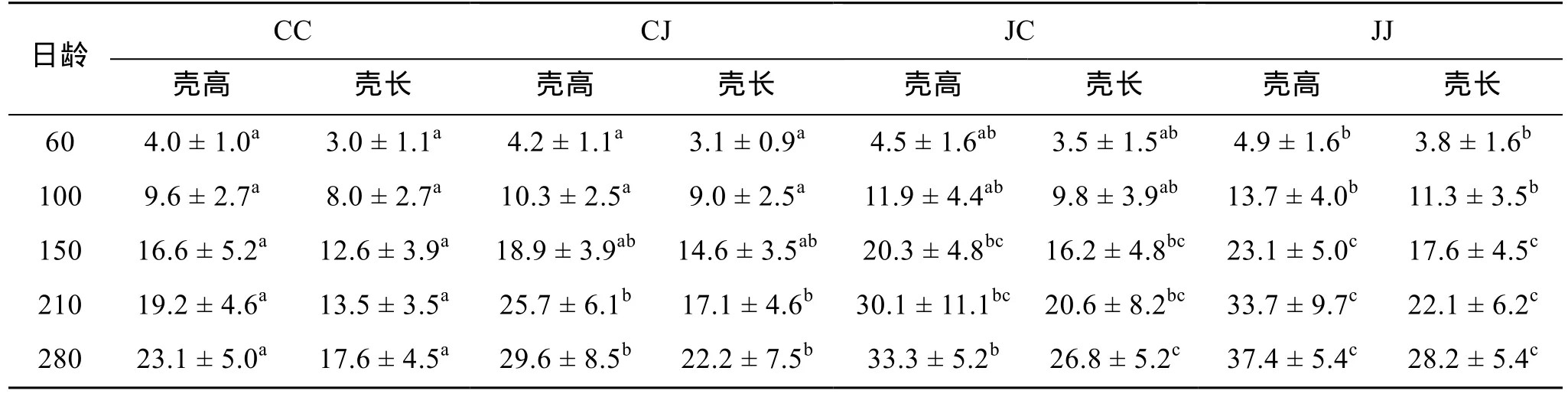
表5 稚贝, 养成期各实验组稚贝的生长Tab. 5 Growth of the four groups at spat and adult stage (mm)

表6 稚贝, 养成期各实验组稚贝的存活率Tab. 6 Percent survival means of the four groups at spat and adult stage (%)
2.3.3 稚贝, 养成阶段杂种优势率的比较分析
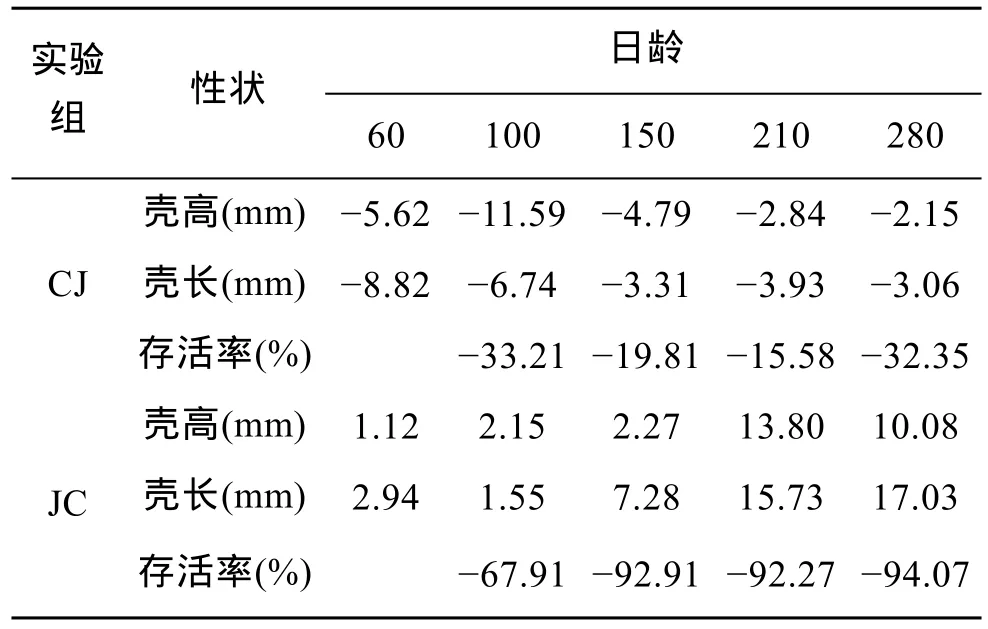
表7 稚贝, 养成期各杂交组生长和存活的杂种优势率Tab. 7 Heterosis for growth and survival of the four groups at spat and adult stage
稚贝, 养成期, 杂交组生长和存活的杂种优势率见表 7。同自交组相比, 杂交组 JC在壳高、壳长上均具有杂种优势, 并且杂交组JC在壳高上的杂种优势率随着日龄的增加而增加(1.12%~13.80%), 壳长的杂种优势率亦是如此(1.55%~17.03%); 而JC在存活率方面的不具有杂种优势。杂交组CJ在壳高、壳长和存活率上都不具有杂种优势率。
3 讨论
杂种优势是杂种子一代在生长力、繁殖力、产量、品质等性状上优于双亲的一种复杂的生物学现象。杂种优势的大小, 大多取决于双亲性状间的相对差异和互补程度。在一定范围内, 双亲的差异越大,往往杂种优势越强; 反之, 越弱。本实验中采用的两个长牡蛎群体, 是中国群体2007年群体选育F1子代与日本群体2007年群体选育F1子代, 两个群体来自不同的地点, 长期的养殖环境差异, 加上各自为群体选育 F1子代, 经过了以生长率、体长和体重为指标的连续歧化选择, 这些因素必然导致期遗传上存在差异。因此, 利用中、日两个长牡蛎群体进行杂交有可能产生较大的杂种优势。
本研究发现, 4个实验组的受精率为 76.76%~91.33%, 经方差分析表明, 杂交组与自交组之间无显著差异; 4个实验组的孵化率为71.25%~96.00%, 其中CJ组的孵化率最低, 为 71.25%, JJ组的孵化率最高,为 96.00%, 相同卵子来源的组合在孵化率上无差异,即CC组与CJ组之间, JC组与JJ组之间无显著差异。这些结果表明了长牡蛎中国群体和日本群体杂交的可行性。其主要原因是中国长牡蛎群体与日本长牡蛎群体之间的亲缘关系较近, 双亲异性配子之间的亲和力较高, 因此正、反杂交的受精率均很高。
本实验中, 杂交组JC在幼虫期的各项形态指标(壳高、壳长和存活率)均表现出明显的杂种优势, 其幼虫阶段壳高、壳长和存活率的杂种优势率分别为0.85%~5.63%, 0.29%~8.64%, 12.31%~96.45%; 到了稚贝养成阶段, JC在壳高和壳长上仍具有明显的杂种优势, 壳高和壳长的杂种优势率分别为 1.12%~13.80%, 1.55%~17.03%。杂交后代在生长存活等方面表现出一定的杂种优势在其他水产动物的杂交实验中也同样得到证实。例如, Newkirk[17]的研究发现长牡蛎 4个群体杂交后代在生长性状和存活率方面明显高于亲本。Rahman等[20]对两种海胆进行杂交, 结果发现杂交组12月龄的平均体重比自交组分别增加51.7%和48.4%。
虽然本实验中, 杂交组JC在幼虫期的各项形态指标上和稚贝养成期的壳高、壳长这些生长性状上表现出明显的杂种优势, 但是在稚贝养成期的存活率上却表现出了不同的现象, 杂种优势为负值, 而杂交组CJ在幼虫期和稚贝养成期的各项形态指标上都没有表现出杂种优势。这种不同的生长阶段表现出不同的杂种优势率, 以及正、反杂交后代在杂种优势上具有不同表现的现象在其他水产动物杂交实验中也有发现。Zhang等[15]对海湾扇贝不同群体(M和C)进行杂交, 结果发现, 幼虫阶段, 杂交组MC生长最快; 到了稚贝养成阶段, 杂交组 CM 超过 MC, 在壳高、壳长和总重这些生长指标上表现最好。Zheng等[21]在海湾扇贝不同地理群体(A和B)杂交效果研究中发现群体 A在幼虫、稚贝以及成贝都获得了较高的杂种优势率, 而群体 B的杂种优势率在各阶段均为负值。正、反杂交后代在杂种优势上具有不同表现, 其主要原因是环境和遗传因素的共同作用[22]。在幼虫期, 由于室内培育的原因, 水质、水温、饵料等因素保持在较适宜的条件下, 水中敌害生物较少,这时幼虫的存活率高低主要取决于幼虫本身的遗传特性。长牡蛎日本群体为选择育种 F1代, 经过一代选择, 各种生长性状优良, 遗传基础优秀, 而且在生物早期阶段的生长与发育中, 母体效应是一个非常重要的影响因素, 因而在幼虫期JJ和JC组的壳高、壳长生长较快, 存活率较高; 而长牡蛎中国群体取自威海乳山, 在中国养殖了多年, 种质出现退化, 遗传特质上不如长牡蛎日本群体, 因而CC和CJ组生长缓慢, 存活率较低。到了稚贝及养成期, 海上养殖的环境条件不可控, 水温、水质、饵料, 敌害等环境因子随着季节变化而变化, 使得环境条件对长牡蛎存活的影响非常大, 长牡蛎中国群体有可能更适应中国水域的变化情况, 加上母体效应即使成体之后依然存在的缘故[19], 因而使得CC和CJ的存活率较高, JJ和JC的存活率反而较低。
本实验通过对长牡蛎群体杂交的受精情况和杂种优势分析, 揭示了长牡蛎日本群体♀×中国群体♂的杂交子代在生长性状方面具有显著的杂种优势。所以, 应用这两个群体进行杂交以改良现有养殖群体可能是一个有效的途径。
[1]Miossec L, Le Deuff R M, Goulletquer P. Alien species alert:Crassostrea gigas(Pacific oyster)[J]. ICES Cooperative Research Report, 2009, 299: 1-42.
[2]FAO. World aquaculture production of fish, crustaceans,molluscs, etc., by principal species [M]. Food and Agriculture Organization, 2012.
[3]中国农业部渔业局.中国渔业统计年鉴 [M]. 北京:中国农业出版社, 2011.
[4]隋锡林, 孙景伟, 王富贵. 大连沿海太平洋牡蛎大量死亡原因解析 [J]. 大连水产学院学报, 2002, 17:272-278.
[5]李木彬. 太平洋牡蛎“种质变异”及对策 [J]. 科学养鱼, 2004, 8: 30-31.
[6]Newkirk G F, Haley L E, Waugh D L, et al. Genetics of larvae and spat growth rate in the oysterCrassostrea virginica[J]. Marine Biology, 1977, 41: 49-52.
[7]楼允东. 鱼类育种学 [M]. 北京: 中国农业出版社,2001.
[8]Madalena F E. A simple scheme to utilize heterosis in tropical dairy cattle [J]. World Animal Review, 1993.http:/ww4.fao.org/faobib sp/index.html.
[9]Crow J F. 90 years ago: The beginning of hybrid maize[J]. Genetics, 1998, 148: 923–928.
[10]Li Z K, Luo L J, Mei H W, et al. Overdominant epistatic loci are the primary genetic basis of inbreeding depression and heterosis in rice I. biomass and grain yield [J]. Genetics, 2001, 158: 1737-1753.
[11]Apostolov A, Slanev S. Heterosis effect in different schemes of crossing and hybridization in pig breeding[J]. Zhivotnov'Dni Nauki, 2002, 39: 75-78.
[12]吴仲庆. 水产生物遗传育种学(第三版)[M]. 厦门:厦门大学出版社, 2000.
[13]Cruz P, Ibarra A M. Larval growth and survival of two catarina scallop (Argopecten circularis, Sowerby, 1835)populations and their reciprocal crosses [J]. Journal of Experimental Marine Biology and Ecology, 1997,95-110.
[14]刘小林, 常亚青, 相建海, 等. 栉孔扇贝不同种群杂交效果的初步研究Ⅰ. 中国种群与俄罗斯种群的杂交 [J]. 海洋学报, 2003, 25: 93-99.
[15]Zhang H B, Liu X, Zhang G F, et al. Growth and survival of reciprocal between two bay scallop,Argopecten irradians concentricusSay andA. irradians irradiansLamarck [J]. Aquaculture, 2007, 272: 88-93.
[16]Newkirk G F, Haley L E, Waugh D L, et al. Genetics of larvae and spat growth rate in the oysterCrassostrea virginica[J]. Marine Biology, 1977, 41: 49-52.
[17]Newkirk G F. Interaction of genotype and salinity in larvae of the oysterCrassostrea virginica[J]. Marine Biology, 1978, 48: 227-234.
[18]Stiles S. Conventional and experimental approach to hybridization and inbreeding research in the oyster [J].Proceedings of the ninth annual meeting of the World Mariculture Society, Atlanda, Georgia, 1978, 557-586.
[19]Falconer D S. Introduction to Quantitative Genetics,2nd eds [M]. London: Longman, 1981.
[20]Rahman M A, Uehara T, Aslan L M. Comparative viability and growth of hybrids between two sympatric species of sea urchins (GenusEchinometra)in Okinawa[J]. Aquaculture, 2000, 183: 45-56.
[21]Zheng H P, Zhang G F, Guo X M. Heterosis between two stocks of the bay scallop,Argopecten irradians irradiansLamarck (1819)[J]. Journal of Shellfish Research, 2006, 25: 807-812.
[22]Husband B, Schemske D W. Evolution of the magnitude and timing of inbreeding depression in plants [J]. Evolution, 1996, 50: 54-70.
