高碱性脉石低品位混合镍矿氧压浸出行为与机制研究
2013-09-27李启厚刘智勇王红军刘志宏
李启厚,姜 波,刘智勇,王红军,刘志宏
(中南大学 冶金科学与工程学院,湖南 长沙 410083)
随着镍矿资源的日趋枯竭,高效开发储量可观的低品位镍矿资源日益受到重视[1]。低品位镍矿以传统技术不能经济处理[2]。一般而言,镍品位低于0.8%的氧化镍矿石和低于1.0%的硫化镍矿石都称为低品位镍矿石[3-4]。对于碱性脉石矿物含量较高的低品位矿石,用传统的火法工艺处理能耗高,成本高。而用常规酸浸工艺又会消耗大量酸,且严重环境污染;并且如果矿石硅含量高,则易生成硅酸盐胶体[5],造成矿浆液固分离困难。氨浸法[6]除能处理高硅、高碱性脉石矿物的矿石外,还适宜处理含铁、氟、氯、砷、锑等杂质含量高的矿石,具有溶液易循环利用、镍回收率高、环境污染小等优点。
Kyung-Ho Park[7]等利用氧压氨浸法研究了Cu-Ni-Co-Fe硫 化 物 的 共 熔 体 在 (NH4)2SO4/NH3体系中的浸出行为。共熔体中镍的硫化物主要以Ni9S8和Ni3S2形式存在,最优条件下,镍浸出 率 达 85.3%。 巨 少 华[8]采 用 氨-氯 化 铵(MACA)体系处理金川含硫化镍与硅酸镍的低品位镍矿石,镍浸出率为64.10%。本研究以某公司低品位混合镍矿为研究对象,在氨-硫酸铵-水体系中采用氧压氨浸法浸出镍,以期为工业实践提供参考依据。
1 试验部分
1.1 试验原料
试验所用矿石为某公司提供的含高碱性脉石矿物的贫镍矿。主要化学成分及镍的物相见表1、2。主要试剂为氨水(分析纯,湖南株洲石英化玻有限公司),硫酸铵(分析纯,上海国药集团),水为去离子水。
矿石中,硫化镍占52.38%,氧化镍和硅酸镍各占23.81%,矿石属于混合型镍矿。

表1 矿石主要化学成分的质量分数 %
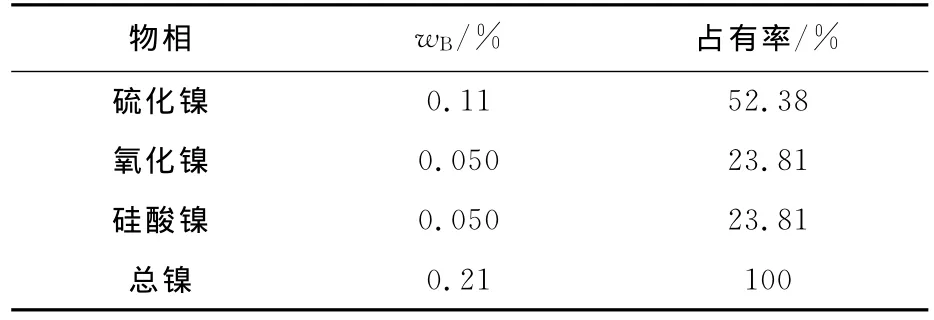
表2 矿石中镍的化学物相
1.2 试验设备与方法
浸出试验在WHF-2T型2L高压釜中进行。浸出剂根据设定的总氨浓度、NH+4/NH3物质的量比,用(NH4)2SO4、NH3·H2O 和去离子水配制而成,每次配制1L。将100g矿石与1L浸出剂同时加入高压釜中,在一定温度与压力下浸出,浸出结束后,冷却并进行液固分离,分别取浸出液及浸出渣分析其中镍的含量,计算镍浸出率。
1.3 分析与表征
Ni(Ⅱ)质量浓度采用 WFX-100型原子吸收分光光度计测定。矿石的物相组成采用日本理学公司的X射线衍射仪(RIGAKU-TTRⅢ)表征,测试条件为:工作电压40kV,工作电流250mA,Cu/Kα,扫描速度10°/min,步长0.02。样品形貌及表面成分用日本JSM-6360LV型扫描电镜(SEM)及美国EDAX公司的能谱仪(EDS)观察。
2 试验结果与讨论
2.1 氧压对镍浸出率的影响
在总氨浓度9mol/L、浸出温度150℃、c(NH3)∶c((NH4)2SO4)=2.5∶1、液固体积质量比10∶1、搅拌速度200r/min、浸出3h条件下,氧分压对矿石中镍浸出率的影响如图1所示。
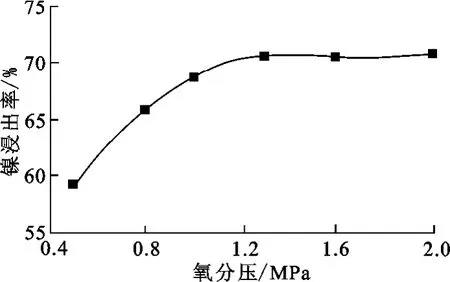
图1 氧压对镍浸出率的影响
从图1可知:镍浸出率先随氧分压增大而显著增大;当氧分压增加到1.3MPa后,再提高氧分压,镍浸出率变化不大。浸出过程中,溶解的氧分子只有裂解为活性氧原子时才能与硫化物反应,其氧化动力学方程为
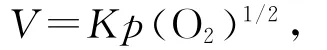
反应速率与p(O2)成正比关系[9],故提高氧分压,反应速率增大,浸出率增大;但随着反应的进行,氧的需要量逐渐减少,氧分压对反应速率的影响也逐渐减弱;当氧分压达到1.3MPa时,镍浸出率达到最高值。
对氧分压为2MPa时的浸出渣(相比原矿,其质量分数仅减少0.8%)进行化学物相分析,结果见表3。可以看出,浸出渣中仅含有微量的硫化镍和氧化镍,而硅酸镍质量分数与原矿中的基本相同,表明硫化镍和氧化镍得到浸出,而硅酸镍在此条件下未被浸出。
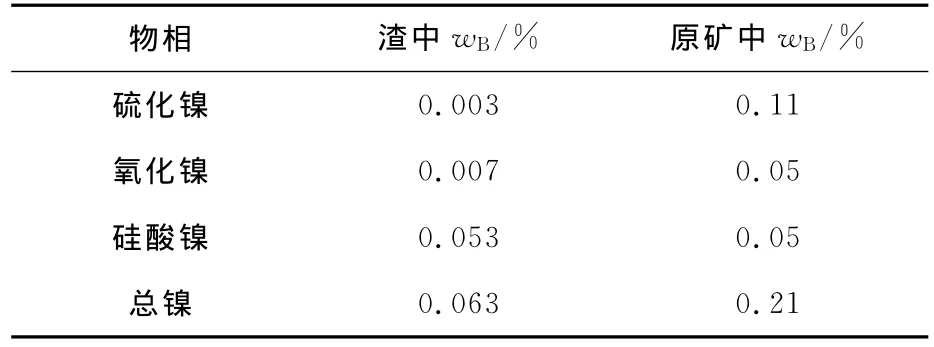
表3 氧压为2MPa条件下浸出渣的物相分析结果
硅酸镍氨浸反应方程式为:
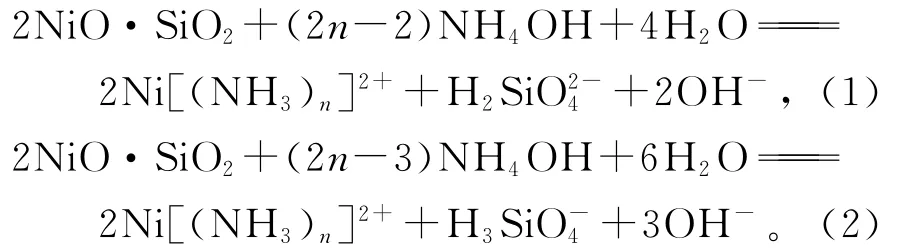
从可能生成的6种 (n=1~6)镍氨络合物Ni[(NH3)n]2+中选取3种,根据热力学数据[10]计算反应式(1)、(2)的吉布斯自由能,得吉布斯自由能随温度的变化曲线分别如图2、3所示。
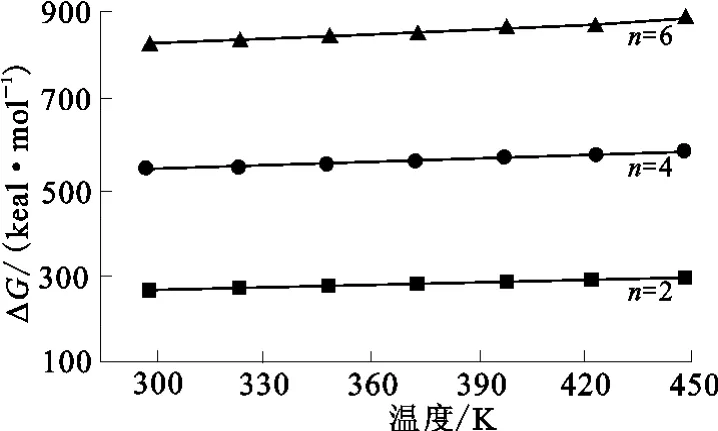
图2 反应式(1)的吉布斯自由能随温度的变化曲线
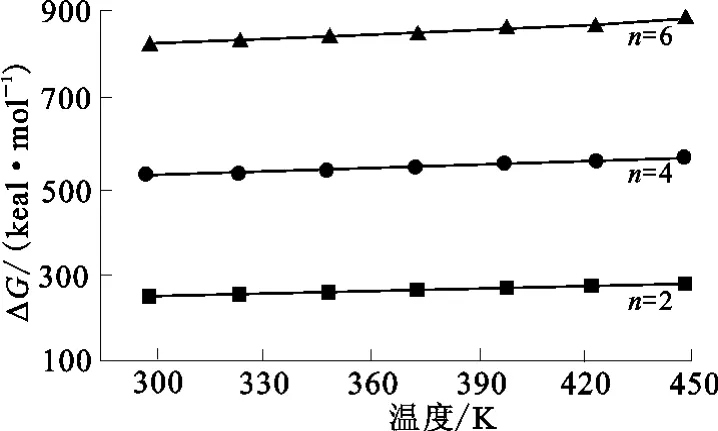
图3 反应式(2)的吉布斯自由能随温度的变化曲线
从图2、3可知:随温度升高,反应吉布斯自由能增大;不同产物在不同温度下的吉布斯自由能均大于0。因此,硅酸镍与氨水的反应从热力学上来讲是不可能发生的。这从理论上证明了硅酸镍在试验体系中不能被浸出,只有硫化镍和氧化镍能被浸出。
2.2 总氨浓度对镍浸出率的影响
在氧分压1.3MPa、浸出温度150℃、NH3与(NH4)2SO4的浓度比为2.5∶1、液固体积质量比10∶1、搅拌速度200r/min、浸出时间3h条件下,总铵浓度对镍浸出率的影响如图4所示。
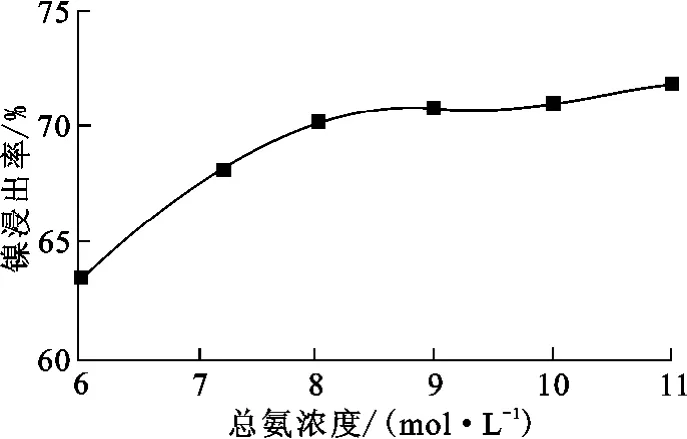
图4 总氨浓度对镍浸出率的影响
从图4可知,随溶液中总氨浓度增大,镍浸出率增大。在一定范围内对镍浸出速度和浸出率有影响的主要是NH3(aq),而且氨水浓度越大,其离解的数量就越少[9],故当总铵浓度增大时,NH+4的添加量增大,致使反应

向左移动,溶液中NH3(aq)的含量增多,从而使浸出率提高;但总铵浓度升高到8mol/L时,镍浸出率提高甚微。考虑到成本和镍浸出率,确定8 mol/L总氨浓度为最佳条件。
2.3 NH3与(NH4)2SO4浓度比对镍浸出率的影响
在氧分压1.3MPa、浸出温度150℃、总氨浓度8mol/L、液固体积质量比10∶1、搅拌速度200 r/min、浸出时间3h条件下,NH3与(NH4)2SO4的浓度比对镍浸出率的影响如图5所示。
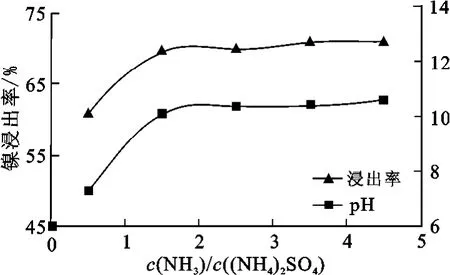
图5 NH3与(NH4)2SO4的浓度比对镍浸出率的影响
从图5可知:镍浸出率与浸出剂的pH都随NH3与(NH4)2SO4的浓度比增大而显著增大,最后都趋于稳定。在氧压氨浸过程中,当溶液pH介于6~8之间时,矿石中的镍与氧结合生成一种稳定的镍氧化物,从而导致镍浸出率较低[9];但随着NH3与(NH4)2SO4的浓度比增大,溶液pH升高,当pH大于8时,产生的镍氧化物迅速溶解并生成稳定的镍氨络合物,使镍浸出率增大。试验条件下,当 NH3与(NH4)2SO4浓度比为1.5∶1时,镍浸出率最高,故确定 NH3与(NH4)2SO4适宜的浓度比为1.5∶1。
2.4 浸出温度对镍浸出率的影响
在氧分压1.3MPa、总铵浓度8mol/L、NH3与(NH4)2SO4的浓度比1.5∶1、液固体积质量比10∶1、搅拌速度200r/min、浸出时间3h条件下,温度对矿石中镍浸出率的影响如图6所示。
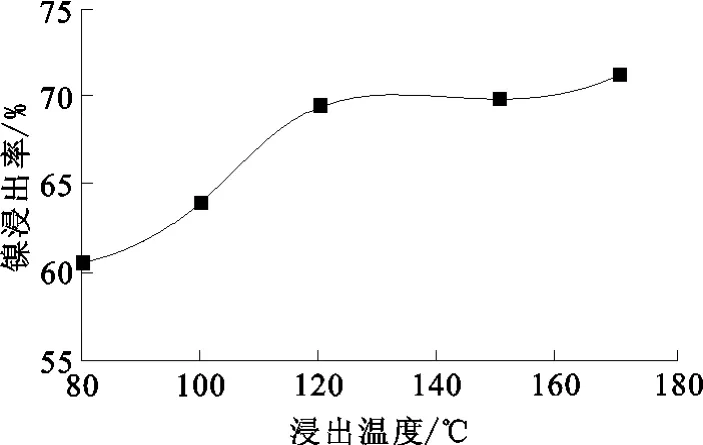
图6 温度对镍浸出率的影响
从图6可知,随温度升高,镍浸出率增大。由阿累尼乌斯方程[9]
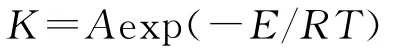
可知,温度升高,K增大,镍浸出率相应提高。在密闭的反应器中,温度适当提高不受浸出剂沸点和挥发性的控制,使反应得以快速充分进行[10]。当温度上升到120℃时,镍浸出率达69.44%,相当于矿石中的氧化镍与硫化镍基本浸出完全;温度继续升高,镍浸出率增大不明显。故确定浸出温度以120℃为宜。
2.5 浸出时间对镍浸出率的影响
在氧分压1.3MPa、浸出温度120℃、总氨浓度8mol/L、NH3与(NH4)2SO4浓度比为1.5∶1,液固体积质量比10∶1,搅拌速度200r/min条件下,浸出时间对镍浸出率的影响如图7所示。
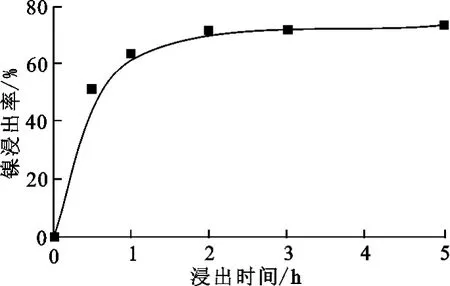
图7 浸出时间对镍浸出率的影响
由图7可知:随浸出的进行,镍浸出率不断升高;浸出前2h之内,反应剧烈,浸出速度快,镍浸出率达到70%,这时硫化镍和氧化镍已基本浸出完全,而硅酸镍仍保留在渣中。试验确定最佳浸出时间为2h。
3 结论
某公司的含硫化镍(0.11%)、氧化镍(0.05%)和硅酸镍(0.05%)的高碱性脉石低品位混合镍矿在NH3/(NH4)2SO4体系中浸出镍是可行的,最佳反应条件为:氧分压1.3MPa,温度120℃,总氨浓度8mol/L,NH3与(NH4)2SO4浓度比1.5∶1,浸出时间2h。最佳条件下,镍浸出率为70.86%,矿石中以氧化镍和硫化镍形式存在的镍基本浸出完全,而以硅酸盐类存在的镍因热力学原因不能被浸出。氨浸法处理含高碱性脉石矿物的低品位混合镍矿,镍回收率高,浸出液易循环利用,对环境污染小,可进一步研究并推广应用。
[1]温建康,阮仁满,孙雪南.金川低品位镍矿资源微生物浸出研究[J].矿冶,2002,11(1):55-58.
[2]方兆珩.生物浸出低品位镍铜硫化矿[J].有色金属:冶炼部分,2002(4):2-7.
[3]Deng T.Nickel and Cobalt Extraction by Pressure Hydrometallurgy[C]//Chongyue F,Huanhua H,Chuanfu Z.Proceedings of the International Conference on Mining and Metallurgy of Complex Nickel Ores.Beijing:International Academic Publishers,1993:59-64.
[4]聂珍媛,张在海,夏金兰.高碱性脉石低品位铜镍复合矿的诱变细菌浸出[J].有色矿冶,2002,18(5):17-19.
[5]符剑刚,王辉.从镍蛇纹石矿石中浸出Ni、Mg的实验研究[J].湿法冶金,2008,27(2):92-95.
[6]张保平,唐谟堂.氨浸法在湿法炼锌中的优点及展望[J].江西有色金属,2001,15(4):27-28.
[7]Park Kyung-Ho,Debasish Mohapatra,Reddy B Ramachandra.A study on the Oxidative Ammonia/ammonium Sulphate Leaching of Complex Matte[J].Hydrometallurgy,2007,86(3/4):164-171.
[8]巨少华.MACA体系中铜、镍和金的冶金热力学及低品位矿的堆浸工艺研究[D].长沙:中南大学,2006.
[9]徐采栋,林蓉.锌冶金物理化学[M].上海:上海科学技术出版社,1978:72-73.
[10]杨显万,何蔼平.高温水溶液热力学数据计算手册[M].北京:科学出版社,1983:48.
