液相色谱-质谱法测定人血浆氢氯噻嗪浓度的研究
2013-09-19余继英李晋奇师健友
余继英,何 林,傅 川,董 芸,陈 璐,李晋奇,师健友
(1.四川省医学科学院·四川省人民医院,a.药剂科,b.急诊内科,四川 成都 610072;2.四川大学华西药学院,四川 成都 610041)
氢氯噻嗪属噻嗪类利尿剂,除利尿作用外,在高血压治疗中也具有重要作用[1],其降压机制除减少血容量之外,还可降低外周血管阻力,是抗高血压复方制剂中常用的组分[2],如血管紧张素Ⅱ受体拮抗剂(ARB)+噻嗪类利尿剂,是各国高血压指南推荐的联合降压方案之一[3]。相关研究也表明ARB+氢氯噻嗪对老年单纯收缩期高血压具有较好的疗效[4]。对生物样本中氢氯噻嗪的测定,文献报道的有 HPLC-UV 法[5,6]及 HPLC-MS-MS 法[7~9]。本研究参考有关文献,利用现有条件,所建立的测定血浆氢氯噻嗪的LC-MS法灵敏准确,可用于人血浆中氢氯噻嗪浓度的测定。
1 材料与方法
1.1 仪器与试药 Waters 2695高效液相色谱仪;Waters ZQ质谱仪,Waters MassLynx V4.1色谱工作站(美国Waters公司);沙多利斯BP211型电子天平(德国沙多利斯);DIKA®Genius 3漩涡混合器(德国);HC-2517高速离心机(安徽中科中佳科学仪器有限公司);320R型低温离心机(德国)。氢氯噻嗪对照品,批号:100309-200702,含量99.8%,中国药品生物制品检定所;对乙酰氨基酚对照品(内标),批号:100018-200408,中国药品生物制品检定所。乙腈为色谱纯,其余试剂为分析纯,水为纯净水。
1.2 方法
1.2.1 色谱、质谱条件 ①色谱条件:色谱柱选用XTerra® MSC18柱(5 μm,2.1 mm×150 mm);保护柱:Diamonsil C18(2)Gartridges(3 μm,2.1 mm×10 mm),柱温30℃。流动相:水:乙腈-60:40;流速:0.2 ml/min。进样量:5μl。②质谱条件:电喷雾电离源(ESI-);选择离子监测(SRM;氢氯噻嗪 m/z 296,锥孔电压35 V;对乙酰氨基酚 m/z 150,锥孔电压30 V);毛细管电压2.5 kV;锥孔电压40 V;二级锥孔电压4 V;六级杆透镜电压0.4 V;源温度120℃;脱溶剂气温度350℃;脱溶剂气流量650 L/H。
1.2.2 溶液配制 精密称取氢氯噻嗪对照品10.52 mg于10 ml容量瓶,用50%甲醇溶解并定容,得氢氯噻嗪标准品储备液1(1.05 mg/ml),-4℃冷藏保存,临用前用50%甲醇稀释为系列浓度工作液。精密称取对乙酰氨基酚10.61 mg于10 ml容量瓶中,用甲醇溶解并定容至刻度,摇匀即得浓度为1.06 mg/ml的对乙酰氨基酚内标储备液,4℃冷藏保存,临用前用50%甲醇稀释为1μg/ml的溶液,即得对乙酰氨基酚内标工作液。
1.2.3 样品预处理与测定 取血浆样品0.5 ml,加50%乙腈50μl,再加入25μl内标工作液(对乙酰氨基酚,1μg/ml),漩涡混匀后,加乙酸乙酯3 ml,漩涡混合2分钟,于低温离心机(3000转/分,6℃)离心8分钟,取上清液于干燥玻璃管中,50℃水浴氮气挥干,残渣中加入50%乙腈120μl溶解后,分装入全自动进样器,进样5μl,在设定的色谱和质谱条件下测定。记录氢氯噻嗪和内标的色谱峰面积,以氢氯噻嗪峰面积和内标的峰面积之比代入当日标准曲线,算出样品氢氯噻嗪的浓度。
1.2.4 方法学考察 ①专属性:在选定的色谱和质谱条件下,取氢氯噻嗪和内标对照品溶液、空白血浆及空白血浆加氢氯噻嗪和内标样品经预处理后进样分析,考察方法的专属性。②标准曲线及定量下限:取空白血浆0.5 ml共9份,分别加入50μl氢氯噻嗪系列浓度溶液,使血浆氢氯噻嗪为0.5、1、2.5、5、10、25、50、100 和 150 μg/L,按“1.2.3”项下,自“再加入25μl内标工作液(对乙酰氨基酚,1μg/ml)”起操作。同法制备并测定空白样品。记录氢氯噻嗪和内标的色谱峰面积,以氢氯噻嗪峰面积和内标的峰面积之比对应其浓度进行线性回归,得出氢氯噻嗪血浆标准曲线回归方程。③方法精密度与准确度:取空白血浆0.5 ml,配制含氢氯噻嗪三种浓度分别为1,10 和 100 μg/L 的质控样品,按“1.2.3”项下,自“再加入25μl内标工作液”起操作,以药物和内标的峰面积比在当日标准曲线上求出氢氯噻嗪浓度,每一浓度于同日内进行5样本制备与分析,计算其准确度及批内RSD。于不同日连续测定3批,计算其批间RSD。④提取回收率:取离心管3支,分别加入浓度为10、100和1000μg/L的氢氯噻嗪工作液各50μl,各管再加入25μl内标工作液(对乙酰氨基酚,1μg/ml),50℃水浴氮气挥干,残渣以50%乙腈120μl溶解后进样,记录色谱图,所得峰面积记为A1;取空白血浆,配制含氢氯噻嗪三种浓度分别为1,10和100μg/L的质控样品,每种浓度各配制3个样品,按“1.2.3”项下,自“再加入25 μl内标工作液”起操作,进样并记录色谱图,所得峰面积记为A2。以A2/A1×100计算氢氯噻嗪及内标对乙酰氨基酚提取回收率。⑤基质效应:取离心管3支,分别加入浓度为10,100和1000μg/L的氢氯噻嗪工作液各50μl,各管再加入25μl内标工作液(对乙酰氨基酚,1μg/ml),50℃水浴氮气挥干,残渣以50%乙腈120μl溶解后进样,记录色谱图,所得峰面积记为A1。取空白血浆样品0.5 ml,加入50%乙腈75μl,乙酸乙酯3 ml,漩涡混合2分钟,于低温离心机(3000转/分,6℃)离心8分钟,取上清液于干燥玻璃管中,50℃水浴氮气挥干,残渣以50%乙腈120μl溶解后混匀。同法制备20份,合并作为空白基质溶液备用。取离心管,分别加入浓度为10、100和1000μg/L的氢氯噻嗪工作液各50μl(每种浓度各5份),各管再加入25μl内标工作液(对乙酰氨基酚,1μg/m l),50℃水浴氮气挥干后,分别加入空白基质溶液各120μl,混匀后进样并记录其色谱峰面积A2;以A2/A1×100计算基质效应。⑥血样稳定性:分别取在室温放置4和8 h后、-20℃冷冻后冻融1,2,3 次、-20 ℃保存14、24 和48 天的含氢氯噻嗪三种浓度分别为1,10和100μg/L的血浆样品,按“1.2.3”项下操作,由当日标准曲线计算氢氯噻嗪浓度,每一浓度测定3份样品。
2 结果
2.1 方法学考察 ①专属性、标准曲线及定量下限:由图1~图3可见,氢氯噻嗪和内标的保留时间分别约为2.4 min和2.1 min,血浆内源性杂质基本不影响样品的分离测定;氢氯噻嗪血浆标准曲线回归方程证明氢氯噻嗪血药浓度在0.5~150μg/L范围内与峰面积比之间有良好线性关系。氢氯噻嗪的最低定量限为0.5μg/L。②方法精密度与准确度:见表1。③氢氯噻嗪及内标对乙酰氨基酚提取回收率分别为57.0% ~72.8%及(56.3±3.3)%。④基质效应:氢氯噻嗪在1、10和100μg/L三种血浆浓度水平的基质效应平均值分别为(93.5±8.1)%、(93.8±6.1)%和(94.5±6.0)%;内标对乙酰氨基酚的基质效应值为(74.6±8.75)%。氢氯噻嗪及内标对乙酰氨基酚的基质效应均可满足测定要求。⑤血样稳定性:氢氯噻嗪血浆样品在室温放置8h、经-20℃反复冻融3次、在-20℃保存48天,氢氯噻嗪浓度无明显变化。含氢氯噻嗪血浆样品经处理后室温放置24 h,氢氯噻嗪浓度无明显变化;氢氯噻嗪储备液于4℃下保存65天仍然稳定,对乙酰氨基酚储备液于4℃下保存47天仍然稳定,均能满足生物样品测定要求。
2.2 方法应用 本方法应用于氯沙坦钾氢氯噻嗪片生物等效性试验。试验方案经院伦理委员会批准,志愿者在知情情况下填写知情同意书。按照试验方案选择21名健康男性受试者参加试验。试验当日晨给药前在前臂静脉安置留置针(可保留至给药后12小时),抽取空白血样4 ml后,分别空腹用200 ml温水送服氯沙坦钾氢氯噻嗪试验制剂和参比制剂62.5mg,并于服药后0.33、0.67、1、1.33、1.67、2、2.5、3、4、6、8、10、12、24、36 和 48 h 各采静脉血4 ml置于含肝素的试管中,抽取的血样于2500 rpm离心,分离血浆,置 -20℃的低温冰箱保存备测。21例受试者交叉口服试验制剂和参比制剂后均值血药浓度-时间曲线见图4。
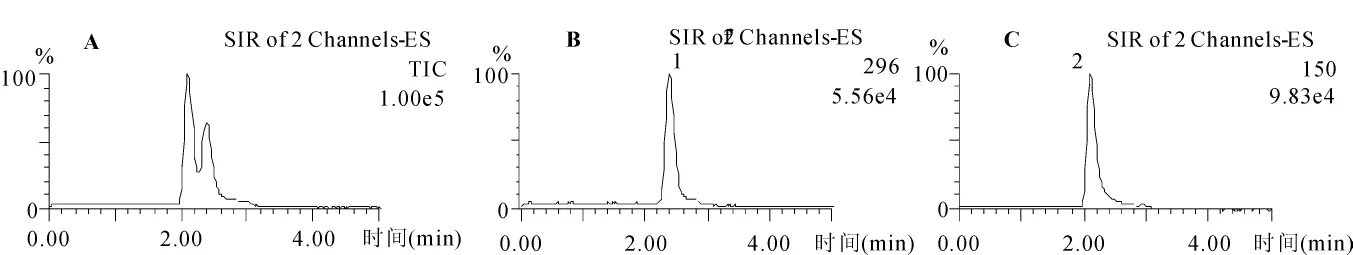
图1 氢氯噻嗪和内标对乙酰氨基酚对照品的总离子色谱图(A)、选择离子色谱图B(m/z296)和C(m/z150)1氢氯噻嗪;2对乙酰氨基酚

图2 空白血浆的总离子色谱图(A)、选择离子色谱图B(m/z296)和C(m/z150)

图3 空白血浆加氢氯噻嗪和内标对乙酰氨基酚的总离子色谱图(A)、选择离子色谱图B(m/z296)和C(m/z150)1氢氯噻嗪;2对乙酰氨基酚

表1 精密度与回收率试验结果 (n=15)
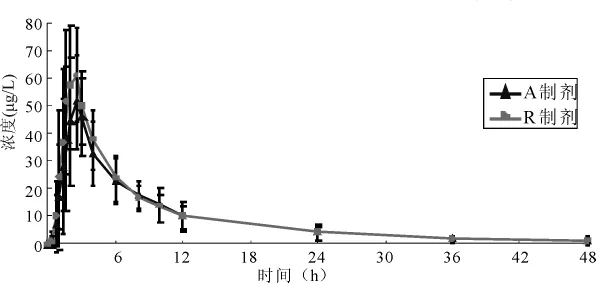
图4 21例健康受试者口服62.5 mg氯沙坦钾氢氯噻嗪片试验制剂与参比制剂后氢氯噻嗪的均值药时曲线
3 讨论
氢氯噻嗪的水溶性较强,但仅以甲醇、乙腈进行去蛋白处理后进样分析,内源性杂质干扰较大,因此考虑用液-液萃取法对血样进行预处理。在对比了乙醚、甲基叔丁基醚、醋酸乙酯及二氯甲烷的提取效果后,发现醋酸乙酯提取效率较高,内源性杂质基本不干扰测定,因此选择醋酸乙酯为提取溶剂。
氢氯噻嗪在ES-模式下才可电离,在流动相的选择方面,考虑通过在流动相中加入乙酸铵以得到更高的灵敏度,实验后发现,与不加乙酸铵相比,加入乙酸铵后在测定物峰形、灵敏度方面并无明显改善,因此最终选择流动相为水:乙腈-60:40。方法学考察结果表明,本试验所建立的方法专属性强,灵敏度高,能满足生物样品测定的要求。
21名健康受试者口服单剂量氯沙坦钾氢氯噻嗪片试验制剂和参比制剂后,氢氯噻嗪主要药动学参数无显著性差异,体内过程与文献[10]报道基本吻合。
[1]郝玉明,韩永燕.噻嗪类利尿药在高血压患者中的应用[J].临床药物治疗杂志,2012,10(1):4-7.
[2]杜海洲,刘娜,刘桂玲,等.国际抗高血压复方制剂研发进展[J].中国新药杂志,2010,19(18):1676-1679.
[3]孙宁玲.血管紧张素受体拮抗剂联合利尿剂的治疗方案在高血压治疗中的地位[J].中华高血压杂志,2010,18(8):712-715.
[4]邹文淑,陈德助,彭良君,等.国产替米沙坦与苯磺酸左旋氨氯地平联合氢氯噻嗪治疗老年单纯收缩期高血压的疗效及安全性比较[J].实用医院临床杂志,2011,8(5):52-54.
[5]孙莹莹,韦阳,王恪申,等.HPLC法测定人血浆中氢氯噻嗪的浓度[J].药物分析杂志,2010,30(3):396-398.
[6]胡连栋,邢倩斌,刘慈,等.复方氢氯噻嗪片在家犬体内的药动学和相对生物利用度研究[J].中国药房,2010,21(1):30-31.
[7]王蓉,杨昆,谭洁.人体氢氯噻嗪血药浓度测定与药代动力学研究[J].中国药业,2011,20(23):17-18.
[8]潘杰,张全英,张逸凡,等.健康受试者口服复方替米沙坦片后氢氯噻嗪的药物动力学[J].中国药师,2009,12(5):563-566.
[9]许莉,蒋娟娟,田蕾,等.复方缬沙坦在健康人体的生物等效性[J].中国临床药理学杂志,2011,27(11):856-870.
[10]刘茜,王鹭,尚宏伟,等.液相色谱串联质谱法测定人血浆中氯沙坦/氢氯噻嗪的浓度及其人体相对生物利用度研究[J].中国临床药理学杂志,2009,25(4):341-345.
