磁性氧化石墨烯制备及去除水中刚果红的研究
2013-09-07张秀蓉龚继来曾光明邓久华湖南大学环境科学与工程学院湖南长沙410082
张秀蓉,龚继来,曾光明,邓久华 (湖南大学环境科学与工程学院,湖南 长沙 410082)
印染废水中的染料具有化学结构复杂,稳定性高,难以生化降解,色度大,浊度高,COD高等特点,如果直接排入水体,将会严重影响水体的美观及水环境中动植物的生存,已经成为当前最难处理的废水之一[1-3].刚果红作为一种典型直接偶氮染料,用量大且易于进入水体,对环境的影响很大.
吸附法在染料废水处理中被视为一种经济有效的方法[1].然而,传统的吸附剂存在着吸附容量不高、不便分离等缺点.碳纳米材料吸附剂具有高比表面积、容易获得、合成步骤简单、物理化学结构稳定等特点,近年来已成为研究的热点[4-6].氧化石墨烯(GO)是一种新型二维碳纳米材料,表面有大量的含氧官能团(包括羟基、环氧基、羧基),广泛应用于电子、生物传感器、药物传输、环境水质净化等领域[7].把碳纳米材料赋予磁性,所形成的磁性碳纳米材料既具有纳米材料的高吸附特性,又具有磁性材料的易分离特性,并被应用于水质净化处理中[8-10].本研究小组长期致力于磁性纳米材料吸附剂设计、合成并应用于水质净化处理[11-14].本研究,制备了磁性氧化石墨烯,并作为一种纳米材料吸附剂去除水介质中刚果红,考察了氧化石墨烯负载磁性粒子后对刚果红的吸附性能及吸附时间、初始pH值、离子强度对吸附的影响.
1 实验部分
1.1 材料
硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]、硫酸铁铵[NH4Fe(SO4)2·12H2O]、氢氧化钠、98%浓硫酸、氨水、双氧水(H2O2)、高锰酸钾、硝酸钠、刚果红均为分析纯.石墨粉购于上海金山亭新化工试剂厂.实验用水均为超纯水.
所用仪器:电热恒温水/油浴锅,JHS-1恒速搅拌器(杭州仪表电机厂),真空干燥箱,SHY-2A数显恒温水浴振荡器(常州普天仪器制造有限公司),751型可见分光光度计.
1.2 磁性氧化石墨烯(MGO)的制备
GO的合成采用Hummer方法[15].称取1.0g石墨粉和0.5g硝酸钠加入到23mL 98%的浓硫酸中,冰浴,使温度冷却到0℃.强烈搅拌的同时将3.0g高锰酸钾加入混合液,严格控制加入的速度,使混合液温度不超过20℃.除去冰浴,将混合液移入水温为35℃的恒温水浴锅中保持30min,然后在混合液中缓慢加入46mL温水,将混合液移到98℃的恒温油浴锅中,保持15min.将混合液用温水稀释到 140mL,加入2.5mL 30%的双氧水,过滤,蒸馏水洗涤3次,70℃真空干燥12h.
将1.0g合成的GO分散于100mL超纯水中.在氮气保护下,将 5.8g(NH4)2Fe(SO4)2·6H2O 和10.7g NH4Fe(SO4)2·12H2O溶于100mL超纯水中(Fe3+:Fe2+=1.5:1,摩尔比),快速加入10mL 25%的氨水,将GO悬浮液缓慢加入.混合液在85℃,300r/min条件下搅拌45 min.冷却至室温,用磁铁将合成的MGO从混合液中分离出来,用超纯水和无水乙醇分别洗涤3次,70℃真空干燥12h,磨碎放入干燥器备用.
1.3 磁性氧化石墨烯的表征
使用扫描电子显微镜(SEM,JSM-6700F)和透射电子显微镜(TEM,JEOL-1230,日本)观察吸附剂的表面形态特征,使用震动样品磁强计(VSM,Lake Shore 7410)记录磁滞回线;使用Zeta电位仪(ZETASIZER)获得吸附剂表面电位值.
1.4 吸附试验
所有实验设置2组平行实验,用0.1mol/L NaOH和HCl调节pH到指定值.刚果红浓度使用可见分光光度法测定,吸收波长500nm[16].
1.4.1 初始pH值的影响 将20mg吸附剂加入到一系列初始浓度为90mg/L的刚果红溶液中,调节pH值为3~10,置于25℃,130r/min的恒温水浴振荡器中振荡24h,磁性分离后测定剩余刚果红浓度.
1.4.2 离子强度对吸附的影响 将20mg吸附剂加入到一系列含有不同浓度NaCl(0.001,0.01,0.1mol/L)的刚果红溶液中,调节pH值为6.0±0.1,置于25℃,130r/min的恒温水浴振荡器中振荡24h,磁性分离后测定剩余刚果红浓度.
1.4.3 吸附动力学实验 将20mg吸附剂加入到一系列初始浓度为90mg/L的刚果红溶液中,调节pH值为6.0±0.1,置于25℃,130r/min的恒温水浴振荡器中振荡一定时间,取样,磁性分离后测定剩余刚果红浓度.
1.4.4 吸附等温线实验 将20mg吸附剂加入到一系列初始浓度分别为10~120mg/L的刚果红溶液中,调节pH值为6.0±0.1,置于25℃,130 r/min的恒温水浴振荡器中振荡24h,磁性分离后测定剩余刚果红浓度.
1.4.5 自来水中刚果红的吸附 刚果红溶液用自来水配制.将20mg吸附剂加入到系列初始浓度分别为10~500mg/L的刚果红溶液中,调节pH值为6.0±0.1,置于25℃,130r/min的恒温水浴振荡器中振荡24h,磁性分离后测定剩余刚果红浓度.
2 结果与讨论
2.1 MGO与GO的表征
图1(a,c)显示,GO是片状的二维纳米材料,其表面有很多的褶皱,这样可以增大比表面积,有利于磁性粒子覆盖到GO的表面[17].图1(b,d)表明,磁性纳米粒子成功地覆盖在GO表面上.关于负载磁性粒子到GO表面的反应机理已有相关文献报道[18],即GO表面含有丰富的羧基,制备磁性氧化石墨烯时,可溶性铁盐和亚铁盐与GO上的羧基形成配合物,从而化学沉积在GO载体上,在碱性条件下形成铁氧化物纳米粒子负载的氧化石墨烯.图2为MGO的红外光谱图,其中3055,3265cm-1的宽峰是—OH伸缩振动所引起,1591cm-1的强峰来源于C=O基团伸缩振动[18],1031,1236cm-1来源于C—O伸缩振动,1300,1448cm-1是C—O—C伸缩振动引起[19],601cm-1峰来源于Fe—O伸缩振动.图3为MGO的磁滞回线,饱和磁强度为31.2emu/g,足够用磁铁将其分离出来[13];不同pH值条件下,吸附剂表面的zeta电位不同,在pH值3~10的范围内,随着pH值的增加,磁性氧化石墨烯表面的电荷由正变负,等电点为3.5,当pH<3.5,吸附剂表面带正电荷,当pH>3.5,吸附剂表面带负电荷.

图1 GO和MGO扫描电镜和透射电镜照片Fig.1 SEM and TEM images of GO and MGO
2.2 pH值对吸附的影响
从图4可以看出,随着pH值的增加,刚果红的吸附量先增加到最大值,然后再逐渐减少,Feng等[20]在用壳聚糖覆盖的石英砂去除刚果红也报道了相同的趋势.为了分析产生这种结果的原因,本实验从吸附剂的表面特性及刚果红本身的结构两方面加以探讨.刚果红的结构会随着pH值的变化而改变,当pH<5.2时,刚果红的颜色从红色变为蓝紫色[21].pH<5.2,刚果红的氨基得到H+而被质子化,刚果红染料表面带正电,当pH<3.5,吸附剂表面带正电荷,当pH>3.5,吸附剂表面带负电荷,所以,刚果红与磁性氧化石墨烯之间的静电排斥力使得pH3时的吸附量最小(47.9mg/g).随着pH值的增加,刚果红表面电荷由正变负,静电引力使吸附量增加,在pH值4~5达到最大值.当pH≥6时,刚果红结构发生改变,表面电荷由正变负,且pH值越大,吸附剂表面所带负电荷越多,静电排斥力越大,故吸附量逐渐减少.综合考虑,后续实验将pH6作为实验条件.

图2 MGO的傅里叶红外光谱图Fig.2 FTIR of MGO

图3 MGO的磁滞回线Fig.3 Magnetization curve of MGO

图4 初始pH值对刚果红吸附量的影响Fig.4 Effect of initial solution pH on the adsorption of congo red
2.3 离子强度对吸附的影响
由图5可见,加入的离子对刚果红的吸附有抑制作用,这可能由于离子强度的增加导致刚果红阴离子移动系数减小,从而阻碍其吸附在MGO表面,使吸附量减少[21].加入的离子强度越大,抑制作用越明显,说明MGO不适宜处理高盐度的废水.此外,离子强度对低浓度的刚果红影响很小,刚果红浓度越大,影响越明显.
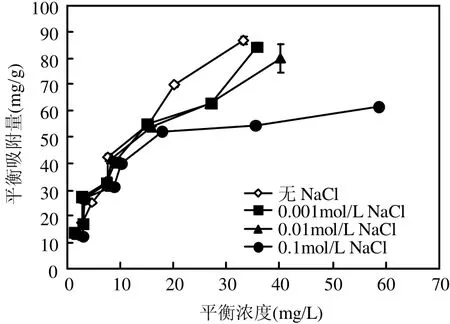
图5 离子强度对吸附的影响Fig.5 Effect of ion strength on the adsorption of congo red onto MGO
2.4 吸附动力学
从图6中可以看出,在吸附开始的4.75h以内,吸附量快速增加,这是由于吸附剂表面刚果红与水溶液之间的浓度差促使溶液中的刚果红快速移动到吸附剂的表面,从而使水中的刚果红快速减少,此时吸附剂表面大量的吸附位点也是快速吸附的一个原因.然后吸附量缓慢增加直到达到平衡.在7h内,吸附基本上达到平衡.本实验中,选用24h作为吸附时间,以确保实验充分达到平衡.选用准一级动力学模型和准二级动力学模型来模拟动力学.
表1列出了这2种模型拟合的参数,表明准二级动力学模型能够更好的模拟刚果红动力学过程,吸附过程为化学吸附[22].
2.5 等温吸附研究
采用Langmuir等温吸附模型和Frenudlich等温吸附模型对实验数据进行拟合,由表2可知,Langmuir和Freundlich模拟的相关系数R2分别为0.9820和0.9788,说明2种模型都能很好的描述刚果红的吸附过程.根据Langmuir方程计算得出最大吸附容量为143.6mg/g.Freundlich方程参数0<1/n<1,表明刚果红易于吸附到MGO上[23].
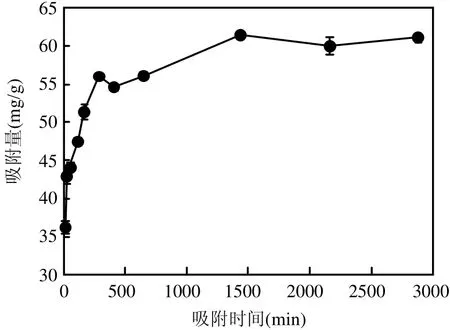
图6 MGO吸附水中刚果红的动力学Fig.6 Time-dependent congo red adsorption on MGO

表1 MGO吸附刚果红动力学参数Table 1 Kinetics parameters for adsorption of congo red by MGO

图7 刚果红的等温吸附线Fig.7 Adsorption isotherm of the adsorption for congo red onto MGO
2.6 与其他吸附剂的比较
表3列出了其他几种吸附剂对刚果红的去除效果[20,24-27].MGO对刚果红的高去除效率可能是因为染料的芳香结构与MGO的π共轭部分形成了π-π键[28],刚果红与MGO之间的静电引力也会促进吸附.

表2 MGO吸附刚果红Langmuir和Freundlich方程参数Table 2 Langmuir and Freundlich adsorption isotherm constants for adsorption of congo red by MGO

表3 与其他吸附剂吸附刚果红最大容量比较Table 3 The maximum adsorption capacity of congo red on various adsorbent
2.7 自来水中刚果红的吸附

图8 自来水中刚果红的吸附Fig.8 The adsorption of congo red onto MGO in tap water
由图8可见,刚果红在自来水中的最大吸附容量为287.6mg/g,为超纯水中的2倍,表明磁性
氧化石墨烯对刚果红的去除是一种有前景的吸附剂.Sun等人报道了类似的结果,他们发现磁性还原性氧化石墨烯纳米复合物去除湖水和工业废水中的亚甲基蓝比去除去离子水中的亚甲基蓝效率更高[2].从表2中可以看出,Langmuir线性方程能更好的描述刚果红在自来水中的吸附过程,R2=0.9696.在本研究中,自来水中含有大量的阴阳离子,其离子强度比在超纯水中强,但是在自来水中的最大吸附容量比在超纯水中高,其原因应该不完全来源于离子强度的影响,其具体原因和相关机理有待进一步研究.
3 结论
3.1 MGO饱和磁强度为31.2emu/g,具有足够的磁性,很容易从水溶液中分离出来.
3.2 刚果红的初始pH值对吸附的影响很大,随着pH值的增加,刚果红的吸附量先增加到最大值然后逐渐减少,在pH4~5达到最大值.
3.3 在水中加入NaCl,会抑制刚果红的吸附,且离子强度越强,抑制越明显.
3.4 吸附动力学符合准二级动力学模型,且吸附速率较快,吸附7h基本上达到平衡.
3.5 MGO对刚果红具有很好的去除效果,最大吸附容量可达140.6mg/g,Langmuir和Freundlich两种模型均能很好的描述刚果红的吸附过程.
3.6 刚果红在自来水中的最大吸附容量为超纯水中的2倍,表明MGO有望用于实际水处理中.
[1]Luo Peng,Zhang Bing,Zhao Yafei,et al.Removal of methylene blue from aqueous solutions by adsorption onto chemically activated halloysite nanotubes[J].korean Journal of Chemical Engineering,2011,28(3):800-807.
[2]Sun Hongmei, Cao Linyuan, Lu Lehui.Magnetite/reduced graphene oxide nanocomposites:One step solvothermal synthesis and use as a novel platform for removal of dye pollutants[J].Nano Research,2011,4(6):550-562.
[3]Guo Jianzhong,Chen Shunwei,Liu Li,et al.Adsorption ofdye from wastewaterusing chitosan–CTAB modi fi ed bentonites[J].Journal of Colloid and Interface Science,2012,382:61-66.
[4]Chen Guang-Cai,Shan Xiao-Quan,Wang Yu-Sheng,et al.Adsorption of 2,4,6-trichlorophenol by multi-walled carbon nanotubes as affected by Cu(II)[J].Water Research,2009,43:2409-2418.
[5]崔春月,马 东,郑庆柱.Fenton改性多壁碳纳米管对亚甲基蓝的吸附性能研究 [J].中国环境科学,2011,31(12):1972-1976.
[6]Gupta V K,Agarwal S,Saleh TA.Chromium removal by combining the magnetic properties of iron oxide with adsorption properties of carbon nanotubes[J].Water Research,2011,45:2207-2212.
[7]KuilaT,BoseS,Mishra A K,etal.Chemical functionalization of graphene and its applications[J].Progress in Materials Science,2012,57:1061-1105.
[8]王 彬,龚继来,杨春平,等.磁性多壁碳纳米管吸附去除水中罗丹明 B的研究 [J].中国环境科学,2008,28(11):1009-1013.
[9]Tang Wang-Wang,Zeng Guang-Ming,Gong Ji-Lai,et al.Simultaneous adsorption of atrazine and Cu(II)from wastewater by magnetic multi-walled carbon nanotube [J].Chemical Engineering Journal,2012,211-212:470-478.
[10]Gong Ji-Lai,Wang Bin,Zeng Guang-Ming,et al.Removal of cationic dyes from aqueous solution using magnetic multi-wall carbon nanotube nanocomposite as adsorbent[J].Journal of Hazardous Materials,2009,264:1517-1522.
[11]Feng Yuan,Gong Ji-Lai,Zeng Guang-Ming,et al.Adsorption of Cd(II)and Zn(II)from aqueous solutions using magnetic hydroxyapatite nanoparticles as adsorbents [J].Chemical Engineering Journal,2010,162:487-494.
[12]Long Fei,Gong Ji-Lai,Zeng Guang-Ming,etal.Removal of phosphate from aqueous solution by magnetic Fe–Zr binary oxide [J]. Chemical Engineering Journal,2011,171:448-455.
[13]Gong Ji-Lai,Wang Xi-Yang,Zeng Guang-Ming,et al.Copper (II) removal by pectin–iron oxide magnetic nanocomposite adsorbent[J].Chemical Engineering Journal,2012,(185/186):100-107.
[14]Gong Jilai,Chen Long,Zeng Guangming.Shellac-coated iron oxide nanoparticles for removal of cadmium(II)ions from aqueous solution [J].JournalofEnvironmentalSciences,2012,24(7):1165-1173.
[15]Hummers W S,Offeman R E.Preparation of graphitic oxide [J].Journal of the American Chemical Society,1958,80(6):1339-1339.
[16]Dawood S,Sen T K.Removal of anionic dye congo red from aqueous solution by raw pine and acid-treated pine cone powderas adsorbent:Equilibrium,thermodynamic,kinetics,mechanism and process design [J]. Water Research,2012,46:1933-1946.
[17]Liu Mancheng,Chen Changlun,Hu Jun,et al.Synthesis of magnetite/graphene oxide composite and application cobalt(II)removal[J].JournalofPhysicalChemistry C,2011,115:25234-25240.
[18]Yang Xiaoying,Zhang Xiaoyan,Ma Yanfeng,et al.Superparamagnetic graphene oxide–Fe3O4nanoparticles hybrid for controlled targeted drug carriers[J].Journal of Materials Chemistry,2009,19:2710-2714.
[19]Peng E,Choo E S G,Chandrasekharan P,et al.Synthesis of manganese ferrite/graphene oxide nanocomposites for biomedicalapplications[J].MagneticNanoparticles,2012,8(23):3620-3630.
[20]Feng Tao,Zhang Fan,Wang Jie.Application of Chitosan-Coated Quartz Sand for Congo ed Adsorption from Aqueous Solution[J].Journal of Applied Polymer Science,2012,125:1766-1772.
[21]Yang Shubin,Hu Jun,Chen Changlun,et al.Mutual effects of Pb(II)and humic acid adsorption on multiwalled carbon nanotubes/polyacrylamide composites from aqueous solutions[J].Environmental Science and Technology,2011,45:3621-3627.
[22]BarkauskasJ,StankevicieneI,DaksevicJ,etal.Interaction between graphite oxide and Congo red in aqueous Media[J].Carbon,2011,49:5373-5381.
[23]王 雯,谢 丽,王 帅.钢渣对阴离子染料刚果红的吸附特性和机理 [J].同济大学学报(自然科学版),2010,38(8):1182-1187.
[24]GhaediM,BiyarehM N,KokhdanSN,etal.Comparison of the ef fi ciency of palladium and silver nanoparticles loaded on activated carbon and zinc oxide nanorods loaded on activated carbon as new adsorbents for removal of congo red from aqueous solution:Kinetic and isotherm study[J].Materials Science and Engineering C,2012,32:725-734.
[25]Zhao Yahong,Xue Zhenhua,Wang Ximing,et al.Adsorption of congo red onto lignocellulose/montmorillonite nanocomposite [J]. Journal of Wuhan University of Technology-Mater.Sci.Ed,2012,10:931-938.
[26]Zhang Zhanying,Lalehvash Moghaddam,Ian M O’Hara,et al.Congo Red adsorption by ball-milled sugarcane bagasse[J].Chemical Engineering Journal,2011,178:122-128.
[27]Grabowska L,Gryglewicz G.Adsorption characteristics of congo red on coal-based mesoporous activated carbon[J].Dyes Pigments,2007,74:34-40.
[28]Ramesha G K,Kumara A V,Muralidhara H B,et al.Grphene and graphene oxide as effective adsorbents toward anionic and cationic dye [J]. J. Colloid Interf. Sci.,2011,361:270-277.
