血浆中莪术醇和吉马酮的测定及其大鼠体内的药代动力学研究
2013-09-06严鹏程黄可新
潘 瑜, 张 园, 向 铮 , 严鹏程, 黄可新
(1.温州医学院药学院,浙江温州 325035;2.温州医学院分析测试中心,浙江温州 325035)
莪术是姜科植物蓬莪术Curcuma phaeocaulisVal、广西莪术Curcuma kwangsiensisS.G.Lee et C.F.Liang或温郁金Curcuma wenyujinY.H.Chen et C.Ling,习称温莪术的干燥根茎[1],具有行气破血,消积止痛之功效,是一种活血化瘀类的传统中药。莪术的主要成分为挥发油和姜黄素,挥发油的主要成分是莪术醇、莪术二酮、吉马酮等,其中莪术醇具有抗肝纤维化、抗氧化等生物活性[2],也是发展前景良好的抗肿瘤药物[3]。吉马酮对D-半乳糖胺/脂多糖诱导的肝疾病具有保护作用[4],是抗肿瘤的活性成分,对癌细胞有一定的抑制作用[5]。许多传统复方制剂如木香分气丸、止痛化癥胶囊、保妇康栓、痛经宝颗粒[6]等都包含莪术;莪术也作为单味药如莪术油等用于治疗消积化滞、散结止痛、瘀血经闭[6]。煎剂是中医方剂用药的基本形式,目前鲜有其煎剂的药代动力学研究报道。本实验建立了大鼠口服莪术水提物血浆中莪术醇和吉马酮 (如图1)的高效液相色谱法分析方法,此方法简便、准确、稳定,适用于莪术醇和吉马酮的血药浓度测定和药动学研究。
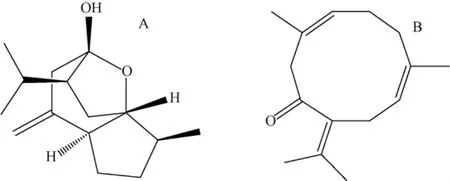
图1 莪术醇 (A)和吉马酮 (B)的化学结构Fig.1 Structures of curcumenol and germacrone
1 材料与方法
1.1 仪器 Agilent 1100高效液相色谱系统 (美国Agilent公司);XW-80A型漩涡混合器 (上海医科大学仪器厂);Sartorius BS224S电子天平 (赛多利斯科学仪器 (北京)有限公司);TU-1901型双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);FD-1C型冷冻干燥机(北京德天佑科技发展有限公司)。
1.2 药品与试剂 莪术醇标准品 (中国药品生物制品鉴定所,批号:100185-200506),吉马酮标准品(中国药品生物制品鉴定所,批号:111665-200902),甲醇、乙腈 (美国Spectrum公司,色谱纯),超纯水 (Milli-Q系统),莪术 (温州医学院附属第一医院中药房提供)。
1.3 实验动物 SD大鼠5只,雄性,6~7周龄,体质量 (250±20)g,温州医学院实验动物中心提供。
1.4 给药方案 莪术药材经水煎煮1 h后经冷冻干燥成浸膏后4℃保存,给药时用超纯水配制成质量浓度为0.15 g/mL(浸膏中含莪术醇的量为0.276 mg/g,吉马酮为0.164 mg/g)。SD大鼠 5只,禁食不禁水12 h,按照1 mL/100 g的剂量,灌胃给予莪术提取液。于灌胃后 0,0.083,0.167,0.333,0.5,1,2,4,8,12,24 h 尾静脉取血每次约0.5 ml,置于肝素化管中,4℃静置5 min,13 000 r/min离心10 min,分离血浆保存在-20℃。
1.5 色谱条件 Hypersil ODS色谱柱(4.6 mm×250mm,5 μm,大连依利特分析仪器有限公司),流动相为乙腈-水 (0~20 min:63% ~66%),体积流量为1.0 mL/min,柱温25℃,检测波长210 nm,进样量20 μL。
1.6 血浆样品处理 取血浆室温下融冻,各精密吸取200 μL于离心管中,精密加入300 μL乙腈,涡旋1 min,离心 (13 000 r/min)15 min,取上清液,进样20 μL作HPLC分析。
1.7 数据处理 利用药理学计算软件DAS 2.1.1版计算主要药代学参数(t1/2、AUC等)。
2 结果
2.1 色谱行为 在1.5项色谱条件下,空白血浆、含药血浆和含标准品血浆的色谱如图2所示,各组分色谱峰充分分离,不受内源性杂质峰干扰,莪术醇的保留时间为10.095 min,吉马酮的保留时间为13.595 min。
2.2 标准曲线 取莪术醇对照品和吉马酮对照品适量,精密称定,加甲醇制成每1 mL含莪术醇200 μg,吉马酮200 μg的对照品贮备液。将上述配制好的莪术醇、吉马酮对照品贮备液用甲醇依次稀释成质量浓度分别为50,25,10,5,2.5,1,0.5,0.25,0.1,0.05 μg/mL。取大鼠空白血浆200 μL,精密加入上述配制好的莪术醇、吉马酮对照品稀释液,得到一系列不同质量浓度分别含莪术醇 5,2.5,1,0.5,0.25,0.1,0.05,0.025 μg/mL和 含 吉马 酮 2.5,1,0.5,0.25,0.1,0.05,0.025 μg/mL。按照1.6项下进行操作。以血浆中待测物对照品质量浓度 (C)为横坐标,相应峰面积 (Y)为纵坐标进行回归计算,得标准曲线方程,如表1。
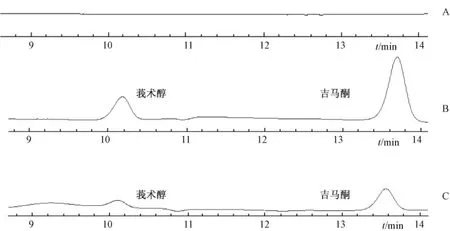
图2 空白血浆 (A)、含标准品血浆 (B)及含药血浆 (C)的HPLC色谱图Fig.2 Chromatograms of blank plasma(A),blank plasma spiked with curcumenol and germacrone(B)and plasma sample(C)
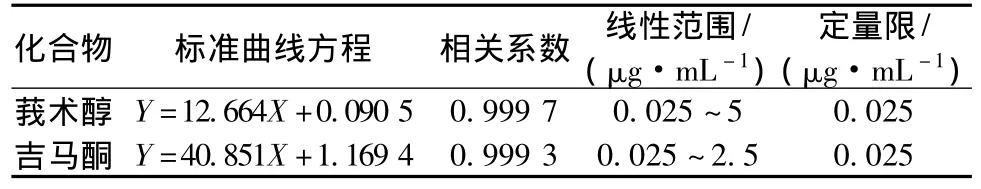
表1 莪术醇和吉马酮的标准曲线、相关系数、线性范围和定量限Tab.1 Standard curves,correlation coefficients,linear ranges and LOQs of curcumenol and germacrone
2.3 回收率和精密度 取空白血浆200 μL,精密加入已配制好的莪术醇和吉马酮对照品溶液,配成高、中、低质量浓度,按照1.6项下进行操作,每一质量浓度进样5次分析,计算求得其在大鼠血浆中的方法回收率、提取回收率,在1 d内不同时间进样,测得3种质量浓度标准血浆的日内变异系数,相同质量浓度的标准血浆在5 d内的日间变异系数,结果如表2所示。
表2 莪术醇和吉马酮在大鼠血浆中的回收率和精密度(±s,n=5)Tab.2 Recoveries and precisions of curcumenol and germacrone in rat plasma(±s,n=5)
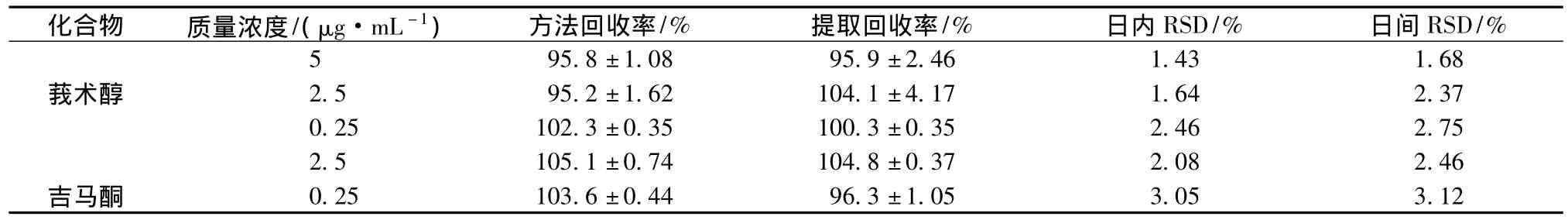
表2 莪术醇和吉马酮在大鼠血浆中的回收率和精密度(±s,n=5)Tab.2 Recoveries and precisions of curcumenol and germacrone in rat plasma(±s,n=5)
化合物 质量浓度/(μg·mL-1) 方法回收率/% 提取回收率/% 日内RSD/% 日间RSD/%5 95.8±1.08 95.9±2.46 1.43 1.68莪术醇 2.5 95.2±1.62 104.1±4.17 1.64 2.37 0.25 102.3±0.35 100.3±0.35 2.46 2.75 2.5 105.1±0.74 104.8±0.37 2.08 2.46吉马酮0.25 103.6±0.44 96.3±1.05 3.05 3.12
2.4 稳定性考察 制备高、中、低(含莪术醇5,2.5,0.25 μg/mL)的质控样品,分别室温放置12 h,反复冻融2次,-20℃冻存1 d,1周后测定。结果样品在室温放置12 h,冻融前,冻融1次,冻融2次,冷冻1 d和7 d后,测定的标准偏差均小于5%,稳定性良好。
2.5 莪术醇和吉马酮在大鼠体内的药代动力学研究 血浆按照1.6项下进行操作,测得大鼠灌胃服用莪术水提液后的平均血药浓度—时间曲线,结果见图3。
利用药理学计算软件 DAS 2.1.1版处理,自动推算、模型、权重选择,拟合的血药浓度—时间曲线符合二室模型,有关药动学参数 (t1/2、AUC等)见表3。
3 讨论
本实验建立了RP-HPLC测定莪术醇和吉马酮
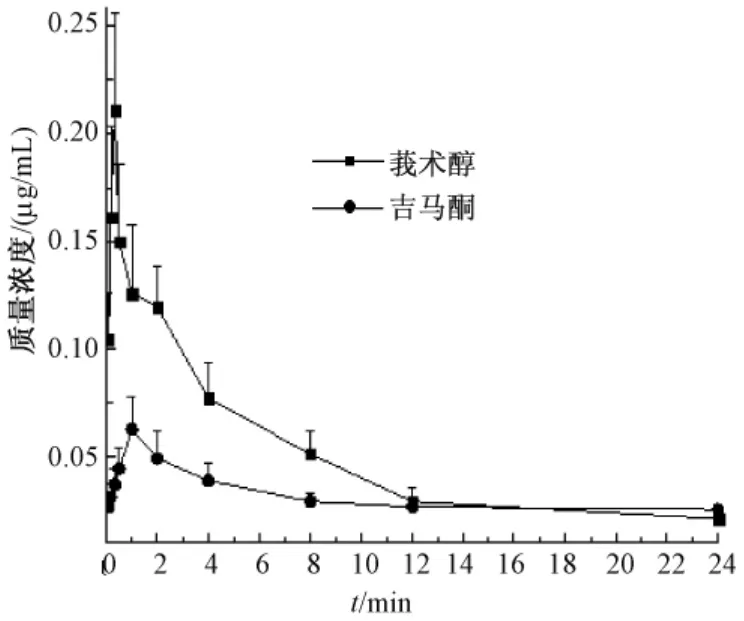
图3 莪术提取物大鼠灌胃给药后莪术醇和吉马酮的血药浓度—时间曲线Fig.3 Mean plasma concentration-time curves of curcumenol and germacrone after intragastric administration of zedoary turmeric aqueous extract
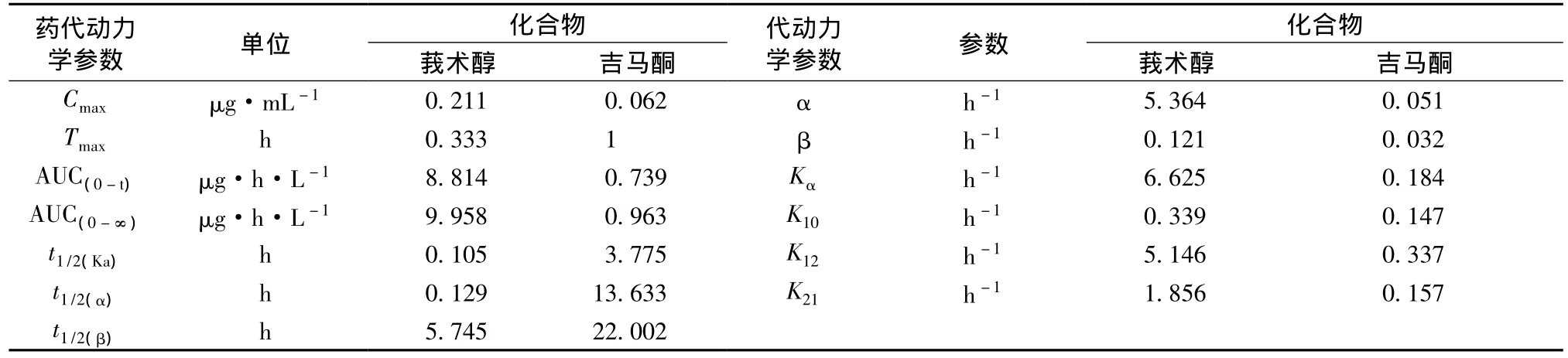
表3 莪术醇和吉马酮的药动学参数Tab.3 Pharmacokinetic parameters of curcumenol and germacrone
在大鼠体内血药浓度的方法,并进行了药代动力学研究。根据紫外分光光度计测定,莪术醇的最大紫外吸收波长是207 nm,吉马酮的最大紫外吸收波长是217 nm,二者在210 nm处均有较大吸收,故选择此波长作为检测波长。
中药所含成分的复杂性、有效成分的不确定性以及成分微量等使分离测定的难度增加,血浆样品处理的过程至关重要。莪术醇和吉马酮为莪术中主要的活性成分,具有一定挥发性,其在氮气挥干的过程中易损失导致定量结果不准确,因此实验选用乙腈沉淀蛋白法代替乙酸乙酯萃取的方法处理血浆。
高效液相法的药物体内分析,通常因提取方法对含量准确测定影响较大而采用内标法,但内标法测定操作过程较繁琐,成本高。本实验因在210 nm处内源性物质干扰较多,难以在较短的保留时间内选择合适的内标物。此外,本实验血样处理操作简单易行,经方法学验证,精密度较好,回收率高,故选择外标法进行含量测定。
药代动力学处理结果表明,大鼠灌胃服用莪术水提液后的药代动力学过程用二室模型描述较为合理。莪术醇在胃肠道能迅速吸收(Kα=6.625 h-1),灌服莪术提取液后莪术醇的血药浓度在0.333 h达到峰值,说明莪术醇进入大鼠体循环后迅速分布(α=5.364 h-1),发挥药效迅速。血浆中莪术醇的消除速率常数β为0.121 h-1,血中的t1/2(α)=0.129 h,t1/2(β)=5.745 h,t1/2(β)>t1/2(α),可知大鼠灌服莪术提取液后莪术醇在体内消除也迅速,属于吸收快、消除快的代谢过程。吉马酮在胃肠道内吸收稍慢 (Kα=0.184 h-1),灌服莪术提取液后吉马酮的血药浓度在1 h达峰,表明吉马酮进入大鼠体循环后分布慢于莪术醇 (α=0.051 h-1),血浆中吉马酮的消除速率常数β为0.032 h-1,血中的t1/2(α)=13.633 h,t1/2(β)=22.002 h,提示大鼠灌服莪术提取液后吉马酮属于慢速消除类。莪术醇和吉马酮的K12均大于K21,说明二者从中央房室向周边房室的转运速率大于从周边房室向中央房室的转运速率。表明莪术提取液大鼠灌胃后以不同速度从肠道吸收,进入体循环,随机分布到体内的组织、器官,然后分别表现出不同的清除过程。
经方法学验证,本方法简便、准确、稳定,回收率、精密度均符合生物样本中微量测定[7]要求,可用于莪术煎剂中药代动力学研究。
[1]国家药典委员会.中华人民共和国药典:2005年版一部[S].北京:中国医药科技出版社,2005:194.
[2]Lou Yan,Zhang Hui,He Hao,et al.Isolation and identification of phase 1 metabolites of curcumol in rats[J].Drug Meta Dispos,2010,38(11):2014-2022.
[3]王 琰,王慕邹.莪术的质量研究[J].药学学报,2001,36(11):849-853.
[4]Matsuda H,Ninomiya K,Morikawa T,et al.Inhibitory effect and action mechanism of sesquiterpenes fromZedoariae RhizomaonD-galactosamine/lipopolysaccharide-induced liver injury[J].Bioorg Med ChemLett,1998,8(4):339-344.
[5]Zhong Zhangfeng,Chen Xiuping,Tan Wen,et al.Germacrone inhibits the proliferation of breast cancer cell lines by inducing cell cycle arrest and promoting apoptosis[J].Eur J Pharmacol,2011,667(1-3):50-55.
[6]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[7]Causon R.Validation of chromatographic methods in biomedical analysis.Viewpoint and discussion[J].J Chromatogr B,1997,689(1):175-180.
