高速剪切乳化机制备纳米氧化锌及形貌控制
2013-08-29徐国旺杨中华黄新堂
徐国旺 ,杨中华,黄新堂
(1.湖北工业大学,武汉 430068;2.湖北省广播电视大学,武汉 430074;3.华中师范大学 物理科学与技术学院,武汉 430079)
氧化锌是一种Ⅱ-Ⅵ族直接宽带隙(带隙3.37eV)半导体材料,由于人们发现纳米氧化锌具有奇特的光学和电学性能,因此氧化锌纳米材料(纳米棒、纳米线、纳米带、纳米管等)得到了广泛的研究[1-4].一维氧化锌纳米结构是一种具有重要应用价值的半导体材料,广泛用于短波激光器、太阳能电池、光电子仪器、表面声波和压电材料.特别是氧化锌纳米线(棒)在室温下光致紫外发光的发现,一维氧化锌纳米结构的制备、表征与相关性能研究受到了人们的特别关注.在合成一维氧化锌纳米材料方面,已进行过大量卓有成效的研究.目前合成氧化锌纳米材料的方法很多,包括气相合成法[5-8],如金属有机气体外延生长(MOVPE)法、热蒸发法、分子束外延(MBE)法等;液相法[9-12],如电化学沉积法、水热法等基于溶液的生长方法.
本文以Zn(NO3)2·6H2O、氨水为原料,通过控制实验条件,研究了高速剪切乳化机制备的ZnO 的结构、形貌与团聚性.
1 实验
1.1 试剂与仪器
实验中所用Zn(NO3)2·6H2O(分析纯,含量≥99%,中国医药(集团)上海化学试剂公司);氨水(含量≥25%,中国医药(集团)上海化学试剂公司);高速剪切乳化机(JRD300-D-I,上海标本模型厂);超声清洗器(KQ-250B 型超声波清洗器,昆山市超声仪器有限公司);场发射扫描电子显微镜(FESEM,JEOL JSM 6700F).X 射线衍射仪(Y-2000Cu Kα,λ=0.15418nm).
1.2 实验方法
取一定量的Zn(NO3)2·6H2O 溶于水,超声至完全溶解,加入氨水,用高速剪切乳化机搅拌一定时间,冷却至室温后,再清洗过滤数次,烘干得到ZnO粉末样品.用场发射扫描电子显微镜观察样品形貌及尺寸,用X射线衍射仪分析样品的晶体结构.
改变反应温度、溶液浓度、PH值、反应时间及乳化机转速和搅拌方式,得到不同形貌、不同粒度的纳米氧化锌.
2 结果与讨论
2.1 氧化锌样品形貌和结构
取4.5g Zn(NO3)2·6H2O 溶于500ml水(室温)中,超声至完全溶解,将5.2g氨水加入150ml水(室温)中,将两种溶液混合,用高速剪切乳化机搅拌,转速为10 000r/m,调节搅拌头高度,让溶液在容器上形成涡流,20 min 后,溶液温度接近100 ℃,继续搅拌10min后停止.冷却后清洗过滤数次,在60 ℃干燥,得到ZnO 粉末样品.
图1为样品的X 射线衍射图.上图为样品的衍射结果,下图为氧化锌的标准衍射图.所有的衍射峰均与标准结果一致.所以,制备的样品是氧化锌.图2为样品的SEM 图,从图中可以看出,样品是截面为近六边形的纳米棒,其直径为70~80nm,长度约为1μm.
在XRD 分析的实验结果中没有发现杂质的衍射峰,所有衍射峰的位置与相对强度均与标准的氧化锌XRD 衍射结果一致.说明氧化锌样品的纯度较高,从SEM 图中可以看出,样品的几何结构比较均一,长度与直径分布基本控制在相对比较小的范围.
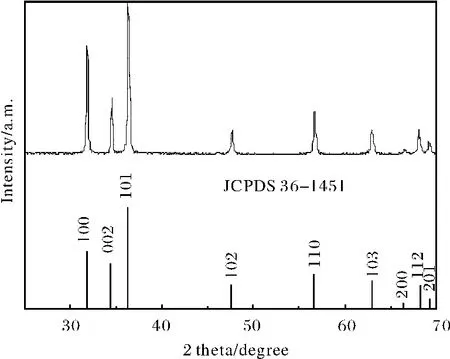
图1 样品的XRD 图Fig.1 XRD image of the sample

图2 氧化锌纳米棒的SEM 图Fig.2 SEM images of ZnO nanorods
2.2 反应条件对产物形貌的影响
2.2.1 乳化机转速对形貌的影响 取1.00g硝酸锌溶于400mL、12℃水中,再加入1.37g氨水,第一次用乳化机高速(10 000r/m)搅拌20min,反应温度为12~100℃,第二次中速(6 000r/m)搅拌20min,反应温度为12~88℃.所得样品形貌如图3.从图中可以看出:转速高时生成的氧化锌粒度趋于一致,纵向约为500nm,横向约为200nm;转速低时样品的粒度分布较分散,且有较为严重的团聚效应.
实验结果表明,在其它条件(浓度、时间、化学物质的比例、搅拌方式等)相同的情况下,乳化机的转速(溶液升温状态)不同时,转速快(升温快)的实验条件,纳米氧化锌样品比较均一,而且分散状况好;转速慢(升温慢)的实验条件,氧化锌样品的均一性较差,而且容易团聚.

图3 不同反应温度下样品的SEM 图Fig.3 SEM images of samples in different temperatures
2.2.2 pH值对形貌的影响 用乳化机搅拌溶液15min,在反应温度(12~88℃)相同、pH值不同的条件下,所得样品的形貌如图4.从图中可以看出,在相同的反应温度下,pH值为11时所得样品由长约600nm 左右的椭球组成花形,pH值为9时,样品中虽然可以看出有氧化锌椭球形成,但并没形成花形,并且样品均一性较差.在实验中,样品1是在pH值较大,碱性强的条件下完成的,这时容易结晶形成纳米氧化锌颗粒;但由于转速低(反应温度低),颗粒的分散状况较差,形成了椭球体聚集的氧化锌花.对于样品2,氨水分量少,样品无专一的形貌,所以颗粒均一性不好.
这一结果与前面实验结果相比较,样品的分散性不好,主要是由于转速低(温度低)和反应时间短所造成的.因此,如果需要制备样品均一,长径比较大和分散性较好的纳米氧化锌样品,需提高转速(提高反应温度)和适当增加反应时间.

图4 不同pH值下样品的SEM 图Fig.4 SEM images of samples in different pH values
2.2.3 溶液浓度对形貌的影响 在相同的反应温度(12~88℃)下,溶液的浓度不同,得到样品的形貌如图5.从图中看出,溶液浓度高的得到的是花形氧化锌;浓度低的得到的是大量的椭球,其中只有很少的花形氧化锌,但团聚现象较为严重,分散性较差.
实验结果说明:(1)低温、低转速和反应时间短的条件下,样品的团聚现象严重.在本实验中由于浓度的差别,虽然所得样品得形貌有些差别,但总的结果是样品均一性和分散性都不好.因此温度、转速或以时间为代价是得到均一性和分散性好的纳米氧化锌样品的关键因素.(2)浓度高时,氧化锌颗粒(椭球状)结晶快,在相同的时间段内椭球相对较大;浓度低时,氧化锌颗粒相对较小.因此,为了得到颗粒相对较小、分散性好和几何形状均一的纳米氧化锌样品,除了要提高乳化机的转速,提高实验反应温度和适当延长反应时间外,还需适当地降低溶液的浓度,如果希望所制备的纳米氧化锌样品颗粒相对较大,可以适当增加溶液浓度.因此,为了达到控制所制备的纳米氧化锌颗粒大小的目的,可以控制浓度指标.

图5 不同浓度下样品的SEM 图Fig.5 SEM images of samples in different solid contents
2.2.4 搅拌方式对形貌的影响 在溶液浓度相同、pH值相同、反应时间和温度基本一致的条件下,采取不同的搅拌方式搅拌溶液,得到氧化锌样品的形貌如图6.其中图(a)是用高速剪切乳化机以最大速度(10 000r/m)搅拌,使得溶液形成急速的涡流而得到的样品.图(b)是把高速剪切乳化机搅拌头的内环去掉,减少搅拌时的剪切力,同样以最大速度(10 000r/m)搅拌时得到的结果.在去掉乳化机搅拌头后,容器中各部分溶液的流向与流速都是随机的、杂乱的.从图中可以看出,采用不同的搅拌方式,得到的最终产物的形貌完全不同,利用不同的搅拌方式,可控制纳米氧化锌的形貌.

图6 不同的搅拌方式下样品的SEM 图Fig.6 SEM images of samples in different agitation ways
3 结论
本文提出了以六水合硝酸锌和氨水为原料,用高速剪切乳化机制备纳米氧化锌的新方法,并用此方法成功地制备了氧化锌纳米棒、纳米花,纳米椭球.
该方法制备纳米氧化锌,与其它方法相比,具有方法简单,条件易控,成本低廉,易量产,产品质量好、形状均一等优点.目前,高速剪切乳化机生产厂家具有生产单机一次处理十几吨、几十吨溶液的大型乳化机的能力,所以用此方法完全可用于大规模的工业生产.在大规模的工业生产中,该方法还有生产周期短、产量高、产品质量可靠等优点.
通过多次实验对比,找出了反应温度、溶液浓度、pH值、以及搅拌方式对生成氧化锌形貌的影响.首先反应温度或反应时间和乳化机的强剪切效应是制备产品均一、分散性好和长径比可控的关键因素.控制溶液的浓度可以达到控制纳米氧化锌颗粒大小的目的.
[1]Vayssieres L.Growth of arrayed nanorods and nanowires of ZnO from aqueous solutions[J].Adv Mater,2003,15:464-466.
[2]Li Y,Meng G W,Zhang L D,et al.Ordered semiconductor ZnO nanowire arrays and their photoluminescence properties[J].Appl Phys Lett,2000,76:2011-2013.
[3]Jih-Jen Wu,Sai-Chang Liu.Catalyst-free growth and characterization of ZnO nanorods[J].J Phys Chem B,2002,106:9546-9551.
[4]Yang P,Yan H,Mao S,et al.Controlled growth of ZnO nanowires and their optical properties[J].Adv Func Mater,2002(12):323-330.
[5]Park W I,Kim D H,Jung S-W,et al.Metalorganic vaporphase epitaxial growth of vertically well-aligned ZnO nanorods[J].Appl Phys Lett,2002,80:4232-4234.
[6]Wu J J,Liu S-C.Low-temperature growth of well-aligned ZnO nanorods by chemical vapor deposition[J].Adv Mater,2002,14:215-218.
[7]Yao B D,Chan Y F,Wang N.Formation of ZnO nanostructures by a simple way of thermal evaporation[J].Appl Phys Lett,2002,81:757-759.
[8]Huang M H,Mao S,Feick H,et al.Room-temperature Ultraviolet nanowire nanolasers[J].Science,2001,292:1897-1899.
[9]Zheng M J,Zhang L D,Li G H,et al.Fabrication and optical properties of large-scale uniform zinc oxide nanowire arrays by one-step electrochemical deposition technique[J].Chem Phys Lett,2002,363:123-128.
[10]Sun X M,Chen X,Deng Z X,et al.A CTAB-assisted hydrothermal orientation growth of ZnO nanorods[J].Mater Chem Phys,2003,78:99-104.
[11]Liu B,Zeng H C.Hydrothermal synthesis of ZnO nanorods in the diameter regime of 50nm[J].J Am Chem Soc,2003,125:4430-4431.
[12]Zhang J,Sun L D,Yin J L,et al.Control of ZnO morphology via a simple solution route[J].Chem,Mater,2002,14:4172-4177.
