顶空毛细管气相色谱法测定福尔可定原料药中5种有机溶剂的残留量
2013-08-29刘胜春赵学刚冯雅慧康海霞滑千里王乃浩河北省中医院石家庄050011河北奥星集团药业有限公司石家庄050700
刘胜春,赵学刚,冯雅慧,康海霞,滑千里,王乃浩(1.河北省中医院,石家庄050011;.河北奥星集团药业有限公司,石家庄 050700)
福尔可定是中枢性镇咳药,与磷酸可待因具有相似的中枢性镇咳作用,也有镇静和镇痛作用,但成瘾性较磷酸可待因弱,常用于剧烈干咳和中度疼痛。临床上已有的制剂有福尔可定片、复方福尔可定糖浆、复方福尔可定口服溶液。新生儿和儿童易于耐受此药,不会引起便秘和消化紊乱[1]。根据河北奥星集团药业有限公司提供的福尔可定及其合成起始原料的工艺路线得知,福尔可定原料药在合成过程中使用了甲醇、乙醇、苯、丁醇、甲苯5种有机溶剂,这些溶剂对人体健康和环境可造成危害。为了保证药品的安全,笔者建立了福尔可定原料药中5种有机溶剂残留量的检查方法。笔者根据2010年版《中国药典》(二部)[2]的相关规定和人用药品注册技术规范的国际协调会(ICH)指导原则[3],同时参考文献[4]方法以0.25mol/L硫酸溶液为介质,采用顶空毛细管气相色谱法,同时测定上述5种有机溶剂的残留量。结果表明,建立的方法快速、灵敏、准确,可用于福尔可定原料药中有机溶剂残留量的测定。
1 材料
1.1 仪器
6890N气相色谱仪、7694E顶空进样器(美国Agilent公司);CPA225D电子天平(德国Sartorius公司)。
1.2 药品与试剂
福尔可定原料药(河北奥星集团药业有限公司,批号:061101、061102、061103,纯度:99.87%、99.88%、99.87%);甲醇、乙醇、苯、丁醇、甲苯均为分析纯(含量:均>99%),水为纯化水。
2 方法与结果
2.1 色谱条件
色谱柱:DB-624毛细管柱(30m×530μm,3μm);柱温:80℃维持7min,以15℃/min的速率升至120℃,维持10min;检测器:氢火焰离子化检测器(FID),检测器温度:250℃;分流进样,分流比:1∶1;进样口温度:200℃;载气:氮气,流速:3.0ml/min;顶空进样,平衡温度:85℃,平衡时间:30min,顶空瓶加压时间:0.2min,进样时间:1min,定量环体积:1ml,定量环温度:95℃,传输线温度:105℃。
2.2 专属性试验
分别取甲醇、乙醇、苯、丁醇、甲苯、N,N-二甲基甲酰胺(DMF)制备成单独的对照品溶液和“2.3.2”项下的对照品混合溶液,分别按“2.1”项下条件顶空进样,记录色谱图。结果,出峰顺序依次为甲醇、乙醇、苯、丁醇、甲苯、DMF;取福尔可定原料药约0.5g,精密称定,置于20ml顶空瓶中,精密加入0.25 mol/L硫酸溶液5ml,密封,振摇使溶解,作为供试品溶液。顶空进样,记录色谱图。结果各有机溶剂间的分离良好,专属性良好。6种有机溶剂的色谱图见图1A,混合溶液色谱图见图1B,供试品溶液色谱图见图1C。

图1 专属性试验气相色谱图A.溶剂对照品溶液;B.对照品混合溶液;C.供试品溶液;1.甲醇;2.乙醇;3.苯;4.丁醇;5.甲苯;6.DMFFig 1 GC chromatograms of specificity testA.control solutions;B.mixed control solutions;C.test samples solution;1.methanol;2.ethanol;3.benzene; 4.butanol;5.toluene;6.DMF
2.3 溶液的制备
2.3.1 对照品混合贮备液。精密称取甲醇3000mg、乙醇5000mg、丁醇5000mg、苯2mg、甲苯890mg,置于同一100ml量瓶中,加入体积分数50%的DMF水溶液溶解并稀释至刻度,摇匀。精密量取上述溶液5ml,置于50ml量瓶中,用0.25mol/L硫酸溶液稀释至刻度,摇匀,即得。
2.3.2 对照品混合溶液。精密量取对照品混合贮备液5ml,置于50ml量瓶中,用0.25mol/L硫酸溶液稀释至刻度,摇匀,即得。
2.4 线性关系考察
精密量取对照品混合贮备液1、2、4、5、6、7ml,分别置于50ml量瓶中,用0.25mol/L硫酸溶液稀释至刻度,摇匀。进样分析,以峰面积(y)为纵坐标、样品质量浓度(x)为横坐标,进行线性回归,结果见表1。
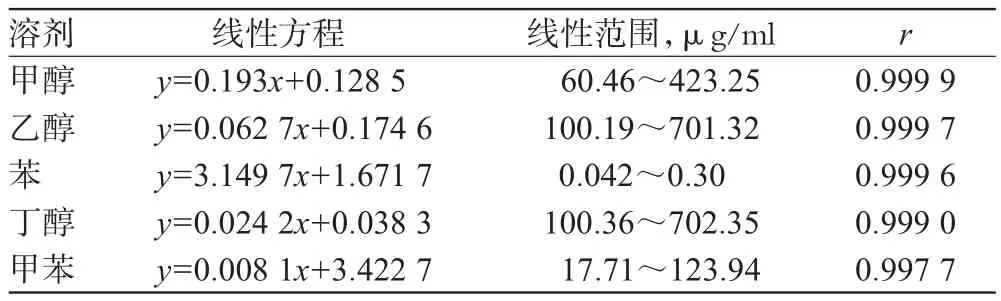
表1 各溶剂线性关系Tab 1 Linear relationship of each solvents
2.5 精密度试验
精密量取对照品混合溶液5ml,置于20ml顶空瓶中,共6份,密封;进样分析,计算甲醇、乙醇、苯、丁醇、甲苯的峰面积的RSD值分别为4.59%、4.01%、3.49%、3.57%、4.01%,均小于10%,表明精密度良好。
2.6 回收率试验
取样品约0.5g,精密称定,置于20ml顶空瓶中,共9份;分别精密量取对照品混合贮备液0.8、1.0、1.2ml,各3份,置于10ml量瓶中,再用0.25mol/L硫酸溶液稀释至刻度,摇匀。分别精密量取9份溶液各5ml,分别置于上述20ml顶空瓶中,密封,分析、测定。结果表明,测定方法准确可靠,详见表2。
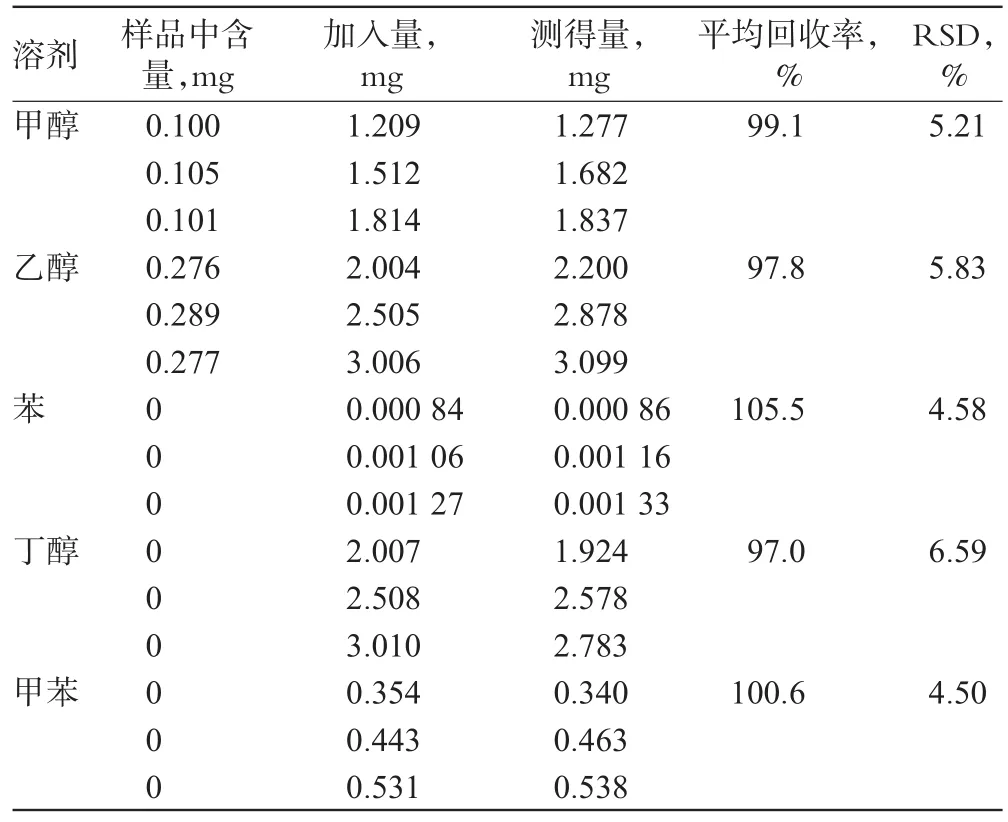
表2 回收率试验结果(n=3)Tab 2Results of recovery tests(n=3)
2.7 稳定性试验
精密量取对照品混合溶液5ml,分别置于20ml顶空瓶中,密封,于室温下放置0、1、4、8、12h,进样分析,记录色谱图。结果,甲醇、乙醇、苯、丁醇、甲苯在12h测定的峰面积的RSD分别为1.43%、1.36%、3.29%、1.21%、2.69%,表明溶液均在12h内稳定。
2.8 定量限试验
取对照品混合溶液逐步稀释,然后顶空进样,以峰高为基线噪声的10倍计算,结果甲醇、乙醇、苯、丁醇、甲苯的定量限分别为0.5、0.5、0.02、0.08、0.5μg/ml。
2.9 耐用性试验
将对照品混合溶液按照改变柱温起始温度(±5℃)、载气柱流速(±1.0ml/min),分别顶空进样分析,记录色谱图,分别考察甲醇、乙醇、苯、丁醇、甲苯在不同条件下的分离度。结果表明分离度均符合方法学要求,耐用性良好。
2.10 样品有机溶剂残留量测定及限度的确定
取3批样品制备成供试品溶液,按外标法计算5种有机溶剂的含量。结果3批样品中甲醇的残留量均为0.02%,乙醇的残留量均为0.05%,苯、丁醇、甲苯均未检出。
根据ICH指导原则和2010年版《中国药典》(二部)残留溶剂限度和样品的实测结果,将甲醇、乙醇、苯、丁醇、甲苯的检查均纳入质量标准之中,限度分别为0.3%、0.5%、0.0002%、0.5%、0.089%。
3 讨论
3.1 进样方法的选择
笔者根据残留溶剂测定的推荐方法,首选毛细管色谱柱-顶空进样系统,首先因为顶空分析法操作简单,只取气相部分进行分析,因此大大减少了样品基质对分析的干扰;其次,顶空分析有不同模式,可以通过优化操作参数而适合于各种样品;第三,顶空分析的灵敏度能满足方法学的要求;最后,顶空气相色谱完全能够进行准确的定量分析。
3.2 介质的选择
因为福尔可定略溶于水,为了使样品完全溶解,笔者选用了无挥发性的硫酸溶液为介质(顶空进样中不能使用挥发性的酸,对色谱柱有损害);并且对硫酸溶液的浓度进行筛选,确定最低浓度为0.25mol/L。
3.3 色谱柱的选择
笔者先后考察了HP-5、FFAP、DB-624等不同极性的色谱柱,结果以在DB-624色谱柱上的峰形和分离度最佳,因此最终选择DB-624色谱柱作为本次试验的色谱柱。
3.4 顶空温度的选择
参照2010年版《中国药典》(二部)附录ⅧP残留溶剂测定法项下内容[2],并参考ICH指导原则,考察了不同的顶空平衡温度对样品测定的影响,结果详见表3。
表3结果表明,随着温度的升高,苯和甲苯的峰面积减少,甲醇、乙醇、丁醇峰面积则增大。为了提高检测灵敏度,同时考虑到甲苯的响应值过大也会影响到检测的准确性,因此选择85℃作为顶空平衡温度。

表3 平衡温度考察结果Tab 3 Results of equilibrium temperature inspection
[1] 陈新谦,金有豫,汤光.新编药物学[M].17版.北京:人民卫生出版社,2007:427.
[2] 国家药典委员会.中华人民共和国药典:二部[S].2010年版.北京:中国医药科技出版社,2010:1092、附录61-65.
[3] 周海钧.药品注册的国际技术要求:质量部分[M].北京:人民卫生出版社,2007:126.
[4] 陈宁,陈朝艳.顶空气相色谱法测定头孢替坦二钠中的残留溶剂[J].中国抗生素杂志,2010,36(11):849.
