缬沙坦和阿托伐他汀治疗高血压合并持续性心房颤动疗效研究
2013-08-22吴建国河源市源城区人民医院内科广东河源517000
吴建国(河源市源城区人民医院内科,广东河源 517000)
持续性心房颤动是常见到心律失常之一,随着心房肌重构,有可能发展至永久性心房颤动,且患者年龄越大,其危害性越强。高血压是引起心房颤动的最常见原因。高血压合并持续性心房颤动主要依赖于药物治疗。本研究比较了缬沙坦联合阿托伐他汀与单独服用阿托伐他汀对高血压合并持续性心房颤动的疗效,结果报道如下。
1 资料与方法
1.1 一般资料 本院2010年1月至2012年10月收治的高血压合并持续性心房颤动患者108例,男66例、女42例,年龄49~81岁,平均65.43岁,符合高血压(收缩压不低于140mm Hg,舒张压不低于90mm Hg)及持续性房颤(发病时间超过1周,发病时伴随心悸气短、胸闷、眩晕、出汗等症状)诊断标准[1],排除甲状腺功能亢进、原发性及风湿性心脏病、肿瘤、呼吸道及消化道急性炎症、血液病等疾病患者。108例患者随机分为治疗组54例和对照组54例,年龄、性别、体质量、病程、左心房内径(LAD)组间比较差异无统计学意义(P>0.05)。
1.2 方法 治疗组采用口服缬沙坦联合阿托伐他汀治疗,缬沙坦(瑞氏诺华)80mg/d,阿托伐他汀(美国辉瑞)第1周600 mg/d,第2周400mg/d,第3周开始维持200mg/d。对照组只采用阿托伐他汀治疗,用法及用量同治疗组。每个月随访患者2次,有心房复颤临床表现时进行心电图/动态心电图检测以确诊是否发生心房复颤。在入院及治疗第6、12、18个月分别进行LAD检测、超敏C反应蛋白(hs-CRP)及肾功能、血脂、心电图等检测。
1.3 统计学处理 采用SPSS16.0软件进行数据分析;计量资料±s表示,组间比较采用t检验;显著性检验水准为α=0.05,P<0.05为比较差异有统计学意义。
2 结 果
治疗前各指标组间比较差异无统计学意义(P>0.05)。第18个月治疗组及对照组患者血压均恢复至正常范围,且组间比较差异无统计学意义(P>0.05),但三酰甘油(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、hs-CRP、LAD、左室质量指数(LVMI)组间比较差异均有统计学意义(P<0.05)。见表1。
表1 治疗前后各指标检测结果比较(±s,n=54)
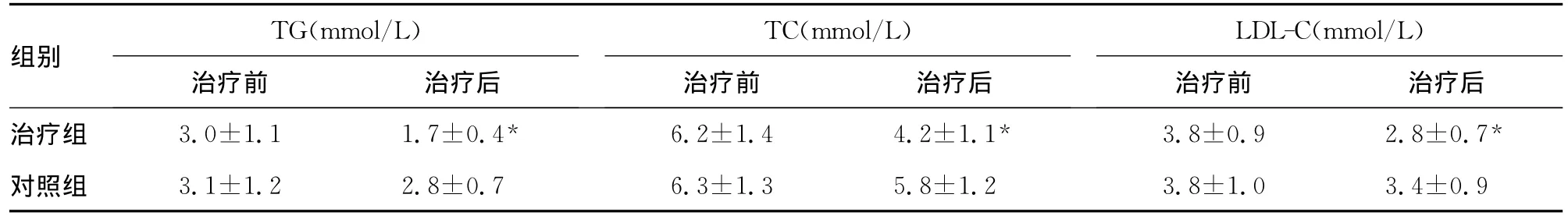
表1 治疗前后各指标检测结果比较(±s,n=54)
TG(mmol/L)TC(mmol/L)LDL-C(mmol/L)组别治疗前 治疗后治疗组 3.0±1.1 1.7±0.4* 6.2±1.4 4.2±1.1* 3.8±0.9 2.8±0.7治疗前 治疗后 治疗前 治疗后*对照组 3.1±1.2 2.8±0.7 6.3±1.3 5.8±1.2 3.8±1.0 3.4±0.9
续表1 治疗前后各指标检测结果比较(±s,n=54)

续表1 治疗前后各指标检测结果比较(±s,n=54)
注:与对照组比较,*P<0.05。
LAD(cm)hs-CRP(mg/L)LVMI(g/m2)组别治疗前 治疗后治疗组 4.6±0.5 2.9±0.4* 11.3±0.8 3.5±0.4* 116.5±1.9 82.6±1.3治疗前 治疗后 治疗前 治疗后*对照组 4.5±0.6 4.3±0.6 11.4±0.5 8.9±0.5 115.8±1.6 107.7±1.5
3 讨 论
高血压所致心房颤动已成为常见心律失常类型之一。高血压患者动脉压不断升高,导致左心室内径粗大并且肥厚,心肌间质内的纤维和二尖瓣乳头肌增生,室间隔增厚,腱索松弛,使左心室舒张力减弱,左心房容积扩大,心肌纤维化,进而导致左心房重构[2]。与此同时,高血压也可引起左心室肥厚,使左心室的顺应性降低,并导致左心房压力升高,使心房肌的多数小动脉管腔内膜增厚而导致狭窄或完全闭塞,局部心肌发生缺血变性及纤维化。发生于小动脉的病变在心房肌中形成大量缺乏应激功能的小岛,进而为阵发性房颤的发生提供了心房电活动不一致的病理基础[3]。另一方面,在上述病理因素的作用下,心房肌电活动的非均质性程度进一步加重,导致心房的除极速度减慢,而不同部位心房的自律性和兴奋性的差异进一步增大,使不同部位心房电活动的空间向量及弥散度出现显著差异。上述因素共同构成了高血压发颤的基础。高血压合并房颤患者外周血内皮素水平的升高,则可能与房颤导致血流动力学异常,即心房肌收缩功能减弱、出现不规则心室律、血管壁应力性异常及局部心肌组织缺血、缺氧有关[4]。
高血压之所以能够诱发心房颤动,与多种因素有关。高血压可导致心房结构及生物信号传导的重构,进而导致心房颤动的发生,其中与炎症及氧化应激等不良刺激的关系较为显著[5-6]。此外,高血压导致心房颤动,可能也与血管内皮功能损伤有关。缬沙坦属于选择性血管紧张素Ⅱ受体拮抗剂,可抑制血管紧张素Ⅱ和AT1受体结合,进而阻止由其导致的心脏血管收缩。缬沙坦对高血压的治疗效果好,耐受性高且不良反应小。Skalidis等[7]发现心房对NO的生物利用不足、心肌NO合成酶表达量下降与心房颤动关系紧密。他汀类药物具有恢复血管内皮功能的作用,而氧化应激和炎症可导致心房重构及心肌电生理紊乱,使心房扩张、有效不应期缩短,最终形成心房颤动[8-9]。
本研究证实缬沙坦联合阿托伐他汀治疗高血压合并持续性心房颤动,可有效降低患者TG、TC、LDL-C、hs-CRP、LAD和LVMI等指标的水平,说明缬沙坦联合阿托伐他汀可能是高血压合并持续性心房颤动的有效治疗方法。
[1]刘力生,王文,姚崇华.2009年基层版《中国高血压防治指南》(摘录)[J].柳州医学,2011,4(2):104-117.
[2]戚文航.血管紧张素受体拮抗剂与心房颤动[J].中华心血管病杂志,2004,32(11):1042-1043.
[3]Blender S,Gerstenfeld EP,Lin D,et al.Ablation of atrial fibrillation:localizing triggers,mapping systems and ablation techeniques[J].Minerva Cardioangiol,2004,52(2):95-109.
[4]Gosselink ATM,Smith AJ,Crijn CJ,et al.Alteration of peripheral vasodilatory reservecapacity after cardioversion of atrial fibrilation[J].Eur Heart J,1996,17(8):926-934.
[5]van Wagoner DR.Oxidative stress and inflammation in atrial fibrillation:rold in pathogenesis and potential as a therapeutic target[J].J Cardiovasc Pharmacol,2008,52(4):306-313.
[6]Kourliouros A,Savelieva I,Kiotsekoglou A,et al.Current concepts in the pathogenesis of atrial fibrillation[J].Am Heart J,2009,157(2):243-252.
[7]Skalidis EI,Zacharis EA,Tsetis DK,et al.Endothelial cell function during atrial fibrillation and after restoration of sinus rhythm[J].Am J Cardiol,2007,99(9):1258-1262.
[8]Guazzi M,Berti M,Belletti S,et al.Exercise metaboreflex activation and endothelial function impairment in atrial fibrillation[J].Am J Physiol Heart Circ Physiol,2006,291(5):2396-2402.
[9]Adam O,Neuberger HR,Bohm M,et al.Prevention of atrial fibrillation with 3-hydroxy-3-methylglutaryl coenzyme A reductase inhibitors[J].Circulation,2008,118(12):1285-1293.
