UFLC-MS/MS法测定氨茶碱制剂中的氨茶碱含量Δ
2013-08-10张娟红王荣谢华贾正平李文斌谢希晖兰州军区兰州总医院全军高原损伤防治重点实验室兰州730050兰州大学药学院兰州730050
张娟红,王荣,谢华,贾正平,,李文斌,谢希晖,(.兰州军区兰州总医院全军高原损伤防治重点实验室,兰州 730050;.兰州大学药学院,兰州 730050)
氨茶碱为茶碱和乙二胺的复合物,主要用于支气管哮喘和喘息性支气管炎,与受体激动药合用可提高疗效。虽然许多新的抗哮喘药物不断涌现,但是氨茶碱仍是当今最广泛使用的抗哮喘药物之一。其还可用于治疗急性心功能不全和心源性哮喘、胆绞痛[1-2],近年来还发现氨茶碱对急性缺氧动物吸氧后再缺氧损伤有预防作用[3]。
目前,氨茶碱含量测定方法主要有高效液相色谱(HPLC)法[4-5]、毛细管电泳(CE)法[6]、拉曼光谱法[7]等。《中国药典》2010年版[8]收载了氨茶碱片剂、注射剂及缓释片的含量测定方法为紫外分光光度(UV)法,但此方法存在分析时间长、灵敏度低、辅料干扰多等缺点。随着液相色谱质谱联用技术的逐步推广,建立氨茶碱不同剂型超快速液相色谱串联质谱联用(UFLC-MS/MS)法用于其质量控制有着重要的意义。本试验通过优化色谱和质谱条件建立了测定氨茶碱制剂含量的UFLC-MS/MS法,该方法缩短了分析时间,大大提高了分析工作效率,尤其可能适用于微量样品的分析,比如可用于药动学的研究。
1 材料
UFLC仪(日本岛津公司);API 3200三重四极杆串联质谱仪(美国AB公司);高速离心机(上海安亭科学仪器厂);超声波清洗器(奥特赛恩斯仪器有限公司);涡旋混匀器(金坛市金城教学仪器厂)。
氨茶碱标准品(中国食品药品检定研究院,批号:0844-9802,纯度:供含量测定用);氨茶碱片(山西云鹏制药有限公司,批号:B110101、A100302、A101002,规格:每片0.1 g);氨茶碱注射液(上海现代哈森药业有限公司,批号:10091612,规格:2 ml∶0.25 g;山西晋新双鹤药业有限公司,批号:1005161,规格:2 ml∶0.25 g;常州兰陵制药有限公司,批号:1010202,规格:10 ml∶0.25 g;河南润弘制药股份有限公司,批号:1011231,规格:2 ml∶0.25 g);乙腈、甲醇、甲酸均为色谱纯,水为灭菌注射用水。
2 方法与结果
2.1 色谱、质谱条件的建立
色谱柱:Shim-pack XR-ODS(75 mm×3.0 mm,2.0 μm);流动相:乙腈-0.4%甲酸水溶液(54∶46,V/V),流速:0.40 ml/min;柱温:25 ℃;进样量:10 μl;整个分析流程用时3 min。
质谱采用电喷雾离子源(ESI)正离子多反应(MRM)方式检测;氨茶碱在ESI源正离子电离方式下,有较好的质谱响应,主要生成[M+H]+离子峰,为m/z181.0;喷雾电压(IS):4 500 V;雾化温度(TEM):450℃;氨茶碱检测离子对m/z181.0→124.0;碰撞诱导解离电压(DP):35 psi;碰撞能量(CE):25 psi。选择性对[M+H]+离子进行碎片质谱分析得相应的二级扫描质谱图,见图1。
2.2 方法的专属性
在“2.1”项色谱条件下,分别取空白溶液(流动相)、“2.3”项下标准品溶液与供试品溶液(片剂,批号:B110101)进样测定,得到特征峰。结果,氨茶碱保留时间附近未见杂质峰,说明辅料对测定无干扰,详见图2。

图1 氨茶碱扫描质谱图A.母离子;B.碎片离子Fig1 MS/MS spectra of aminophyllineA.parent ion;B.fragment ion
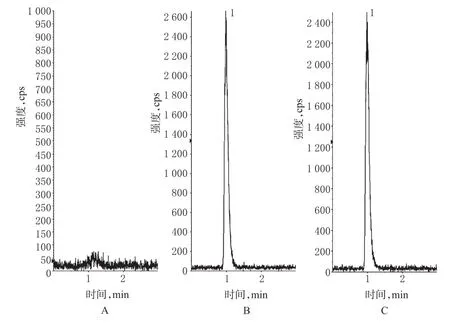
图2 超快速液相色谱串联质谱图A.空白溶液;B.标准品溶液;C.供试品溶液;1.氨茶碱Fig 2UFLC-MS/MS chromatogramsA.blank solution;B.standard solution;C.test sample solution;1.aminophylline
2.3 溶液的制备
标准品溶液:精密称取氨茶碱标准品0.002 0 g于10 ml量瓶中,加入灭菌注射用水溶解并定容,得质量浓度为200 μg/ml氨茶碱标准溶液作为贮备液;将贮备液依次用流动相稀释成质量浓度为0.25、0.5、1.0、2.5、5.0、10.0、25.0、50.0、100.0 ng/ml的系列标准品溶液。
供试品溶液:取氨茶碱片20片,精密称定,研细。精密称取适量(约相当于氨茶碱50 mg),置于200 ml量瓶中,加0.1 mol/L氢氧化钠溶液10 ml与水30 ml,振摇10 min使氨茶碱溶解,用水稀释至刻度,摇匀,滤过。精密吸取续滤液20 μl,置于100 ml量瓶中,用流动相稀释至刻度,摇匀,即得。
精密量取氨茶碱注射液适量,用0.1 mol/L氢氧化钠溶液定量稀释制成每1 ml中约含氨茶碱100 μg的溶液。精密吸取溶液50 μl,置于100 ml量瓶中,用甲醇稀释至刻度,摇匀,即得供试品溶液。
供试品溶液进样前于10 000 r/min离心3 min,吸取上清液于进样瓶中待测。
2.4 标准曲线的制备
取“2.3”项下氨茶碱系列标准品溶液进样分析,以质量浓度(X)为横坐标、峰面积(Y)为纵坐标进行线性回归,得方程Y=353X+1.1×103(r=0.999 8),权重:1/x2。结果表明,氨茶碱检测质量浓度线性范围为0.25~100 ng/ml,最低定量限为0.25 ng/ml。
2.5 精密度试验
取一定量的氨茶碱标准品贮备液用甲醇稀释成质量浓度为0.3、50、85 ng/ml的质量控制(QC)样品各5份,进样分析,计算得日内RSD分别为2.45%、1.85%、0.90%;取上述浓度的QC样品连续测定3 d,得日间RSD分别为2.84%、1.91%、1.13%。RSD均≤2.84%,符合制剂分析的方法学要求。
2.6 重复性试验
精密称取同一批氨茶碱片5份,按“2.3”项下方法平行制备5份供试品溶液,进样分析,结果含量的RSD=1.11%,表明本方法有较好的重复性。
2.7 回收率试验
取已知含量的氨茶碱供试品溶液(片剂,批号:B110101)0.5 ml共5份,分别加入100 ng/ml的氨茶碱标准品溶液10、25、50、100、200、500 μl,涡旋混匀后进样分析,计算回收率。结果氨茶碱回收率分别为99.10%、99.50%、99.29%、100.29%、99.66%、100.64%,平均值为99.75%,符合要求。
2.8 稳定性试验
取同一份供试品溶液,分别于制备后0、6、24 h后依法测定,结果,峰面积的RSD=1.67%,表明供试品溶液于室温下放置24 h稳定。
2.9 2种氨茶碱制剂含量测定结果
按“2.3”项下方法制备不同批号氨茶碱供试品溶液,进样分析。结果不同厂家的药品含量测定结果均符合《中国药典》要求,但不同剂型的氨茶碱含量有一定差异,详见表1。

表1 7批氨茶碱制剂含量测定结果(n=3)Tab1 Content determination of aminophylline in 7 batches ofAminophylline preparation(n=3)
3 讨论
3.1 色谱条件的选择
本试验前期考察了流动相中不同体积分数(0.2%、0.3%、0.4%)的甲酸水溶液对氨茶碱检测的影响,发现当甲酸体积分数为0.4%时,氨茶碱峰形、响应值和分析时间均较好,所以选择以乙腈-0.4%甲酸水溶液(54∶46,V/V)为流动相,同时检测限更低。
3.2 质谱条件的选择
选用1 μg/ml氨茶碱标准品溶液进行质谱条件的选择,以ESI+作为电离模式,氨茶碱有较好的质谱响应,且分别对IS、DP、TEM、CE等质谱参数进行了优化,使得质谱扫描达到最佳,以便检测,最终确立了“2.1”项下的各项质谱条件为最优。
虽然已有报道采用HPLC法、UV法测定氨茶碱制剂含量的方法,但目前尚未见采用UFLC-MS/MS法测定氨茶碱制剂含量的文献报道。本试验方法具有简单可靠、准确灵敏、快速高效的优点,并且重复性好,辅料未见干扰。
研究结果发现,不同剂型的氨茶碱含量有一定差异,故建立氨茶碱质量控制的UFLC-MS/MS方法具有重要意义,本方法氨茶碱定量限为0.25 ng/ml,适用于少量样品及生物样品的分析,与已有报道的HPLC法、UV法相比,本方法更加灵敏、准确、专属性好,减少了操作误差,且取样量少,适用于氨茶碱制剂的含量测定,同时也可能适用于血样等生物样品的分析。
[1]陈新谦,金有豫,汤光.新编药物学[M].17版.北京:人民卫生出版社,2011:446.
[2]陈怡禄,邓力,吕回,等.婴儿氨茶碱急性中毒的临床诊断治疗及药物代谢动力学[J].中国临床药理学杂志,2002,18(2):145.
[3]牟信兵,廖国云,高钰琪,等.速尿和氨茶碱对小猪再缺氧损伤的预防效果[J].中华航空航天医学杂志,2004,15(3):137.
[4]黄跃生,刘志松,吕荷,等.高效液相色谱法测定复方茶碱片中主要成分的含量[J].药物分析杂志,1992,12(1):28.
[5]Yin C,Tang C,Wu X.HPLC determination of aminophylline,methoxyphenamine hydrochloride,noscapine and chlorphenamine maleate in compound dosage forms with an aqueous-organic mobile phase[J].J Pharm Biomed Anal,2003,33(1):39.
[6]Chen G,Chu Q,Zhang L,et al.Separation of six purine bases by capillary electrophoresis with electrochemical detection[J].Analytica Chimica Acta,2002,457(2):225.
[7]Mazurek S,Szostak R.Quantitative determination of diclofenac sodium and aminophylline in injection solutions by FT-Raman spectroscopy[J].J Pharm Biomed Anal,2006,40(5):1 235.
[8]国家药典委员会.中华人民共和国药典:二部[S].2010年版.北京:中国医药科技出版社,2010:836-837.
