高铁酸钾的制备工艺研究与表征
2013-08-08刘汝锋刘婷灵尚小琴钟建明何柳红邓炳财李淑妍
刘汝锋,刘婷灵,尚小琴,钟建明,何柳红,邓炳财,李淑妍
(广州大学化学化工学院,广东 广州 510006)
高铁酸钾凭借其超强的氧化能力和絮凝、脱色、除臭、杀菌等特性,以及在反应过程中不会产生二次污染和其它有毒副产物等环境友好特征,在水处理方面已显示出其特有的优势,被广泛应用于水处理领域[1-5]。作为一种新型绿色高效的水处理剂,高铁酸钾不仅可以去除水中的有机和无机污染物,特别是对一些难降解的有机污染物处理效果更为显著,而且其还原产物Fe3+还具有良好的吸附和絮凝效果,通过高铁酸钾的絮凝处理,可去除水中的固体悬浮物。随着高铁酸钾研究的不断深入,近年来其在污泥脱水除臭处理中的作用也越来越被关注[6-7],利用高铁酸钾的强氧化性,可氧化降解污泥中的H2S、CH3SH和NH3等恶臭、有毒物质,分解污泥中的胞外多聚物和破坏污泥细胞的刚性结构,从而有效地提高污泥的脱水除臭性及微生物的利用率。
高铁酸钾的制备方法通常有高温氧化法、电解法和次氯酸钠法,其中以次氯酸钠法最为常用。本文作者以次氯酸钙为主要原料替代传统方法中的次氯酸钠制备高铁酸钾,考察次氯酸钙制备高铁酸钾反应过程中的影响因素,探讨获取高产率高铁酸钾的合成工艺。与传统的次氯酸钠法比较,本工艺可以充分利用次氯酸钙氯含量高的特点,制备过程中不需要加入氯气,可有效提高合成过程的安全性和操作的可控性,同时可简化次氯酸钙工艺流程,缩短反应时间,提高产率和产品纯度。
1 实验部分
1.1 试剂及仪器
氢氧化钾、次氯酸钙、九水硝酸铁、正戊烷,分析纯,天津市福晨化学试剂厂;异丙醇、乙醚,分析纯,天津市百世化工有限公司。数显可调速电子搅拌器,HJ-3 型,河南巩义市予华仪器有限责任公司;真空干燥箱,DZF-6-6000,上海一恒科技有限公司;紫外分光光度计,TU-2820,北京普希通用;红外分光光度仪,SDTQ600,天津天光光学仪器有限公司。
1.2 高铁酸钾的制备
配制一定量的饱和氢氧化钾溶液,冷却后加入盛有次氯酸钙粉末的三口烧瓶中,搅拌混合均匀后静置10 min,缓慢滴加九水硝酸铁溶液,搅拌反应一定时间,控制反应温度不高于35℃,反应结束后用玻璃砂芯漏斗抽滤,得到粗产品。用3 mol/L的KOH 溶液溶解粗产品、抽滤、洗涤,除去不溶性杂质,加入一定浓度的KOH 溶液,冰水浴中搅拌重结晶,抽滤、洗涤、真空干燥,得高铁酸钾样品。
1.3 产率和纯度的测定
称取高铁酸钾产品重量和计算理论产量,按式(1)计算产率Y(%)。

式中,w、w0分别为高铁酸钾实际产量和高铁酸钾理论产量。
按Fe2+-phen 分光光度法测定高铁酸钾的纯度。
1.4 傅里叶红外光谱表征
采用KBr 压片法,KBr 与产物比例为100∶1,在红外灯照射下置于玛瑙研钵中研磨2~3 min,使其充分混合,并在10 MPa的压力下进行压片。将样品放置于红外光谱仪内,扫描绘出红外光谱图。
2 结果与讨论
2.1 反应时间对高铁酸钾产率的影响
控制反应温度为25℃,次氯酸钙过量20%,冰水浴的条件下重结晶,考察不同反应时间t对高铁酸钾产率Y的影响,实验结果如图1所示。从图1 可知,反应初期产率随反应时间的增加快速提高,40 min时达到最大值,随后产率随时间的增加逐渐降低。出现折点的原因是因为高铁酸钾化学性质不稳定,在水溶液中发生分解等所致,所以最佳反应时间40 min为宜。
2.2 反应温度对高铁酸钾产率的影响
反应时间为40 min,其它条件与2.1 节相同,改变反应温度(T),考察反应温度对高铁酸钾产率的影响,结果如图2所示。由图2 可知,当反应温度低于25℃时,反应产率随温度的升高而增大,25℃时达到最大值;但当温度高于25℃,反应产率随温度的升高反而快速下降。根据反应动力学,反应温度较低时反应速度较小,反应所需的时间增长,所以适当提高温度有利于高铁酸钾的合成;但是温度过高次氯酸钾容易分解,次氯酸根的降低致使Fe3+不能完全转化成,产生其它的副产物,加速了高铁酸钾的分解。所以反应温度应控制在20~25℃。
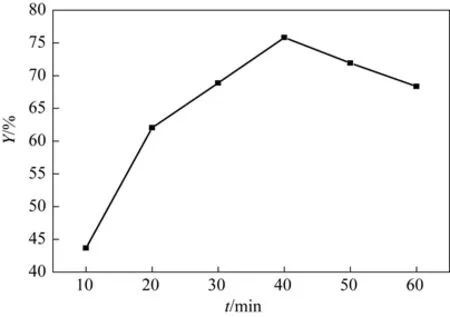
图1 反应时间对产率的影响
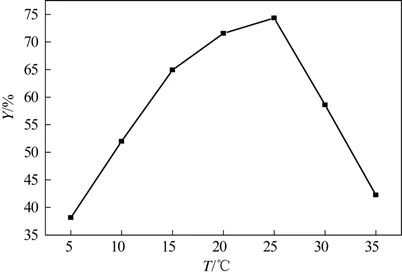
图2 反应温度对产率的影响
2.3 次氯酸钙用量对高铁酸钾产率的影响
在相同的反应条件下改变次氯酸钙的用量,考察次氯酸钙用量对高铁酸钾产率的影响,实验结果如图3所示。由图3 可知,在一定范围内,高铁酸钾的产率随次氯酸钙用量的增大而增大,当次氯酸钙用量与理论用量的质量比(M)为1.2∶1时产率达到极大值,继续增加次氯酸钙用量高铁酸钾的产率反而降低。因为当高铁酸钾用量过大时,体系中的ClO-会发生自分解反应,其浓度越高分解速度越快,分解产生的Cl-可加速高铁酸钾的分解,从而导致产率的降低,故次氯酸钙用量与理论用量的质量比为1.2∶1时最佳。
2.4 重结晶的碱度对产率和纯度的影响
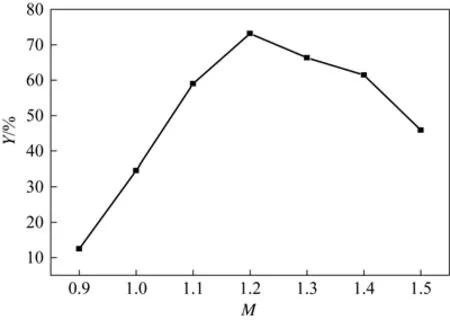
图3 Ca(ClO)2用量对产率的影响

图4 重结晶时KOH 浓度对产率和纯度的影响
重结晶时KOH的碱度对产率和纯度的影响结果如图4所示。由图4 可知,高铁酸钾的产率随碱度的升高而升高,但碱度升高到11 mol/L 后产物的纯度有所下降,这是因为碱性越强,高铁酸钾的溶解度越低,析出的量越多,所以产率随之升高;但浓度过高,杂质析出机会增加,导致高铁酸钾的纯度降低。综合考虑碱度对纯度和产率的影响,故确定重结晶时KOH的浓度(C碱)为11 mol/L 最佳。
2.5 重结晶的温度对产率的影响
重结晶温度(T重)是影响产率的重要因素,重结晶温度对高铁酸钾产率的影响结果如图5所示。实验结果表明,重结晶的温度越低,高铁酸钾析出量越多,产率越高。因为高铁酸钾的溶解度随温度的降低而降低,因此温度越低,高铁酸钾析出的速度越快,产率也越高。低于0℃时,高铁酸钾析出量的变化不大,综合方便操作等因素,重结晶在0℃(冰水浴)的条件下进行为宜。
2.6 FT-IR 分析
采用红外光谱对高铁酸钾产品进行了分析和表征,其FT-IR 谱图如图6所示。在823 cm-1左右出现了宽而强的特征吸收峰,在781 cm-1处有一肩峰,为高铁酸钾Fe—O键v3(F2)伸缩振动的特征吸收峰;在1130 cm-1、1113 cm-1处出现两个微弱的伸缩振动峰,为Fe—O键v1(Al)+v2(F2)的伸缩振动特征吸收峰;在1383 cm-1左右还有一个衍射峰,这可能是Fe—O键v3(F2)+v4(F2)的振动频率的吸收波数,由分析结果可以证明该合成产物为高铁酸钾晶体。
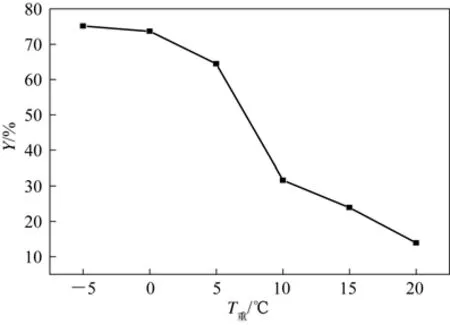
图5 重结晶温度对产率的影响

图6 高铁酸钾产物红外图谱
3 结论
以次氯酸钙为主要原料替代次氯酸钠可制得高铁酸钾,产品产率可达75%以上,反应时间、反应温度、次氯酸钙用量、重结晶温度和碱度是影响高铁酸钾产率的主要因素。合成高铁酸钾的最佳工艺条件为:反应温度25℃,反应时间40 min,次氯酸钙用量与理论用量的质量比为1.2∶1,重结晶碱度和温度分别为11 mol/L和0℃;红外光谱表征显示合成产物为高铁酸钾。
[1]Jiang J Q,Lloyd B.Progress in the development and use of ferrate(Ⅵ) salt as an oxidant and coagulant for water and wastewater treatment[J].Water Research,2002,36(6):1397-1408.
[2]阚连宝,段庆茹,王宝辉,等.Fe(Ⅵ)的特性分析及在水处理中的应用[J].化工进展,2011,30(8):1848-1853.
[3]张春玲,朱琨,蒋煜峰.高铁酸钾的制备及其在水处理中的应用前景[J].环境科学与管理,2010,35(6):75-79.
[4]崔建国,刘幼琼,李娜.高铁酸钾同时降解微污染水中苯酚和Cr(Ⅵ)的研究[J].中国环境科学,2011,31(9):1461-1465.
[5]陈武,彭友新.高铁酸钾的制备及应用研究进展[J].无机盐工业,2009,41(5):9-11
[6]冀海壮,叶芬霞.高铁酸钾预处理对活性污泥脱水性能的影响[J].环境工程学报,2012,6(8):2837-2840
[7]苗宗成,王蕾,张永明,等.高铁酸钾对COD 去除作用的机理研究[J].工业水处理,2011,31(8):32-34.
