固相微萃取-气相色谱-质谱及气相色谱-嗅闻技术分析美味牛肝菌风味活性物质
2013-08-07齐玉刚张春霞刘安军王丽霞宋晓娣
曹 蓓,齐玉刚,张春霞,刘安军,王丽霞,郑 捷,白 云,宋晓娣
(天津科技大学食品工程与生物技术学院,天津300457)
美味牛肝菌(Boletus edulis)俗称大脚菇,属层菌纲,伞菌目,牛肝菌科,牛肝菌属,子实体粘软多汁,香滑可口,富含蛋白质维生素多糖类物质氨基酸和多种矿物元素,其提取物具有增强免疫力抗癌抗辐射等功能[1]。除营养和药用外,可食用牛肝菌的的风味也引人关注,其所特有的风味异于芳香植物和其他菌类食品。近年来,随着生活水平的提高和消费观念的转变,人们在追求摄入食品营养的同时,对食品风味的追求日益增加。对于美味牛肝菌风味成分的研究,对于阐明其呈味机理并且为开发新一代调味品奠定理论基础,具有深远的现实意义。目前,有关牛肝菌营养成分的研究较多[2-5],而对于其挥发性成分研究较少。顶空固相微萃取(HS-SPME)方法是把取样、萃取、富集、进样等过程在同一个装置完成。与其他分离方法相比,此方法选择性好,不需要溶剂,所需样品用量少,且操作简单、快速、费用低,并可与气相色谱或液相色谱直接联用[6]。气相色谱-嗅觉测量法(GC-O)是近年来发展起来的鉴定食品风味活性物质的技术手段,这种方法弥补了气相色谱-质谱联用技术(GC-MS)不能检测到一些阈值很低的痕量风味物质的缺陷。本实验以美味牛肝菌为原料,通过HS-SPME技术萃取样品中的挥发性成分,并将GCMS与GC-O方法结合起来,对样品中的挥发性成分进行定性、定量及风味活性成分分析,为牛肝菌调味品的开发提供一定的理论基础。
1 材料与方法
1.1 材料与仪器
美味牛肝菌干品 购于昆明农贸市场,将样品粉碎,过40目筛;C6~C20正构烷烃标准品 德国Sigma公司。
4000MS气相色谱-质谱联用仪 美国瓦里安Varian 技术有限公司;Sniffer 系列嗅觉计 瑞士Brechbuhler公司;手动固相微萃取进样器、65μm PDMS/DVB萃取头、15mL顶空进样瓶 美国Supelco公司;高速中药粉碎机 武义县屹立工具有限公司;电子分析天平 上海精天电子仪器有限公司;HH-8型数显恒温水浴锅 天津玻璃仪器厂。
1.2 实验方法
1.2.1 HS-SPME处理 称取样品粉末2.0g置于15mL顶空样品瓶中,用聚四氟乙烯衬里的硅橡胶垫密封,置于45℃水浴锅中平衡30min后,将经过老化处理的固相微萃取头通过瓶盖的橡皮垫插入到样品瓶中大约1cm处,推出纤维头。于45℃水浴中萃取30min后,将萃取头迅速插入GC-MS联用仪的进样口,于250℃下解析15min,同时启动仪器采集数据。
1.2.2 GC-MS分析条件 色谱条件:色谱柱型号为VF-5ms(30m×0.25mm×0.25μm),载气为高纯度氦气(99.999%),流速为1mL/min,进样口温度为250℃,进样时以分流方式进样。采用两段式程序升温:起始温度为40℃,保持3min,然后以4.0℃min升温至150℃,并保持1min,再以8℃/min升温至250℃,保持6min。
质谱条件:电离源为EI,离子阱温度为220℃,GC-MS传输线温度为280℃,EI电子能量为70eV,溶剂延迟时间1.5min。扫描方式为全扫描(fμμ),范围为43~500m/z。
1.2.3 定性分析 实验数据处理由Xaclbiur软件系统完成,未知化合物经计算机检索同时与NSIT05谱库(107k compounds)相匹配,仅当正反匹配度均大于800(最大值为1000)的鉴定结果才予以报道。采用相同的升温程序,以C6~C20的正构烷烃作为标准,以其保留时间计算样品测试中的化合物的保留指数,再通过查阅相关文献,与文献中的化合物的保留指数(RI)相比较,与质谱数据库检索结果共同定性。
化合物保留指数RI计算公式:

式中,RI样品—样品色谱峰的RI;RI前—样品色谱峰前面烷烃标样的RI;Rt样品—样品色谱峰的Rt;Rt前—前面烷烃标样的Rt;Rt后—后面烷烃标样的Rt;Rt—色谱峰的保留时间。
1.2.4 定量分析 通过Xaclbiur工作站数据处理系统,按峰面积归一化法进行定量分析,从而得出各化学成分在美味牛肝菌物质中的相对百分含量。
1.2.5 GC-O分析 样品前处理同样采用HS-SPME方法,同1.2.1;色谱条件和质谱条件同1.2.2;色谱柱与嗅闻口的分流比设置为1∶1。本实验选择5名有经验的感官评价员进行嗅觉分析,记录风味特征和强度。在实验过程中至少有3名感官评价员在同一嗅闻时间处能得到相同的感官描述,则将该记录记入最终结果,气味的强度以星号个数做记号。没有嗅闻到气味不计星号,“*”表示该化合物气味微弱,“**”表示该化合物气味中等,“***”表示该化合物气味强烈。统计5位感官评价员对记入最终结果的每种化合物所进行的星号标记,最后计算每种气味成分所得星号的平均值(四舍五入取整),作为该化合物气味强度的最终结果。实验过程中感官评价员轮流分析,以避免嗅觉疲劳。
2 结果与分析
2.1 美味牛肝菌的挥发性成分鉴定
美味牛肝菌挥发性成分的总离子流色谱图见图1。从图1可见,在此分析条件下得到的图谱分离度和定量准确度均较好。通过NSIT05谱库进行匹配度和图谱比较,初步确定样品中挥发性成分。同时,根据Kovats计算式,得到各未知物的RI实验测得值。然后在NSIT05谱库数据库以及相关网络数据库(www.webbook.nist.gov)、(www.odour.org.uk)和相关文献资料中检索各未知物的RI值,进行比较,进一步确认样品中的挥发性成分,见表1。其中,C6~C20正构烷烃标准品的保留时间与对应RI值的标准曲线如图2所示。
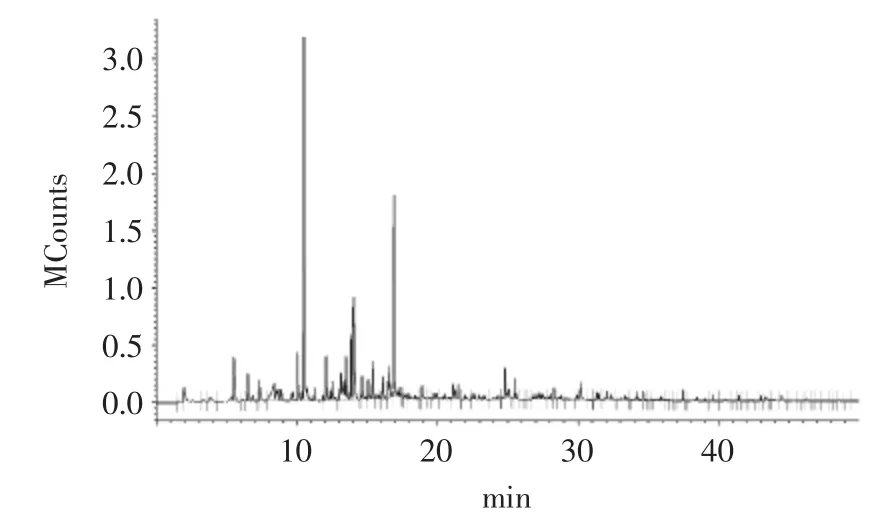
图1 美味牛肝菌挥发性成分GC-MS总离子流色谱图Fig.1 GC-MS total ion chromatogram of volatile components of Boletus edulis
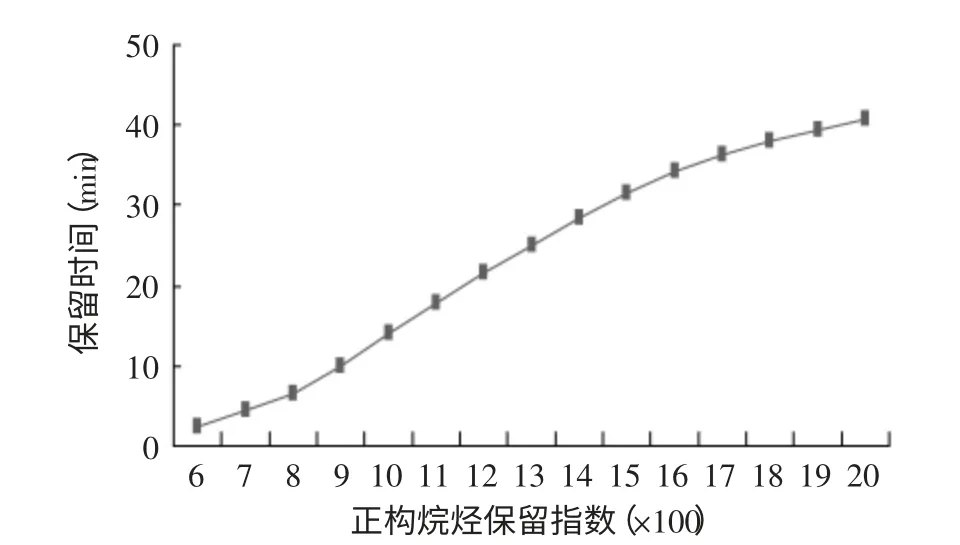
图2 C6~C20正构烷烃标准品的保留指数-保留时间图Fig.2 Retention index(RI)and retention time(RT)relations of C6~C20 hydrocarbon standard compounds
由表1中可知,从美味牛肝菌中分离鉴定得到53种挥发性化合物,主要由吡嗪类、烃类、醇类、酮类、醛类、酸类、酯类、含硫类、呋喃等化合物组成。其中含量最高的吡嗪类化合物有12 种,占总成分的58.87%;其次酸类化合物有4种,占总成分的5.15%;醛类化合物有5种,占总成分的4.73%;烃类化合物有
9种,占总成分的3.57%;酯类化合物有2种,占总成分的3.36%;醇类化合物有6种,占总成分的2.95%;酮类化合物有6种,占总物质的2.49%;同时,一些杂环及其他化合物含量也很高,如2-噻吩甲醛(10.50%)、2-正戊己呋喃(2.296%)、2-乙酰基吡咯(1.963%)等。在这53种挥发性成分中,相对含量较高的有2,6-二甲基吡嗪、3-乙基-2,5-二甲基吡嗪、2-噻吩甲醛、2-乙基-3-甲基吡嗪、2-乙基-6-甲基吡嗪、丙位戊内酯、己醛、2-戊基呋喃、甲酚、4-羟基-2-酮丁酸、1-辛烯-3-醇、2-乙酰基吡咯、异丙烯基吡嗪、2-十一酮、甲基吡嗪、苯甲醛、己酸、2,5-二甲基-3-异戊基吡嗪和柠檬烯。
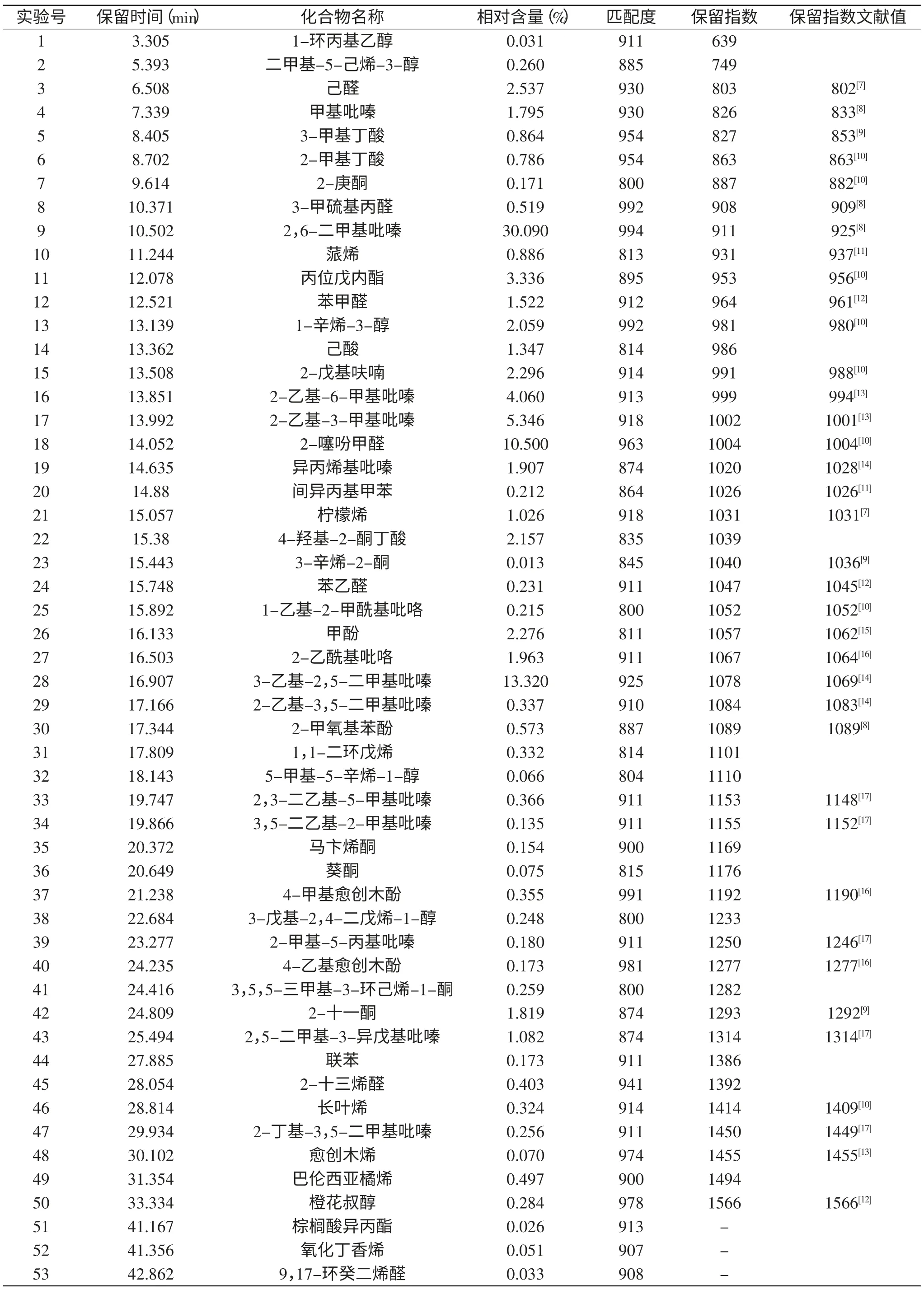
表1 牛肝菌挥发性成分的分析及鉴定结果Table 1 Analysis and identification of volatile components of Boletus
2.2 美味牛肝菌的特征性风味物质鉴定
仅通过各挥发性物质的相对含量不能确定美味牛肝菌的特征性挥发性化合物,还需要利用GC-O来鉴定对风味有贡献的物质,分析鉴定结果列于表2。
如表2所示,在53种已定性的美味牛肝菌挥发性成分中,有29种可被感官评价员嗅闻到,此外还有3种未知化合物呈现特殊气味,但是不能被GC-MS检测到,这是因为这些化合物阈值较低,且在样品中的含量极低,不能为质谱所鉴定。分析结果表明,美味牛肝菌的特征性风味主要以坚果香、烤肉香、蘑菇味、花香、烤面包香味等风味特征为主。这些风味主要由吡嗪类、醛类、醇类、酮类等化合物释放出来的。
吡嗪类化合物是美味牛肝菌中鉴定出来的种类最多、含量最丰富的挥发性化合物,且由于其阈值较低,普遍带有令人愉悦的坚果、烧烤等气味,对美味牛肝菌特征性风味的贡献很大。吡嗪类化合物是美味牛肝菌中的糖及其分解产物与氨基酸发生了美拉德反应的产物[18],样品中检测到大量这类化合物,可能是美味牛肝菌在干制过程中发生了美拉德反应。Thomas[19]在干制牛肝菌中也检测到了9种吡嗪类化合物,其中有4种与本实验检测到的一致。2-戊基呋喃也是阈值很低(4×10-9g/mL)的含氮杂环化合物,具有豆香、果香、泥土、青香及类似蔬菜的香韵[20],对美味牛肝菌的香气也有很大贡献。
醛类化合物也是美味牛肝菌香气的重要的成分,如样品中检测到的己醛、苯甲醛、苯乙醛等。这些醛类化合物主要是脂质的氧化或氨基酸的strecker降解生成的[21],一般阈值都较低,己醛的阈值为4.5×10-9g/mL[22],是中等分子质量的醛,具有清香、酯香风味,在样品中提供了青草香气。苯甲醛、苯乙醛属于芳香醛,由苯丙氨酸降解生成[23],具有令人愉悦的杏仁香和花香。酮类化合物的生成和醛类化合物类似,具有独特的清香和果香风味,且阈值较低[24],对美味牛肝菌的花香、果香风味有贡献。
醇类化合物多为脂质氧化或羰基化合物还原生成的,通常具有芳香、植物香、酸败和土腥味,因其自身的阈值对食品风味的贡献很小,但某些不饱和醇类却是食品香气的重要组成部分。1-辛烯-3-醇是八碳化合物的代表,八碳化合物对食用菌的风味有着直接的影响,这些短链的八碳化合物,是由不饱和脂肪酸,尤其以亚油酸和亚麻酸为主,经脂肪氧化酶催化转变而成的。1-辛烯-3-醇具有浓郁的蘑菇风味,素有“蘑菇醇”称号,它几乎存在于所有品种的食用菌中,在美味牛肝菌中,1-辛烯-3-醇相对含量为2.059%,且气味强度很大,对其呈味有非常重要的作用。
一般来讲,饱和烃类化合物的阈值都较高,对食品的风味贡献不大。但是萜烯类化合物相对饱和烃类阈值较小,具有一定风味。如长叶烯具有松节油香气,柠檬烯具有橙皮清香,对美味牛肝菌的风味呈现均有一定贡献。

表2 美味牛肝菌中特征性挥发性化合物的分析及鉴定结果Table 2 Analysis and identification of specific volatile components in Boletus edulis
在美味牛肝菌特征性挥发性化合物中还有一类含硫化合物,如3-甲硫基丙醛、2-噻吩甲醛,这类化合物是含硫氨基酸降解产生的,呈现一种硫化物气味。此外,还有一些酸类、酯类、酚类及一些未知化合物在牛肝菌香气中起着调和互补的作用,共同构成了美味牛肝菌的风味特征。
3 结论
本研究使用HS-SPME方法对美味牛肝菌的挥发性成分进行提取,再通过GC-MS对其挥发性成分进行了分析,并结合保留指数鉴定出53种化合物,其中有12种吡嗪类化合物,占总挥发性成分的58.87%,是美味牛肝菌的主要挥发性成分。美味牛肝菌挥发性成分中含量较高的化合物有2,6-二甲基吡嗪(30.09%)、3-乙基-2,5-二甲基吡嗪(13.32%)、2-噻吩甲醛(10.50%)、2-乙基-3-甲基吡嗪(5.35%)、2-乙基-6-甲基吡嗪(4.06%)、丙位戊内酯(3.34%)、己醛(2.54%)、2-正戊基呋喃(2.30%)等。
通过GC-O方法鉴定美味牛肝菌的特征性挥发性物质,共得到32种特征性香气成分,其中有3种物质不能通过GC-MS检测到。通过对美味牛肝菌特征性挥发性化合物的气味强度进行记录,气味强度较大的主要有己醛(青草味)、甲基吡嗪(坚果香味)、3-甲硫基丙醛(焦香)、2,6-二甲基吡嗪(烤肉香)、1-辛烯-3-醇(蘑菇味)、2-戊基呋喃(豆香)、2-乙基-6-甲基吡嗪(烤香)、3-辛烯-2-酮(蘑菇味)、苯乙醛(花香)等化合物,它们对美味牛肝菌的整体风味贡献很大,是主要的挥发性风味活性物质。
[1] Hiroyuki T,Tomonori N,Hiroyuki W. Energy value and digestibility of dietary oil containing mainly 1,3-diacylglycerol are similar to those of triacylglycerol[J]. Lipids,2001,36(8):379-382.
[2] 李志洲. 美味牛肝菌多糖的抗氧化性[J]. 食品与发酵工业,2007,33(4):49-51.
[3] 吴学谦,李海波,吴庆其,等. 黄靛牛肝菌子实体营养成分分析评价[J]. 食用菌学报,2005,12(2):19-23.
[4] 张春霞,纪开萍,何明霞,等. 暗褐网柄牛肝菌子实体营养成分分析[J]. 云南大学学报:自然科学版,2010,32(6):702-704.
[5] Sandrina A,Heleno,Lillian Barros,et al. Targeted metabolites analysis in wild Boletus species[J]. LWT-Food Science and Technology,2011,44:1343-1348.
[6] 田宏哲,杨丙成,观文娜. 微柱固相萃取-毛细管液相色谱在线联用技术[J]. 分析化学,2006,34(6):759-763.
[7] Gez E,Ledbitter C A,Hartsell P L. Volatile compounds in apricot,plum,and thier interspecific hybrids[J]. Journal of Agricultural Food Chemistry,1993,41:1669-1676.
[8] Madruga M. LRI-values of authentic compounds on DB5 column(GC-MS)[M]. Reading:University of Reading,1993.
[9] Taylor A. LRI-values on DB1 column and odours of authentic compounds[M]. Nottingham:University of Nottingham,1994.
[10] Leseigneur A,Heinen P. LRI-values of authentic compounds on DB5 column(GC)[M]. Reading:University of Reading,1990.
[11] Hartman T G. Volatile compounds generated from the Maillard reaction of pro-gly,gly-pro,and a mixture of glycine and proline with glucose[J]. Journal of Agricultural Food Chemistry,1992,40,1878-1880.
[12] Adams R P. Identification of essential oil components by gas chromatography/mass spectroscopy[M]. Carol Stream:Allured Publishing Corporation,1995.
[13] Beal A D,Mottram D S. Compounds contributing to the characteristic aroma of malted barley[J]. Journal of Agricultural Food Chemistry,1994,42:2880-2884.
[14] Jennings W,Shibamoto T. Qualitative Analysis of Flavor and Fragrance Volatiles by Glass Capillary Gas Chromatography[M].London:Academic Press,1980.
[15] Ramarathnam N,Rubin L J,Diosady L L. Studies on meat flavor- A novel method for trapping volatile components from uncured and cured pork[J].Journal of Agricultural Food Chemistry,1993,41:933-988.
[16] Shibamoto T,Kamiya Y,Mihara S.Isolation and identification of volatile compounds in cooked meat:Sukiyaki[J]. Journal of Agricultural Food Chemistry,1981,29:57-63.
[17] Yu T H,Chi T H.Volatile compounds generated from thermal reaction of methionine and methionine sulfoxide with or without glucose[J]. Journal of Agricultural Food Chemistry,1995,43:1641-1646.
[18] Alasalvar C,Shahidi F,Cadwallader K R. Comparison of natural and roasted Turkish tombul hazelnut(Corylus avellana L.)volatiles and flavor by DHA/GC/MS and descriptive sensory analysis[J]. Journal of Agricultural and Food Chemistry,2003,51(17):5067-5072.
[19] Thomas A F. An analysis of the flavor of dried mushroom,Boletus edulis[J]. Journal of Agricultural and Food Chemistry,1973,21(6):955-958.
[20] Andres A I,Cava R,Ruiz J. Monitoring volatile compounds during dry-cured ham ripening by solid-phase micro-extraction coupled to a new direct-extraction device[J]. Chromatogr A,2002,963:83-88.
[21] Noleau I,Toulemonde B.Volatile components of roast chicken fat[J]. Lebensm Wiss Technol,1987,20(1):37-41.
[22] Mani V. Application of solid phase micro-extraction[M].UK:Cambridge,1999:57.
[23] Mason M E,Johnson B,Hamming M C. Volatile components of roasted peanuts -The major monocarbonyls and some noncarbonyl components[J]. Journal of Agricultural and Food Chemistry,1967,15:66-70.
[24] Alasalvar C,Taylor K D A,Shahidi F.Comparison of volatiles of cultured and wild sea bream(Sparus aurata)during storage in ice by dynamic headspace analysis gas chromatography mass spectrometry[J]. Journal of Agricultural and Food Chemistry,2005,53(7):2616-2622.
