不同添加剂预处理核桃壳真空热裂解
2013-07-31吴文彪许妍丘克强
吴文彪,许妍,丘克强
(中南大学 化学化工学院,湖南 长沙,410083)
随着世界经济的迅速发展,全球能源需求迅速增长,能源和环境问题日益突出。生物质作为可再生能源,由于具有种类多,数量丰富并具有低硫和二氧化碳净排放为零等特点,在能源结构中的地位越来越高。核桃作为重要的干果油料树种,既是传统的营养保健果品,又是重要的油料能源资源。数据显示,2008年中国核桃年总产量为8.3×105t,居世界前列。按取仁率55%计算,中国每年产生核桃壳达3.735×105t,大量集中的核桃壳被丢弃或焚烧,不仅污染环境,而且造成资源的极大浪费。加强对核桃壳资源的综合利用,避免资源的浪费,生产高附加值的产品,不仅可以有效处理固体废弃物,而且能够变废为宝,具有重要的现实意义。目前,核桃壳的应用研究已有大量的报道,主要集中于油田污水处理过滤器中的滤料[1-2]、吸附剂[3-5]、聚合物基复合刨花板的生产[6]、提取棕色素[7-8]以及制备碳分子筛[9-10]和活性炭[11-17]中。当然,也有一些研究者进行核桃壳的热裂解研究[18-24]。郑志峰等[18-21]主要研究核桃壳的热解特性及其动力学。张蕾等[22]采用3种金属氧化物(二氧化锰、氧化铝和氧化钙)作为催化剂,进行核桃壳催化裂解制取氢气的研究。Onay等[23]在固定床反应器中裂解核桃壳,研究热解温度、升温速率、颗粒粒度和扫气流量对热解产品的产率及化学成分的影响。Mathias等[24]利用制备薄层色谱、气质联用和核磁共振等手段对核桃壳油中的木质素化合物进行分析表征。然而,目前仍没有采用不同添加剂对核桃壳进行预处理后的热裂解研究。采用不同添加剂对生物质进行预处理,生物质原料的性质会发生较大的变化,对其进行热裂解,所得到的生物油的性质及组成也会发生较大变化,甚至能使某种或某类物质在生物油中的含量得到较大的提升。真空条件可以使反应产生的裂解气迅速离开反应器,有效地降低二次热裂解反应发生的可能性,因此,对于油产量的提高具有较大作用。在此,本文作者在真空条件下对不同添加剂处理过的核桃壳进行热裂解制备生物油的研究,并利用气相色谱-质谱联用仪(GC-MS)对收集到的各种热解油进行分析表征。
1 实验部分
1.1 仪器与试剂
实验仪器包括:SHZMADZU-QP2010气相色谱-质谱联用仪(日本岛津公司生产);Vario EL Ⅲ CHNS元素分析仪(德国Elementar公司生产);DWJ-3L低温冷阱(北京松源华兴科技发展有限公司);FW177型中草药粉碎机(天津市泰斯特仪器有限公司生产);WTS型温控装置(东南大学自动化仪表研究所生产);DP-A型精密数字压力计(南京桑力电子设备厂生产);TW-1A型旋片式真空泵(温岭市挺威真空设备有限公司生产);自制加热电阻炉及不锈钢反应器。试剂为分析纯氢氧化钠、氢氧化钙、无水碳酸钠、无水氯化锌、盐酸、硝酸、硫酸和氯苯,色谱纯甲醇。实验所用核桃壳来自于湖南省长沙市农贸市场。
1.2 实验流程和方法
1.2.1 样品预处理
将核桃壳洗净、烘干、破碎,筛取粒度为75~355 μm的颗粒为样品。然后,对样品进行预处理。样品预处理主要分为以下几种:(1) 未作任何处理(S1);(2) 用蒸馏水处理(S2),即称取160 g左右核桃壳样品,放入1 L的烧杯中,加入500 mL蒸馏水,用电炉加热约1 h,至样品为糊状,停止加热,将样品置于105 ℃的烘箱内烘干 24 h,至样品恒质量为止;(3) 添加剂处理,但未洗涤(S3),即称取160 g左右核桃壳样品,放入1 L的烧杯中,加入500 mL配置的指定浓度的添加剂溶液 (NaOH, Ca(OH)2, Na2CO3, ZnCl2, HCl,HNO3和 H2SO4),用电炉加热约1 h,至样品为糊状,停止加热,将样品置于105 ℃的烘箱内烘干24 h,至样品恒质量为止;(4) 添加剂处理,已洗涤(S4),即:将步骤3得到的样品两等分,取其中1份用蒸馏水洗至液体pH值为7,将所得样品置于105 ℃的烘箱内烘干24 h,至样品恒质量为止。
1.2.2 实验流程
称取20.00 g样品,装入自制热裂解反应器中。实验流程如图1所示。在真空条件下,通过针阀控制体系初始压力为 10 kPa,以设定的升温速率(实验采取90 ℃/min)将样品加热到实验所需的最终热解温度(650 ℃),保温30 min,使反应发生完全。裂解反应发生后,产生的气体和气溶胶被真空泵迅速抽离反应器进入低温冷阱(–40℃),冷凝得到产物油;未冷凝的部分则通过吸收塔(碱石灰为吸收剂)除去气溶胶和酸性气体,剩下的气体由真空泵抽出,进入气体吸收池(质量分数为30% 的NaOH溶液),净化后的气体直接排空。实验结束后,称量固体和液体产物的质量,每个实验至少平行2次。

图1 实验流程示意图Fig.1 Schematic diagram of experimental process
1.2.3 实验方法
取60 μL氯苯(内标物质)溶于色谱纯甲醇,并定容至25 mL容量瓶中。将收集到的热解油用上述溶液稀释,稀释比为 1∶2(V(热解油)∶V(内标溶液))。取 1 μL稀释液进行GC-MS分析。GC条件: DB-5色谱柱(30 m×0.25 mm×0.25 μm);升温程序为 60 ℃保温 1 min,以10 ℃/min升温速度升温到140 ℃,接着以20 ℃/min升温到240 ℃,在该温度下保温1 min;分流比为15;气化室温度为280 ℃;柱流量为1.20 mL/min;载气(He)流量为3.0 mL/min。MS条件:标准EI源;离子源温度为 200 ℃;接口温度为 250 ℃;质荷比(m/z)为35~800;扫描间隔为0.4 s;电子倍增器电压为0.9 kV;溶剂切除时间为2 min。
2 结果与讨论
2.1 工业分析及元素分析
采用GB/T 212—2001对核桃壳进行工业分析,并利用Vario EL Ⅲ CHNS分析仪对核桃壳原料及裂解产物进行元素分析,实验结果如表1所示。由表1可知:裂解残渣中C的质量分数明显比原料中的高,H和差减O质量分数则相应降低,N和S的质量分数变化不大,表明核桃壳的裂解反应主要发生在其中的 CHO化合物中。
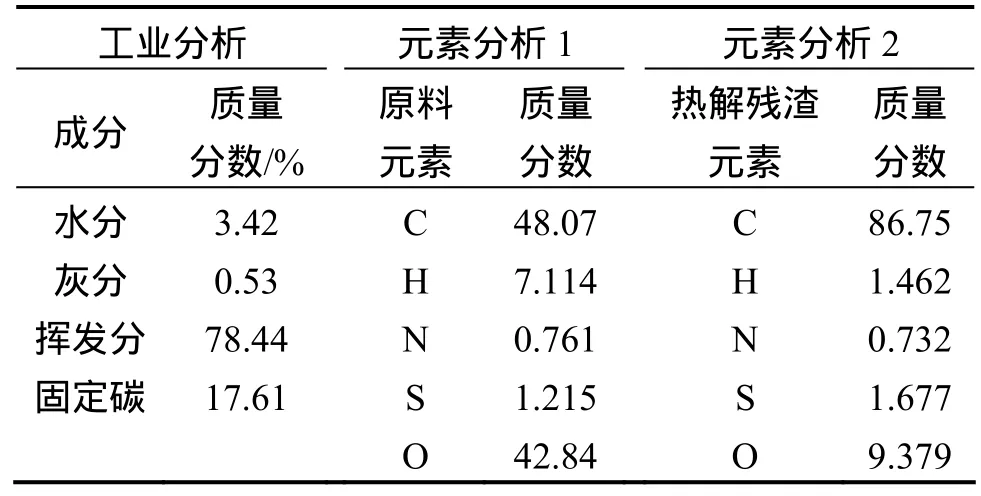
表1 工业分析和元素分析结果Table 1 Results of proximate and ultimate analyses
2.2 热解实验
按照1.2.2节所述的流程进行实验,各产物产率的计算公式如下:
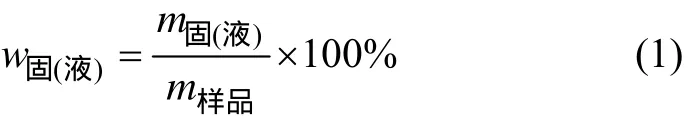
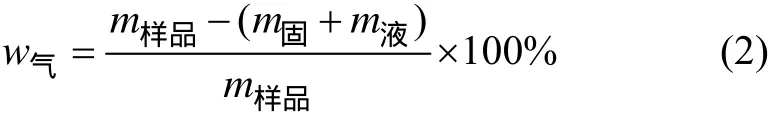
其中:w代表产率;m代表质量。
2.2.1 NaOH浓度对热解产物产率的影响
实验中配制0.5,1.0,1.5和2.0 mol/L的NaOH溶液对样品进行预处理,经过热解后各产物产率的变化规律如图2所示。由图2可知:未洗涤条件下(S3),固体产率随NaOH浓度升高而增大,液体和气体产率均是下降趋势。其原因主要是:该条件下,NaOH浓度越高,样品中残留的NaOH的量越大,导致发生反应的核桃壳的量减少,从而固体产率增大,挥发分(液、气)产率下降。在已洗涤条件下(S4),固体产率随NaOH浓度升高而减少,液体产率在1.0 mol/L处最高,气体产率在1.0 mol/L处最低。其原因可能是:NaOH浓度越高,对样品的活化作用越强,导致样品中化合键越容易断裂,从而反应越剧烈,固体产率越少,而气体和液体的产率是由裂解气化产物的组成所决定的,气化产物中若含有越多易冷凝的物质,则液体产率越高,相应的气体产率则变小。
2.2.2 不同添加剂对热解产物产率的影响
实验中分别配制浓度为 1.0 mol/L的 NaOH,Ca(OH)2, Na2CO3, ZnCl2, HCl, HNO3和H2SO4溶液对样品进行预处理,经过热解后各产物产率的结果如表2所示。由表2可知:未作任何处理的样品(S1)的固体产率普遍比经过添加剂处理过的样品的固体产率要低,这主要是因为在预处理过程中,核桃壳中一些结合度较低的组分或者较容易发生反应的成分在该过程中损失,从而在后续的热解反应中较易发生热解的成分变少,导致在实验热解温度下不能发生热解的成分相应变大。
由于热解残渣的质量分数越小,热解反应发生得越充分,所以,可以用热解残渣的质量分数大小来衡量热解反应发生的程度。在实验中热解条件固定的情况下,影响产物产率变化的因素主要包括:(1) 添加剂掺入核桃壳中的质量;(2) 添加剂对核桃壳的活化强度;(3) 添加剂对裂解反应的催化或阻化作用。第1项对产物产率的影响主要是因为样品的质量是固定的,若添加剂质量分数变大,则参与裂解反应的核桃壳的质量相应就变小,挥发分产率自然变小。第2项中,若添加剂对核桃壳的活化作用越强,则核桃壳中原本较难断裂的化合键变得更容易断裂,导致固体产率降低,挥发分产率变大。第3项则主要影响化合物的生成,在添加剂的作用下,可以使某些反应变得更容易或更难发生,导致该反应产物的含量相应增加或减少。
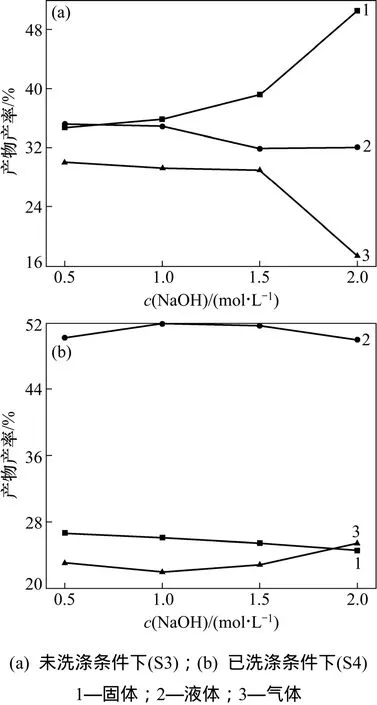
图2 热解产物产率随NaOH摩尔浓度的变化规律Fig.2 Trend of pyrolysis product yield changes by molecular concentration of NaOH
在表2中,对于未洗涤条件下,固体产率的变化规律基本上随所加入添加剂(酸除外)的相对分子质量的减小而减少,这是因为相同浓度下,添加剂相对分子质量越大,则其在样品中的质量分数越高,导致发生裂解的核桃壳质量分数变小。对于酸添加剂,在温和条件下,其对生物质的活化作用更强,并且在实验温度下,3种酸也会发生分解或挥发,从而导致固体产物含量变低。对于已洗涤条件,各产物产率的变化主要源自于添加剂对样品的活化作用或催化作用,由于这2种作用比较复杂,相关机理还有待深入研究,实验中暂时未能得出较普遍的结论。
2.3 GC-MS分析
按1.2.3节进行GC-MS分析。其中,定性结果是在 NIST05标准质谱库中匹配得到的。为在不同条件下得到热解产物组成的变化规律,定量结果则结合面积归一化法和内标法得到,即对于所有在色谱图中流出的组分峰进行面积归一化处理(各组分峰面积Ai与所有流出的组分峰总面积∑Ai之比为该组分的相对含量),并且利用内标物质比较不同条件下内标物的相对含量。若内标物质的相对含量相差不大,则认为其他组分的相对含量是可靠的,可以用于横向比较。实验中,为得到添加剂活化效果对后续热解反应的影响规律,只给出已洗涤条件下的 GC-MS检测结果,而未洗涤条件的则由于还包含添加剂本身可能的对热解反应的催化或阻化作用,导致最终的变化规律过于复杂,所以实验中暂不讨论。

表2 不同添加剂处理的热解产物产率Table 2 Results of pyrolysis product yield pretreated by different additives %
2.3.1 NaOH浓度对热解产物组成的影响
表3 给出已洗涤条件下,不同NaOH浓度热解油中主要物质的相对含量。由表3中可知,内标物质氯苯在各个样品中的相对含量基本一致,因此,其余成分相对含量的数据可用于横向比较。多数物质的相对含量在NaOH浓度为1.0 mol/L处最高,并且相对含量的变化规律与产物液体产率的变化规律一致,均是先升后降,说明该浓度的NaOH溶液对核桃壳的活化效果最佳,从而在后续的热解反应中更容易形成相关组分。需提出的是,左旋葡萄糖的相对含量在低浓度NaOH溶液的预处理下,几乎未检测到,而在高浓度NaOH溶液中,其含量则显著增大。根据该结果,可以通过改变添加剂的浓度来富集目标组分。
2.3.2 不同添加剂对热解产物产率的影响
表4所示为不同样品热解油中主要物质的相对含
量。氯苯在各个样品中的相对含量也基本一致,所以,其余成分相对含量的数据也可用于横向比较。由表 4可知:各种条件的热解油都主要由苯酚、愈创木酚、紫丁香酚及其衍生物等酚类物质,1-羟基-2-丁酮、2(5H)-呋喃酮、3-甲基-1,2-环戊二酮等酮类物质,糠醛、5-甲基糠醛等呋喃类物质,以及左旋葡萄糖、1,4∶3,6-二酐-α-d-吡喃葡萄糖等糖类物质组成。而且,在酸性条件下(HCl,HNO3,H2SO4和ZnCl2),酮类物质的相对含量比碱性条件下(NaOH,Ca(OH)2和 Na2CO3)的低,而呋喃类物质的则更高,其中糠醛的相对含量尤其高。同时,左旋葡萄糖的相对含量在HNO3和ZnCl2的活化处理下也显著增加,而 1,4∶3,6-二酐-α-d-吡喃葡萄糖的相对含量在H2SO4的活化处理下也相对较高。酚类物质的相对含量虽然没有明显的变化规律,但总的来说,其总相对含量在碱性条件下更占优势。

表3 已洗涤条件下,不同摩尔浓度NaOH预处理热解油中主要物质的相对含量Table 3 Relative content of main compounds in pyrolysis oil of S4 pretreated by different molecular concentrations of NaOH %
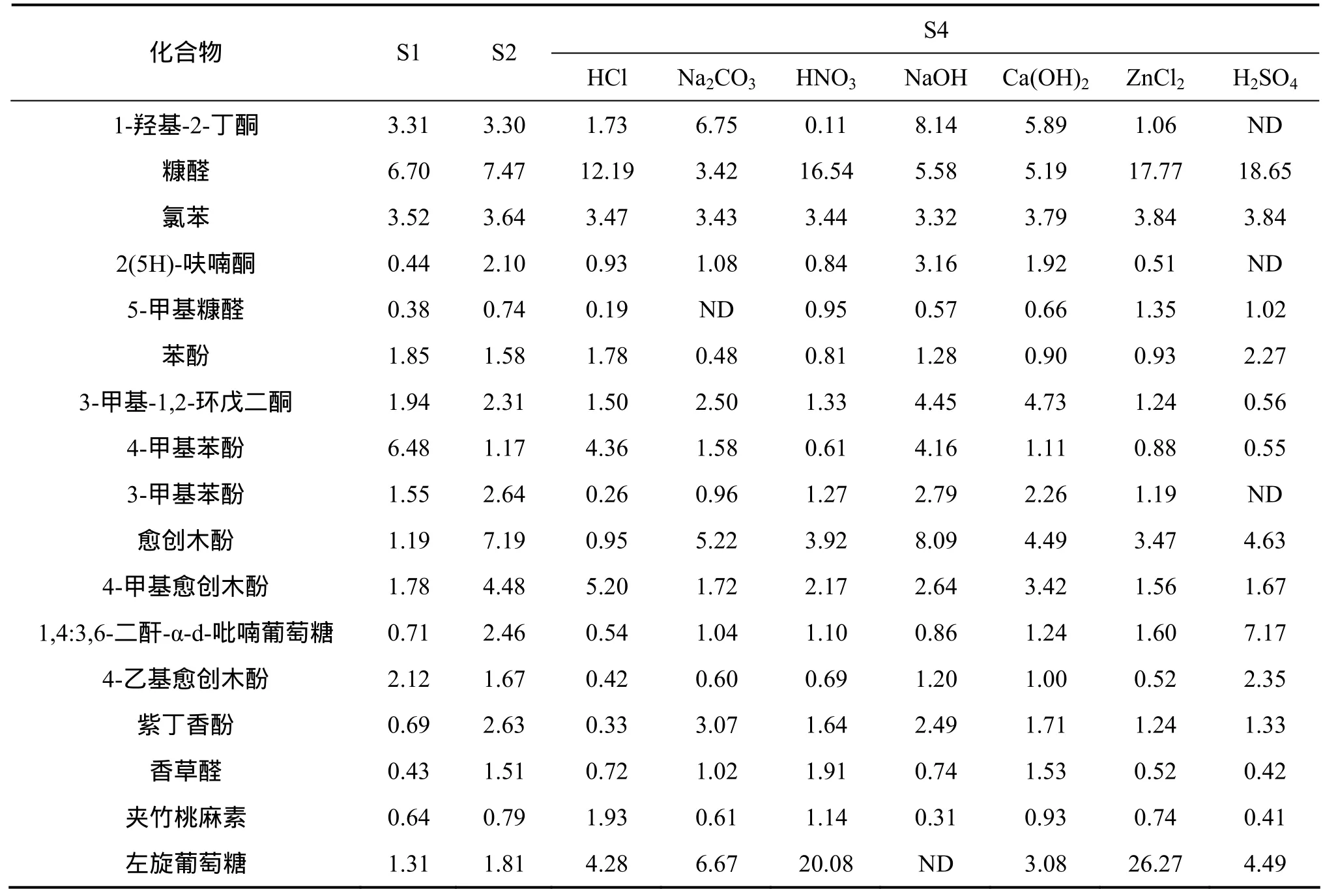
表4 不同样品热解油中主要物质的相对含量Table 4 Relative content of main compounds in pyrolysis oil of different samples %
由于生物质热解反应非常复杂,目前关于其机理的研究还有很多不清楚的地方。本文由于缺乏相关机理实验的印证,所以暂不讨论不同性质的添加剂预处理得到不同相对含量某种或某类物质的原因。
4 结论
(1) 不同添加剂预处理所得到的样品经过热解后的各产物产率有较大差别;而同种添加剂,浓度不同,各产物产率也不同。对于NaOH预处理的样品,在未洗涤条件下(S3),固体产率随NaOH浓度升高而增大,液体和气体产率均是下降趋势;已洗涤条件下(S4),固体产率随NaOH浓度升高而减少,液体产率在1.0 mol/L处最高,气体产率在1.0 mol/L处最低。
(2) 各种条件下的热解油都主要由酚类、酮类、呋喃类以及糖类等物质组成。酮类物质的相对含量在酸性条件下比碱性条件下的低,而呋喃类和糖类物质则相反。酚类物质的总相对含量在碱性条件下更占优势。对于不同浓度NaOH溶液预处理的热解油,多数物质的相对含量在1.0 mol/L处最高,并且变化规律与产物液体产率的变化规律一致,说明该浓度的 NaOH溶液对核桃壳的活化效果最好。
[1]赵军凯, 李勇, 张晓冬, 等.核桃壳过滤器运行现状分析与改进[J].工业水处理, 2008, 28(2)∶ 75-78.ZHAO Junkai, LI Yong, ZHANG Xiaodong, et al.Analysis of the present status of the walnut shell filter and its Improvement[J].Industrial Water Treatment, 2008, 28(2)∶75-78.
[2]李相远, 邵长新, 万世清, 等.核桃壳滤料粒径对油田污水过滤的影响研究[J].石油机械, 2005, 33(7)∶ 23-25.LI Xiangyuan, SHAO Changxin, WAN Shiqing, et al.Influence of grain size of walnut shell filter material on oilfield waste water filtering.China Petroleum Machinery, 2005, 33(7)∶ 23-25.
[3]Sumanjit W, Tejinder P S, Kansal I.Removal of Rhodamine-B by adsorption on walnut shell charcoal[J].Journal of Surface Science and Technology, 2008, 24(3/4)∶ 179-193.
[4]Nazari M A A, Najafpour G D, Ghoreyshi A A, et al.Adsorption of Methylene Blue in aqueous phase by fly ash, clay and walnut shell as adsorbents[J].World Applied Sciences Journal, 2010,8(2)∶ 229-234.
[5]Srinivasan A, Viraraghavan T.Removal of oil by walnut shell media[J].Bioresource Technology, 2008, 99(17)∶ 8217-8220.
[6]Gürü M, Atar M, Yildirim R.Production of polymer matrix composite particleboard from walnut shell and improvement of its requirements[J].Materials and Design, 2008, 29(1)∶ 284-287.
[7]陈志勇, 薛灵芬.核桃壳棕色素的提取及性能研究[J].信阳师范学院学报, 2001, 14(1)∶ 99-101.CHEN Zhiyong, XUE Lingfen.The extraction and property determination of brown matter in walnut pericarp[J].Journal of Xinyang Teachers College∶ Natural Science Edition, 2001, 14(1)∶99-101.
[8]李维莉, 马银海, 刘增康, 等.核桃壳棕色素的提取及性质研究[J].食品科学, 2008, 29(12)∶ 339-341.LI Weili, MA Yinhai, LIU Zengkang, et al.Extraction and characteristics of brown pigment from walnut shell[J].Food Science, 2008, 29(12)∶ 339-341.
[9]HU Z H, Vansant E F.Carbon molecular sieves produced from walnut shell[J].Carbon, 1995, 33(5)∶ 561-567.
[10]David E, Talaie A, Stanciu V, et al.Synthesis of carbon molecular sieves by benzene pyrolysis over microporous carbon materials[J].Journal of Materials Processing Technology,2004(157/158)∶ 290-296.
[11]Bagreev A A, Broshnik A P, Strelko V V, et al.Effect of chemical modification of walnut shell on the yield and pore structure of activated carbon[J].Russian Journal of Applied Chemistry∶ Translation of Zhurnal Prikladnoi Khimii, 2001,74(2)∶ 205-208.
[12]Bagreev A A, Broshnik A P, Strelko V V, et al.Effect of oxidizing treatment of walnut shell on the properties of activated carbon[J].Russian Journal of Applied Chemistry∶ Translation of Zhurnal Prikladnoi Khimii, 2001, 74(9)∶ 1453-1457.
[13]Zabihi M, Ahmadpour A, Haghighi Asl A.Removal of mercury from water by carbonaceous sorbents derived from walnut shell[J].Journal of Hazardous Materials, 2009, 167(1/2/3)∶230-236.
[14]Zabihi M, Haghighi A A, Ahmadpour A.Studies on adsorption of mercury from aqueous solution on activated carbons prepared from walnut shell[J].Journal of Hazardous Materials, 2010,174(1/2/3)∶ 251-256.
[15]WANG Gang, LI Aimin, LI Mingzhi.Sorption of nickel ions from aqueous solutions using activated carbon derived from walnut shell waste[J].Desalination and Water Treatment, 2010,16(1/3)∶ 282-289.
[16]Abechi S E, Gimba C E.Adsorption of cadmium from aqueous solution by activated carbon prepared from sawdust and walnut shell[J].Journal of Chemical Society of Nigeria, 2010, 35(1)∶1-4.
[17]Saeedi M, Jamshidi A, Abessi O, et al.Removal of dissolved cadmium from water by adsorption onto walnut and almond shell charcoal and its comparison with granular activated carbon[J].Water & Wastewater, 2009, 70∶ 16-22.
[18]郑志锋, 黄元波, 蒋剑春, 等.核桃壳热解行为及动力学研究[J].林产化学与工业, 2010, 30(2)∶ 6-10.ZHENG Zhifeng, HUANG Yuanbo, JIANG Jianchun, et al.Study on pyrolysis characteristics and kinetics of walnut shell[J].Chemistry and Industry of Forest Products, 2010, 30(2)∶6-10.
[19]张磊, 张蕾, 舒新前, 等.核桃壳与花生壳催化热解制氢的动力学研究[J].太阳能学报, 2009, 30(3)∶ 402-406.ZHANG Lei, ZHANG Lei, SHU Xinqian, et al.Study on the kinetics of catalytic pyrolysis of walnut shell and peanut shell[J].Acta Energiae Solaris Sinica, 2009, 30(3)∶ 402-406.
[20]曲雯雯, 夏洪应, 彭金辉, 等.核桃壳热解特性及动力学分析[J].农业工程学报, 2009, 25(2)∶ 194-198.QU Wenwen, XIA Hongying, PENG Jinhui, et al.Pyrolysis characteristics and kinetic analysis of walnut shell[J].Transactions of the Chinese Society of Agricultural Engineering,2009, 25(2)∶ 194-198.
[21]Yuan H R, Liu R H.Study on pyrolysis kinetics of walnut shell[J].Journal of Thermal Analysis and Calorimetry, 2007,89(3)∶ 983-986.
[22]张蕾, 张磊, 舒新前, 等.核桃壳催化热解制取氢气[J].吉林大学学报∶ 工学版, 2008, 38(2)∶ 287-291.ZHANG Lei, ZHANG Lei, SHU Xin-qian, et al.Producing hydrogen by catalytic pyrolysis of walnut shell.Journal of Jilin University∶ Engineering and Technolog y Edition, 2008, 38(2)∶287-291.
[23]Onay O, Beis S H, Kockar O M.Pyrolysis of walnut shell in a well-swept fixed-bed reactor[J].Energy Sources, 2004, 26(8)∶771-782.
[24]Mathias E V, Halkar U P.Separation and characterization of lignin compounds from the walnut (Juglans regia) shell oil using preparative TLC, GC–MS and 1H NMR[J].Journal of Analytical and Applied Pyrolysis, 2004, 71(2)∶ 515-524.
