Her-2基因特异性核酶体外表达载体的建立
2013-07-08麻馨月
麻馨月 赵 雪
(吉林农业科技学院生物工程学院,吉林 吉林 132101)
Her-2基因特异性核酶体外表达载体的建立
麻馨月 赵 雪
(吉林农业科技学院生物工程学院,吉林 吉林 132101)
目的构建人表皮生长因子受体-2(HER-2)特异性核酶(ribozyme,RZ)体外表达载体的建立。方法设计合成RZ基因,将该RZ克隆到真核表达载体pcDNA3.1(+)中,测序鉴定。结果经DNA测序分别证实合成的RZ基因序列克隆入pcDNA3.1(+)中。结论构建HER-2特异性RZ真核表达载体有助于进一步研究RZ对靶基因切割作用及雌激素受体阴性乳腺癌细胞MDA-MB-453中HER-2信号转导.
人表皮生长因子受体-2(HER-2);核酶
雌激素受体阴性乳腺癌恶性程度比较高,对内分泌治疗具有效率低,易转移复发,预后较差,生存率较低等特点,因而成为研究的热点和难点问题之一[1]。在雌激素受体阴性乳腺癌中,人表皮生长因子受体-2(HER-2)[2-4]常常呈现高表达状态,进行雌激素受体阴性乳腺癌HER-2及其相关因子的研究,有助于确定HER-2在雌激素受体阴性乳腺癌细胞生长、增殖及乳腺癌从激素依赖型转变为非激素依赖型中的作用,寻找可能的治疗靶点。本研究根据HER-2基因序列,设计并合成核酶基因,构建HER-2基因特异性锤头状核酶真核表达载体,为检测该核酶在体外对靶基因HER-2的作用,研究雌激素受体阴性乳腺癌细胞中HER-2信号转导途径相关因子的相关性及其分子机制和HER-2作为肿瘤基因治疗靶点提供实验与理论依据。
1 材料与方法
1.1 材料
限制性内切酶、DNA连接试剂盒、质粒小提试剂盒、DNA凝胶回收试剂盒、RT-PCR试剂盒均购自Takara公司;MDA-MB-453细胞购自中国科学院上海生命科学研究院细胞库;RPMI-1640培养基、DEPC、Trizol总RNA提取剂为Invitrogen公司产品;体外转录试剂盒为promage公司产品。
1.2 方法
1.2.1 核酶的设计
用计算机人工设计HER-2特异性核酶。选择HER-2mRNA基因序列(NM-004448)第2502位点的GTT为核酶切割位点,在核酶基因序列两端分别加上BamHⅠ和EcoRⅠ限制性内切酶位点及保护碱基。以核酶基因的非模板链为HA链,模板链为HB链,经设计后的核酶基因序列共58bp。
HA链:5'-GCGGAATTCTTTCCCTCCTGATGAG
TCCGTGAGGACGAAACACTTTGATGGATCCCGC-3';
HB链:5'-GCGGGATCCATCAAAGTGTTTCGTC
CTCACGGACTCATCAGGAGGGAAAGAATTCCGC-3'。
1.2.2 核酶基因的合成
设计核酶基因HA链和HB链,并由上海生物工程技术服务有限公司合成,取50μL A、B链混合经95℃加热变性5min,逐渐冷却到室温,退火形成互补双链,命名为RZ基因。
1.2.3 核酶基因重组子的构建及鉴定
RZ基因与pcDNA3.1(+)载体EcoRⅠ和BamHⅠ双酶切消化,并经凝胶回收。将RZ基因和pcDNA3.1(+)载体按摩尔比10∶1混合进行连接反应后,转化入大肠杆菌JM109,挑取单个菌落提取质粒,应用EcoRⅠ和BamHⅠ双酶切初步鉴定,DNA测序鉴定重组子。
1.2.4 核酶靶基因HER-2重组子的构建及鉴定
MDA-MB-453细胞悬浮生长于10%小牛血清的RPMI-1640培养基中(含100U/mL青霉素,100U/mL链霉素), 37℃,在体积分数为5%的CO2中培养。Trizol试剂提取细胞总RNA。利用PrimerPremier 5软件设计引物。上游引物:5'-GAATTCCGGCACAGTCTACAAGGGCATC-3';下游引物:5'-GGGGTACCCCAGGCGTCCGCGGTTT-3'。RT-PCR扩增靶基因HER-2 cDNA片段,也将其插入载体pcDNA3.1(+),重组子经PCR反应后电泳及测序鉴定。
2 结 果
核酶基因真核表达载体的鉴定:
2.1 酶切鉴定
应用BamHⅠ,EcoRⅠ双酶切载体,室温,2.0%琼脂糖凝胶,80V,电泳30min。电泳未见到<100bp的小片段。结果见图1。
2.2 核酶基因真核表达载体DNA测序鉴定
将构建出的载体进行DNA测序分析,由上海生物工程公司测定。所合成的核酶基因序列正确,并已被准确地克隆入pcDNA3.1(+)的BamHⅠ和EcoRⅠ两个酶切位点之间,该序列于T7启动子的下游。结果见图2。
3 讨 论
核酶是一类具有催化活性的RNA分子,本实验采用锤头状核酶。锤头状核酶能与特异性的HER-2靶基因结合,并且能切割HER-2靶基因,因此具有较强的抑制效率。锤头状核酶分子较小,结构简单,其催化活性中心只含有13个保守序列,加上两端与靶基因结合的结合臂,即组成了与靶基因GUC序列结合的具有催化活性的核酶,广泛应用于基因治疗领域[5-8]。由于核酶的本质是RNA,在细胞内不稳定,易被细胞内的RNA酶降解,本实验构建稳定而高表达的核酶载体成为发挥核酶较强抑制效率的首要步骤。所构建核酶的靶基因载体,在体外检测RZ活性及最佳反应条件,能增大其在体内发挥作用的可能性,保证为催化切割靶基因提供基本条件。
本实验RZ切割位点是根据毕锋等[9]设计的HER-2特异性核酶切割位点设计的,在基本核酶序列两端加入EcoRⅠ和BamHⅠ酶切位点,定向插入pcDNA3.1(+)载体的T7启动子下游,这样核酶基因既能在真核细胞中表达又能在原核细胞中表达,便于核酶基因的扩增及细胞转染的研究。本实验构建的RZ表达载体,结果有效表达,可用于后续的体外转录及体外切割活性实验,以便提供核酶的体外切割活性及最适反应条件,为下一步研究核酶在细胞内发挥较强抑制作用提供了可能性。
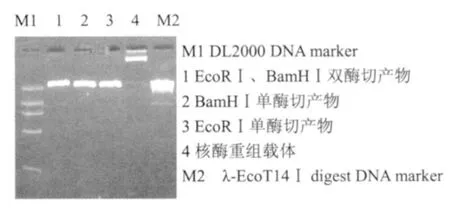
图1 核酶载体的鉴定
[1] 李少林,陈晓品,吴凯南.乳腺癌的生物学特性和临床对策[M].北京:科学出版社,2004:65-67.
[2] 田秀娟.乳腺癌C-erbB-3、C-erbB-4和C-erbB-2癌基因蛋白的表达及临床意义[J].肿瘤研究与临床,2005,17(1): 16-17.
[3] 杨金巧,陈琳,幸天勇,等.乳腺癌中C-erbB2癌基因与雌、孕激素受体和PS2的关系及其预后意义[J].四川大学学报:医学版,2004, 35(3): 334-336.
[4] Suzuki T,Anderegg B.Adenovirus-mediated Ribozyme Targeting of HER-2/neu Inhibits in Vivo Growth of Breast Cancer Cells[J]. Gene Ther,2000,7(3):241-248.
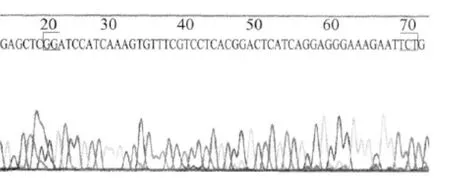
图2 核酶重组载体DNA序列分析
[5] 石建林,章为,周雪.核酶技术简介[J].四川解剖学杂志,2002,10 (1): 25-29.
[6] 程晋,张学庸,胡家露,等.核酶技术研究进展[J].国外医学肿瘤学分册,1997,24(1): 32-34.
[7] Tuschl T,Eckstein F.Hammerhead Ribozymes:Importance ofStemloopⅡforActivity[J].Proceedings of the National Academy of Sciences of the USA,1993,90(15): 6991-6994.
[8] McCall MJ,Hendry P,Jennings PA.Minimal Sequence Requirements for Ribozyme Activity[J].Proceedings of the National Academy of Sciences of the USA,1992,89(13):5710-5714.
[9] 毕锋,张学庸,樊代明,等.抗c-erbB-2Ribozyme的计算机设计[J].第四军医大学学报,1997,18(1): 6-9.
R3
B
1671-8194(2013)17-0080-02
吉林农业科技学院青年教师科研基金资助项目{赵雪:吉农院合字[2012第123号];麻馨月:吉农院合字[2012127]号}
